第10章金属检测题—2021-2022学年九年级化学京改版下册(word版 含答案)
文档属性
| 名称 | 第10章金属检测题—2021-2022学年九年级化学京改版下册(word版 含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 291.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-10 22:05:20 | ||
图片预览



文档简介
第10章《金属》检测题
一、单选题
1.下列实验中对物质的鉴别或除杂质,提供的方案不能达到目的的是
选项 物质鉴别 实验方案
A 鉴别生石灰和熟石灰 分别取少量固体放入试管中,再加入少量水,然后用手摸两支试管温度的变化。
B 鉴别二氧化碳和氮气 分别将两种气体通入澄清的石灰水,看是否变浑浊
C 除去铁粉中少量氧化铁杂质 将该固体放入玻璃管内,通入一氧化碳后再加热直到固体颜色全部变黑。
D 除去CO2中少量杂质CO 将该混合气体在空气中点燃。
A.A B.B C.C D.D
2.下列实验内容符合坐标图所示变化趋势的是
序号 实验内容 横坐标表示的量 纵坐标表示的量
① 用过量红磷测定空气中氧气含量 时间 红磷的质量
② 过氧化氢溶液与二氧化锰制氧气 时间 二氧化锰的质量
③ 生锈铁钉放入一定量稀盐酸 加入盐酸的质量 剩余固体的质量
④ 向一定量硝酸银溶液中放入铜片 反应时间 固体质量
A.①② B.①③ C.②③ D.③④
3.下列实验现象,描述正确的是
A.红热的铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
B.用火柴去点蜡烛刚熄灭时产生的白烟,蜡烛不能重新燃烧
C.将光亮的铁钉放入硫酸铜溶液中,铁钉表面变红
D.硫在空气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体
4.物质的结构决定物质的性质,下列关于物质结构与性质的说法不正确的是
A.金属钠与钾的化学性质相似,是由于构成它们原子的最外层电子数目都为1
B.金刚石和石墨的物理性质不同,是由于构成它们的碳原子不同
C.生铁和钢的性质不同,是因为它们的含碳量不同
D.金属钠和镁的性质不同,是由于钠和镁的原子结构不同
5.下列实验操作能达到目的的是
选项 实验目的 实验操作
A 比较铜片与铝片的硬度 滴盐酸,观察反应情况
B 鉴别CO2与CO 通入石蕊溶液,观察颜色
C 除去CO2中少量CO 点燃得合气体
D 除去ZnCl2溶液中的少量CuCl2 加足量铁粉,搅拌,过滤
A.A B.B C.C D.D
6.下列实验现象的描述错误的是
A.铁丝在氧气中燃烧发出白光,生成白色固体
B.把铁粉放入稀硫酸中可以看到有气泡产生,溶液逐渐由无色变为浅绿色
C.将铜片在空气中加热,表面逐渐变黑
D.镁带在空气中燃烧,发出耀眼白光,生成白色固体
7.如图为治理汽车尾气反应的微观示意图。下列有关说法正确的是
A.该反应属于置换反应 B.参加反应的两种物质的分子个数比为 2:3
C.该反应前后元素的化合价均改变 D.参加反应 NO 和 CO 的质量比为 15∶14
8.下列物质在给定条件下不能完全实现转化的是
A. B.
C. D.
9.下列化学反应属于置换反应的是
A. B.
C. D.
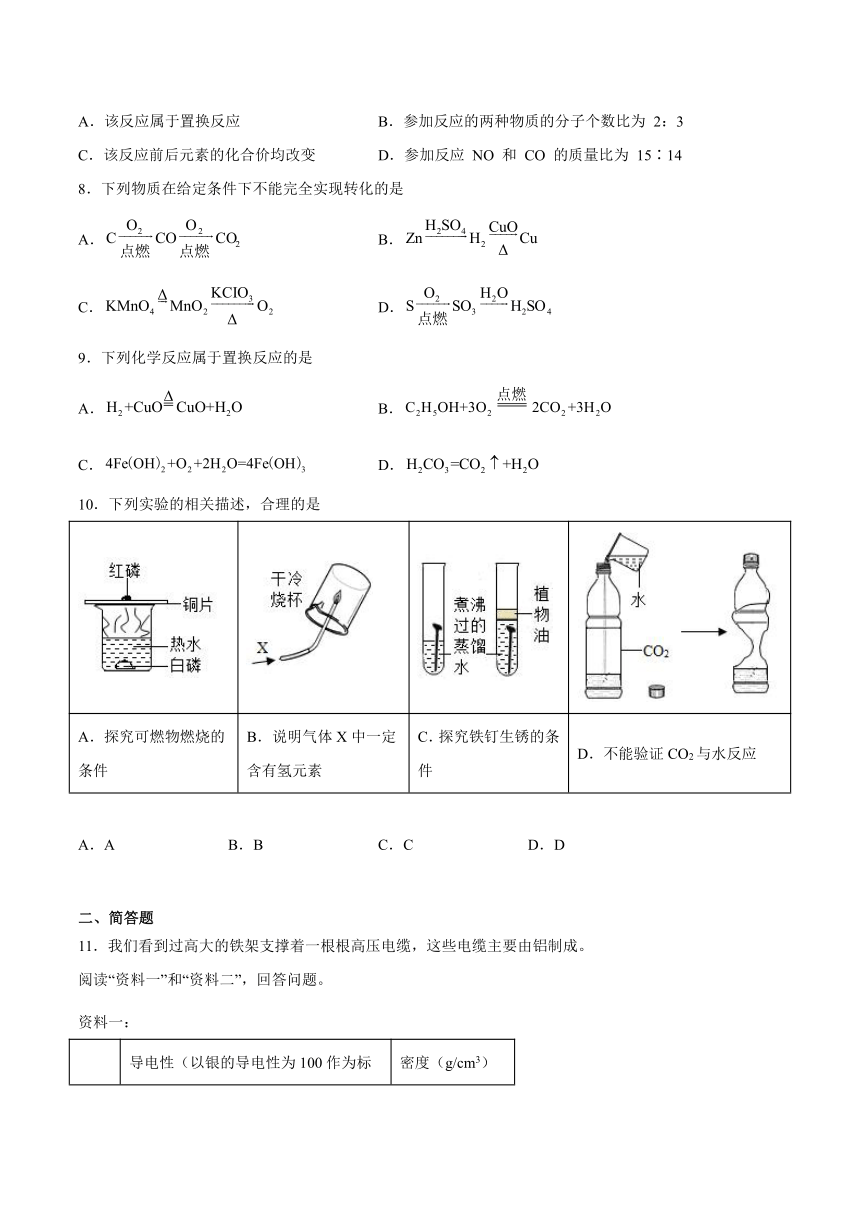
10.下列实验的相关描述,合理的是
A.探究可燃物燃烧的条件 B.说明气体X中一定含有氢元素 C.探究铁钉生锈的条件 D.不能验证CO2与水反应
A.A B.B C.C D.D
二、简答题
11.我们看到过高大的铁架支撑着一根根高压电缆,这些电缆主要由铝制成。
阅读“资料一”和“资料二”,回答问题。
资料一:
导电性(以银的导电性为100作为标准) 密度(g/cm3)
铜 99 8.92
铝 61 2.70
资料二:地壳中各元素的含量(质量分数)
(1)通过对上资料的分析,说明高压电缆用铝制而不用铜制的原因。
(2)铝在常温下能与氧气反应,但铝制的高压电缆却很耐腐蚀。说明其原因。
12.化学与我们的生活息息相关,请你结合生活常识解决下列问题:
(1)铁制品是怎样锈蚀的?家用的菜刀怎样防止它生锈?
(2)生活中可用汽油,洗洁精除去衣服上油污,二者去油污的原理不一样,请说明理由。
三、推断题
13.爱好化学的体育老师在体育课上请7名同学做排队游戏,A ~ G 7名同学分别代表氧气、木炭、一氧化碳、二氧化碳、铜、氧化铁、硝酸银7种初中化学常见物质中的一种物质。
(游戏规则)
规则①:相对分子质量最大的A排在最前面。
规则②:A、B、C、D、E、F、G相邻之间能发生化学反应。
(1)写出以下物质的化学式:A_________;E___________。
(2)写出符合要求的化学方程式:
①A + B____________;
②C + D_____________;
③E→G______________。
(3)B与C反应的现象___________。
(4)D的一种用途是 ____________。
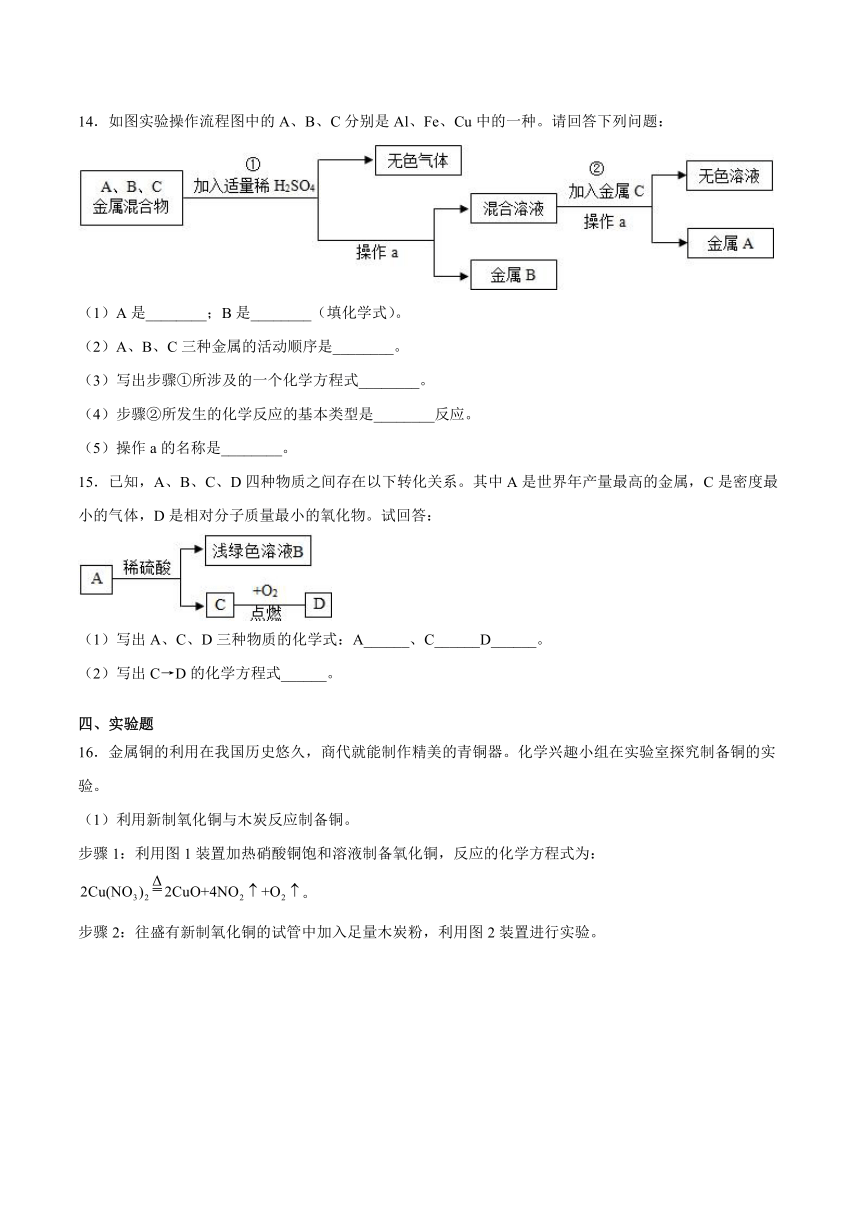
14.如图实验操作流程图中的A、B、C分别是Al、Fe、Cu中的一种。请回答下列问题:
(1)A是________;B是________(填化学式)。
(2)A、B、C三种金属的活动顺序是________。
(3)写出步骤①所涉及的一个化学方程式________。
(4)步骤②所发生的化学反应的基本类型是________反应。
(5)操作a的名称是________。
15.已知,A、B、C、D四种物质之间存在以下转化关系。其中A是世界年产量最高的金属,C是密度最小的气体,D是相对分子质量最小的氧化物。试回答:
(1)写出A、C、D三种物质的化学式:A______、C______D______。
(2)写出C→D的化学方程式______。
四、实验题
16.金属铜的利用在我国历史悠久,商代就能制作精美的青铜器。化学兴趣小组在实验室探究制备铜的实验。
(1)利用新制氧化铜与木炭反应制备铜。
步骤1:利用图1装置加热硝酸铜饱和溶液制备氧化铜,反应的化学方程式为:。
步骤2:往盛有新制氧化铜的试管中加入足量木炭粉,利用图2装置进行实验。
①步骤1加热时,观察到试管中有红棕色的有毒气体产生,该气体是______,据此推测气囊的作用是______。
②在图1气囊中画出主要粒子的微观示意图并进行必要的标注______(粒子数目不作要求:不考虑空气、水)。
③图2中,A试管内所观察到的实验现象为______。
(2)请选择下列试剂设计两种制备铜的方案(要求每种试剂只能使用一次)。
限选试剂:CuO、Fe2O3、CO、H2、Fe、CuSO4溶液
方案 预期反应的化学方程式 依据的反应规律
① ______ 金属活动性顺序里,前面的金属能把后面的金属从它化合物的溶液里置换出来
② ______ (略)
17.古文献记载:距今5000~4000年我国古代人们已开始冶铸青铜器(如图1)。青铜器表面常会有一层铜锈,同学们对铜锈开展了以下探究活动。
查阅资料:
活动一:探究铜锈的组成
用图2所示的实验装置隔绝空气加热铜锈,观察到澄清石灰水变浑浊,干燥管内白色粉末变为蓝色,试管中固体由绿色变为黑色。
(交流讨论)
(1)由活动一推测,铜锈中含有的元素有________;烧杯中发生反应的化学方程式为________。
活动二:探究铜生锈的条件
(做出猜想)在活动一的基础上,猜想铜生锈的条件是铜与H2O、CO2同时接触。
(进行实验)
序号 ① ② ③ ④
实验
现象 铜片表面有绿色物质 无明显现象 无明显现象 无明显现象
(得出结论)铜生锈的条件是与H2O、CO2同时接触。
(反思评价)
(2)小组同学做出“铜生锈的条件是铜与H2O、CO2同时接触”这一猜想的理由是____________。
(3)对比实验①③得到的结论是____________。
(4)能说明铜生锈与H2O有关的实验是____________(填序号)
(5)经过反思,小刚同学对所得结论提出疑问:与氧气接触也可能是铜生锈的条件之一。小丽同学认为实验①、④对比即可说明铜生锈与氧气有关。请判断小丽的说法是否正确并说明理由:____________。
(6)通过实验证明,铜生锈的条件是铜与氧气、二氧化碳和水同时接触。由此,你对保存铜制品的建议是____________。
五、计算题
18.将8g含杂质的粗锌,加入到盛有100g稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应),恰好完全反应,称得烧杯内物质的总质量为107.8g。试计算:
(1)生成氢气的质量为______g。
(2)所用粗锌中锌的质量是多少?所用稀硫酸中溶质的质量分数是多少?
19.日常生活中接触的金属材料,大多属于合金。其中黄铜是以锌作主要添加元素的铜合金。已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示。试计算:
(1)由题意可知,反应生成氢气的质量共_______g
(2)若欲计算反应后所得溶液的质量,你认为至少还应该补充的一个条件是_______
(3)弹壳中铜的质量______(计算结果精确至0.1,请书写出计算过程)
20.某地“铁画”(镀金)含有金、铁(其他成分忽略不计)。某同学取一定质量的铁画边角料,加入足量稀盐酸,充分反应后,放出0.3g H2,剩余固体质量为1.6g。
(1)求样品中铁的质量。
(2)求样品中金的质量分数。
参考答案
1.D 2.B 3.C 4.B 5.B 6.A 7.D 8.D 9.A 10.D
11.
(1)铝在地壳中含量比铜在地壳中含量高;铝的导电性大约是铜的导电性的2/3,但密度不到铜的1/3,制相同长度、相同导电能力的电缆,铝的质量比铜小,避免铁架承受过大的压力和电缆承受过大的拉力
(2)铝在常温下与空气中的氧气反应,其表面生成一层致密的氧化铝薄膜,隔绝了与空气的接触,阻止了铝的进一步反应
12.
(1)铁与空气中的水蒸气、氧气同时发生化学反应的过程。保持菜刀表面洁净、干燥
(2)汽油除油污的原理是溶解,洗洁精除油污的原理是乳化
13.
(1)
(2)
(3)红色固体变黑
(4)作燃料、冶炼金属等
14.
(1) Fe Cu
(2)C>A>B
(3)2Al+3H2SO4=Al2(SO4)3+3H2↑(或Fe+H2SO4=FeSO4+H2↑)
(4)置换
(5)过滤
15.
(1) Fe H2 H2O
(2)2H2+ O22H2O
16.
(1) 二氧化氮2 收集气体, 防止污染空气 黑色固体变红
(2) 或
17.
(1) 铜、碳、氢、氧
(2)根据质量守恒定律,化学反应前后,元素的种类不变,铜锈中含氢元素、碳元素,故铜生锈的条件是铜与水、二氧化碳同时接触
(3)铜生锈的条件之一是与二氧化碳接触
(4)①②
(5)不正确,要证明铜生锈与O2是否有关,与①对比的实验应该是铜片与H2O、CO2接触,而④中铜片只与H2O接触(或④实验中没有CO2)
(6)保持铜制品干燥
18.
(1)0.2
(2)解:设粗锌中锌的质量为 x;所用稀硫酸中溶质的质量为y
答:所用粗锌中锌的质量是6.5g;所用稀硫酸中溶质的质量分数是9.8%。
19.
(1)0.2
(2)稀硫酸的质量
(3)
设黄铜中锌的质量为x
x=6.5g
弹壳中铜的质量为:22g﹣6.5g=15.5g
答:弹壳中铜的质量为15.5g。
20.(1)解:设样品中铁的质量为x
x=8.4g
答:样品中铁的质量为8.4g;
(2)样品中金的质量分数为:
答:样品中金的质量分数为16%。
一、单选题
1.下列实验中对物质的鉴别或除杂质,提供的方案不能达到目的的是
选项 物质鉴别 实验方案
A 鉴别生石灰和熟石灰 分别取少量固体放入试管中,再加入少量水,然后用手摸两支试管温度的变化。
B 鉴别二氧化碳和氮气 分别将两种气体通入澄清的石灰水,看是否变浑浊
C 除去铁粉中少量氧化铁杂质 将该固体放入玻璃管内,通入一氧化碳后再加热直到固体颜色全部变黑。
D 除去CO2中少量杂质CO 将该混合气体在空气中点燃。
A.A B.B C.C D.D
2.下列实验内容符合坐标图所示变化趋势的是
序号 实验内容 横坐标表示的量 纵坐标表示的量
① 用过量红磷测定空气中氧气含量 时间 红磷的质量
② 过氧化氢溶液与二氧化锰制氧气 时间 二氧化锰的质量
③ 生锈铁钉放入一定量稀盐酸 加入盐酸的质量 剩余固体的质量
④ 向一定量硝酸银溶液中放入铜片 反应时间 固体质量
A.①② B.①③ C.②③ D.③④
3.下列实验现象,描述正确的是
A.红热的铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
B.用火柴去点蜡烛刚熄灭时产生的白烟,蜡烛不能重新燃烧
C.将光亮的铁钉放入硫酸铜溶液中,铁钉表面变红
D.硫在空气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体
4.物质的结构决定物质的性质,下列关于物质结构与性质的说法不正确的是
A.金属钠与钾的化学性质相似,是由于构成它们原子的最外层电子数目都为1
B.金刚石和石墨的物理性质不同,是由于构成它们的碳原子不同
C.生铁和钢的性质不同,是因为它们的含碳量不同
D.金属钠和镁的性质不同,是由于钠和镁的原子结构不同
5.下列实验操作能达到目的的是
选项 实验目的 实验操作
A 比较铜片与铝片的硬度 滴盐酸,观察反应情况
B 鉴别CO2与CO 通入石蕊溶液,观察颜色
C 除去CO2中少量CO 点燃得合气体
D 除去ZnCl2溶液中的少量CuCl2 加足量铁粉,搅拌,过滤
A.A B.B C.C D.D
6.下列实验现象的描述错误的是
A.铁丝在氧气中燃烧发出白光,生成白色固体
B.把铁粉放入稀硫酸中可以看到有气泡产生,溶液逐渐由无色变为浅绿色
C.将铜片在空气中加热,表面逐渐变黑
D.镁带在空气中燃烧,发出耀眼白光,生成白色固体
7.如图为治理汽车尾气反应的微观示意图。下列有关说法正确的是
A.该反应属于置换反应 B.参加反应的两种物质的分子个数比为 2:3
C.该反应前后元素的化合价均改变 D.参加反应 NO 和 CO 的质量比为 15∶14
8.下列物质在给定条件下不能完全实现转化的是
A. B.
C. D.
9.下列化学反应属于置换反应的是
A. B.
C. D.
10.下列实验的相关描述,合理的是
A.探究可燃物燃烧的条件 B.说明气体X中一定含有氢元素 C.探究铁钉生锈的条件 D.不能验证CO2与水反应
A.A B.B C.C D.D
二、简答题
11.我们看到过高大的铁架支撑着一根根高压电缆,这些电缆主要由铝制成。
阅读“资料一”和“资料二”,回答问题。
资料一:
导电性(以银的导电性为100作为标准) 密度(g/cm3)
铜 99 8.92
铝 61 2.70
资料二:地壳中各元素的含量(质量分数)
(1)通过对上资料的分析,说明高压电缆用铝制而不用铜制的原因。
(2)铝在常温下能与氧气反应,但铝制的高压电缆却很耐腐蚀。说明其原因。
12.化学与我们的生活息息相关,请你结合生活常识解决下列问题:
(1)铁制品是怎样锈蚀的?家用的菜刀怎样防止它生锈?
(2)生活中可用汽油,洗洁精除去衣服上油污,二者去油污的原理不一样,请说明理由。
三、推断题
13.爱好化学的体育老师在体育课上请7名同学做排队游戏,A ~ G 7名同学分别代表氧气、木炭、一氧化碳、二氧化碳、铜、氧化铁、硝酸银7种初中化学常见物质中的一种物质。
(游戏规则)
规则①:相对分子质量最大的A排在最前面。
规则②:A、B、C、D、E、F、G相邻之间能发生化学反应。
(1)写出以下物质的化学式:A_________;E___________。
(2)写出符合要求的化学方程式:
①A + B____________;
②C + D_____________;
③E→G______________。
(3)B与C反应的现象___________。
(4)D的一种用途是 ____________。
14.如图实验操作流程图中的A、B、C分别是Al、Fe、Cu中的一种。请回答下列问题:
(1)A是________;B是________(填化学式)。
(2)A、B、C三种金属的活动顺序是________。
(3)写出步骤①所涉及的一个化学方程式________。
(4)步骤②所发生的化学反应的基本类型是________反应。
(5)操作a的名称是________。
15.已知,A、B、C、D四种物质之间存在以下转化关系。其中A是世界年产量最高的金属,C是密度最小的气体,D是相对分子质量最小的氧化物。试回答:
(1)写出A、C、D三种物质的化学式:A______、C______D______。
(2)写出C→D的化学方程式______。
四、实验题
16.金属铜的利用在我国历史悠久,商代就能制作精美的青铜器。化学兴趣小组在实验室探究制备铜的实验。
(1)利用新制氧化铜与木炭反应制备铜。
步骤1:利用图1装置加热硝酸铜饱和溶液制备氧化铜,反应的化学方程式为:。
步骤2:往盛有新制氧化铜的试管中加入足量木炭粉,利用图2装置进行实验。
①步骤1加热时,观察到试管中有红棕色的有毒气体产生,该气体是______,据此推测气囊的作用是______。
②在图1气囊中画出主要粒子的微观示意图并进行必要的标注______(粒子数目不作要求:不考虑空气、水)。
③图2中,A试管内所观察到的实验现象为______。
(2)请选择下列试剂设计两种制备铜的方案(要求每种试剂只能使用一次)。
限选试剂:CuO、Fe2O3、CO、H2、Fe、CuSO4溶液
方案 预期反应的化学方程式 依据的反应规律
① ______ 金属活动性顺序里,前面的金属能把后面的金属从它化合物的溶液里置换出来
② ______ (略)
17.古文献记载:距今5000~4000年我国古代人们已开始冶铸青铜器(如图1)。青铜器表面常会有一层铜锈,同学们对铜锈开展了以下探究活动。
查阅资料:
活动一:探究铜锈的组成
用图2所示的实验装置隔绝空气加热铜锈,观察到澄清石灰水变浑浊,干燥管内白色粉末变为蓝色,试管中固体由绿色变为黑色。
(交流讨论)
(1)由活动一推测,铜锈中含有的元素有________;烧杯中发生反应的化学方程式为________。
活动二:探究铜生锈的条件
(做出猜想)在活动一的基础上,猜想铜生锈的条件是铜与H2O、CO2同时接触。
(进行实验)
序号 ① ② ③ ④
实验
现象 铜片表面有绿色物质 无明显现象 无明显现象 无明显现象
(得出结论)铜生锈的条件是与H2O、CO2同时接触。
(反思评价)
(2)小组同学做出“铜生锈的条件是铜与H2O、CO2同时接触”这一猜想的理由是____________。
(3)对比实验①③得到的结论是____________。
(4)能说明铜生锈与H2O有关的实验是____________(填序号)
(5)经过反思,小刚同学对所得结论提出疑问:与氧气接触也可能是铜生锈的条件之一。小丽同学认为实验①、④对比即可说明铜生锈与氧气有关。请判断小丽的说法是否正确并说明理由:____________。
(6)通过实验证明,铜生锈的条件是铜与氧气、二氧化碳和水同时接触。由此,你对保存铜制品的建议是____________。
五、计算题
18.将8g含杂质的粗锌,加入到盛有100g稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应),恰好完全反应,称得烧杯内物质的总质量为107.8g。试计算:
(1)生成氢气的质量为______g。
(2)所用粗锌中锌的质量是多少?所用稀硫酸中溶质的质量分数是多少?
19.日常生活中接触的金属材料,大多属于合金。其中黄铜是以锌作主要添加元素的铜合金。已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示。试计算:
(1)由题意可知,反应生成氢气的质量共_______g
(2)若欲计算反应后所得溶液的质量,你认为至少还应该补充的一个条件是_______
(3)弹壳中铜的质量______(计算结果精确至0.1,请书写出计算过程)
20.某地“铁画”(镀金)含有金、铁(其他成分忽略不计)。某同学取一定质量的铁画边角料,加入足量稀盐酸,充分反应后,放出0.3g H2,剩余固体质量为1.6g。
(1)求样品中铁的质量。
(2)求样品中金的质量分数。
参考答案
1.D 2.B 3.C 4.B 5.B 6.A 7.D 8.D 9.A 10.D
11.
(1)铝在地壳中含量比铜在地壳中含量高;铝的导电性大约是铜的导电性的2/3,但密度不到铜的1/3,制相同长度、相同导电能力的电缆,铝的质量比铜小,避免铁架承受过大的压力和电缆承受过大的拉力
(2)铝在常温下与空气中的氧气反应,其表面生成一层致密的氧化铝薄膜,隔绝了与空气的接触,阻止了铝的进一步反应
12.
(1)铁与空气中的水蒸气、氧气同时发生化学反应的过程。保持菜刀表面洁净、干燥
(2)汽油除油污的原理是溶解,洗洁精除油污的原理是乳化
13.
(1)
(2)
(3)红色固体变黑
(4)作燃料、冶炼金属等
14.
(1) Fe Cu
(2)C>A>B
(3)2Al+3H2SO4=Al2(SO4)3+3H2↑(或Fe+H2SO4=FeSO4+H2↑)
(4)置换
(5)过滤
15.
(1) Fe H2 H2O
(2)2H2+ O22H2O
16.
(1) 二氧化氮2 收集气体, 防止污染空气 黑色固体变红
(2) 或
17.
(1) 铜、碳、氢、氧
(2)根据质量守恒定律,化学反应前后,元素的种类不变,铜锈中含氢元素、碳元素,故铜生锈的条件是铜与水、二氧化碳同时接触
(3)铜生锈的条件之一是与二氧化碳接触
(4)①②
(5)不正确,要证明铜生锈与O2是否有关,与①对比的实验应该是铜片与H2O、CO2接触,而④中铜片只与H2O接触(或④实验中没有CO2)
(6)保持铜制品干燥
18.
(1)0.2
(2)解:设粗锌中锌的质量为 x;所用稀硫酸中溶质的质量为y
答:所用粗锌中锌的质量是6.5g;所用稀硫酸中溶质的质量分数是9.8%。
19.
(1)0.2
(2)稀硫酸的质量
(3)
设黄铜中锌的质量为x
x=6.5g
弹壳中铜的质量为:22g﹣6.5g=15.5g
答:弹壳中铜的质量为15.5g。
20.(1)解:设样品中铁的质量为x
x=8.4g
答:样品中铁的质量为8.4g;
(2)样品中金的质量分数为:
答:样品中金的质量分数为16%。
