〖卷11〗人教九年级化学下册同步高效作业本:第九单元 溶液(阶段知识整合与训练)(含解析)
文档属性
| 名称 | 〖卷11〗人教九年级化学下册同步高效作业本:第九单元 溶液(阶段知识整合与训练)(含解析) | 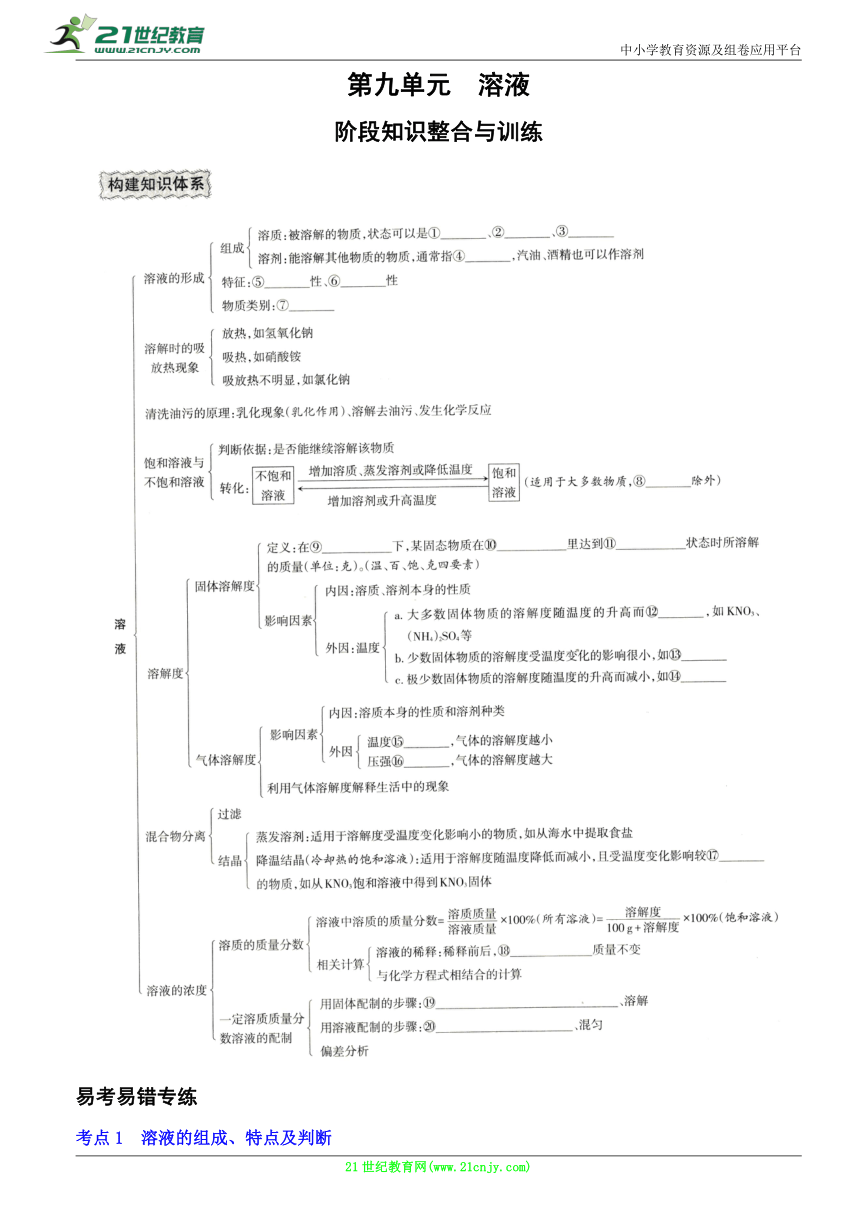 | |
| 格式 | docx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-09 19:15:14 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
第九单元 溶液
阶段知识整合与训练
易考易错专练
考点1 溶液的组成、特点及判断
1.溶液与人们的生活息息相关。下列有关溶液的说法正确的是 ( )
A.溶质可以是固体,也可以是液体或气体
B.将汽油与水充分混合,得到的是溶液
C.将10%的某溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.某饱和溶液降温到t℃析出晶体后,得到的是t℃时的不饱和溶液
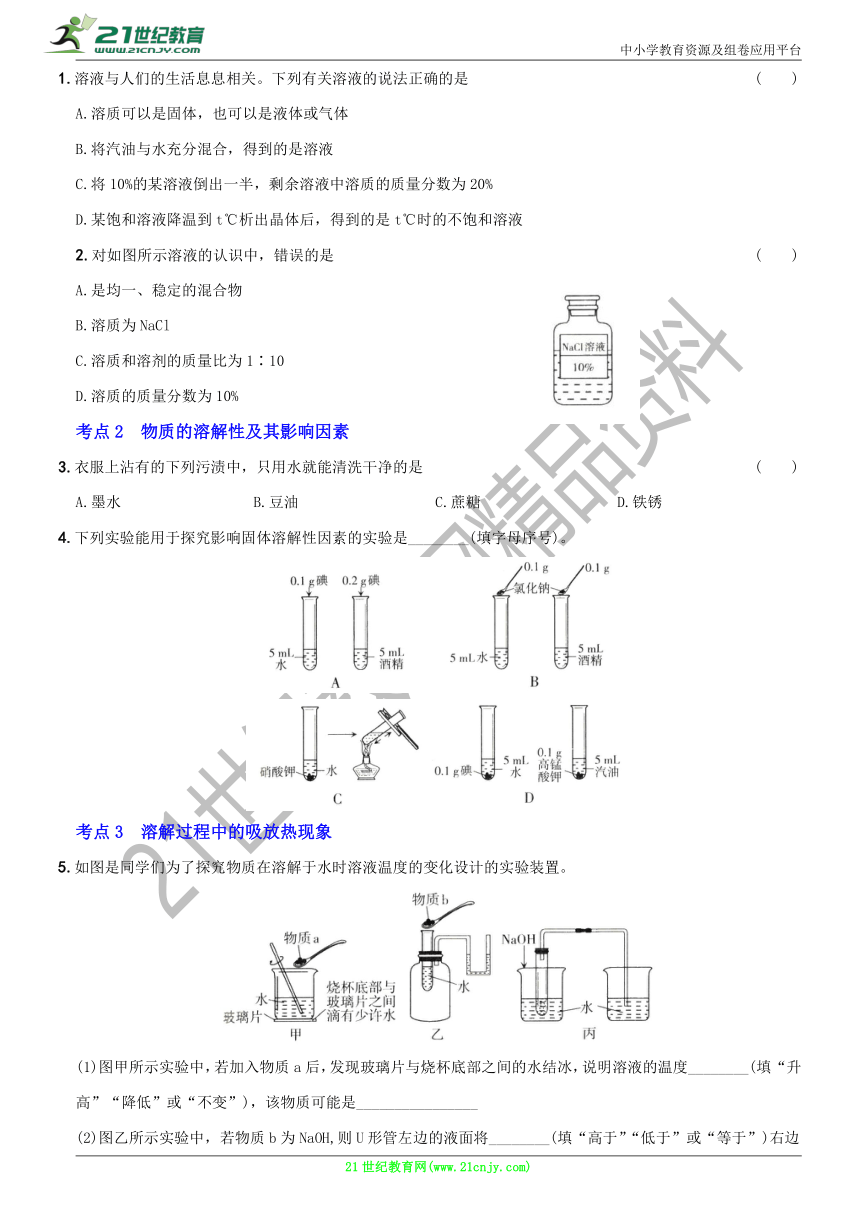
2.对如图所示溶液的认识中,错误的是 ( )
A.是均一、稳定的混合物
B.溶质为NaCl
C.溶质和溶剂的质量比为1∶10
D.溶质的质量分数为10%
考点2 物质的溶解性及其影响因素
3.衣服上沾有的下列污渍中,只用水就能清洗干净的是 ( )
A.墨水 B.豆油 C.蔗糖 D.铁锈
4.下列实验能用于探究影响固体溶解性因素的实验是________(填字母序号)。
考点3 溶解过程中的吸放热现象
5.如图是同学们为了探究物质在溶解于水时溶液温度的变化设计的实验装置。
(1)图甲所示实验中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度________(填“升高”“降低”或“不变”),该物质可能是________________
(2)图乙所示实验中,若物质b为NaOH,则U形管左边的液面将________(填“高于”“低于”或“等于”)右边的液面。
(3)图丙所示实验中,
①如果把氢氧化钠固体换成硝酸铵,产生的现象是________________________________
②如果把氢氧化钠固体换成氯化钠,产生的现象是________________________________________
③如果把氢氧化钠固体换成氧化钙,产生的现象是________________________________;与氢氧化钠溶于水的现象________(填“相同”或“不相同”),原理________(填“相同”或“不相同”),其原因为________________
________________________
考点4 乳化现象
6.写出下列过程的去污原理。
用洗涤剂洗去餐具上的油脂:____________________________________________________________
用汽油除去衣服上的油污:____________________________________________________________
用酒精除去附着在试管内壁的碘:____________________________________________________________
用热水洗去附着在烧杯底部的硝酸钾:____________________________________________________________
考点5 固体物质的溶解度
7.KCl和KNO3的溶解度如下表,下列说法错误的是 ( )
A.50℃时,100g水最多溶解85.5gKNO3
B.升高温度可以使KNO3的饱和溶液变为不饱和溶液
C.KNO3中混有少量的KCl2可用冷却热的饱和溶液的方法提纯
D.20℃时,100gKCl饱和溶液中溶质的质量为34g
8.如图是a、b、c三种固体物质的溶解度曲线,下列分析正确的是 ( )
A.50℃时,用不断搅拌的方法能增大b在水中的溶解度
B.20℃时,a、c两种物质的溶液中溶质的质量分数相等
C.50℃时,将等质量的a和b固体溶于水配制饱和溶液,得到b溶液的质量大于a溶液的质量
D.若将c物质的不饱和溶液转化为饱和溶液,可采用降低温度的方法
9.已知在20℃和60℃时,CaCl2的溶解度分别为74.5g和137g。现配制5%的CaCl2溶液,操作过程如图所示,下列说法正确的是 ( )
A.②溶液和③溶液分别为20℃和60℃时的饱和溶液 B.②至③的过程中溶质质量分数不变
C.③稀释至④的过程需加水1420g D.③中溶液的溶质质量大于④中溶液的溶质质量
考点6 气体物质的溶解度
10.可乐是我们经常饮用的一种饮料,如图所示是一种瓶装可乐外观上的部分文字。
(1)该饮料里的溶剂是________________。
(2)常温下,一瓶合格的可乐密封放置一段时间后,是否会出现浑浊现象?________(填“是”或“否”),原因是________________________________________
(3)喝了这种饮料后常常会打嗝,这种现象说明二氧化碳的溶解度与________有关。
(4)配制该饮料需要使用________(填“热水”或“凉开水”)。
考点7 配制一定溶质质量分数的溶液
11.配制50g质量分数为6%的氯化钠溶液,某同学有如图所示的部分操作,其中正确的是 ( )
12.3%的硼酸溶液是实验室常备的药品,现要配制300g质量分数为3%的硼酸溶液,操作步骤如图所示。正确的顺序是 ( )
13.小明欲配制氢氧化钠溶液。
(1)将10gNaOH固体完全溶解在40mL的水中(水的密度为1g/cm3),所配溶液中溶质的质量分数为________。
(2)配制过程中需要使用的玻璃仪器有________________________。
(3)小明在配制过程中,若量取水时仰视读数(其他操作均正确),则他所配NaOH溶液中溶质的质量分数将________(填“偏大”或“偏小”)。
(4)将该溶液蒸发一定量的水变成溶质的质量分数为40%的NaOH溶液,则需要蒸发的水的质量为________
考点8 溶质质量分数的相关计算
14.化学兴趣小组测定某硫酸铜溶液的浓度。向盛有40g硫酸铜溶液的烧杯中加入50g溶质质量分数为20.8%的氯化钡溶液,恰好完全反应。(已知硫酸铜溶液与氯化钡溶液反应的化学方程式为CuSO4+BaCl2=CuCl2+BaSO4↓,钡的相对原子质量为137)试计算:
(1)氯化钡溶液中溶质的质量为________g.
(2)硫酸铜溶液中溶质的质量分数。
《参考答案及解析》
构建知识体系
①固态 ②液态 ③气态 ④水 ⑤均一 ⑥稳定 ⑦混合物 ⑧氢氧化钙 ⑨一定温度
100g溶剂 饱和 增大 NaCl Ca(OH)2 越高 越大 大 溶质
计算、称量、量取 计算、量取
易考易错专练
1.A
[解析]气体、液体和固体都可以作溶质,故A正确;汽油难溶于水,将汽油与水充分混合,得到的是乳浊液,故B错误:将10%的某溶液倒出一半,剩余溶液中溶质的质量分数仍为10%,故C错误;饱和溶液降温析出晶体后仍是饱和溶液,故D错误。
2.C
[解析]溶液是均
一、稳定的混合物,故A正确;固体溶于液体时,固体是溶质,液体是溶剂,所以氯化钠为溶质,故B正确;由标签内容可知,此NaCl溶液中溶质的质量分数为10%,即100g该溶液中溶质和溶剂的质量比是10∶90=1∶9,故C错误,D正确。
3.C
[解析]溶于水的污渍能用水清洗干净。墨水中含有一些难溶于水的物质,豆油、铁锈也难溶于水,所以都不能只用水清洗干净.故选C
4.BC
[解析]A中溶质的质量、溶剂的种类均不同。B中溶质的种类相同,溶剂的种类不同,通过对比实验能说明影响固体溶解性的因素是溶剂的种类。中温度升高,硝酸钾溶解,能说明影响固体溶解性的因素是温度。D中溶质、溶剂的种类均不同。
5.(1)降低 硝酸铵(或NH4NO3)
(2)低于
(3)①导管内的液面会高于烧杯内的液面 ②没有明显现象 ③导管口有气泡冒出相同不相同氢氧化钠溶于水是物理变化,氧化钙与水反应是化学变化
[解析]
(1)题图甲中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度下降,该物质可能是硝酸铵(NH4NO3)。
(2)题图乙中,若物质b为氢氧化钠,氢氧化钠溶于水放热,装置内的气压升高,则形管左边的液面将低于右边的液面。
(3)①硝酸铵溶于水吸热,会使溶液的温度降低,使图丙装置中试管内的压强变小,烧杯内的水会进入导管,使导管内的液面高于烧杯内的液面。②氯化钠溶于水,溶液的温度不会发生明显的变化,图丙装置内的压强没有明显变化,故没有明显现象。③氧化钙与水发生化学反应,生成氢氧化钙,同时放出大量的热,会使溶液的温度升高,使图丙装置中试管内的压强高于大气压,使导管口有气泡冒出,这与氢氧化钠溶于水时的现象相同,但是原理不同,氢氧化钠溶于水是物理变化,氧化钙与水反应是化学变化。
6.乳化作用 溶解现象 溶解现象 溶解现象
7.D
[解析]50℃时,KNO3的溶解度为85.5g,此温度下,100g水最多溶解85.5g KNO3,A正确;KNO3的溶解度随温度的升高而增大,所以升高温度可以使KNO3的饱和溶液变为不饱和溶液,B正确;由KCl和KNO3的溶解度数据可知,KNO3的溶解度随温度的升高而明显增大,KCl的溶解度随温度升高变化不大,所以KNO3中混有少量KCl时,可用冷却热的饱和溶液的方法提纯,C正确;20℃时,KCl的溶解度为34.0g,即100g水最多溶解34.0gKCl,134gKCl饱和溶液中溶质的质量为34g,D错误。
8.C
[解析]1搅拌能够加快溶解速率,不能改变溶解度,故A错误;20℃时,a、c两种物质的溶解度相等,则20℃时,a、c两种物质的饱和溶液中溶质的质量分数相等,题中未指明饱和,故B错误;50℃时,a的溶解度大于b的溶解度,等质量的a和b固体溶于水,b所需要的水多,所以,50℃时将等质量的a和b固体溶于水配制饱和溶液,得到b溶液的质量大于a溶液的质量,故C正确;c的溶解度随温度的升高而降低,若将c物质的不饱和溶液转化为饱和溶液,可采用升高温度的方法,故D错误。
9.C
[解析]120℃和60℃时,氯化钙的溶解度分别为74.5g和137g,②溶液温度为20℃,而20℃时100g水中最多溶解氯化钙74.5g,故②溶液为饱和溶液;③溶液温度为60℃,而60℃时100g水中最多溶解氯化钙137g,故③溶液为不饱和溶液。A错误。②至③的过程中,温度升高,氯化钙的溶解度增大,②中未溶解的固体继续溶解,溶质增多,溶质的质量分数增大,故错误。根据溶液稀释前后溶质的质量不变,设③稀释至④的过程中需加水的质量为x,可得80g=(180g+x)×5%,解得x=1420g,故C正确,D错误。
10.(1)水
(2)否 溶液具有稳定性
(3)温度
(4)凉开水
[解析]
(2)溶液具有稳定性,所以常温下一瓶合格的可乐密封放置一段时间后,不会出现浑浊现象。
(3)喝了这种饮料后常常会打嗝,这是因为温度升高,气体的溶解度减小,说明二氧化碳的溶解度与温度有关。
(4)凉开水温度较低,二氧化碳的溶解度随温度的降低而增大,所以配制该饮料需要使用凉开水。
11.A
[解析]向量筒中倾倒液体药品时,瓶塞要倒放,标签向着手心,瓶口紧挨量筒口,图A所示操作正确。使用胶头滴管滴加少量液体时,胶头滴管不能伸入量筒内或接触量筒内壁,应垂直悬空于量筒口正上方,防止污染胶头滴管或试剂,图所示操作错误。读数时,视线应与量筒内液体凹液面的最低处保持水平,图所示操作错误。配制氯化钠溶液时,溶解操作应在烧杯中进行,先加氯化钠,再加水,量筒是量度液体体积的容器,不能在量筒中进行溶解、稀释操作,图D所示操作错误。
12.C
[解析]配制300g质量分数为3%的硼酸溶液,首先计算配制溶液所需硼酸和水的质量,再称量所需的硼酸和量取水,最后进行溶解,故正确的操作顺序是⑤③①④②。
13.(1)20%
(2)烧杯、玻璃棒、量筒、胶头滴管
(3)偏小
(4)25g
[解析]
(1)将10gNaOH固体完全溶解在40mL水中,水的质量是40mL×1g/mL=40g,所配溶液中溶质的质量分数为×100%=20%。
(3)在配制过程中,若量取水时仰视读数,则所取的水的体积偏大,所配氢氧化钠溶液中溶质的质量分数将偏小。
(4)根据溶液稀释前后溶质质量不变,设需要蒸发水的质量为x,则10g=(50g-x)×40%,解得x=25g,即需要蒸发水的质量为25g。
14.(1)10.4
(2)解:设硫酸铜溶液中溶质的质量为x。
CuSO4+BaCl2=BaSO4↓+CuCl2
160 208
x 10.4g
= x=8g
此硫酸铜溶液中溶质的质量分数为×100%=20%
答:此硫酸铜溶液中溶质的质量分数为20%。
[解析]
(1)氯化钡溶液中溶质的质量为50g×20.8%=10.4g。
21世纪教育网(www.21cnjy.com)
第九单元 溶液
阶段知识整合与训练
易考易错专练
考点1 溶液的组成、特点及判断
1.溶液与人们的生活息息相关。下列有关溶液的说法正确的是 ( )
A.溶质可以是固体,也可以是液体或气体
B.将汽油与水充分混合,得到的是溶液
C.将10%的某溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.某饱和溶液降温到t℃析出晶体后,得到的是t℃时的不饱和溶液
2.对如图所示溶液的认识中,错误的是 ( )
A.是均一、稳定的混合物
B.溶质为NaCl
C.溶质和溶剂的质量比为1∶10
D.溶质的质量分数为10%
考点2 物质的溶解性及其影响因素
3.衣服上沾有的下列污渍中,只用水就能清洗干净的是 ( )
A.墨水 B.豆油 C.蔗糖 D.铁锈
4.下列实验能用于探究影响固体溶解性因素的实验是________(填字母序号)。
考点3 溶解过程中的吸放热现象
5.如图是同学们为了探究物质在溶解于水时溶液温度的变化设计的实验装置。
(1)图甲所示实验中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度________(填“升高”“降低”或“不变”),该物质可能是________________
(2)图乙所示实验中,若物质b为NaOH,则U形管左边的液面将________(填“高于”“低于”或“等于”)右边的液面。
(3)图丙所示实验中,
①如果把氢氧化钠固体换成硝酸铵,产生的现象是________________________________
②如果把氢氧化钠固体换成氯化钠,产生的现象是________________________________________
③如果把氢氧化钠固体换成氧化钙,产生的现象是________________________________;与氢氧化钠溶于水的现象________(填“相同”或“不相同”),原理________(填“相同”或“不相同”),其原因为________________
________________________
考点4 乳化现象
6.写出下列过程的去污原理。
用洗涤剂洗去餐具上的油脂:____________________________________________________________
用汽油除去衣服上的油污:____________________________________________________________
用酒精除去附着在试管内壁的碘:____________________________________________________________
用热水洗去附着在烧杯底部的硝酸钾:____________________________________________________________
考点5 固体物质的溶解度
7.KCl和KNO3的溶解度如下表,下列说法错误的是 ( )
A.50℃时,100g水最多溶解85.5gKNO3
B.升高温度可以使KNO3的饱和溶液变为不饱和溶液
C.KNO3中混有少量的KCl2可用冷却热的饱和溶液的方法提纯
D.20℃时,100gKCl饱和溶液中溶质的质量为34g
8.如图是a、b、c三种固体物质的溶解度曲线,下列分析正确的是 ( )
A.50℃时,用不断搅拌的方法能增大b在水中的溶解度
B.20℃时,a、c两种物质的溶液中溶质的质量分数相等
C.50℃时,将等质量的a和b固体溶于水配制饱和溶液,得到b溶液的质量大于a溶液的质量
D.若将c物质的不饱和溶液转化为饱和溶液,可采用降低温度的方法
9.已知在20℃和60℃时,CaCl2的溶解度分别为74.5g和137g。现配制5%的CaCl2溶液,操作过程如图所示,下列说法正确的是 ( )
A.②溶液和③溶液分别为20℃和60℃时的饱和溶液 B.②至③的过程中溶质质量分数不变
C.③稀释至④的过程需加水1420g D.③中溶液的溶质质量大于④中溶液的溶质质量
考点6 气体物质的溶解度
10.可乐是我们经常饮用的一种饮料,如图所示是一种瓶装可乐外观上的部分文字。
(1)该饮料里的溶剂是________________。
(2)常温下,一瓶合格的可乐密封放置一段时间后,是否会出现浑浊现象?________(填“是”或“否”),原因是________________________________________
(3)喝了这种饮料后常常会打嗝,这种现象说明二氧化碳的溶解度与________有关。
(4)配制该饮料需要使用________(填“热水”或“凉开水”)。
考点7 配制一定溶质质量分数的溶液
11.配制50g质量分数为6%的氯化钠溶液,某同学有如图所示的部分操作,其中正确的是 ( )
12.3%的硼酸溶液是实验室常备的药品,现要配制300g质量分数为3%的硼酸溶液,操作步骤如图所示。正确的顺序是 ( )
13.小明欲配制氢氧化钠溶液。
(1)将10gNaOH固体完全溶解在40mL的水中(水的密度为1g/cm3),所配溶液中溶质的质量分数为________。
(2)配制过程中需要使用的玻璃仪器有________________________。
(3)小明在配制过程中,若量取水时仰视读数(其他操作均正确),则他所配NaOH溶液中溶质的质量分数将________(填“偏大”或“偏小”)。
(4)将该溶液蒸发一定量的水变成溶质的质量分数为40%的NaOH溶液,则需要蒸发的水的质量为________
考点8 溶质质量分数的相关计算
14.化学兴趣小组测定某硫酸铜溶液的浓度。向盛有40g硫酸铜溶液的烧杯中加入50g溶质质量分数为20.8%的氯化钡溶液,恰好完全反应。(已知硫酸铜溶液与氯化钡溶液反应的化学方程式为CuSO4+BaCl2=CuCl2+BaSO4↓,钡的相对原子质量为137)试计算:
(1)氯化钡溶液中溶质的质量为________g.
(2)硫酸铜溶液中溶质的质量分数。
《参考答案及解析》
构建知识体系
①固态 ②液态 ③气态 ④水 ⑤均一 ⑥稳定 ⑦混合物 ⑧氢氧化钙 ⑨一定温度
100g溶剂 饱和 增大 NaCl Ca(OH)2 越高 越大 大 溶质
计算、称量、量取 计算、量取
易考易错专练
1.A
[解析]气体、液体和固体都可以作溶质,故A正确;汽油难溶于水,将汽油与水充分混合,得到的是乳浊液,故B错误:将10%的某溶液倒出一半,剩余溶液中溶质的质量分数仍为10%,故C错误;饱和溶液降温析出晶体后仍是饱和溶液,故D错误。
2.C
[解析]溶液是均
一、稳定的混合物,故A正确;固体溶于液体时,固体是溶质,液体是溶剂,所以氯化钠为溶质,故B正确;由标签内容可知,此NaCl溶液中溶质的质量分数为10%,即100g该溶液中溶质和溶剂的质量比是10∶90=1∶9,故C错误,D正确。
3.C
[解析]溶于水的污渍能用水清洗干净。墨水中含有一些难溶于水的物质,豆油、铁锈也难溶于水,所以都不能只用水清洗干净.故选C
4.BC
[解析]A中溶质的质量、溶剂的种类均不同。B中溶质的种类相同,溶剂的种类不同,通过对比实验能说明影响固体溶解性的因素是溶剂的种类。中温度升高,硝酸钾溶解,能说明影响固体溶解性的因素是温度。D中溶质、溶剂的种类均不同。
5.(1)降低 硝酸铵(或NH4NO3)
(2)低于
(3)①导管内的液面会高于烧杯内的液面 ②没有明显现象 ③导管口有气泡冒出相同不相同氢氧化钠溶于水是物理变化,氧化钙与水反应是化学变化
[解析]
(1)题图甲中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度下降,该物质可能是硝酸铵(NH4NO3)。
(2)题图乙中,若物质b为氢氧化钠,氢氧化钠溶于水放热,装置内的气压升高,则形管左边的液面将低于右边的液面。
(3)①硝酸铵溶于水吸热,会使溶液的温度降低,使图丙装置中试管内的压强变小,烧杯内的水会进入导管,使导管内的液面高于烧杯内的液面。②氯化钠溶于水,溶液的温度不会发生明显的变化,图丙装置内的压强没有明显变化,故没有明显现象。③氧化钙与水发生化学反应,生成氢氧化钙,同时放出大量的热,会使溶液的温度升高,使图丙装置中试管内的压强高于大气压,使导管口有气泡冒出,这与氢氧化钠溶于水时的现象相同,但是原理不同,氢氧化钠溶于水是物理变化,氧化钙与水反应是化学变化。
6.乳化作用 溶解现象 溶解现象 溶解现象
7.D
[解析]50℃时,KNO3的溶解度为85.5g,此温度下,100g水最多溶解85.5g KNO3,A正确;KNO3的溶解度随温度的升高而增大,所以升高温度可以使KNO3的饱和溶液变为不饱和溶液,B正确;由KCl和KNO3的溶解度数据可知,KNO3的溶解度随温度的升高而明显增大,KCl的溶解度随温度升高变化不大,所以KNO3中混有少量KCl时,可用冷却热的饱和溶液的方法提纯,C正确;20℃时,KCl的溶解度为34.0g,即100g水最多溶解34.0gKCl,134gKCl饱和溶液中溶质的质量为34g,D错误。
8.C
[解析]1搅拌能够加快溶解速率,不能改变溶解度,故A错误;20℃时,a、c两种物质的溶解度相等,则20℃时,a、c两种物质的饱和溶液中溶质的质量分数相等,题中未指明饱和,故B错误;50℃时,a的溶解度大于b的溶解度,等质量的a和b固体溶于水,b所需要的水多,所以,50℃时将等质量的a和b固体溶于水配制饱和溶液,得到b溶液的质量大于a溶液的质量,故C正确;c的溶解度随温度的升高而降低,若将c物质的不饱和溶液转化为饱和溶液,可采用升高温度的方法,故D错误。
9.C
[解析]120℃和60℃时,氯化钙的溶解度分别为74.5g和137g,②溶液温度为20℃,而20℃时100g水中最多溶解氯化钙74.5g,故②溶液为饱和溶液;③溶液温度为60℃,而60℃时100g水中最多溶解氯化钙137g,故③溶液为不饱和溶液。A错误。②至③的过程中,温度升高,氯化钙的溶解度增大,②中未溶解的固体继续溶解,溶质增多,溶质的质量分数增大,故错误。根据溶液稀释前后溶质的质量不变,设③稀释至④的过程中需加水的质量为x,可得80g=(180g+x)×5%,解得x=1420g,故C正确,D错误。
10.(1)水
(2)否 溶液具有稳定性
(3)温度
(4)凉开水
[解析]
(2)溶液具有稳定性,所以常温下一瓶合格的可乐密封放置一段时间后,不会出现浑浊现象。
(3)喝了这种饮料后常常会打嗝,这是因为温度升高,气体的溶解度减小,说明二氧化碳的溶解度与温度有关。
(4)凉开水温度较低,二氧化碳的溶解度随温度的降低而增大,所以配制该饮料需要使用凉开水。
11.A
[解析]向量筒中倾倒液体药品时,瓶塞要倒放,标签向着手心,瓶口紧挨量筒口,图A所示操作正确。使用胶头滴管滴加少量液体时,胶头滴管不能伸入量筒内或接触量筒内壁,应垂直悬空于量筒口正上方,防止污染胶头滴管或试剂,图所示操作错误。读数时,视线应与量筒内液体凹液面的最低处保持水平,图所示操作错误。配制氯化钠溶液时,溶解操作应在烧杯中进行,先加氯化钠,再加水,量筒是量度液体体积的容器,不能在量筒中进行溶解、稀释操作,图D所示操作错误。
12.C
[解析]配制300g质量分数为3%的硼酸溶液,首先计算配制溶液所需硼酸和水的质量,再称量所需的硼酸和量取水,最后进行溶解,故正确的操作顺序是⑤③①④②。
13.(1)20%
(2)烧杯、玻璃棒、量筒、胶头滴管
(3)偏小
(4)25g
[解析]
(1)将10gNaOH固体完全溶解在40mL水中,水的质量是40mL×1g/mL=40g,所配溶液中溶质的质量分数为×100%=20%。
(3)在配制过程中,若量取水时仰视读数,则所取的水的体积偏大,所配氢氧化钠溶液中溶质的质量分数将偏小。
(4)根据溶液稀释前后溶质质量不变,设需要蒸发水的质量为x,则10g=(50g-x)×40%,解得x=25g,即需要蒸发水的质量为25g。
14.(1)10.4
(2)解:设硫酸铜溶液中溶质的质量为x。
CuSO4+BaCl2=BaSO4↓+CuCl2
160 208
x 10.4g
= x=8g
此硫酸铜溶液中溶质的质量分数为×100%=20%
答:此硫酸铜溶液中溶质的质量分数为20%。
[解析]
(1)氯化钡溶液中溶质的质量为50g×20.8%=10.4g。
21世纪教育网(www.21cnjy.com)
同课章节目录
