2013化学复习知识点深度剖析教案: 实验过关专题六 物质结构(人教版)
文档属性
| 名称 | 2013化学复习知识点深度剖析教案: 实验过关专题六 物质结构(人教版) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-11-27 00:00:00 | ||
图片预览




文档简介
2013化学复习知识点深度剖析教案: 实验过关专题六 物质结构(人教版)
第一类 验证型实验大题过关
【典例解析】
1.向某晶体的水溶液中加入Fe2+的溶液后,无明显变化,当滴入几滴溴水后,混合液中出现血红色,那么由此得出下列结论错误的是( )
A.该晶体中一定含有SCN-
B.Fe3+的氧化性比Br2的氧化性强
C.Fe2+不能与SCN-形成血红色的化合物
D.Fe2+被Br2氧化成Fe3+
【高考真题解析】
1.(2011安徽高考) 中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是( )
A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大
B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7
C.根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性
D.根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO
2.(2011四川高考)甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和。甲、乙组成的成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L也能与Z的水溶液反应生成盐;丙、戊可组成化合物M。
请回答下列问题
(1)戊离子的结构示意图为_______。
(2)写出乙的单质的电子式:_______。
(3)戊的单质与X反应生成的Y和Z的物质的量之比为2 :4,反应中被氧化的物质与被还原的物质的物质的量之比为________。
(4)写出将少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:
_________________________。
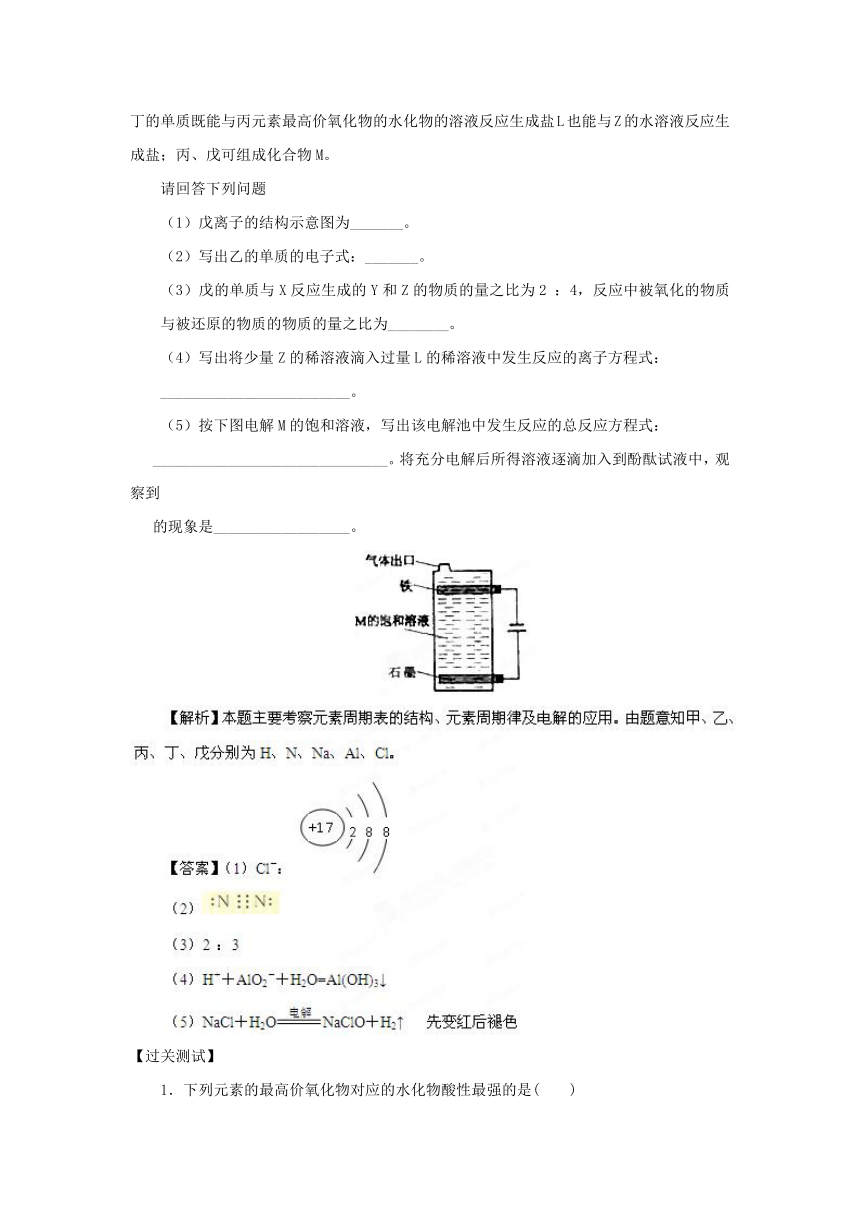
按下图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:
_______________________________。将充分电解后所得溶液逐滴加入到酚酞试液中,观察到
的现象是__________________。
【过关测试】
1.下列元素的最高价氧化物对应的水化物酸性最强的是( )
A.原子的L电子层p轨道只填了两个电子的元素
B.外围电子排布式为3s23p2的元素
C.第三周期有7个价电子的元素
D.3p轨道电子半充满的元素
【解析】 A项元素为C,B项元素为Si,C项元素为Cl,D项元素为P。最高价氧化物对应水化物的酸性:HClO4>H3PO4>H2CO3>H2SiO3。
【答案】 C
2.为了证明(NH4)2Fe(SO4)2?6H2O(硫酸亚铁铵晶体)的成分中含有NH、Fe2+、SO和 H2O,下列实验叙述中不正确的是( )
A.取少量硫酸亚铁铵晶体放入试管,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水
B.硫酸亚铁铵晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+
C.硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO
D.取少量硫酸亚铁铵晶体放入试管中,加入浓NaOH溶液,加热,试管口湿润的蓝色石蕊试纸变红,则可证明晶体的成分中含有NH
【解析】 D项中检验NH时,加入浓NaOH溶液,加热,能产生NH3,NH3可使试管口湿润的红色石蕊试纸变蓝色,因为氨气遇水能生成显碱性的NH3·H2O。故D不正确。
【答案】 D
3.(2012九江市第一次统考)对实验I~Ⅳ的实验现象预测正确的是( )
A.实验I:液体分层,下层呈无色
B.实验Ⅱ:烧杯中先出现白色沉淀,后溶解
C.实验Ⅲ:试管中立刻出现红色沉淀
D.实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
【解析】实验I的四氯化碳密度比水大,下层为紫红色,A项不正确;实验ⅡNH3溶于水形成的一水合氨不能使氢氧化铝沉淀溶解,B项不正确;实验Ⅲ溶液变红色,而不是生成沉淀,C项不正确。
【答案】D
4.写出下列反应的离子方程式:
(1)在氯化锌溶液中加入过量的氨水____________________________________;
(2)在硫酸铜溶液中加入过量的浓氨水____________________________;
(3)氯化银溶于浓氨水_____________________________________________________;
(4)在FeCl3溶液中加入过量的氨水
________________________________________________________________________。
5.(2012年济宁期末)A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次
增大。已知:A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,D与E同主族,E元素原子的最外层电子数比次外层电子数少2。请回答:
(1)元素C在周期表中的位置是 。
(2)元素D的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物与水反应的离子方程式: 。
(3)D和E两种元素相比较,其原子得电子能力较强的是 (写名称)。
以下说法中,可以证明上述结论的是 (填写编号)。
a. 比较这两种元素的常见单质的沸点
b.二者形成的化合物中,D元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氢化物的水溶液的酸性
(4)元素A、D、E与钠元素可形成两种酸式盐(均含有该四种元素),这两种酸式盐
在水溶液中反应的离子方程式是: 。
由元素A、B、D组成的一元酸X为日常生活中的调味剂,元素A、F组成的化合物为Y。
在等体积、等pH的X、Y的溶液中分别加入等质量的锌粉,反应后若最后仅有一份溶液中存在
锌粉,则反应过程中两溶液中反应速率的大小关系是:X Y(填“>”、“<”或“=”)。
(6)元素F的单质常温下是一种气体,工业上主要是通过电解其钠盐的饱和溶液的方法获得该气体,假定装入的饱和溶液为100mL(电解前后溶液体积变化可忽略),当测得阴极上产生11.2mL(标准状况)气体时停止通电,将溶液摇匀,此时溶液的pH为 。
氧 bc
(5)> (6)12
第二类 定量型实验大题过关
【典例解析】
1.金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以HCN、CN-和金属离子的配离子的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和EDTA,在pH<2的条件下加热蒸馏,蒸出所有的HCN,并用NaOH溶液吸收;
②滴定:将吸收液调节至pH>11,以试银灵作指示剂,用AgNO3标准溶液滴定终点时,溶液由黄色变成橙红色。Ag++2CN-===[Ag(CN)2]-。
根据以上知识回答下列问题:
(1)水样预处理的目的是
________________________________________________________________________。
(2)水样预处理的装置如图,细导管插入吸收液中是为了
________________________________________________________________________。
(3)蒸馏瓶比吸收液面要高出很多,其目的是
________________________________________________________________________。
(4)如果用盐酸代替磷酸进行预处理,实验结果将________(填“偏高”、“无影响”或“偏低”)。
(5)准确移取某工厂污水100 mL,经处理后用浓度为0.01000 mol·L-1的硝酸银标准溶液滴定,终点时消耗了21.00 mL。此水样中含氰化合物的含量为________mg·L-1(以CN-计,计算结果保留一位小数)。
【高考真题解析】
1.(2011安徽高考)科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2) 3的说法正确的是( )
A.分子中N、O间形成的共价键是非极性键
B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性
D.15.2g该物质含有6.02×1022个原子
2.(2011安徽高考)W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
(1)X位于元素周期表中第 周期第 族;W的基态原子核外有
个未成对电子。
(2)X的单质和Y的单质相比,熔点较高的是 (写化学式);Z的气态氢化物和溴化氢相比,较稳定的是 (写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是 。
(4)在25oC、101 kPa下,已知Y的气态氢化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是 。
3.(2011山东高考) 氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为 个。
(2)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为 。
(3) H+可与H2O形成H3O+,H3O+中O原子采用 杂化。H3O+中H-O-H的键角比H2O中H-O-H的键角大,原因是 。
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为ag·cm-3,表示阿伏加德罗常数,则CaO晶胞体积为 cm3。
因此该晶胞中含有的氯离子个数为8×1/8+6×1/3=4,同样也可以计算出钠离子个数为4。由于CaO与NaCl的晶胞同为面心立方结构,所以CaO晶胞中也含有4个钙离子和4个氧离子,因此CaO晶胞体积为。
【答案】(1)2
(2)O-H键、氢键、范德华力 邻羟基苯甲醛形成分子内氢键,而对羟基苯甲醛形成分子间氢键,分子间氢键是分子间作用力增大
(3)sp3 H2O中O原子有2对孤对电子,H3O+只有1对孤对电子,排斥力较小
(4)
【过关测试】
1.(2012年南昌市调研)A、B、C、D、E是原子序数依次递增的五种短周期元素,已知:
①B原子核外电子总数与最外层电子数之比为4:3
②D原子最外层电子数与次外层电子数之比为3:4
③E?,C+,A+的离子半径逐渐减小
④A单质在E单质中燃烧火焰呈苍白色
请回答下列问题:
(1)E的最高价氧化物对应水化物的化学式为:___________。它的酸性比D的最高价氧化物对应水化物的酸性:____________。(填“强”或“弱”)
(2)X、Y是由上述元素中任意3种组成的强电解质,且构成的原子个数比均为1:1:1。已知X溶液中水电离出来的C(H+)=10-12mol/L,则X的电子式为:_____________;Y的水溶液酸碱性与X相同,则其原因是(写离子方程式):_______________________________;
(3)B与C构成原子个数比为1:1的化合物与H2O反应的化学方程式为:
_________________________________________________________;
(4)A与B,A与D均可形成18个电子的分子,这两种分子在水溶液中反应生成物之一是含10电子的化合物;该反应可观察到现象是:____________________________________,原因是(用化学方程式表示)_______________________________________________。
2.印刷电路的废腐蚀液中含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5 mol/L,含FeCl2 3.0 mol/L,含FeCl3 1.0 mol/L,含HCl 3.0 mol/L.取废腐蚀液200 mL按如下流程在实验室进行实验:
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂所需试剂是________(填化学式)。
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物。反应的化学方程式为__________________________________________。
(3)下图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置。
从下图挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管,固定装置不用画),并标明容器中所装试剂。
(4)实验中,必须控制生成氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收。控制生成氯气速度的操作是: _____________________________。
(5)按上述流程操作,需称取Fe粉的质量应不少于_________ g(精确到0.1 g),需通入Cl2的物质的量不少于________ mol,加入烧瓶中的KClO3的质量应不少于________ g(精确到0.1 g)。
【解析】本题是一道定性分析和定量分析相结合的综合实验题,明确反应原理是解题的关键。(1)由于是加入的过量的铁,所以得到的铜中含有铁粉,可以用酸溶解铁反应掉。
(2)根据题意,KClO3中Cl的化合价从+5价降低到0价,HCl中Cl的化合价从-13.(2012阳泉一模)W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第________周期第________族。W的气态氢化物稳定性比H2O(g)____
(填“强”或“弱”)。
Y的基态原子核外电子排布式是________________________________________________,
Y的第一电离能比X的________(填“大”或“小”)。
Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式:
_______________________________________________________________________。
(4)已知下列数据:
Fe(s)+O2(g)===FeO(s) ΔH=-272.0 kJ·mol-1
2X(s)+O2(g)===X2O3(s) ΔH=-1675.7 kJ·mol-1
X的单质和FeO反应的热化学方程式:
________________________________________________________________________。
4.(2011重庆)用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。
(1)Al的原子结构示意图为_____________________;Al与NaOH溶液反应的离子方程式:
________________________________________________。
(2)30Si的原子的中子数为_________;SiO2晶体类型为__________________。
(3)Al3+与Yn-的电子数相同,Y所在族的各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是________。
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是__________。
(5)经处理后的熔渣36.0g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0g固体;滤液中加入过量NaOH溶液,分离得到21.4g固体;则此熔渣中Al2O3的质量分数为__________________。
【解析】本题考察原子的结构、晶体类型、方程式的书写以及有关计算。
Al在周期表中位于第三周期第ⅢA族,其原子结构示意图为;单质铝既能与酸反应产生氢气,又能与强碱反应产生氢气,与NaOH溶液反应的离子方程式:
2Al+2OH-+2H2O=2AlO2-+3H2↑。
第三类 探究型实验大题过关
【典例解析】
1.(1)下列说法正确的是________(选填序号)。
A.在进行物质检验时,一般先对试样进行外观观察,确定其状态、颜色、气味等
B.配制银氨溶液时,应把硝酸银溶液逐滴加入氨水中
C.一般在实验室点燃可燃性气体时,必须先要检验纯度
D.测定硫酸铜晶体结晶水的质量分数时,若用潮湿的坩埚会使测定结果偏小
E.酸碱中和滴定实验中根据碱式滴定管的两次读数得出NaOH溶液体积为22.0 mL
F.实验室制取氯气等有毒气体时,必须在密闭体系或通风橱中进行
(2)补铁剂中铁元素的含量是质检部门衡量其质量的重要指标,实验主要包括如下步骤:
a.配制0.01 mol/L到0.008 mol/L等一系列浓度的[Fe(SCN)6]3-(红色)溶液作为标准比色液。
b.样品处理:
c.准确量取一定体积的待测液于比色管中,加入稍过量的KSCN溶液,并稀释到10 mL。
d.比色:选取与待测液颜色一致或相近的标准比色液即可判断待测液的浓度。
试回答下列问题:
①配制100 mL 0.01mol/L标准溶液,需要的玻璃仪器有:烧杯、玻璃棒、量筒,还需要:________、________。
②步骤b脱色过程包括加入:________(填:脱有机色素的吸附剂名称)→搅拌→煮沸→冷却→________(填操作)。
③步骤b样品处理中,氧化的目的是________。
【高考真题解析】
12.(2011海南)
I(6分)下列分子中,属于非极性的是
A.SO2 B.BeCl2 C.BBr3 D.COCl2
解析:根据价层电子对互斥理论(VSEPR)可得四种分子的结构如下:
答案:BC
II(14分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为___________;
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是_______;
(3)SO42-的立体构型是________,其中S原子的杂化轨道类型是_______;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为______;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为__________。
【过关测试】
1.有关溶液中所含离子的检验,下列判断正确的是( )
A.加入硝酸酸化,再滴加KSCN溶液后有血红色物质生成,则原溶液中一定有Fe3+存在
B.加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO存在
C.用某溶液做焰色反应实验时火焰为黄色,则该溶液中一定有钠元素,可能有钾元素
D.分别含有Mg2+、Cu2+、Fe2+和Na+的四种盐酸盐溶液,只用NaOH溶液是不能一次鉴别开的
2.(2012年浙江省宁波市八校高三学期初测试)下列实验设计能完成或实验结论合理的是( )
A.证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾一淀粉试纸检验,观察试纸颜色的变化
B.铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,该铝热剂不含氧化铁
C.测氯水的pH可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较
D.用新制氢氧化铜悬浊液可以鉴别甲酸、甲酸甲酯、乙酸、乙酸乙酯四种物质
3.锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)]。
回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式
________________________________________________________________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是________。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式
________________________________________________________________________。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备Zn(OH)2的原因
________________________________________________________________________。
4.(2012潮州模拟)下表为元素周期表的一部分。请回答下列问题:
(1)上述元素中,属于s区的是____________(填元素符号)。
(2)写出元素⑩的基态原子的电子排布式____________________。
(3)元素第一电离能为⑤________⑨(填“大于”或“小于”)。
(4)元素③气态氢化物的中心原子有________对弧对电子,其VSEPR模型为________;中心原子的杂化类型为________;该分子为________分子(填“极性”或“非极性”)。向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为_______________________________________________。
(5)元素⑦的钠盐晶胞结构如图所示,每个Na+周围与之距离最近的Na+的个数为________。
第四类 设计型实验大题过关
【典例解析】
1.某同学设计了如下所示的方法,鉴定盐A的组成成分。下列结论中正确的是( )
(血红色溶液)
(浅黄色沉淀)
A.A中一定有Fe3+
B.C中一定有Fe3+
C.B为AgI沉淀
D.A一定为FeBr2溶液
【解析】KSCN溶液是检验Fe3+的特效试剂,加入KSCN溶液出现血红色,表明C中一定含Fe3+,故B正确,但A中不一定有Fe3+,有可能含Fe2+,当Fe2+遇硝酸酸化时,会被氧化生成Fe3+:3Fe2++NO+4H+===3Fe3++NO↑+2H2O,故A、D错误;又因为AgI是黄色沉淀,而B为浅黄色沉淀,C错误。
【答案】B
【高考真题解析】
1.(2011天津高考)以下有关原子结构及元素周期律的叙述正确的是( )
A.第IA族元素铯的两种同位素137Cs比133Cs多4个质子
B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小
C.第 ⅦA元素从上到下,其氢化物的稳定性逐渐增强
D.同主族元素从上到下,单质的熔点逐渐降低
2.(2011新课标全国)短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是( )
A.元素W、X的氯化物中,各原子均满足8电子的稳定结构
B.元素X与氢形成的原子比为1:1的化合物有很多种
C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D.元素Z可与元素X形成共价化合物XZ2
化钠溶液或盐酸反应均有氢气生成,C正确;C和S均属于非金属元素,二者可以形成共价化合物CS2,D正确。
【答案】A
【过关测试】
1.某氯碱厂利用废铁皮制取净水剂FeCl3溶液,最合理的生产途径是( )
A. Cl2FeCl3FeCl3溶液
B.Cl2HCl盐酸FeCl2溶液FeCl3溶液
C.Cl2HCl盐酸FeCl2溶液FeCl3溶液
D.―→FeCl3溶液
2.(2012年合肥市第一次质量检测)磷有三种同素异形体,分别为白磷(P4)、红磷和黑磷。
(1)白磷常温下为白色或淡黄色固体,在40℃左右自燃,实验室保存少量白磷的方法是 。
(2)白磷黑磷,黑磷比白磷稳定,结构与石墨相似,下列叙述正确的是
(填选项字母)
A.黑磷与白磷互为同分异构体 B.黑磷能导电
C.白磷转化为黑磷为氧化还原反应 D.白磷转化为黑磷为放热反应
(3)红磷在氯气中燃烧生成两种氯化物,其中一种氯化物分子是每个原子最外层都满足8个电子的结构,则该氯化物的空间构型与下列 分子最相似。(填选项字母)
A.H2O B.CCl4 C.NH3 D.CS2
(4)已知白磷、红磷燃烧的热化学方程式分别为
P4(s、白磷)+5O2(g)=P4O10(s);△H=-986KJ·mol-1
P(s、红磷)+O2(g)=P4O10(s);△H=-739KJ·mol-1
写出红磷转化为白磷的热化学方程式 。
3.(2012安庆统测) C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Ge的原子核外电子排布式为______________________。
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是________。
(3)按要求指出下列氧化物的空间构型、成键方式或性质:
①CO2分子的空间构型及碳氧之间的成键方式________________;
②SiO2晶体的空间构型及硅氧之间的成键方式_______________________________________
______________________________________________________________________________;
③已知SnO2是离子晶体,写出其主要物理性质_____________________________________
_________________________________________________________________(写出2条即可)。
(4)CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为________。
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060 cm-1,CO分子中碳氧键的伸缩振动频率为2143 cm-1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度________(填字母)。
A.强 B.弱
C.相等 D.无法判断
第一类 验证型实验大题过关
【典例解析】
1.向某晶体的水溶液中加入Fe2+的溶液后,无明显变化,当滴入几滴溴水后,混合液中出现血红色,那么由此得出下列结论错误的是( )
A.该晶体中一定含有SCN-
B.Fe3+的氧化性比Br2的氧化性强
C.Fe2+不能与SCN-形成血红色的化合物
D.Fe2+被Br2氧化成Fe3+
【高考真题解析】
1.(2011安徽高考) 中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是( )
A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大
B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7
C.根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性
D.根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO
2.(2011四川高考)甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和。甲、乙组成的成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L也能与Z的水溶液反应生成盐;丙、戊可组成化合物M。
请回答下列问题
(1)戊离子的结构示意图为_______。
(2)写出乙的单质的电子式:_______。
(3)戊的单质与X反应生成的Y和Z的物质的量之比为2 :4,反应中被氧化的物质与被还原的物质的物质的量之比为________。
(4)写出将少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:
_________________________。
按下图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:
_______________________________。将充分电解后所得溶液逐滴加入到酚酞试液中,观察到
的现象是__________________。
【过关测试】
1.下列元素的最高价氧化物对应的水化物酸性最强的是( )
A.原子的L电子层p轨道只填了两个电子的元素
B.外围电子排布式为3s23p2的元素
C.第三周期有7个价电子的元素
D.3p轨道电子半充满的元素
【解析】 A项元素为C,B项元素为Si,C项元素为Cl,D项元素为P。最高价氧化物对应水化物的酸性:HClO4>H3PO4>H2CO3>H2SiO3。
【答案】 C
2.为了证明(NH4)2Fe(SO4)2?6H2O(硫酸亚铁铵晶体)的成分中含有NH、Fe2+、SO和 H2O,下列实验叙述中不正确的是( )
A.取少量硫酸亚铁铵晶体放入试管,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水
B.硫酸亚铁铵晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+
C.硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO
D.取少量硫酸亚铁铵晶体放入试管中,加入浓NaOH溶液,加热,试管口湿润的蓝色石蕊试纸变红,则可证明晶体的成分中含有NH
【解析】 D项中检验NH时,加入浓NaOH溶液,加热,能产生NH3,NH3可使试管口湿润的红色石蕊试纸变蓝色,因为氨气遇水能生成显碱性的NH3·H2O。故D不正确。
【答案】 D
3.(2012九江市第一次统考)对实验I~Ⅳ的实验现象预测正确的是( )
A.实验I:液体分层,下层呈无色
B.实验Ⅱ:烧杯中先出现白色沉淀,后溶解
C.实验Ⅲ:试管中立刻出现红色沉淀
D.实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
【解析】实验I的四氯化碳密度比水大,下层为紫红色,A项不正确;实验ⅡNH3溶于水形成的一水合氨不能使氢氧化铝沉淀溶解,B项不正确;实验Ⅲ溶液变红色,而不是生成沉淀,C项不正确。
【答案】D
4.写出下列反应的离子方程式:
(1)在氯化锌溶液中加入过量的氨水____________________________________;
(2)在硫酸铜溶液中加入过量的浓氨水____________________________;
(3)氯化银溶于浓氨水_____________________________________________________;
(4)在FeCl3溶液中加入过量的氨水
________________________________________________________________________。
5.(2012年济宁期末)A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次
增大。已知:A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,D与E同主族,E元素原子的最外层电子数比次外层电子数少2。请回答:
(1)元素C在周期表中的位置是 。
(2)元素D的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物与水反应的离子方程式: 。
(3)D和E两种元素相比较,其原子得电子能力较强的是 (写名称)。
以下说法中,可以证明上述结论的是 (填写编号)。
a. 比较这两种元素的常见单质的沸点
b.二者形成的化合物中,D元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氢化物的水溶液的酸性
(4)元素A、D、E与钠元素可形成两种酸式盐(均含有该四种元素),这两种酸式盐
在水溶液中反应的离子方程式是: 。
由元素A、B、D组成的一元酸X为日常生活中的调味剂,元素A、F组成的化合物为Y。
在等体积、等pH的X、Y的溶液中分别加入等质量的锌粉,反应后若最后仅有一份溶液中存在
锌粉,则反应过程中两溶液中反应速率的大小关系是:X Y(填“>”、“<”或“=”)。
(6)元素F的单质常温下是一种气体,工业上主要是通过电解其钠盐的饱和溶液的方法获得该气体,假定装入的饱和溶液为100mL(电解前后溶液体积变化可忽略),当测得阴极上产生11.2mL(标准状况)气体时停止通电,将溶液摇匀,此时溶液的pH为 。
氧 bc
(5)> (6)12
第二类 定量型实验大题过关
【典例解析】
1.金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以HCN、CN-和金属离子的配离子的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和EDTA,在pH<2的条件下加热蒸馏,蒸出所有的HCN,并用NaOH溶液吸收;
②滴定:将吸收液调节至pH>11,以试银灵作指示剂,用AgNO3标准溶液滴定终点时,溶液由黄色变成橙红色。Ag++2CN-===[Ag(CN)2]-。
根据以上知识回答下列问题:
(1)水样预处理的目的是
________________________________________________________________________。
(2)水样预处理的装置如图,细导管插入吸收液中是为了
________________________________________________________________________。
(3)蒸馏瓶比吸收液面要高出很多,其目的是
________________________________________________________________________。
(4)如果用盐酸代替磷酸进行预处理,实验结果将________(填“偏高”、“无影响”或“偏低”)。
(5)准确移取某工厂污水100 mL,经处理后用浓度为0.01000 mol·L-1的硝酸银标准溶液滴定,终点时消耗了21.00 mL。此水样中含氰化合物的含量为________mg·L-1(以CN-计,计算结果保留一位小数)。
【高考真题解析】
1.(2011安徽高考)科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2) 3的说法正确的是( )
A.分子中N、O间形成的共价键是非极性键
B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性
D.15.2g该物质含有6.02×1022个原子
2.(2011安徽高考)W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
(1)X位于元素周期表中第 周期第 族;W的基态原子核外有
个未成对电子。
(2)X的单质和Y的单质相比,熔点较高的是 (写化学式);Z的气态氢化物和溴化氢相比,较稳定的是 (写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是 。
(4)在25oC、101 kPa下,已知Y的气态氢化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是 。
3.(2011山东高考) 氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为 个。
(2)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为 。
(3) H+可与H2O形成H3O+,H3O+中O原子采用 杂化。H3O+中H-O-H的键角比H2O中H-O-H的键角大,原因是 。
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为ag·cm-3,表示阿伏加德罗常数,则CaO晶胞体积为 cm3。
因此该晶胞中含有的氯离子个数为8×1/8+6×1/3=4,同样也可以计算出钠离子个数为4。由于CaO与NaCl的晶胞同为面心立方结构,所以CaO晶胞中也含有4个钙离子和4个氧离子,因此CaO晶胞体积为。
【答案】(1)2
(2)O-H键、氢键、范德华力 邻羟基苯甲醛形成分子内氢键,而对羟基苯甲醛形成分子间氢键,分子间氢键是分子间作用力增大
(3)sp3 H2O中O原子有2对孤对电子,H3O+只有1对孤对电子,排斥力较小
(4)
【过关测试】
1.(2012年南昌市调研)A、B、C、D、E是原子序数依次递增的五种短周期元素,已知:
①B原子核外电子总数与最外层电子数之比为4:3
②D原子最外层电子数与次外层电子数之比为3:4
③E?,C+,A+的离子半径逐渐减小
④A单质在E单质中燃烧火焰呈苍白色
请回答下列问题:
(1)E的最高价氧化物对应水化物的化学式为:___________。它的酸性比D的最高价氧化物对应水化物的酸性:____________。(填“强”或“弱”)
(2)X、Y是由上述元素中任意3种组成的强电解质,且构成的原子个数比均为1:1:1。已知X溶液中水电离出来的C(H+)=10-12mol/L,则X的电子式为:_____________;Y的水溶液酸碱性与X相同,则其原因是(写离子方程式):_______________________________;
(3)B与C构成原子个数比为1:1的化合物与H2O反应的化学方程式为:
_________________________________________________________;
(4)A与B,A与D均可形成18个电子的分子,这两种分子在水溶液中反应生成物之一是含10电子的化合物;该反应可观察到现象是:____________________________________,原因是(用化学方程式表示)_______________________________________________。
2.印刷电路的废腐蚀液中含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5 mol/L,含FeCl2 3.0 mol/L,含FeCl3 1.0 mol/L,含HCl 3.0 mol/L.取废腐蚀液200 mL按如下流程在实验室进行实验:
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂所需试剂是________(填化学式)。
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物。反应的化学方程式为__________________________________________。
(3)下图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置。
从下图挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管,固定装置不用画),并标明容器中所装试剂。
(4)实验中,必须控制生成氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收。控制生成氯气速度的操作是: _____________________________。
(5)按上述流程操作,需称取Fe粉的质量应不少于_________ g(精确到0.1 g),需通入Cl2的物质的量不少于________ mol,加入烧瓶中的KClO3的质量应不少于________ g(精确到0.1 g)。
【解析】本题是一道定性分析和定量分析相结合的综合实验题,明确反应原理是解题的关键。(1)由于是加入的过量的铁,所以得到的铜中含有铁粉,可以用酸溶解铁反应掉。
(2)根据题意,KClO3中Cl的化合价从+5价降低到0价,HCl中Cl的化合价从-13.(2012阳泉一模)W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第________周期第________族。W的气态氢化物稳定性比H2O(g)____
(填“强”或“弱”)。
Y的基态原子核外电子排布式是________________________________________________,
Y的第一电离能比X的________(填“大”或“小”)。
Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式:
_______________________________________________________________________。
(4)已知下列数据:
Fe(s)+O2(g)===FeO(s) ΔH=-272.0 kJ·mol-1
2X(s)+O2(g)===X2O3(s) ΔH=-1675.7 kJ·mol-1
X的单质和FeO反应的热化学方程式:
________________________________________________________________________。
4.(2011重庆)用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。
(1)Al的原子结构示意图为_____________________;Al与NaOH溶液反应的离子方程式:
________________________________________________。
(2)30Si的原子的中子数为_________;SiO2晶体类型为__________________。
(3)Al3+与Yn-的电子数相同,Y所在族的各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是________。
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是__________。
(5)经处理后的熔渣36.0g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0g固体;滤液中加入过量NaOH溶液,分离得到21.4g固体;则此熔渣中Al2O3的质量分数为__________________。
【解析】本题考察原子的结构、晶体类型、方程式的书写以及有关计算。
Al在周期表中位于第三周期第ⅢA族,其原子结构示意图为;单质铝既能与酸反应产生氢气,又能与强碱反应产生氢气,与NaOH溶液反应的离子方程式:
2Al+2OH-+2H2O=2AlO2-+3H2↑。
第三类 探究型实验大题过关
【典例解析】
1.(1)下列说法正确的是________(选填序号)。
A.在进行物质检验时,一般先对试样进行外观观察,确定其状态、颜色、气味等
B.配制银氨溶液时,应把硝酸银溶液逐滴加入氨水中
C.一般在实验室点燃可燃性气体时,必须先要检验纯度
D.测定硫酸铜晶体结晶水的质量分数时,若用潮湿的坩埚会使测定结果偏小
E.酸碱中和滴定实验中根据碱式滴定管的两次读数得出NaOH溶液体积为22.0 mL
F.实验室制取氯气等有毒气体时,必须在密闭体系或通风橱中进行
(2)补铁剂中铁元素的含量是质检部门衡量其质量的重要指标,实验主要包括如下步骤:
a.配制0.01 mol/L到0.008 mol/L等一系列浓度的[Fe(SCN)6]3-(红色)溶液作为标准比色液。
b.样品处理:
c.准确量取一定体积的待测液于比色管中,加入稍过量的KSCN溶液,并稀释到10 mL。
d.比色:选取与待测液颜色一致或相近的标准比色液即可判断待测液的浓度。
试回答下列问题:
①配制100 mL 0.01mol/L标准溶液,需要的玻璃仪器有:烧杯、玻璃棒、量筒,还需要:________、________。
②步骤b脱色过程包括加入:________(填:脱有机色素的吸附剂名称)→搅拌→煮沸→冷却→________(填操作)。
③步骤b样品处理中,氧化的目的是________。
【高考真题解析】
12.(2011海南)
I(6分)下列分子中,属于非极性的是
A.SO2 B.BeCl2 C.BBr3 D.COCl2
解析:根据价层电子对互斥理论(VSEPR)可得四种分子的结构如下:
答案:BC
II(14分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为___________;
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是_______;
(3)SO42-的立体构型是________,其中S原子的杂化轨道类型是_______;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为______;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为__________。
【过关测试】
1.有关溶液中所含离子的检验,下列判断正确的是( )
A.加入硝酸酸化,再滴加KSCN溶液后有血红色物质生成,则原溶液中一定有Fe3+存在
B.加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO存在
C.用某溶液做焰色反应实验时火焰为黄色,则该溶液中一定有钠元素,可能有钾元素
D.分别含有Mg2+、Cu2+、Fe2+和Na+的四种盐酸盐溶液,只用NaOH溶液是不能一次鉴别开的
2.(2012年浙江省宁波市八校高三学期初测试)下列实验设计能完成或实验结论合理的是( )
A.证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾一淀粉试纸检验,观察试纸颜色的变化
B.铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,该铝热剂不含氧化铁
C.测氯水的pH可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较
D.用新制氢氧化铜悬浊液可以鉴别甲酸、甲酸甲酯、乙酸、乙酸乙酯四种物质
3.锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)]。
回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式
________________________________________________________________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是________。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式
________________________________________________________________________。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备Zn(OH)2的原因
________________________________________________________________________。
4.(2012潮州模拟)下表为元素周期表的一部分。请回答下列问题:
(1)上述元素中,属于s区的是____________(填元素符号)。
(2)写出元素⑩的基态原子的电子排布式____________________。
(3)元素第一电离能为⑤________⑨(填“大于”或“小于”)。
(4)元素③气态氢化物的中心原子有________对弧对电子,其VSEPR模型为________;中心原子的杂化类型为________;该分子为________分子(填“极性”或“非极性”)。向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为_______________________________________________。
(5)元素⑦的钠盐晶胞结构如图所示,每个Na+周围与之距离最近的Na+的个数为________。
第四类 设计型实验大题过关
【典例解析】
1.某同学设计了如下所示的方法,鉴定盐A的组成成分。下列结论中正确的是( )
(血红色溶液)
(浅黄色沉淀)
A.A中一定有Fe3+
B.C中一定有Fe3+
C.B为AgI沉淀
D.A一定为FeBr2溶液
【解析】KSCN溶液是检验Fe3+的特效试剂,加入KSCN溶液出现血红色,表明C中一定含Fe3+,故B正确,但A中不一定有Fe3+,有可能含Fe2+,当Fe2+遇硝酸酸化时,会被氧化生成Fe3+:3Fe2++NO+4H+===3Fe3++NO↑+2H2O,故A、D错误;又因为AgI是黄色沉淀,而B为浅黄色沉淀,C错误。
【答案】B
【高考真题解析】
1.(2011天津高考)以下有关原子结构及元素周期律的叙述正确的是( )
A.第IA族元素铯的两种同位素137Cs比133Cs多4个质子
B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小
C.第 ⅦA元素从上到下,其氢化物的稳定性逐渐增强
D.同主族元素从上到下,单质的熔点逐渐降低
2.(2011新课标全国)短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是( )
A.元素W、X的氯化物中,各原子均满足8电子的稳定结构
B.元素X与氢形成的原子比为1:1的化合物有很多种
C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D.元素Z可与元素X形成共价化合物XZ2
化钠溶液或盐酸反应均有氢气生成,C正确;C和S均属于非金属元素,二者可以形成共价化合物CS2,D正确。
【答案】A
【过关测试】
1.某氯碱厂利用废铁皮制取净水剂FeCl3溶液,最合理的生产途径是( )
A. Cl2FeCl3FeCl3溶液
B.Cl2HCl盐酸FeCl2溶液FeCl3溶液
C.Cl2HCl盐酸FeCl2溶液FeCl3溶液
D.―→FeCl3溶液
2.(2012年合肥市第一次质量检测)磷有三种同素异形体,分别为白磷(P4)、红磷和黑磷。
(1)白磷常温下为白色或淡黄色固体,在40℃左右自燃,实验室保存少量白磷的方法是 。
(2)白磷黑磷,黑磷比白磷稳定,结构与石墨相似,下列叙述正确的是
(填选项字母)
A.黑磷与白磷互为同分异构体 B.黑磷能导电
C.白磷转化为黑磷为氧化还原反应 D.白磷转化为黑磷为放热反应
(3)红磷在氯气中燃烧生成两种氯化物,其中一种氯化物分子是每个原子最外层都满足8个电子的结构,则该氯化物的空间构型与下列 分子最相似。(填选项字母)
A.H2O B.CCl4 C.NH3 D.CS2
(4)已知白磷、红磷燃烧的热化学方程式分别为
P4(s、白磷)+5O2(g)=P4O10(s);△H=-986KJ·mol-1
P(s、红磷)+O2(g)=P4O10(s);△H=-739KJ·mol-1
写出红磷转化为白磷的热化学方程式 。
3.(2012安庆统测) C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Ge的原子核外电子排布式为______________________。
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是________。
(3)按要求指出下列氧化物的空间构型、成键方式或性质:
①CO2分子的空间构型及碳氧之间的成键方式________________;
②SiO2晶体的空间构型及硅氧之间的成键方式_______________________________________
______________________________________________________________________________;
③已知SnO2是离子晶体,写出其主要物理性质_____________________________________
_________________________________________________________________(写出2条即可)。
(4)CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为________。
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060 cm-1,CO分子中碳氧键的伸缩振动频率为2143 cm-1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度________(填字母)。
A.强 B.弱
C.相等 D.无法判断
同课章节目录
