2022年鲁教版九年级化学下册第七单元常见的酸和碱测试题(word版 含答案)
文档属性
| 名称 | 2022年鲁教版九年级化学下册第七单元常见的酸和碱测试题(word版 含答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 149.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-14 00:00:00 | ||
图片预览



文档简介
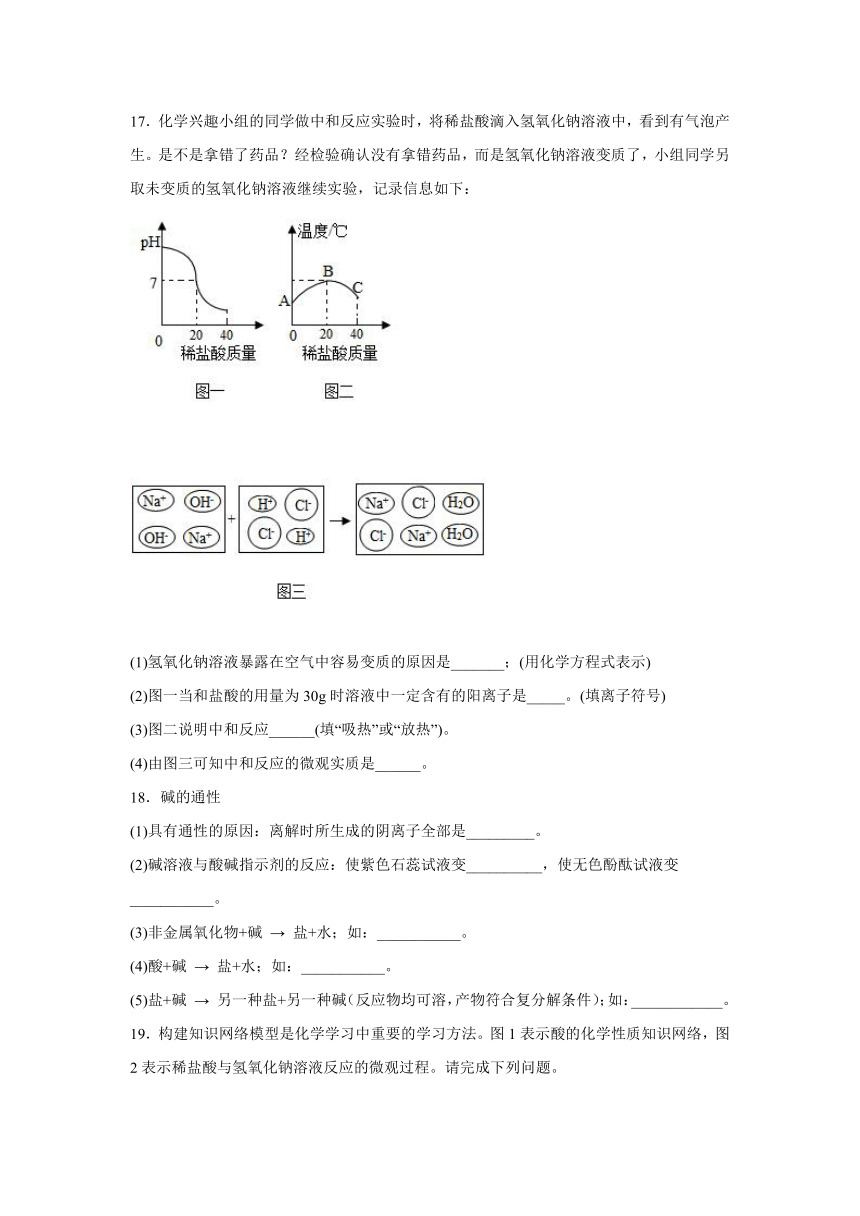
第七单元《常见的酸和碱》测试题
一、单选题
1.物质用途主要由化学性质决定的是
A.稀有气体作电光源 B.氯化钠配制生理盐水
C.干冰用于人工降雨 D.生石灰用于食品加热
2.下列有关实验现象的描述,正确的是
A.打开浓盐酸的瓶盖,瓶口冒白烟
B.高锰酸钾溶于汽油形成紫红色溶液
C.铁溶解在稀盐酸中,溶液颜色变成浅绿色
D.电解水时负极产生的气体能使带火星的木条复燃
3.下列实验基本操作规范的是
A.称量氢氧化钠 B.蒸发氯化钠溶液
C.稀释浓硫酸 D.测定溶液pH
4.我们生活中一些食物的近似pH值如下,其中碱性最强的是
食物 葡萄汁 苹果汁 牛奶 鸡蛋淸
pH 3.5~4.5 2.9~3.3 6.3~6.6 7.6~8.0
A.葡萄汁 B.苹果汁 C.牛奶 D.鸡蛋清
5.物质的性质和用途密切相关。下列物质的用途体现其化学性质的是
A.用石墨制作铅笔芯 B.用铜丝制作导线
C.用生石灰制作干燥剂 D.用氙气制作电光源
6.下列物质露置在空气中,一段时间后,因发生化学变化而质量增加的是
A.氧化钙 B.浓硫酸 C.浓盐酸 D.浓氨水
7.下列溶液长时间露置在空气中(不考虑水的蒸发),会发生变质且溶液质量增加的是
A.氢氧化钠溶液 B.浓硫酸 C.澄清石灰水 D.浓盐酸
8.我国研制的航天服为航天员的舱外行走提供了安全保障。航天服内含有与氢氧化钠性质相似的氢氧化锂(LiOH),它不可能有的化学性质是
A.能与二氧化碳反应 B.能与氧化铁反应
C.能与氯化铁溶液反应 D.能与稀硫酸反应
9.化学实验中常会呈现颜色之美。下列化学实验中的颜色变化与实验事实不符的是
A.将生锈铁钉投入到稀盐酸中,溶液逐渐变为浅黄色
B.将少量氧化铜粉末加入稀硫酸中,微热,浑浊液体会逐渐变为蓝色溶液
C.向硫酸铜溶液中滴加氢氧化钠溶液会产生蓝色沉淀
D.将通入滴有石蕊的水中,溶液颜色由紫色逐渐变为蓝色
10.20gKOH加入100g水中,配制成溶液。下列说法错误的是
A.该溶液的溶质质量分数为20% B.KOH在水中解离出K+和OH-
C.一个K+带一个单位正电荷 D.向该溶液中滴入无色酚酞试液,试液变红
11.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下;
物质 甲 乙 丙 丁
反应前质量(g) 8 10 18 64
反应后质量(g) 待测 32 36 32
关于此反应,下列认识确的是A.实验后甲物质“待测”质量为16g
B.反应生成的丙的质量与参加反应的丁的质量之比为9:16
C.乙、丁的相对分子质量比为1:1
D.该反应一定属于复分解反应
12.“证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推断合理的是
A.因为碱溶液呈碱性,所以显碱性的溶液一定都是碱的溶液
B.混合物中至少含有两种物质,则混合物中至少含有两种元素
C.同种元素的原子质子数相同,则质子数相同的原子一定是同种元素
D.化学变化常常伴随能量的变化,所以有能量变化的一定属于化学变化
13.蓝莓中含有的花青素(化学式为C15H11O6)具有缓解眼睛疲劳、保护视力的作用。酸能使花青素溶液变成红色,碱能使花青素溶液变成蓝色。下列说法不正确的是
A.花青素的相对分子质量为287 B.向白醋中滴加花青素溶液,溶液变成红色
C.花青素中共有32个原子 D.花青素中氢元素的质量分数最小
14.推理是化学学习过程中一种重要的思维方法,下列推理正确的是
A.有氧气参加的反应是氧化反应,所以氧化反应一定有氧气参加
B.化合物是由不同种元素组成的纯净物,所以由同种元素组成的物质一定不是化合物
C.铁不断锈蚀使铁制品不断减少,所以随着铁制品不断锈蚀使自然界中的铁元素不断减少
D.活泼金属能与稀盐酸反应产生气体,所以能与稀盐酸反应产生气体的一定是活泼金属
15.科学家用新型催化剂将二氧化碳高效转化为甲醇,其反应的微观示意图如下图。下列说法正确的是
A.该反应的基本反应类型属于复分解反应
B.该反应生成甲醇和水的质量比为16:9
C.反应前后分子和原子的数目均未发生改变
D.甲醇是由一个碳原子,四个氢原子和一个氢原子构成的
二、填空题
16.用化学用语填空。
(1)2个氮原子______;
(2)氨分子______;
(3)体温计中的金属物质______;
(4)4个氢氧根离子______;
(5)最常见的溶剂______;
(6)胃液中的酸______。
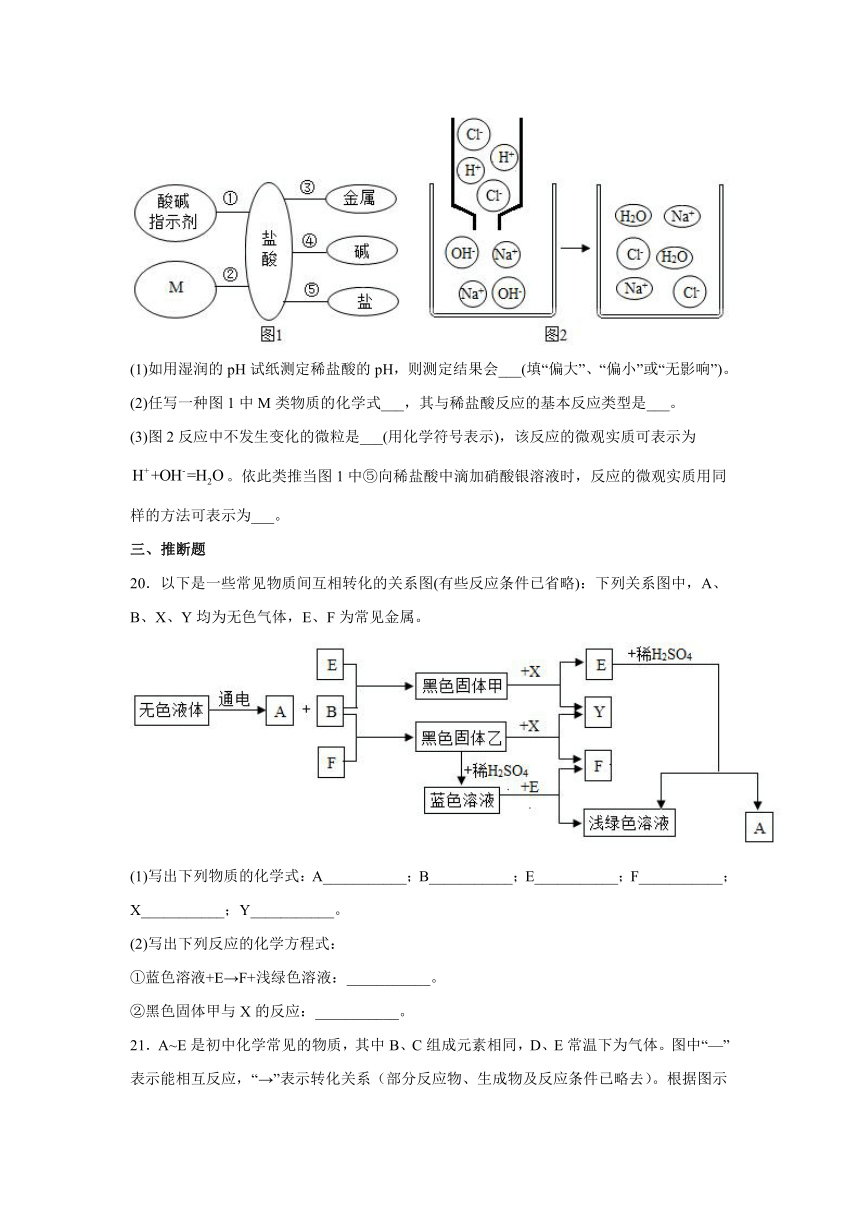
17.化学兴趣小组的同学做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生。是不是拿错了药品?经检验确认没有拿错药品,而是氢氧化钠溶液变质了,小组同学另取未变质的氢氧化钠溶液继续实验,记录信息如下:
(1)氢氧化钠溶液暴露在空气中容易变质的原因是_______;(用化学方程式表示)
(2)图一当和盐酸的用量为30g时溶液中一定含有的阳离子是_____。(填离子符号)
(3)图二说明中和反应______(填“吸热”或“放热”)。
(4)由图三可知中和反应的微观实质是______。
18.碱的通性
(1)具有通性的原因:离解时所生成的阴离子全部是_________。
(2)碱溶液与酸碱指示剂的反应:使紫色石蕊试液变__________,使无色酚酞试液变___________。
(3)非金属氧化物+碱 → 盐+水;如:___________。
(4)酸+碱 → 盐+水;如:___________。
(5)盐+碱 → 另一种盐+另一种碱(反应物均可溶,产物符合复分解条件);如:____________。
19.构建知识网络模型是化学学习中重要的学习方法。图1表示酸的化学性质知识网络,图2表示稀盐酸与氢氧化钠溶液反应的微观过程。请完成下列问题。
(1)如用湿润的pH试纸测定稀盐酸的pH,则测定结果会___(填“偏大”、“偏小”或“无影响”)。
(2)任写一种图1中M类物质的化学式___,其与稀盐酸反应的基本反应类型是___。
(3)图2反应中不发生变化的微粒是___(用化学符号表示),该反应的微观实质可表示为。依此类推当图1中⑤向稀盐酸中滴加硝酸银溶液时,反应的微观实质用同样的方法可表示为___。
三、推断题
20.以下是一些常见物质间互相转化的关系图(有些反应条件已省略):下列关系图中,A、B、X、Y均为无色气体,E、F为常见金属。
(1)写出下列物质的化学式:A___________;B___________;E___________;F___________;X___________;Y___________。
(2)写出下列反应的化学方程式:
①蓝色溶液+E→F+浅绿色溶液:___________。
②黑色固体甲与X的反应:___________。
21.A~E是初中化学常见的物质,其中B、C组成元素相同,D、E常温下为气体。图中“—”表示能相互反应,“→”表示转化关系(部分反应物、生成物及反应条件已略去)。根据图示回答下列问题:
(1)D的化学式是____________。
(2)写出图示中C→E的反应方程式:____________。
四、实验题
22.用如图装置进行实验,挤出滴管内液体。
实验序号 集气瓶内试剂 滴管内试剂
1 二氧化锰 过氧化氢溶液
2 氧化钙 水
3 A B
(1)实验1,观察到U型管中a处液面下降,用化学方程式解释其原因:_____。
(2)实验2,观察到U型管中a处液面先下降,一段时间后恢复原位,原因是_____。
(3)实验3,观察到U型管中 a处液面上升。试剂A、B是_____。
23.据图回答下列有关实验的问题:
(1)如图1,操作一现象:加入硝酸铵后,一会儿发现烧杯与塑料片粘在一起,其原因是硝酸铵晶体溶于水时_____________热量,使溶液的温度降到0℃以下,塑料片上的水结成冰。操作二现象:烧杯与塑料片分离,其原因是_____________。
(2)如图2,探究二氧化碳能否与水、饱和石灰水氢氧化钠溶液反应。
小明分别振荡三个软质塑料瓶,观察到塑料瓶都变瘪且变瘪的程度由大到小的顺序为A>B>C。
①小明认为通过塑料瓶变瘪就可证明二氧化碳与三种物质都能发生反应,你认为小明的结论___________(填“是或否”)正确,理由是_______________________。
②小华取C瓶溶液少量,滴加紫色的石蕊试液,看到_____________现象,说明CO2与水反应生成了酸。对“无明显现象发生”的化学反应,小华的探究思路和方法是_____________。
③B瓶中发生的还有_____________现象能证明反应发生。对比A瓶与_____________瓶的实验现象,可证明二氧化碳能与氢氧化钠溶液发生反应且溶质的溶解性更强,该反应的化学方程式为_____________。
五、计算题
24.洁厕灵的有效成分为HCl,某化学实验小组同学欲测定某品牌洁厕灵中的HCl的质量分数。同学们将100.0g洁厕灵倒入锥形瓶中,逐次加入一定量质量分数的碳酸钠溶液,至不在产生气体为止,共消耗80g碳酸钠溶液,并测得反应后溶液的质量为175.6g.请计算。
(1)生成二氧化碳的质量为___________g。
(2)恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程,计算结果精确到0.1%)
25.某同学探究稀硫酸与氢氧化钠溶液反应的过程,分别取稀硫酸和氢氧化钠溶液各50g进行实验,并用pH传感器测定反应过程中pH的变化如图所示。已知所用稀硫酸的溶质质量分数为9.8%,请回答问题并计算。
(1)A溶液的溶质是___________(填化学式)。
(2)所用氢氧化钠溶液的溶质质量分数。
参考答案:
1.D 2.C 3.B 4.D 5.C 6.A 7.A 8.B 9.D 10.A 11.B 12.C 13.C 14.B 15.B 16.(1)2N(2)NH3(3)Hg(4)4OH-(5)H2O(6)HCl
17.(1)
(2)
(3)放热
(4)
18.(1)OH-##氢氧根离子
(2) 蓝 红
(3)CO2+Ca(OH)2=CaCO3↓+H2O
(4)Ca(OH)2+2HCl= CaCl2+2H2O
(5)Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
19.(1)偏大
(2) CuO 复分解反应
(3) Na+、Cl-
20.(1) H2 O2 Fe Cu CO CO2
(2)
21. H2
22.(1)
(2)氧化钙和水反应放热,温度升高,使密闭装置内压强大于大气压,a处液面下降;一段时间后温度恢复,压强恢复至大气压,a处液面恢复原位
(3)A是二氧化碳;B是澄清石灰水(合理即可)
23.(1) 吸收 浓硫酸稀释放热
(2) 否 C瓶变瘪可能是二氧化碳溶于水 溶液变红 验证生成物 澄清石灰水变浑浊 B 2NaOH+CO2=Na2CO3+H2O
24.(1)4.4
(2)解:设生成NaCl的质量为x
x=11.7g
×100%≈6.7℅
答:恰好完全反应时,所得溶液的溶质质量分数为6.7%。
25.(1)H2SO4
(2)解:设所用氢氧化钠溶液的溶质质量分数x
答:所用氢氧化钠溶液的溶质质量分数为6.4%。
一、单选题
1.物质用途主要由化学性质决定的是
A.稀有气体作电光源 B.氯化钠配制生理盐水
C.干冰用于人工降雨 D.生石灰用于食品加热
2.下列有关实验现象的描述,正确的是
A.打开浓盐酸的瓶盖,瓶口冒白烟
B.高锰酸钾溶于汽油形成紫红色溶液
C.铁溶解在稀盐酸中,溶液颜色变成浅绿色
D.电解水时负极产生的气体能使带火星的木条复燃
3.下列实验基本操作规范的是
A.称量氢氧化钠 B.蒸发氯化钠溶液
C.稀释浓硫酸 D.测定溶液pH
4.我们生活中一些食物的近似pH值如下,其中碱性最强的是
食物 葡萄汁 苹果汁 牛奶 鸡蛋淸
pH 3.5~4.5 2.9~3.3 6.3~6.6 7.6~8.0
A.葡萄汁 B.苹果汁 C.牛奶 D.鸡蛋清
5.物质的性质和用途密切相关。下列物质的用途体现其化学性质的是
A.用石墨制作铅笔芯 B.用铜丝制作导线
C.用生石灰制作干燥剂 D.用氙气制作电光源
6.下列物质露置在空气中,一段时间后,因发生化学变化而质量增加的是
A.氧化钙 B.浓硫酸 C.浓盐酸 D.浓氨水
7.下列溶液长时间露置在空气中(不考虑水的蒸发),会发生变质且溶液质量增加的是
A.氢氧化钠溶液 B.浓硫酸 C.澄清石灰水 D.浓盐酸
8.我国研制的航天服为航天员的舱外行走提供了安全保障。航天服内含有与氢氧化钠性质相似的氢氧化锂(LiOH),它不可能有的化学性质是
A.能与二氧化碳反应 B.能与氧化铁反应
C.能与氯化铁溶液反应 D.能与稀硫酸反应
9.化学实验中常会呈现颜色之美。下列化学实验中的颜色变化与实验事实不符的是
A.将生锈铁钉投入到稀盐酸中,溶液逐渐变为浅黄色
B.将少量氧化铜粉末加入稀硫酸中,微热,浑浊液体会逐渐变为蓝色溶液
C.向硫酸铜溶液中滴加氢氧化钠溶液会产生蓝色沉淀
D.将通入滴有石蕊的水中,溶液颜色由紫色逐渐变为蓝色
10.20gKOH加入100g水中,配制成溶液。下列说法错误的是
A.该溶液的溶质质量分数为20% B.KOH在水中解离出K+和OH-
C.一个K+带一个单位正电荷 D.向该溶液中滴入无色酚酞试液,试液变红
11.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下;
物质 甲 乙 丙 丁
反应前质量(g) 8 10 18 64
反应后质量(g) 待测 32 36 32
关于此反应,下列认识确的是A.实验后甲物质“待测”质量为16g
B.反应生成的丙的质量与参加反应的丁的质量之比为9:16
C.乙、丁的相对分子质量比为1:1
D.该反应一定属于复分解反应
12.“证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推断合理的是
A.因为碱溶液呈碱性,所以显碱性的溶液一定都是碱的溶液
B.混合物中至少含有两种物质,则混合物中至少含有两种元素
C.同种元素的原子质子数相同,则质子数相同的原子一定是同种元素
D.化学变化常常伴随能量的变化,所以有能量变化的一定属于化学变化
13.蓝莓中含有的花青素(化学式为C15H11O6)具有缓解眼睛疲劳、保护视力的作用。酸能使花青素溶液变成红色,碱能使花青素溶液变成蓝色。下列说法不正确的是
A.花青素的相对分子质量为287 B.向白醋中滴加花青素溶液,溶液变成红色
C.花青素中共有32个原子 D.花青素中氢元素的质量分数最小
14.推理是化学学习过程中一种重要的思维方法,下列推理正确的是
A.有氧气参加的反应是氧化反应,所以氧化反应一定有氧气参加
B.化合物是由不同种元素组成的纯净物,所以由同种元素组成的物质一定不是化合物
C.铁不断锈蚀使铁制品不断减少,所以随着铁制品不断锈蚀使自然界中的铁元素不断减少
D.活泼金属能与稀盐酸反应产生气体,所以能与稀盐酸反应产生气体的一定是活泼金属
15.科学家用新型催化剂将二氧化碳高效转化为甲醇,其反应的微观示意图如下图。下列说法正确的是
A.该反应的基本反应类型属于复分解反应
B.该反应生成甲醇和水的质量比为16:9
C.反应前后分子和原子的数目均未发生改变
D.甲醇是由一个碳原子,四个氢原子和一个氢原子构成的
二、填空题
16.用化学用语填空。
(1)2个氮原子______;
(2)氨分子______;
(3)体温计中的金属物质______;
(4)4个氢氧根离子______;
(5)最常见的溶剂______;
(6)胃液中的酸______。
17.化学兴趣小组的同学做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生。是不是拿错了药品?经检验确认没有拿错药品,而是氢氧化钠溶液变质了,小组同学另取未变质的氢氧化钠溶液继续实验,记录信息如下:
(1)氢氧化钠溶液暴露在空气中容易变质的原因是_______;(用化学方程式表示)
(2)图一当和盐酸的用量为30g时溶液中一定含有的阳离子是_____。(填离子符号)
(3)图二说明中和反应______(填“吸热”或“放热”)。
(4)由图三可知中和反应的微观实质是______。
18.碱的通性
(1)具有通性的原因:离解时所生成的阴离子全部是_________。
(2)碱溶液与酸碱指示剂的反应:使紫色石蕊试液变__________,使无色酚酞试液变___________。
(3)非金属氧化物+碱 → 盐+水;如:___________。
(4)酸+碱 → 盐+水;如:___________。
(5)盐+碱 → 另一种盐+另一种碱(反应物均可溶,产物符合复分解条件);如:____________。
19.构建知识网络模型是化学学习中重要的学习方法。图1表示酸的化学性质知识网络,图2表示稀盐酸与氢氧化钠溶液反应的微观过程。请完成下列问题。
(1)如用湿润的pH试纸测定稀盐酸的pH,则测定结果会___(填“偏大”、“偏小”或“无影响”)。
(2)任写一种图1中M类物质的化学式___,其与稀盐酸反应的基本反应类型是___。
(3)图2反应中不发生变化的微粒是___(用化学符号表示),该反应的微观实质可表示为。依此类推当图1中⑤向稀盐酸中滴加硝酸银溶液时,反应的微观实质用同样的方法可表示为___。
三、推断题
20.以下是一些常见物质间互相转化的关系图(有些反应条件已省略):下列关系图中,A、B、X、Y均为无色气体,E、F为常见金属。
(1)写出下列物质的化学式:A___________;B___________;E___________;F___________;X___________;Y___________。
(2)写出下列反应的化学方程式:
①蓝色溶液+E→F+浅绿色溶液:___________。
②黑色固体甲与X的反应:___________。
21.A~E是初中化学常见的物质,其中B、C组成元素相同,D、E常温下为气体。图中“—”表示能相互反应,“→”表示转化关系(部分反应物、生成物及反应条件已略去)。根据图示回答下列问题:
(1)D的化学式是____________。
(2)写出图示中C→E的反应方程式:____________。
四、实验题
22.用如图装置进行实验,挤出滴管内液体。
实验序号 集气瓶内试剂 滴管内试剂
1 二氧化锰 过氧化氢溶液
2 氧化钙 水
3 A B
(1)实验1,观察到U型管中a处液面下降,用化学方程式解释其原因:_____。
(2)实验2,观察到U型管中a处液面先下降,一段时间后恢复原位,原因是_____。
(3)实验3,观察到U型管中 a处液面上升。试剂A、B是_____。
23.据图回答下列有关实验的问题:
(1)如图1,操作一现象:加入硝酸铵后,一会儿发现烧杯与塑料片粘在一起,其原因是硝酸铵晶体溶于水时_____________热量,使溶液的温度降到0℃以下,塑料片上的水结成冰。操作二现象:烧杯与塑料片分离,其原因是_____________。
(2)如图2,探究二氧化碳能否与水、饱和石灰水氢氧化钠溶液反应。
小明分别振荡三个软质塑料瓶,观察到塑料瓶都变瘪且变瘪的程度由大到小的顺序为A>B>C。
①小明认为通过塑料瓶变瘪就可证明二氧化碳与三种物质都能发生反应,你认为小明的结论___________(填“是或否”)正确,理由是_______________________。
②小华取C瓶溶液少量,滴加紫色的石蕊试液,看到_____________现象,说明CO2与水反应生成了酸。对“无明显现象发生”的化学反应,小华的探究思路和方法是_____________。
③B瓶中发生的还有_____________现象能证明反应发生。对比A瓶与_____________瓶的实验现象,可证明二氧化碳能与氢氧化钠溶液发生反应且溶质的溶解性更强,该反应的化学方程式为_____________。
五、计算题
24.洁厕灵的有效成分为HCl,某化学实验小组同学欲测定某品牌洁厕灵中的HCl的质量分数。同学们将100.0g洁厕灵倒入锥形瓶中,逐次加入一定量质量分数的碳酸钠溶液,至不在产生气体为止,共消耗80g碳酸钠溶液,并测得反应后溶液的质量为175.6g.请计算。
(1)生成二氧化碳的质量为___________g。
(2)恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程,计算结果精确到0.1%)
25.某同学探究稀硫酸与氢氧化钠溶液反应的过程,分别取稀硫酸和氢氧化钠溶液各50g进行实验,并用pH传感器测定反应过程中pH的变化如图所示。已知所用稀硫酸的溶质质量分数为9.8%,请回答问题并计算。
(1)A溶液的溶质是___________(填化学式)。
(2)所用氢氧化钠溶液的溶质质量分数。
参考答案:
1.D 2.C 3.B 4.D 5.C 6.A 7.A 8.B 9.D 10.A 11.B 12.C 13.C 14.B 15.B 16.(1)2N(2)NH3(3)Hg(4)4OH-(5)H2O(6)HCl
17.(1)
(2)
(3)放热
(4)
18.(1)OH-##氢氧根离子
(2) 蓝 红
(3)CO2+Ca(OH)2=CaCO3↓+H2O
(4)Ca(OH)2+2HCl= CaCl2+2H2O
(5)Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
19.(1)偏大
(2) CuO 复分解反应
(3) Na+、Cl-
20.(1) H2 O2 Fe Cu CO CO2
(2)
21. H2
22.(1)
(2)氧化钙和水反应放热,温度升高,使密闭装置内压强大于大气压,a处液面下降;一段时间后温度恢复,压强恢复至大气压,a处液面恢复原位
(3)A是二氧化碳;B是澄清石灰水(合理即可)
23.(1) 吸收 浓硫酸稀释放热
(2) 否 C瓶变瘪可能是二氧化碳溶于水 溶液变红 验证生成物 澄清石灰水变浑浊 B 2NaOH+CO2=Na2CO3+H2O
24.(1)4.4
(2)解:设生成NaCl的质量为x
x=11.7g
×100%≈6.7℅
答:恰好完全反应时,所得溶液的溶质质量分数为6.7%。
25.(1)H2SO4
(2)解:设所用氢氧化钠溶液的溶质质量分数x
答:所用氢氧化钠溶液的溶质质量分数为6.4%。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
