第三章烃的衍生物第一节卤代烃——提升训练2021-2022学年高中化学人教版(2019)选择性必修3(含答案)
文档属性
| 名称 | 第三章烃的衍生物第一节卤代烃——提升训练2021-2022学年高中化学人教版(2019)选择性必修3(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 330.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-11 20:10:56 | ||
图片预览




文档简介
第三章烃的衍生物第一节卤代烃——提升训练2021-2022学年高中化学人教版(2019)选择性必修3
一、选择题(共16题)
1.若NA为阿伏加德罗常数的值,下列说法正确的是
A.8.0 g含有的电子数为4.5NA
B.28 g乙烯和丁烯的混合物,含有原子总数为6NA
C.标准状况下,22.4 LCCl4含碳原子数目为NA
D.4.4 g C3H8所含共价键的数目为0.8NA
2.关于卤代烃的下列说法不正确的是
A.卤代烃不属于烃
B.卤代烃难溶于水,易溶于有机溶剂
C.有的卤代烃可用作有机溶剂
D.所有的卤代烃都可以发生消去反应生成相应的烯烃
3.下列有机反应中,C-H键未发生断裂的是
A.苯与浓硝酸、浓硫酸在加热的条件下反应 B.溴乙烷在氢氧化钠乙醇溶液中加热
C.乙醇与乙酸在浓硫酸加热条件下反应 D.苯酚与甲醛在浓盐酸、加热条件下反应
4.下列化学用语或图示表达不正确的是
A.HClO的结构式为:H-O-Cl B.CO2的电子式:
C.溴乙烷的分子模型: D.Na+的结构示意图:
5.下列根据实验操作和现象所得出的结论正确的是
选项 实验操作 实验现象 结论
A 向装有铁粉的三颈烧瓶中滴加苯和液溴的混合物,将产生的气体直接通入溶液 有浅黄色沉淀生成 可证明苯和液溴一定发生了取代反应
B 溴乙烷与KOH溶液混合加热后,再滴加溶液 无浅黄色沉淀 溴乙烷未水解
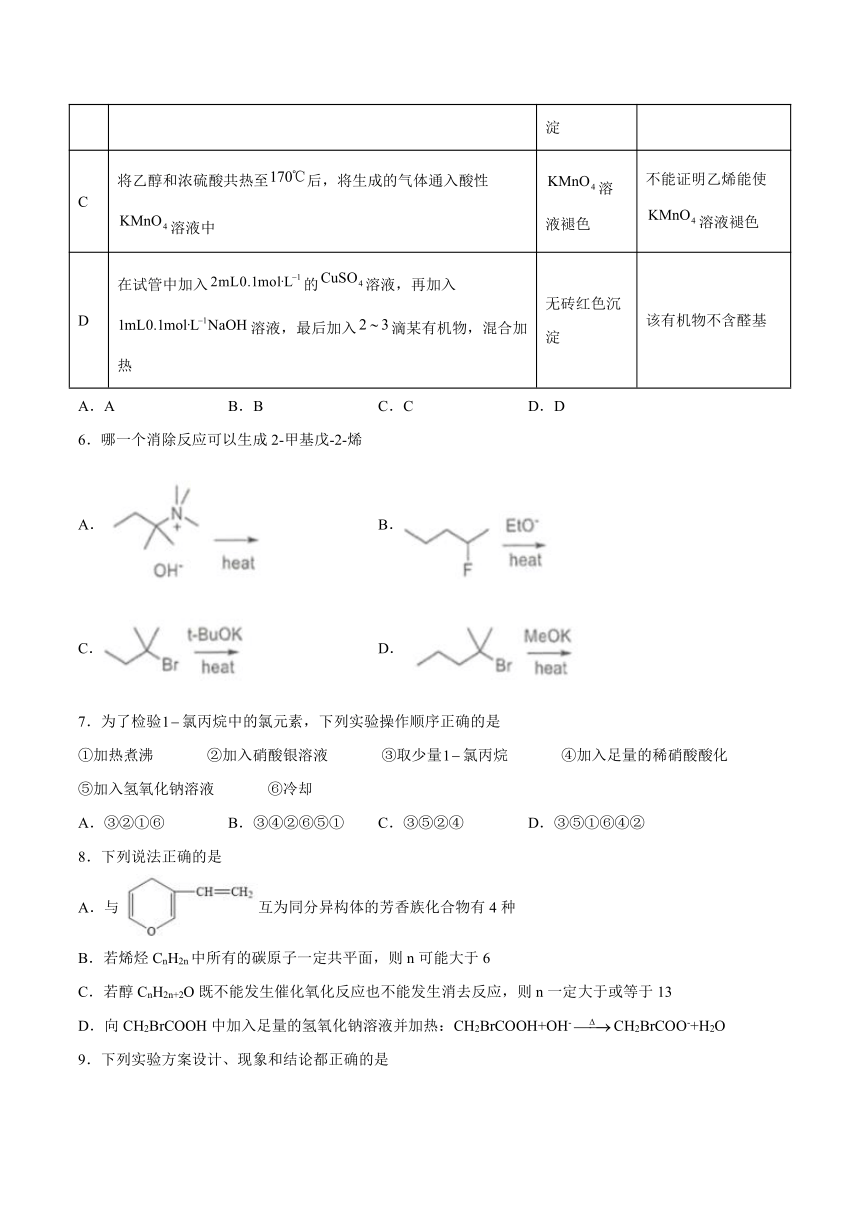
C 将乙醇和浓硫酸共热至后,将生成的气体通入酸性溶液中 溶液褪色 不能证明乙烯能使溶液褪色
D 在试管中加入的溶液,再加入溶液,最后加入滴某有机物,混合加热 无砖红色沉淀 该有机物不含醛基
A.A B.B C.C D.D
6.哪一个消除反应可以生成2-甲基戊-2-烯
A. B.
C. D.
7.为了检验氯丙烷中的氯元素,下列实验操作顺序正确的是
①加热煮沸 ②加入硝酸银溶液 ③取少量氯丙烷 ④加入足量的稀硝酸酸化 ⑤加入氢氧化钠溶液 ⑥冷却
A.③②①⑥ B.③④②⑥⑤① C.③⑤②④ D.③⑤①⑥④②
8.下列说法正确的是
A.与互为同分异构体的芳香族化合物有4种
B.若烯烃CnH2n中所有的碳原子一定共平面,则n可能大于6
C.若醇CnH2n+2O既不能发生催化氧化反应也不能发生消去反应,则n一定大于或等于13
D.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-CH2BrCOO-+H2O
9.下列实验方案设计、现象和结论都正确的是
实验目的 方案设计 现象和结论
A 检验CH3CH2Br在NaOH溶液中是否发生水解 将CH3CH2Br与NaOH溶液共热,冷却后,取少量溶液,加入AgNO3溶液 若有沉淀产生,则CH3CH2Br发生水解
B 比较Br2和I2的氧化性强弱 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置 若下层液体呈紫红色,则Br2的氧化性强于I2
C 检验Fe(NO3)2晶体是否氧化变质 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 若溶液变红,则Fe(NO3)2晶体已氧化变质
D 比较HNO2和CH3COOH电离出H+的能力 用pH试纸分别测CH3COONa溶液和NaNO2溶液的pH 若CH3COONa溶液的pH比NaNO2溶液的pH大,则HNO2电离出H+的能力比CH3COOH的强
A.A B.B C.C D.D
10.由下列实验操作及现象不能得出相应结论的是
实验操作 现象 结论
A 向烧瓶中加入2.0gNaOH和15mL无水乙醇,搅拌。再加入5mL1—溴丁烷和碎瓷片,微热。将产生的气体通入盛水的试管后,再用酸性高锰酸钾溶液进行检验 高锰酸钾溶液褪色 1—溴丁烷发生消去反应
B 向NaClO溶液中滴加酚酞试剂 先变红后褪色 NaClO发生了水解反应
C 向等浓度(c=0.01mol/L)NaCl和Na2CrO4混合液中滴加AgNO3稀溶液(已知AgCl和Ag2CrO4的溶度积常数分别为1.8×10-10,2×10-12) 出现白色沉淀(Ag2CrO4为黄色沉淀) Ag2CrO4的溶解度小于AgCl(以浓度计算)
D 室温,用pH试纸测定0.1mol L-1Na2SO3溶液和0.1mol L-1NaHSO3溶液的pH Na2SO3溶液pH约为10;NaHSO3溶液pH约为5 结合H+的能力: <
A.A B.B C.C D.D
11.下列叙述正确的是
A.检验溴乙烷中的卤原子:先加入NaOH溶液共热,再加AgNO3溶液,观察沉淀颜色
B.属于烯烃的同分异构体有5种(考虑顺反异构)
C.立方烷的六氯取代物有6种
D.和都可有6个原子处于同一直线上
12.下列实验操作能够达到实验目的的是
选项 实验目的 实验操作
A 探究浓度对反应速率的影响 向2支各盛有和酸性溶液的试管中,分别加入5滴记录溶液褪色所需的时间
B 探究淀粉溶液在稀硫酸加热条件下是否水解 取少量的水解液于试管中,先加适量的NaOH溶液,再滴入碘水,观察实验现象
C 检验溴乙烷中的溴元素 取适量溴乙烷于试管中,加入适量NaOH溶液并加热,冷却后加足量稀硝酸,再滴加溶液,观察现象
D 验证酸性: 用pH试纸分别测定同温度同浓度的溶液和NaClO溶液的pH
A.A B.B C.C D.D
13.下列实验方案不能达到实验目的是
实验目的 实验方案
A 证明溴乙烷发生消去反应有乙烯生成 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液
B 检验卤代烃中卤原子的种类 将溴乙烷与氢氧化钠溶液共热,取冷却后反应液滴加硝酸酸化后,滴加硝酸银溶液
C 验证乙炔能被酸性高锰酸钾溶液氧化 将电石与饱和食盐水反应生成的气体先通入足量硫酸铜溶液中,再通入酸性高锰酸钾溶液,观察溶液是否褪色
D 验证苯和液溴在的催化下发生取代反应 将反应产生的混合气体通入溶液中,观察是否有淡黄色沉淀生成
A.A B.B C.C D.D
14.称为环氧乙烷,它在一定条件下,能与氢化物发生加成反应,氢原子加到氧原子上,其他部分加到碳原子上。对下面环氧乙烷的衍生物的叙述中,不正确的是
A.在一定条件下能与水反应生成
B.在一定条件下能与水反应生成
C.在一定条件下可以合成甘油
D.加入AgNO3溶液能生成难溶于HNO3的白色沉淀
15.下表中实验操作能达到实验目的的是
实验操作 实验目的
A 向苯酚浓溶液中滴加少量稀溴水 观察白色沉淀
B 向待测液中加入酸性高锰酸钾溶液 鉴别苯、甲苯
C 向溴乙烷中加氢氧化钠溶液并加热,冷却后再加硝酸银溶液 检验溴乙烷中的溴原子
D 向铁粉中依次加入苯和溴水 制备少量溴苯
A.A B.B C.C D.D
16.有机小分子催化多氟代物的取代反应,机理如图所示,已知反应Ⅰ、反应Ⅱ和反应Ⅲ的活化能中,反应Ⅱ的活化能最大。下列说法不正确的
A.反应方程式为:+→+
B.2是催化剂,4和7都是反应中间体
C.5为时,1是
D.整个取代反应的反应速率主要由反应Ⅱ的速率决定
二、综合题(共4题)
17.完成下列各题:
(1)烃 A 的结构简式为,用系统命名法命名烃A:_________________________________________。
(2)某烃的分子式为 C5H12,核磁共振氢谱图中显示三个峰,则该烃的一氯代物有_______种,该烃的结构简式为 ______________________ 。
(3)聚氯乙烯是生活中常见的塑料。工业生产聚氯乙烯的一种工艺路线如下:
反应①的化学方程式是 ___________________________________________,反应类型为___________________,反应②的反应类型为 ____________________。
(4)麻黄素又称黄碱,是我国特定的中药材麻黄中所含有的一种生物碱。经科学家研究发现其结构如下:
下列各物质:
A . B .
C. D .
E.
与麻黄素互为同分异构体的是 ___________ (填字母,下同),互为同系物的是 ______。
(5)多氯代甲烷作为溶剂,其中分子结构为正四面体的是 ____________。工业上分离这些多卤代甲烷的方法是 _________________。
18.金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
请回答下列问题:
(1)环戊二烯分子中最多有____________个原子共平面;
(2)金刚烷的分子式为_______________,其分子中的CH2基团有_____________个;
(3)面是以环戊烷为原料制备环戊二烯的合成路线:
其中,反应②的反应试剂和反应条件_____________,反应③的反应类型是___________;
(4)A是二聚环戊二烯的同分异构体,A分子结构中有一个甲基,A能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸【提示:苯环上的烷基(一CH3,一CH2R,一CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基】,写出A所有可能的结构简式(不考虑立体异构):______________________________
19.卤代烃在工农业生产和人们的生活中具有广泛的应用。回答下列问题:
(1)四氯化碳(CCl4)可用作灭火剂,其分子结构为___形。多卤代甲烷可用工业上,分离这些多卤代甲烷的方法是___。
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,其有___种同分异构体(不考虑立体异构),写出其中任意两种的结构简式:___。
(3)聚氯乙烯是生活中常见的塑料。工业生产聚氯乙烯的一种工艺路线如下:
乙烯1,2-二氯乙烷氯乙烯聚氯乙烯
反应①的反应类型为___。反应②的化学方程式为___,应类型为___。
20.金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
请回答下列问题:
(1)环戊二烯分子中最多有___________个原子共平面;
(2)金刚烷的分子式为___________,其分子中的CH2基团有___________个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
其中,反应①的产物名称是_______________,反应③的反应类型是____________;
(4)已知烯烃能发生如下反应:
请写出下列反应产物的结构简式:
___________________________。
试卷第页,共页
参考答案:
1.B
【解析】
【分析】
【详解】
A.8.0 g的物质的量是n=,每个中含有10个电子,则0.5 mol中含有的电子数目为5NA,A错误;
B.乙烯和丁烯的最简式是CH2,其中含有3个原子,式量是14,则28 g乙烯和丁烯的混合物中含有最简式的物质的量是2 mol,其中含有原子的物质的量是6 mol,则含有的原子总数为6NA,B正确;
C.在标准状况下CCl4呈液态,不能使用气体摩尔体积进行有关计算,C错误;
D.4.4 g C3H8的物质的量是0.1 mol,由于在1个C3H8分子中含有10个共价键,则在0.1 mol C3H8中所含共价键的数目为NA,D错误;
故合理选项是B。
2.D
【解析】
【详解】
A.卤代烃分子中含有卤素原子,属于烃的衍生物,不属于烃,故A正确;
B.卤代烃具有有机物的通性,难溶于水,易溶于有机溶剂,故B正确;
C.有的卤代烃可用作有机溶剂,如四氯化碳、氯仿都是良好的有机溶剂,故C正确;
D.并不是所有的卤代烃都可以发生消去反应生成相应的烯烃,如一氯甲烷没有邻碳原子,不能发生消去反应,故D错误;
故选D。
3.C
【解析】
【分析】
【详解】
A.苯与浓硝酸、浓硫酸在加热的条件下反应生成硝基苯,C-H键断裂,A错误;
B.溴乙烷在氢氧化钠乙醇溶液中加热发生消去生成双键和HBr,C-H键断裂,B错误;
C.乙醇与乙酸在浓硫酸加热条件下反应生成乙酸乙酯,酸脱羟基醇脱H,C-H键没有断裂,C正确;
D.苯酚与甲醛在浓盐酸、加热条件下,苯酚中与羟基相邻的两个氢会与甲醛中的氧一起去一个水发生缩聚,C-H键断裂,D错误;
答案选C。
4.B
【解析】
【详解】
A.HClO中O原子分别与H原子和Cl原子形成共价键,故其结构式为H-O-Cl,故A正确;
B.二氧化碳中C原子和氧原子之间以双键结合,其电子式为,故B错误;
C.溴乙烷的结构简式为CH3CH2Br,其中Br原子半径大于C和H原子半径,其分子模型为,故C正确;
D.钠离子的核内有11个质子,核外有10个电子,结构示意图为,故D正确;
故选:B。
5.C
【解析】
【分析】
【详解】
A.挥发的溴及生成的HBr均与硝酸银反应,由操作和现象不能证明发生取代反应,故A错误;
B.KOH与硝酸银反应,应在酸性溶液中检验溴离子证明溴乙烷水解,故B错误;
C.挥发的醇及生成的乙烯均使酸性高锰酸褪色,由操作和现象不能证明乙烯能使KMnO4溶液褪色,故C正确;
D.NaOH不足,应在碱性溶液中检验-CHO,应使NaOH过量,故D错误;
故选:C。
6.D
【解析】
略
7.D
【解析】
【详解】
1-氯丙烷不溶于水,在酸性或碱性条件下水解,其中碱性条件下水解程度较大,碱性条件下水解生成氯离子,然后在用硝酸酸化,加入硝酸银进行检验,以排除氢氧根离子的干扰,操作步骤为:③⑤①⑥④②;
答案选D。
8.C
【解析】
【分析】
【详解】
A.与互为同分异构体的芳香族化合物有5种:、、、 、,A错误;
B.若烯烃CnH2n中所有的碳原子一定共平面,C原子数最多6个,n6,乙烯是平面结构,其中的4个H原子被4个甲基取代,其中6个C原子共面,B错误;
C.若醇CnH2n+2O既不能发生催化氧化反应也不能发生消去反应,与羟基相连的C原子上没有H原子,与羟基相连的C原子的邻C上也没有H原子,即这两类C原子上的H原子被烷基取代,符合的结构式为:,则n一定大于或等于13,C正确;
D.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+2OH-CH2OCOO-+Br-+H2O,D错误;
答案选。
9.B
【解析】
【分析】
【详解】
A.检验方法应为将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,加入硝酸酸化后再加入AgNO3溶液,观察是否产生淡黄色沉淀,故A错误;
B.碘单质可使淀粉溶液变蓝,碘离子不可,故B正确;
C.硝酸亚铁溶液溶于稀硫酸中,则溶液中相当于存在硝酸,硝酸具有强氧化性,氧化亚铁离子为铁离子,再加入KSCN溶液,则溶液变红色,不能证明原固体是否变质,故C错误;
D.由于没有给出醋酸钠和亚硝酸钠的起始浓度,所以不能根据盐溶液的pH判断醋酸根离子和亚硝酸根的水解强弱,即不能得出两种酸谁强谁弱,故D错误;
故选B。
10.C
【解析】
【详解】
A.向烧瓶中加入2.0gNaOH和15mL无水乙醇,搅拌。再加入5mL1—溴丁烷和碎瓷片,微热。将产生的气体通入盛水的试管除去乙醇蒸气后,再用酸性高锰酸钾溶液进行检验,高锰酸钾溶液褪色,说明1—溴丁烷发生消去反应生成1-丁烯,选项A正确;
B.NaClO+H2O HClO+NaOH,水解生成NaOH使用酚酞变红,HClO具有漂白性又使红色褪去,选项B正确;
C. AgCl的Ksp=1.8×10-10,Ag2CrO4的Ksp为2×10-12,则S(AgCl)===1.34×10-5,而S(Ag2CrO4)===7.94×10-5,所以AgCl的溶解度小于Ag2CrO4,选项C错误;
D.测定pH可知Na2SO3溶液的碱性强,NaHSO3溶液电离显酸性,则结合H+的能力比的弱,选项D正确;
答案选C。
11.D
【解析】
【分析】
【详解】
A.检验溴乙烷中的卤原子的方法为先加入氢氧化钠溶液共热发生水解反应,加入过量稀硝酸中和氢氧化钠溶液后,再加人硝酸银溶液,观察沉淀颜色为淡黄色,故A错误;
B.C5H10属于烯烃的同分异构体有1—戊烯、2—戊烯、2—甲基—1—戊烯、2—甲基—2—戊烯、3—甲基—1—戊烯,其中2—戊烯存在顺反异构,则C5H10属于烯烃的同分异构体共有6种,故B错误;
C.立方烷的二氯取代物和六氯取代物的数目相同,二氯代物有两个氯原子分别位于同一条棱上、面对角线上和体对角线上3种结构,则立方烷的六氯取代物的数目为3,故C错误;
D.和中处于红线上的4个碳原子和2个氢原子可能处于同一直线上,则两者处于同一直线上的原子数目都为6,故D正确;
故选D。
12.C
【解析】
【详解】
A.高锰酸钾过量,溶液不褪色,A项错误;
B.碘遇淀粉变蓝,若实验中淀粉过量或水解不完全,加入碘水反应后的溶液会变蓝,不能证明淀粉是否水解,检验淀粉在稀硫酸催化条件下是否发生水解,取少量的水解液于试管中,应先加入碱中和稀硫酸,再加入少量新制氢氧化铜悬浊液,加热,观察是否出现砖红色沉淀,若产生砖红色沉淀,则证明淀粉水解,B项错误;
C.取适量溴乙烷于试管中,加入适量NaOH溶液并加热,溴乙烷发生水解反应生成乙醇和NaBr,冷却后加足量稀硝酸,再滴加溶液,生成淡黄色沉淀,C项正确;
D.NaClO具有漂白性,不能用pH试纸测定其水溶液的碱性强弱,D项错误;
答案选C。
13.D
【解析】
【分析】
【详解】
A.溴乙烷和NaOH的乙醇溶液,发生消去反应,乙烯与溴发生加成反应,溴水褪色,则该实验可验证乙烯的生成,故A正确;
B.溴乙烷与氢氧化钠溶液共热,水解后检验溴离子,应在酸性条件下,则取冷却后反应液滴加硝酸酸化后,再滴加硝酸银溶液可检验卤素原子种类,故B正确;
C.电石与饱和食盐水反应生成的乙炔中混有硫化氢,先通入足量硫酸铜溶液中,再通入酸性高锰酸钾溶液,观察溶液是否褪色,能说明乙烯被氧化,故C正确;
D.发生取代反应生成HBr,则反应产生的混合气体先通入溴的四氯化碳溶液再通入溶液中,观察是否有淡黄色沉淀生成,可说明取代反应,故D错误;
故选C。
14.D
【解析】
【分析】
【详解】
A.与水加成反应可生成,A正确;
B.在氢氧化钠溶液中加热水解就可以生成,B正确;
C.与水加成反应可生成,再在氢氧化钠溶液中加热水解就可以生成甘油,C正确;
D.是一种共价化合物,不可能电离出Cl-,因此不能与AgNO3溶液反应,D错误;
故选D。
15.B
【解析】
【分析】
【详解】
A.向苯酚浓溶液中滴加少量稀溴水生成三溴苯酚,三溴苯酚易溶于苯酚,观察不到白色沉淀,故A错误;
B.甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色,可用酸性高锰酸钾鉴别苯和甲苯,故B正确;
C.检验溴乙烷中的溴原子,应向水解后的液体中先加稀硝酸中和氢氧化钠,再加硝酸银溶液,故C错误;
D.苯和液溴在铁作催化剂的条件下发生取代反应生成溴苯和溴化氢,故D错误;
选B。
16.C
【解析】
【详解】
A.由图示知,物质2、4、7在过程中循环使用,故该反应相当于物质3与5反应生成1和6,对应方程式为:+→+,A正确;
B.物质2与物质3反应生成中间产物4,4与物质5反应生成中间产物7,物质7发生反应Ⅲ生成物质1和2,物质2在反应前后没变,可看作催化剂,4、7为中间产物,B正确;
C.若物质5为,即结构-X为,则物质1为:,C错误;
D.相同条件下,反应活化能越大,普通分子变成活化分子越难,反应速率越慢,由于反应Ⅱ活化能最大,故整个过程的反应速率由反应Ⅱ速率决定,D正确;
故答案选C。
17. 2,2,6-三甲基-4-乙基辛烷 3 CH3CH2CH2CH2CH3 H2C=CH2+Cl2→CH2ClCH2Cl 加成反应 消去反应 CD B 四氯化碳 分馏
【解析】
【详解】
(1)烃 A 的结构简式为,主链为8个碳原子,离支链最近的一端对碳原子编号,2号碳上有两个甲基,6号碳上有一个甲基,4号碳上有一个乙基,用系统命名法命名,烃A的名称为2,2,6-三甲基-4-乙基辛烷;
(2)某烃的分子式为 C5H12,核磁共振氢谱图中显示三个峰,说明分子结构中有三种不同环境的氢原子,则该烃的一氯代物有3种,该烃的结构简式为CH3CH2CH2CH2CH3;
(3)反应①为乙烯与氯气发生加成反应生成1,2-二氯乙烷,反应的方程式为H2C=CH2+Cl2→CH2ClCH2Cl;反应②为1,2-二氯乙烷加热480~530℃生成氯乙烯,发生消去反应;
(4)分子式相同而结构不同的有机物互称为同分异构体,根据结构简式可知,麻黄素的分子式为C10H15ON,选项中A、B、C、D、E的分子式分别为C11H17ON、C9H13ON、C10H15ON、C10H15ON、C9H13ON,则与麻黄素互为同分异构体的是C、D;结构相似,类别相同,在分子组成上相差一个或多个“-CH2-”原子团的有机物互称为同系物,麻黄素结构中含有一个苯环,一个亚氨基、一个醇羟基,
A.中无醇羟基,二者结构不同,与麻黄素不互为同系物,故A不符合题意;
B.中与麻黄素所含官能团相同,分子组成上相差一个“-CH2-”原子团,与麻黄素互为同系物,故B符合题意;
C.含有酚羟基,与麻黄素所含官能团不相同,结构不相似,与麻黄素不互为同系物,故C不符合题意;
D.与麻黄素分子式相同,互为同分异构体,不互为同系物,故D不符合题意;
E.含有酚羟基,与麻黄素所含官能团不相同,结构不相似,与麻黄素不互为同系物,故E不符合题意;
答案选B;
(5)甲烷是正正四面体结构,若分子中的四个H原子全部被Cl原子取代得到CCl4,还是有极性键构成的非极性分子。由于这些多卤代甲烷都是分子晶体构成的物质,沸点不同,因此可采取分馏的方法分离。
18. 9 C10H16 6 氢氧化钠乙醇溶液,加热 加成反应 、
【解析】
【分析】
(1)由碳碳双键为平面结构分析环戊二烯分子中最多共平面的原子数;
(2)金刚烷的分子中有6个CH2,4个CH结构,据此判断其分子式,其分子中的CH2基团有6个;
(3)反应①的产物为氯代环戊烷,反应②为氯代烃的消去反应,反应③为加成反应;
(4)能使溴的四氯化碳溶液褪色,应含有碳碳双键,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸,说明烃基位于对位位置。
【详解】
(1)C=C为平面结构,与双键碳直接相连的原子一定在同一平面内,则5个C和4个H在同一平面内,共9个原子共平面;
(2)由结构简式可知金刚烷的分子式为C10H16,分子中又6个CH2,其中4个被三个环共用;
(3)反应①的产物为氯代环戊烷,反应②为氯代烃的消去反应,应在氢氧化钠乙醇溶液,加热反应生成,反应③为加成反应;
(4)能使溴的四氯化碳溶液褪色,应含有碳碳双键,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸,说明烃基位于对位位置,且分子结构中含有一个甲基,则可能的结构有、。
19. 正四面体 分馏(或精馏) 3 、、 加成反应 CH2ClCH2ClHCl↑+CH2=CHCl↑ 消去反应
【解析】
【详解】
(1)四氯化碳的分子结构为正四面体结构,多卤代甲烷是沸点不同的互溶液体,分离这些多卤代甲烷的方法是分馏(或精馏);
(2) 三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,其有3种同分异构体(不考虑立体异构),写出其中任意两种的结构简式:、、;
(3) 反应①是乙烯与氯气反应生成1,2-二氯乙烷,碳碳双键变成碳碳单键,其反应类型为加成反应,反应②是1,2-二氯乙烷氯乙烯,化学方程式为CH2ClCH2ClHCl↑+CH2=CHCl↑,碳碳单键变成碳碳双键,其应类型为消去反应。
20. 9 C10H16 6 氯代环戊烷(一氯环戊烷) 加成反应
【解析】
【分析】
【详解】
试题分析:(1)C=C为平面结构,与双键碳直接相连的原子一定在同一平面内,则5个C和4个H在同一平面内,最多有9个原子共平面;
(2)由C原子形成4个共价键,由结构简式可知金刚烷的分子中有6个CH2,4个CH结构,分子式为C10H16;(3)由合成路线可知,反应①为光照条件下的取代反应,其产物名称为氯代环戊烷;反应③是烯烃的加成反应;
(4)由信息可知,碳碳双键的碳上含H原子被氧化为醛,则发生反应:;产物的结构简式:。
考点:考查有机物的合成,涉及有机物的官能团、碳链骨架等的变化。
一、选择题(共16题)
1.若NA为阿伏加德罗常数的值,下列说法正确的是
A.8.0 g含有的电子数为4.5NA
B.28 g乙烯和丁烯的混合物,含有原子总数为6NA
C.标准状况下,22.4 LCCl4含碳原子数目为NA
D.4.4 g C3H8所含共价键的数目为0.8NA
2.关于卤代烃的下列说法不正确的是
A.卤代烃不属于烃
B.卤代烃难溶于水,易溶于有机溶剂
C.有的卤代烃可用作有机溶剂
D.所有的卤代烃都可以发生消去反应生成相应的烯烃
3.下列有机反应中,C-H键未发生断裂的是
A.苯与浓硝酸、浓硫酸在加热的条件下反应 B.溴乙烷在氢氧化钠乙醇溶液中加热
C.乙醇与乙酸在浓硫酸加热条件下反应 D.苯酚与甲醛在浓盐酸、加热条件下反应
4.下列化学用语或图示表达不正确的是
A.HClO的结构式为:H-O-Cl B.CO2的电子式:
C.溴乙烷的分子模型: D.Na+的结构示意图:
5.下列根据实验操作和现象所得出的结论正确的是
选项 实验操作 实验现象 结论
A 向装有铁粉的三颈烧瓶中滴加苯和液溴的混合物,将产生的气体直接通入溶液 有浅黄色沉淀生成 可证明苯和液溴一定发生了取代反应
B 溴乙烷与KOH溶液混合加热后,再滴加溶液 无浅黄色沉淀 溴乙烷未水解
C 将乙醇和浓硫酸共热至后,将生成的气体通入酸性溶液中 溶液褪色 不能证明乙烯能使溶液褪色
D 在试管中加入的溶液,再加入溶液,最后加入滴某有机物,混合加热 无砖红色沉淀 该有机物不含醛基
A.A B.B C.C D.D
6.哪一个消除反应可以生成2-甲基戊-2-烯
A. B.
C. D.
7.为了检验氯丙烷中的氯元素,下列实验操作顺序正确的是
①加热煮沸 ②加入硝酸银溶液 ③取少量氯丙烷 ④加入足量的稀硝酸酸化 ⑤加入氢氧化钠溶液 ⑥冷却
A.③②①⑥ B.③④②⑥⑤① C.③⑤②④ D.③⑤①⑥④②
8.下列说法正确的是
A.与互为同分异构体的芳香族化合物有4种
B.若烯烃CnH2n中所有的碳原子一定共平面,则n可能大于6
C.若醇CnH2n+2O既不能发生催化氧化反应也不能发生消去反应,则n一定大于或等于13
D.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-CH2BrCOO-+H2O
9.下列实验方案设计、现象和结论都正确的是
实验目的 方案设计 现象和结论
A 检验CH3CH2Br在NaOH溶液中是否发生水解 将CH3CH2Br与NaOH溶液共热,冷却后,取少量溶液,加入AgNO3溶液 若有沉淀产生,则CH3CH2Br发生水解
B 比较Br2和I2的氧化性强弱 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置 若下层液体呈紫红色,则Br2的氧化性强于I2
C 检验Fe(NO3)2晶体是否氧化变质 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 若溶液变红,则Fe(NO3)2晶体已氧化变质
D 比较HNO2和CH3COOH电离出H+的能力 用pH试纸分别测CH3COONa溶液和NaNO2溶液的pH 若CH3COONa溶液的pH比NaNO2溶液的pH大,则HNO2电离出H+的能力比CH3COOH的强
A.A B.B C.C D.D
10.由下列实验操作及现象不能得出相应结论的是
实验操作 现象 结论
A 向烧瓶中加入2.0gNaOH和15mL无水乙醇,搅拌。再加入5mL1—溴丁烷和碎瓷片,微热。将产生的气体通入盛水的试管后,再用酸性高锰酸钾溶液进行检验 高锰酸钾溶液褪色 1—溴丁烷发生消去反应
B 向NaClO溶液中滴加酚酞试剂 先变红后褪色 NaClO发生了水解反应
C 向等浓度(c=0.01mol/L)NaCl和Na2CrO4混合液中滴加AgNO3稀溶液(已知AgCl和Ag2CrO4的溶度积常数分别为1.8×10-10,2×10-12) 出现白色沉淀(Ag2CrO4为黄色沉淀) Ag2CrO4的溶解度小于AgCl(以浓度计算)
D 室温,用pH试纸测定0.1mol L-1Na2SO3溶液和0.1mol L-1NaHSO3溶液的pH Na2SO3溶液pH约为10;NaHSO3溶液pH约为5 结合H+的能力: <
A.A B.B C.C D.D
11.下列叙述正确的是
A.检验溴乙烷中的卤原子:先加入NaOH溶液共热,再加AgNO3溶液,观察沉淀颜色
B.属于烯烃的同分异构体有5种(考虑顺反异构)
C.立方烷的六氯取代物有6种
D.和都可有6个原子处于同一直线上
12.下列实验操作能够达到实验目的的是
选项 实验目的 实验操作
A 探究浓度对反应速率的影响 向2支各盛有和酸性溶液的试管中,分别加入5滴记录溶液褪色所需的时间
B 探究淀粉溶液在稀硫酸加热条件下是否水解 取少量的水解液于试管中,先加适量的NaOH溶液,再滴入碘水,观察实验现象
C 检验溴乙烷中的溴元素 取适量溴乙烷于试管中,加入适量NaOH溶液并加热,冷却后加足量稀硝酸,再滴加溶液,观察现象
D 验证酸性: 用pH试纸分别测定同温度同浓度的溶液和NaClO溶液的pH
A.A B.B C.C D.D
13.下列实验方案不能达到实验目的是
实验目的 实验方案
A 证明溴乙烷发生消去反应有乙烯生成 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液
B 检验卤代烃中卤原子的种类 将溴乙烷与氢氧化钠溶液共热,取冷却后反应液滴加硝酸酸化后,滴加硝酸银溶液
C 验证乙炔能被酸性高锰酸钾溶液氧化 将电石与饱和食盐水反应生成的气体先通入足量硫酸铜溶液中,再通入酸性高锰酸钾溶液,观察溶液是否褪色
D 验证苯和液溴在的催化下发生取代反应 将反应产生的混合气体通入溶液中,观察是否有淡黄色沉淀生成
A.A B.B C.C D.D
14.称为环氧乙烷,它在一定条件下,能与氢化物发生加成反应,氢原子加到氧原子上,其他部分加到碳原子上。对下面环氧乙烷的衍生物的叙述中,不正确的是
A.在一定条件下能与水反应生成
B.在一定条件下能与水反应生成
C.在一定条件下可以合成甘油
D.加入AgNO3溶液能生成难溶于HNO3的白色沉淀
15.下表中实验操作能达到实验目的的是
实验操作 实验目的
A 向苯酚浓溶液中滴加少量稀溴水 观察白色沉淀
B 向待测液中加入酸性高锰酸钾溶液 鉴别苯、甲苯
C 向溴乙烷中加氢氧化钠溶液并加热,冷却后再加硝酸银溶液 检验溴乙烷中的溴原子
D 向铁粉中依次加入苯和溴水 制备少量溴苯
A.A B.B C.C D.D
16.有机小分子催化多氟代物的取代反应,机理如图所示,已知反应Ⅰ、反应Ⅱ和反应Ⅲ的活化能中,反应Ⅱ的活化能最大。下列说法不正确的
A.反应方程式为:+→+
B.2是催化剂,4和7都是反应中间体
C.5为时,1是
D.整个取代反应的反应速率主要由反应Ⅱ的速率决定
二、综合题(共4题)
17.完成下列各题:
(1)烃 A 的结构简式为,用系统命名法命名烃A:_________________________________________。
(2)某烃的分子式为 C5H12,核磁共振氢谱图中显示三个峰,则该烃的一氯代物有_______种,该烃的结构简式为 ______________________ 。
(3)聚氯乙烯是生活中常见的塑料。工业生产聚氯乙烯的一种工艺路线如下:
反应①的化学方程式是 ___________________________________________,反应类型为___________________,反应②的反应类型为 ____________________。
(4)麻黄素又称黄碱,是我国特定的中药材麻黄中所含有的一种生物碱。经科学家研究发现其结构如下:
下列各物质:
A . B .
C. D .
E.
与麻黄素互为同分异构体的是 ___________ (填字母,下同),互为同系物的是 ______。
(5)多氯代甲烷作为溶剂,其中分子结构为正四面体的是 ____________。工业上分离这些多卤代甲烷的方法是 _________________。
18.金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
请回答下列问题:
(1)环戊二烯分子中最多有____________个原子共平面;
(2)金刚烷的分子式为_______________,其分子中的CH2基团有_____________个;
(3)面是以环戊烷为原料制备环戊二烯的合成路线:
其中,反应②的反应试剂和反应条件_____________,反应③的反应类型是___________;
(4)A是二聚环戊二烯的同分异构体,A分子结构中有一个甲基,A能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸【提示:苯环上的烷基(一CH3,一CH2R,一CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基】,写出A所有可能的结构简式(不考虑立体异构):______________________________
19.卤代烃在工农业生产和人们的生活中具有广泛的应用。回答下列问题:
(1)四氯化碳(CCl4)可用作灭火剂,其分子结构为___形。多卤代甲烷可用工业上,分离这些多卤代甲烷的方法是___。
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,其有___种同分异构体(不考虑立体异构),写出其中任意两种的结构简式:___。
(3)聚氯乙烯是生活中常见的塑料。工业生产聚氯乙烯的一种工艺路线如下:
乙烯1,2-二氯乙烷氯乙烯聚氯乙烯
反应①的反应类型为___。反应②的化学方程式为___,应类型为___。
20.金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
请回答下列问题:
(1)环戊二烯分子中最多有___________个原子共平面;
(2)金刚烷的分子式为___________,其分子中的CH2基团有___________个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
其中,反应①的产物名称是_______________,反应③的反应类型是____________;
(4)已知烯烃能发生如下反应:
请写出下列反应产物的结构简式:
___________________________。
试卷第页,共页
参考答案:
1.B
【解析】
【分析】
【详解】
A.8.0 g的物质的量是n=,每个中含有10个电子,则0.5 mol中含有的电子数目为5NA,A错误;
B.乙烯和丁烯的最简式是CH2,其中含有3个原子,式量是14,则28 g乙烯和丁烯的混合物中含有最简式的物质的量是2 mol,其中含有原子的物质的量是6 mol,则含有的原子总数为6NA,B正确;
C.在标准状况下CCl4呈液态,不能使用气体摩尔体积进行有关计算,C错误;
D.4.4 g C3H8的物质的量是0.1 mol,由于在1个C3H8分子中含有10个共价键,则在0.1 mol C3H8中所含共价键的数目为NA,D错误;
故合理选项是B。
2.D
【解析】
【详解】
A.卤代烃分子中含有卤素原子,属于烃的衍生物,不属于烃,故A正确;
B.卤代烃具有有机物的通性,难溶于水,易溶于有机溶剂,故B正确;
C.有的卤代烃可用作有机溶剂,如四氯化碳、氯仿都是良好的有机溶剂,故C正确;
D.并不是所有的卤代烃都可以发生消去反应生成相应的烯烃,如一氯甲烷没有邻碳原子,不能发生消去反应,故D错误;
故选D。
3.C
【解析】
【分析】
【详解】
A.苯与浓硝酸、浓硫酸在加热的条件下反应生成硝基苯,C-H键断裂,A错误;
B.溴乙烷在氢氧化钠乙醇溶液中加热发生消去生成双键和HBr,C-H键断裂,B错误;
C.乙醇与乙酸在浓硫酸加热条件下反应生成乙酸乙酯,酸脱羟基醇脱H,C-H键没有断裂,C正确;
D.苯酚与甲醛在浓盐酸、加热条件下,苯酚中与羟基相邻的两个氢会与甲醛中的氧一起去一个水发生缩聚,C-H键断裂,D错误;
答案选C。
4.B
【解析】
【详解】
A.HClO中O原子分别与H原子和Cl原子形成共价键,故其结构式为H-O-Cl,故A正确;
B.二氧化碳中C原子和氧原子之间以双键结合,其电子式为,故B错误;
C.溴乙烷的结构简式为CH3CH2Br,其中Br原子半径大于C和H原子半径,其分子模型为,故C正确;
D.钠离子的核内有11个质子,核外有10个电子,结构示意图为,故D正确;
故选:B。
5.C
【解析】
【分析】
【详解】
A.挥发的溴及生成的HBr均与硝酸银反应,由操作和现象不能证明发生取代反应,故A错误;
B.KOH与硝酸银反应,应在酸性溶液中检验溴离子证明溴乙烷水解,故B错误;
C.挥发的醇及生成的乙烯均使酸性高锰酸褪色,由操作和现象不能证明乙烯能使KMnO4溶液褪色,故C正确;
D.NaOH不足,应在碱性溶液中检验-CHO,应使NaOH过量,故D错误;
故选:C。
6.D
【解析】
略
7.D
【解析】
【详解】
1-氯丙烷不溶于水,在酸性或碱性条件下水解,其中碱性条件下水解程度较大,碱性条件下水解生成氯离子,然后在用硝酸酸化,加入硝酸银进行检验,以排除氢氧根离子的干扰,操作步骤为:③⑤①⑥④②;
答案选D。
8.C
【解析】
【分析】
【详解】
A.与互为同分异构体的芳香族化合物有5种:、、、 、,A错误;
B.若烯烃CnH2n中所有的碳原子一定共平面,C原子数最多6个,n6,乙烯是平面结构,其中的4个H原子被4个甲基取代,其中6个C原子共面,B错误;
C.若醇CnH2n+2O既不能发生催化氧化反应也不能发生消去反应,与羟基相连的C原子上没有H原子,与羟基相连的C原子的邻C上也没有H原子,即这两类C原子上的H原子被烷基取代,符合的结构式为:,则n一定大于或等于13,C正确;
D.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+2OH-CH2OCOO-+Br-+H2O,D错误;
答案选。
9.B
【解析】
【分析】
【详解】
A.检验方法应为将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,加入硝酸酸化后再加入AgNO3溶液,观察是否产生淡黄色沉淀,故A错误;
B.碘单质可使淀粉溶液变蓝,碘离子不可,故B正确;
C.硝酸亚铁溶液溶于稀硫酸中,则溶液中相当于存在硝酸,硝酸具有强氧化性,氧化亚铁离子为铁离子,再加入KSCN溶液,则溶液变红色,不能证明原固体是否变质,故C错误;
D.由于没有给出醋酸钠和亚硝酸钠的起始浓度,所以不能根据盐溶液的pH判断醋酸根离子和亚硝酸根的水解强弱,即不能得出两种酸谁强谁弱,故D错误;
故选B。
10.C
【解析】
【详解】
A.向烧瓶中加入2.0gNaOH和15mL无水乙醇,搅拌。再加入5mL1—溴丁烷和碎瓷片,微热。将产生的气体通入盛水的试管除去乙醇蒸气后,再用酸性高锰酸钾溶液进行检验,高锰酸钾溶液褪色,说明1—溴丁烷发生消去反应生成1-丁烯,选项A正确;
B.NaClO+H2O HClO+NaOH,水解生成NaOH使用酚酞变红,HClO具有漂白性又使红色褪去,选项B正确;
C. AgCl的Ksp=1.8×10-10,Ag2CrO4的Ksp为2×10-12,则S(AgCl)===1.34×10-5,而S(Ag2CrO4)===7.94×10-5,所以AgCl的溶解度小于Ag2CrO4,选项C错误;
D.测定pH可知Na2SO3溶液的碱性强,NaHSO3溶液电离显酸性,则结合H+的能力比的弱,选项D正确;
答案选C。
11.D
【解析】
【分析】
【详解】
A.检验溴乙烷中的卤原子的方法为先加入氢氧化钠溶液共热发生水解反应,加入过量稀硝酸中和氢氧化钠溶液后,再加人硝酸银溶液,观察沉淀颜色为淡黄色,故A错误;
B.C5H10属于烯烃的同分异构体有1—戊烯、2—戊烯、2—甲基—1—戊烯、2—甲基—2—戊烯、3—甲基—1—戊烯,其中2—戊烯存在顺反异构,则C5H10属于烯烃的同分异构体共有6种,故B错误;
C.立方烷的二氯取代物和六氯取代物的数目相同,二氯代物有两个氯原子分别位于同一条棱上、面对角线上和体对角线上3种结构,则立方烷的六氯取代物的数目为3,故C错误;
D.和中处于红线上的4个碳原子和2个氢原子可能处于同一直线上,则两者处于同一直线上的原子数目都为6,故D正确;
故选D。
12.C
【解析】
【详解】
A.高锰酸钾过量,溶液不褪色,A项错误;
B.碘遇淀粉变蓝,若实验中淀粉过量或水解不完全,加入碘水反应后的溶液会变蓝,不能证明淀粉是否水解,检验淀粉在稀硫酸催化条件下是否发生水解,取少量的水解液于试管中,应先加入碱中和稀硫酸,再加入少量新制氢氧化铜悬浊液,加热,观察是否出现砖红色沉淀,若产生砖红色沉淀,则证明淀粉水解,B项错误;
C.取适量溴乙烷于试管中,加入适量NaOH溶液并加热,溴乙烷发生水解反应生成乙醇和NaBr,冷却后加足量稀硝酸,再滴加溶液,生成淡黄色沉淀,C项正确;
D.NaClO具有漂白性,不能用pH试纸测定其水溶液的碱性强弱,D项错误;
答案选C。
13.D
【解析】
【分析】
【详解】
A.溴乙烷和NaOH的乙醇溶液,发生消去反应,乙烯与溴发生加成反应,溴水褪色,则该实验可验证乙烯的生成,故A正确;
B.溴乙烷与氢氧化钠溶液共热,水解后检验溴离子,应在酸性条件下,则取冷却后反应液滴加硝酸酸化后,再滴加硝酸银溶液可检验卤素原子种类,故B正确;
C.电石与饱和食盐水反应生成的乙炔中混有硫化氢,先通入足量硫酸铜溶液中,再通入酸性高锰酸钾溶液,观察溶液是否褪色,能说明乙烯被氧化,故C正确;
D.发生取代反应生成HBr,则反应产生的混合气体先通入溴的四氯化碳溶液再通入溶液中,观察是否有淡黄色沉淀生成,可说明取代反应,故D错误;
故选C。
14.D
【解析】
【分析】
【详解】
A.与水加成反应可生成,A正确;
B.在氢氧化钠溶液中加热水解就可以生成,B正确;
C.与水加成反应可生成,再在氢氧化钠溶液中加热水解就可以生成甘油,C正确;
D.是一种共价化合物,不可能电离出Cl-,因此不能与AgNO3溶液反应,D错误;
故选D。
15.B
【解析】
【分析】
【详解】
A.向苯酚浓溶液中滴加少量稀溴水生成三溴苯酚,三溴苯酚易溶于苯酚,观察不到白色沉淀,故A错误;
B.甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色,可用酸性高锰酸钾鉴别苯和甲苯,故B正确;
C.检验溴乙烷中的溴原子,应向水解后的液体中先加稀硝酸中和氢氧化钠,再加硝酸银溶液,故C错误;
D.苯和液溴在铁作催化剂的条件下发生取代反应生成溴苯和溴化氢,故D错误;
选B。
16.C
【解析】
【详解】
A.由图示知,物质2、4、7在过程中循环使用,故该反应相当于物质3与5反应生成1和6,对应方程式为:+→+,A正确;
B.物质2与物质3反应生成中间产物4,4与物质5反应生成中间产物7,物质7发生反应Ⅲ生成物质1和2,物质2在反应前后没变,可看作催化剂,4、7为中间产物,B正确;
C.若物质5为,即结构-X为,则物质1为:,C错误;
D.相同条件下,反应活化能越大,普通分子变成活化分子越难,反应速率越慢,由于反应Ⅱ活化能最大,故整个过程的反应速率由反应Ⅱ速率决定,D正确;
故答案选C。
17. 2,2,6-三甲基-4-乙基辛烷 3 CH3CH2CH2CH2CH3 H2C=CH2+Cl2→CH2ClCH2Cl 加成反应 消去反应 CD B 四氯化碳 分馏
【解析】
【详解】
(1)烃 A 的结构简式为,主链为8个碳原子,离支链最近的一端对碳原子编号,2号碳上有两个甲基,6号碳上有一个甲基,4号碳上有一个乙基,用系统命名法命名,烃A的名称为2,2,6-三甲基-4-乙基辛烷;
(2)某烃的分子式为 C5H12,核磁共振氢谱图中显示三个峰,说明分子结构中有三种不同环境的氢原子,则该烃的一氯代物有3种,该烃的结构简式为CH3CH2CH2CH2CH3;
(3)反应①为乙烯与氯气发生加成反应生成1,2-二氯乙烷,反应的方程式为H2C=CH2+Cl2→CH2ClCH2Cl;反应②为1,2-二氯乙烷加热480~530℃生成氯乙烯,发生消去反应;
(4)分子式相同而结构不同的有机物互称为同分异构体,根据结构简式可知,麻黄素的分子式为C10H15ON,选项中A、B、C、D、E的分子式分别为C11H17ON、C9H13ON、C10H15ON、C10H15ON、C9H13ON,则与麻黄素互为同分异构体的是C、D;结构相似,类别相同,在分子组成上相差一个或多个“-CH2-”原子团的有机物互称为同系物,麻黄素结构中含有一个苯环,一个亚氨基、一个醇羟基,
A.中无醇羟基,二者结构不同,与麻黄素不互为同系物,故A不符合题意;
B.中与麻黄素所含官能团相同,分子组成上相差一个“-CH2-”原子团,与麻黄素互为同系物,故B符合题意;
C.含有酚羟基,与麻黄素所含官能团不相同,结构不相似,与麻黄素不互为同系物,故C不符合题意;
D.与麻黄素分子式相同,互为同分异构体,不互为同系物,故D不符合题意;
E.含有酚羟基,与麻黄素所含官能团不相同,结构不相似,与麻黄素不互为同系物,故E不符合题意;
答案选B;
(5)甲烷是正正四面体结构,若分子中的四个H原子全部被Cl原子取代得到CCl4,还是有极性键构成的非极性分子。由于这些多卤代甲烷都是分子晶体构成的物质,沸点不同,因此可采取分馏的方法分离。
18. 9 C10H16 6 氢氧化钠乙醇溶液,加热 加成反应 、
【解析】
【分析】
(1)由碳碳双键为平面结构分析环戊二烯分子中最多共平面的原子数;
(2)金刚烷的分子中有6个CH2,4个CH结构,据此判断其分子式,其分子中的CH2基团有6个;
(3)反应①的产物为氯代环戊烷,反应②为氯代烃的消去反应,反应③为加成反应;
(4)能使溴的四氯化碳溶液褪色,应含有碳碳双键,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸,说明烃基位于对位位置。
【详解】
(1)C=C为平面结构,与双键碳直接相连的原子一定在同一平面内,则5个C和4个H在同一平面内,共9个原子共平面;
(2)由结构简式可知金刚烷的分子式为C10H16,分子中又6个CH2,其中4个被三个环共用;
(3)反应①的产物为氯代环戊烷,反应②为氯代烃的消去反应,应在氢氧化钠乙醇溶液,加热反应生成,反应③为加成反应;
(4)能使溴的四氯化碳溶液褪色,应含有碳碳双键,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸,说明烃基位于对位位置,且分子结构中含有一个甲基,则可能的结构有、。
19. 正四面体 分馏(或精馏) 3 、、 加成反应 CH2ClCH2ClHCl↑+CH2=CHCl↑ 消去反应
【解析】
【详解】
(1)四氯化碳的分子结构为正四面体结构,多卤代甲烷是沸点不同的互溶液体,分离这些多卤代甲烷的方法是分馏(或精馏);
(2) 三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,其有3种同分异构体(不考虑立体异构),写出其中任意两种的结构简式:、、;
(3) 反应①是乙烯与氯气反应生成1,2-二氯乙烷,碳碳双键变成碳碳单键,其反应类型为加成反应,反应②是1,2-二氯乙烷氯乙烯,化学方程式为CH2ClCH2ClHCl↑+CH2=CHCl↑,碳碳单键变成碳碳双键,其应类型为消去反应。
20. 9 C10H16 6 氯代环戊烷(一氯环戊烷) 加成反应
【解析】
【分析】
【详解】
试题分析:(1)C=C为平面结构,与双键碳直接相连的原子一定在同一平面内,则5个C和4个H在同一平面内,最多有9个原子共平面;
(2)由C原子形成4个共价键,由结构简式可知金刚烷的分子中有6个CH2,4个CH结构,分子式为C10H16;(3)由合成路线可知,反应①为光照条件下的取代反应,其产物名称为氯代环戊烷;反应③是烯烃的加成反应;
(4)由信息可知,碳碳双键的碳上含H原子被氧化为醛,则发生反应:;产物的结构简式:。
考点:考查有机物的合成,涉及有机物的官能团、碳链骨架等的变化。
