2021-2022学年下学期高中化学鲁科版(2019)选择性必修3第1章第2节有机化合物的结构与性质——提升训练(word 含解析)
文档属性
| 名称 | 2021-2022学年下学期高中化学鲁科版(2019)选择性必修3第1章第2节有机化合物的结构与性质——提升训练(word 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 311.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-14 00:00:00 | ||
图片预览




文档简介
第1章有机化合物的结构与性质—烃第2节有机化合物的结构与性质——提升训练2021-2022学年高中化学鲁科版(2019)选择性必修3
一、选择题(共16题)
1.下列各组物质,不互为同分异构体的是
A.CH3CH2CH2CH3和CH3CH(CH3)2 B.CH3CH=CH2CH2=CHCH3
C.CH≡CCH2CH3和CH2=CH-CH=CH2 D.CH3CH2OH和CH3OCH3
2.分子式为C8H8O2的芳香族化合物,能发生水解反应的结构有
A.4种 B.5种 C.6种 D.7种
3.如图是几种常见高度对称烷烃的分子碳架结构,这三种烷烃的一氯取代产物的同分异构体数目分别是
A.1种,1种,1种 B.1种,1种,2种 C.2种,3种,6种 D.2种,3种,8种
4.下列各组物质不互为同分异构体的是
A.和 B.和
C.和 D. 和
5.金刚烷(C10H16)是一种重要的脂肪烷烃,其结构高度对称,如图所示。金刚烷能与卤素发生取代反应,其中二氯金刚烷(C10H14Cl2)的同分异构体数目是
A.4种 B.6种
C.8种 D.10种
6.三位分别来自法国、美国、荷兰的科学家因研究“分子机器的设计与合成”而获得2016年诺贝尔化学奖。纳米分子机器日益受到关注,机器的“车轮”常用组件如图。
下列说法不正确的是
A.①②③④均属于烃
B.②与苯是同分异构体
C.③和金刚石是同素异形体
D.①②④的一氯代物分别为3种、1种、2种
7.下列说法正确的是
A.和互为同位素
B.CH2O与C2H4O互为同系物
C.NH4CNO与CO(NH2)2互为同分异构体
D.PCl3和PCl5互为同素异形体
8.分子式为的有机物共有(不含立体异构)
A.5种 B.6种 C.7种 D.8种
9.化合物M是某种药物合成的中间体,其结构简式如图所示,下列关于化合物M的说法不正确的是
A.属于芳香烃
B.不溶于水,且密度比水小
C.既能发生加成反应,又能发生取代反应
D.能使酸性溶液褪色
10.下列化学用语正确的是
A.丙烷分子的分子式:CH3CH2CH3
B.对硝基甲苯的结构简式:
C.2-乙基-1,3-丁二烯分子的键线式:
D.聚丙烯的结构简式:
11.分子式C4H10O的同分异构体有
A.6种 B.7种 C.8种 D.9种
12.下列说法正确的是
A.和互为同位素
B.金刚石和富勒烯互为同素异形体
C.乙醚和乙醇互为同分异构体
D.和互为同系物
13.下列说法不正确的是
A.CH2=CH—CHO、CH≡C—CH2OH互为同分异构体,与足量H2加成后为同一物质
B.CH3CH2NO2与H2NCH2COOH互为同分异构体
C.符合通式CnH2n+2的不同烃一定属于同系物
D.C5H12同分异构体中新戊烷沸点最低
14.下列说法不正确的是
A.乙苯和对二甲苯互为同分异构体
B.石墨烯和C60互为同素异形体
C.H+、H-、D属于同种元素
D.Na2O、Na2O2互为同系物
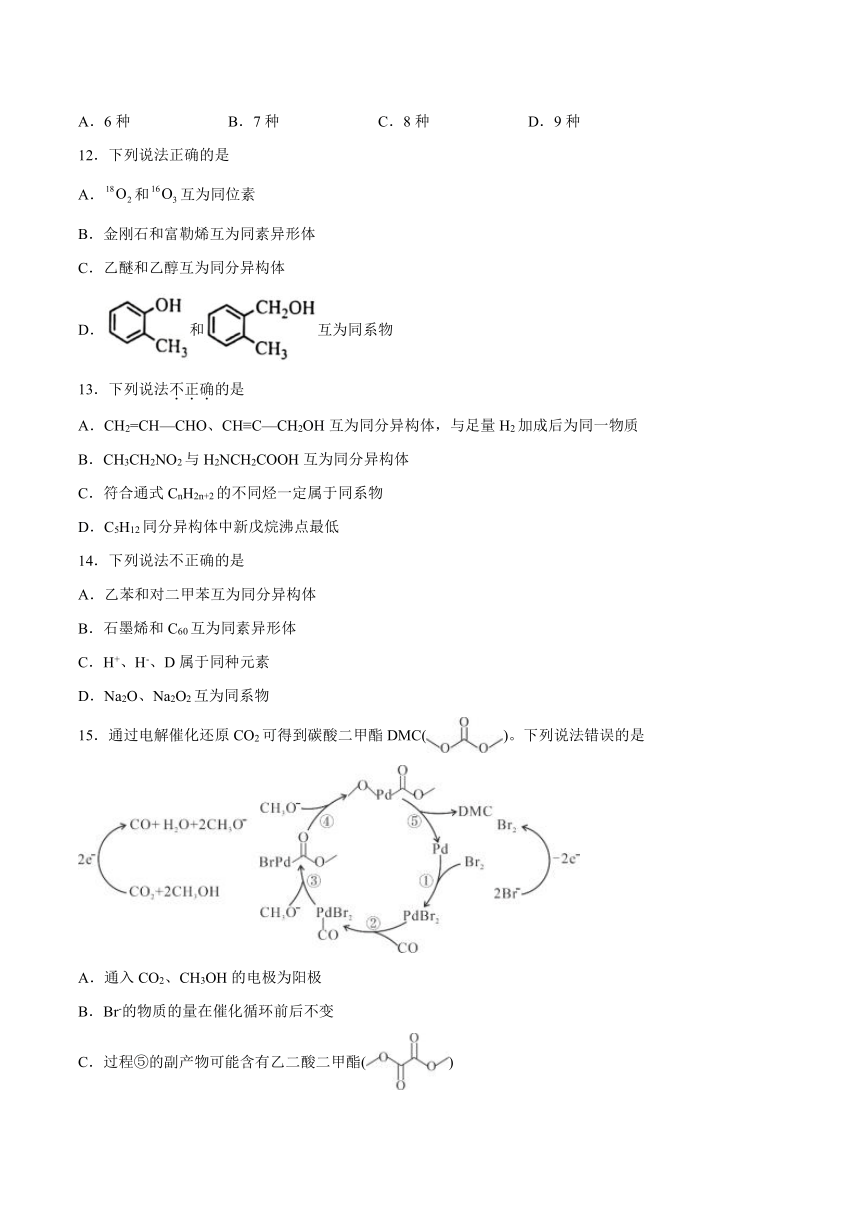
15.通过电解催化还原CO2可得到碳酸二甲酯DMC()。下列说法错误的是
A.通入CO2、CH3OH的电极为阳极
B.Br-的物质的量在催化循环前后不变
C.过程⑤的副产物可能含有乙二酸二甲酯()
D.该电解催化过程的总反应方程式为:CO2+2CH3OH+H2O
16.NA为阿伏加德罗常数的值,下列有关说法正确的是
A.500mL2mol·L-1FeCl3溶液中含有的Fe3+的数目为NA
B.室温下pH=11的Na2CO3溶液,由水电离出的OH-数目为0.001NA
C.0.25molZn与一定量浓硫酸反应后完全溶解,生成气体的分子数为0.25NA
D.46g有机物C2H6O中含有的极性共价键的数目一定为7NA
二、综合题(共6题)
17.按要求回答问题
(1)给有机物命名, 名称________________________。
(2) 写出符合分子式C3H8O的有机物的结构简式(如乙酸结构简式为CH3COOH):CH3CH2CH2OH,__________________________________________________。
(3)配平下列反应离子方程式:
As2S3 + H2O + NO3- AsO + SO + NO↑ + (未配平)
___________________________________________________________
(4)某地污水中的有机污染物主要成分是三氯乙烯(C2HCl3),向污水中加入KMnO4(其还原产物为MnO2)可将三氯乙烯除去,其生成物不污染环境,写出该反应的化学方程式:_____。
(5)根据氧化还原反应:2 Fe3+ + Cu = 2Fe2+ +Cu2+ ,设计一个盐桥原电池。画出原电池结构图(需注明电极、电解质溶液、盐桥)。___
18.乙苯(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是:
C8H10(g) C8H8(g)+H2(g) ΔH=+125 kJ·mol-1
Ⅰ.某温度下,将0.40 mol乙苯充入1 L真空密闭容器中发生上述反应,测定不同时间该容器内物质的物质的量,得到数据见下表:
时间/min 0 10 20 30 40
n(C8H10)/mol 0.40 0.30 0.26 n2 n3
n(C8H8)/mol 0.00 0.10 n1 0.16 0.16
(1)当反应进行到20 min时,该段时间内H2的平均生成速率是__________。
(2)该温度下,反应从开始到平衡的过程中共从环境吸收__________kJ热量。
(3)若保持反应条件不变,用0.40 mol H2(g)和0.40 mol C8H8(g)合成C8H10(g),当有25 kJ热量放出时,该反应中H2的转化率是______,此时该反应的方向是________(填“正向” 或“ 逆向”)。
Ⅱ.氢化热是指在一定条件下,1 mol不饱和化合物加氢时放出的热量,表中是环己烯(g)、1,3- 环己二烯(g)和苯的氢化热数据:
物质 +H2 +2H2 +3H2
氢化热(kJ/mol) 119.7 232.7 208.4
(4)1,3 -环己二烯的稳定性________(填“大于”“小于”或“等于”)苯。
(5)某有机物是苯的同分异构体,其分子中的碳碳键角只有60度和90度两种。请写出这种有机物的键线式结构________,它在核磁共振氢谱上会产生________个吸收峰 。
(6)与环己烯互为同分异构体的炔烃共有________种(不考虑立体异构)。
19.有机化学基础填空题:
⑴具有复合官能团的复杂有机物中官能团具有各自的独立性,在不同条件下所发生的化学反应可分别从各官能团讨论。根据上图回答:该物质具有的官能团是_______________、_____________(填化学式),所以该物质即可以归为_____________类又可以归为____________类(填有机物的类别)。
⑵写出下列化合物的名称或结构简式:
①结构简式为
此烃的名称为__________________
②结构简式为此烃的名称为_______________
③2,4-二甲基已烷的结构简式为_________________
20.(1)现有下列各化合物:
A.CH3CH2CH2CHO和;B.和;C.和;D.CH3CH2C≡CH和CH2=CH-CH=CH2;E.和;F.戊烯和环戊烷
①上述各组化合物属于同系物的是____,属于同分异构体的是_____填入编号。
②根据官能团的特点可将C中两化合物划分为____类和____类。
(2)写出下列有机化合物含氧官能团的名称____。
(3)用系统命名法命名 __。
21.(1)在下列物质中互为同分异构体的有___;互为同素异形体的有___;互为同系物的是___(填序号)。
①2—甲基丁烷②CH3—CH2—CH3③CH3CH2CH2OH④CH3—Cl⑤白磷⑥CH3—O—CH2CH3⑦红磷⑧CH3CH2—Cl
(2)已知有机物:甲:,乙:,丙:。
①请写出甲中含氧官能团的名称:___、___。
②乙中饱和碳原子有___个;丙中一定在同一个平面上的碳原子有___个;
③请判别上述哪些化合物互为同分异构体:___。
(3)某有机物A的结构简式为,该烃用系统命名法命名为:___;有机物A中共有__个手性碳原子;若该有机物A是由烯烃和1molH2加成得到的,则原烯烃的结构有___种。
22.请按要求填空:
(1)简单原子的原子结构如图:
① ② ③
其中“●”表示质子或电子,“○”表示中子。则下列有关①②③的叙述正确的是___________(填标号)。
A.①②③是三种不同的核素 B.①②③具有相同的质量数
C.①②③互为同位素 D.①②③是三种化学性质不同的粒子
(2)的质子数为___________,中子数为___________,电子数为___________,该元素在元素周期表中的位置是第___________周期___________族,该元素的最高价氧化物对应水化物的化学式是___________
(3)1828年,德国化学家维勒通过蒸发氰酸铵()水溶液得到尿素[]。
①氰酸铵和尿素之间的关系是___________(填标号)。
A.同位素B.同素异形体C.同分异构体D.同系物
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为___________。
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为___________。
试卷第页,共页
参考答案:
1.B
【解析】
【分析】
【详解】
A.CH3CH2CH2CH3和CH3CH(CH3)2分子式均为C4H10,分子式相同,结构不同,互为同分异构体,A不符题意;
B.CH3CH=CH2和CH2=CHCH3均为丙烯,为同一种物质,B不符题意;
C.CH≡CCH2CH3和CH2=CH-CH=CH2分子式均为C4H6,分子式相同,结构不同,互为同分异构体,C不符题意;
D.CH3CH2OH和CH3OCH3分子式均为C2H6O,分子式相同,结构不同,互为同分异构体,D不符题意;
答案选B。
2.C
【解析】
【分析】
【详解】
含酯基能发生水解反应,属于芳香族化合物说明含有苯环,则取代基为-C2H3O2,符合条件的有:、、、共6种,故选:C。
3.B
【解析】
【分析】
【详解】
正四面体烷分子中氢原子完全等同,一氯代物只有1种;立方烷分子中氢原子完全等同,一氯代物只有1种;金刚烷分子中氢原子有两种类型,其一氯代物有2种,B项正确。
故选B。
4.C
【解析】
【分析】
同分异构体是指分子式相同,但结构不同的化合物,同分异构体包含碳链异构、官能团异构、位置异构等,据此解答。
【详解】
A.和的分子式都为CH4N2O,二者结构不同,属于同分异构体,故A不选;
B.和的分子式都为C2H6O,二者结构不同,属于同分异构体,故B不选;
C.的分子式为C3H6O2,的分子式为C3H4O2,二者分子式不同,不互为同分异构体,故C选;
D. 和的分子式都为C7H8O,二者结构不同,属于同分异构体,故D不选;
答案选C。
5.B
【解析】
【详解】
金刚烷有2种等效氢,一氯取代物有2种:和,有3种等效氢:,对应二氯代物有3种;有4种等效氢:,对应的二氯代物有4种;两种情况中Cl位于邻位的情况重复,因此共有3+4-1=6种;
选B。
6.A
【解析】
【分析】
【详解】
A.③为富勒烯只含有碳原子,不属于烃,A项错误;
B.②的分子式为C6H6,与苯的分子式相同,结构不同,二者互为同分异构体,B项正确;
C.③和金刚石均为C元素的单质,二者互为同素异形体,C项正确;
D.①中有3种氢原子,一氯代物有3种,②中有1种氢原子,一氯代物有1种,④中含有2种氢原子,一氯代物有2种,D项正确;
答案选A。
7.C
【解析】
【详解】
A.是原子,而是离子,因此二者不能互为同位素,A错误;
B.CH2O表示甲醛,C2H4O表示的物质可能表示乙醛CH3CHO,也可能为乙烯醇CH2=CH-OH,因此二者不一定是同系物,B错误;
C.NH4CNO与CO(NH2)2分子式相同,结构不同,故二者互为同分异构体,C正确;
D.PCl3和PCl5是P与Cl两种元素形成的两种不同的化合物,二者不是单质,因此它们不能互为同素异形体,D错误;
故合理选项是C。
8.C
【解析】
【分析】
【详解】
分子式为的有机物有Cl2C=CHCH3、ClCH=CClCH3、ClCH=CHCH2Cl、CH2=CClCH2Cl、CH2=CHCHCl2、、,共7种,故选C;
9.A
【解析】
【详解】
A.化合物M除了碳、氢元素外还含有氧元素,属于烃的衍生物,A错误;
B.由化合物M的结构可知含有酯基,其不溶于水,且密度比水小,B正确;
C.化合物M中含碳碳双键和酯基,所以既能发生加成反应。又能发生取代反应,C正确;
D.化合物M中含碳碳双键,所以能使酸性溶液褪色,D正确;
答案选A。
10.C
【解析】
【详解】
A.CH3CH2CH3为丙烷的结构简式,分子式为C3H8,故A错误;
B.对硝基甲苯中硝基和甲基处于对位的位置,且硝基的N原子与苯环相连,其结构简式是,故B错误;
C.2-乙基-1,3-丁二烯的结构简式为,键线式中用短线“-”表示化学键,端点、交点表示碳原子,C、H原子不标出,则2-乙基-1,3-丁二烯的键线式为,故C正确;
D.丙烯发生加聚反应生成聚丙烯,其结构简式为,故D错误;
故选C。
11.B
【解析】
【分析】
【详解】
分子式C4H10O的同分异构体有醇类和醚类,醇类有CH3CH2CH2CH2OH、CH3CH2CH(CH3)OH、(CH3)2CHCH2OH、C(CH3)3OH,醚类有CH3OCH2CH2CH3,CH3CH2OCH2CH3,CH3OCH(CH3)2,共7种,选B。
12.B
【解析】
【分析】
【详解】
A.和是由同位素原子构成的分子,而不是原子,因此二者不能互为同位素,A错误;
B.金刚石和富勒烯是C元素形成的不同性质的单质,二者互为同素异形体,B正确;
C.乙醚结构简式是C2H5OC2H5,分子式是C4H10O;乙醇结构简式是CH3CH2OH,分子式是C2H6O,二者的分子式不相同,因此不能互为同分异构体,C错误;
D.羟基直接连接在苯环上,属于酚;羟基连接在侧链上,属于芳香醇,因此二者是不同类别的物质,不能互为同系物,D错误;
故合理选项是B。
13.C
【解析】
【详解】
A.CH2=CH-CHO、CH≡C-CH2OH的分子式相同而结构不同,故互为同分异构体,而加成后均生成CH3CH2CH2OH,是同一种物质,故A正确;
B.分子式相同而结构不同的化合物间互为同分异构体,故CH3CH2NO2与H2NCH2COOH互为同分异构体,故B正确;
C.符合通式CnH2n+2的不同烃,若n相同时属同分异构体,不属于同系物,故C错误;
D.互为同分异构体的烷烃,支链越多,则熔沸点越低,故新戊烷的沸点最低,故D正确;
故选:C。
14.D
【解析】
【分析】
【详解】
A.乙苯和对二甲苯只是甲基位置不相同,分子式相同互为同分异构体,A正确;
B.石墨烯和C60均为单质,且组成元素均为C元素,故互为同素异形体,B正确;
C.H+、H-、D属于同种元素都是氢元素,C正确;
D.Na2O、Na2O2结构不相似,且不相差n个-CH2,故不互为同系物,D错误;
答案选D。
15.A
【解析】
【分析】
【详解】
A.通入的CO2得到电子生成CO,发生还原反应,所以通入CO2、CH3OH的电极为阴极,故A错误;
B.Br-在阳极失去电子生成Br2,Br2参与反应,反应过程中Br2又转化为Br-,所以Br-的物质的量在催化循环前后不变,故B正确;
C.过程⑤中的 在连有碳氧双键的碳原子和Pb之间断键生成DMC,断键后生成的-COOCH3可以两两结合生成乙二酸二甲酯,故C正确;
D.该电解过程是CO2和甲醇反应最终生成DMC和水的反应,总反应方程式为:CO2+2CH3OH +H2O,故D正确;
故选A。
16.C
【解析】
【分析】
【详解】
A.500mL2mol·L-1FeCl3溶液中溶质的物质的量为1mol,但由于Fe3+发生水解,所以溶液中含有的Fe3+的数目小于NA,A错误;
B.溶液体积未知,无法计算由水电离出的OH-数目,B错误;
C.1mol锌和浓硫酸反应生成1mol二氧化硫,1molZn和稀硫酸反应生成1mol氢气,因此0.25molZn与一定量浓硫酸反应后完全溶解,生成气体的分子数为0.25NA,C正确;
D.C2H6O不一定是乙醇,也可能是二甲醚,所以46g有机物C2H6O中含有极性共价键的数目不一定为7NA,D错误;
答案选C。
17. 2-甲基-2丁烯 CH3CH (OH)CH3,CH3-O-CH2CH3 3As2S3+4H2O+28NO3-=6AsO43-+ 9SO42-+28NO↑ +8H+ C2HCl3+2KMnO4 =2CO2↑+2MnO2+HCl+KCl (或其他合理答案)
【解析】
【详解】
(1) 名称2-甲基-2丁烯;
(2) CH3CH2CH2OH可能的结构简式有CH3CH (OH)CH3,CH3-O-CH2CH3;
(3)反应中 ,As元素化合价由+3价升高为+5价,S元素化合价由 2价升高为+6价,化合价共升高2×(5 3)+3×[6 ( 2)]=28, ,N元素化合价由+5价降低为+2价,化合价共降低3价,故化合价升降最小公倍数为84,故 系数为3, 系数为4,根据原子守恒可知, 系数为6, 系数为9,NO系数为28,根据电荷守恒可知,缺项为H+,故H+系数为8,由原子守恒可知,故H2O的系数为4,配平后离子方程式为:3As2S3+4H2O+28NO3-=6AsO43-+ 9SO42-+28NO↑ +8H+;
(4)由题意可知:KMnO4溶液与三氯乙烯反应,产物有 , ,依据原子个数守恒可知其余产物为:KCl,HCl,该反应为氧化还原反应, ,Mn元素由+7价→+4价,一个KMnO4得3个电子;C2HCl3→CO2,C元素由+1价→+4价,一个C2HCl3失去6个电子,依据得失电子守恒可知反应的方程式为:C2HCl3+2KMnO4 =2CO2↑+2MnO2+HCl+KCl;
(5)根据氧化还原反应:2 Fe3+ + Cu = 2Fe2+ +Cu2+ ,依据原电池原理负极失去电子发生氧化反应,正极得到电子发生还原反应,画出结构图如下:
。
18. 0.007 mol·L-1·min-1 20 50% 正向 小于 1 7
【解析】
【详解】
(1)当反应进行到20 min时消耗乙苯0.40mol-0.26mol=0.14mol,根据方程式可知生成氢气是0.14mol,浓度是0.14mol/L,所以该段时间内H2的平均生成速率是0.14mol/L÷20min=0.007 mol·L-1·min-1。
(2)根据表中数据可知平衡时生成苯乙烯是0.16mol,所以该温度下,反应从开始到平衡的过程中共从环境吸收0.16mol×125 kJ·mol-1=20kJ热量。
(3)当有25 kJ热量放出时,消耗氢气是25 kJ÷125 kJ·mol-1=0.2mol,所以氢气的转化率是0.2/0.4×100%=50%,此时该反应的方向是正向;
(4)根据题干信息可知①C6H8+2H2→C6H12 △H=-232.7kJ/mol,②C6H6+3H2→C6H12 △H=-208.4kJ/mol,依据盖斯定律②-①得到:C6H6+H2→C6H8 △H=+24.3kJ/mol,即苯转化为1,3 环己二烯吸热,因此苯的能量低于1,3 环己二烯,所以苯的稳定性强;
(5)某有机物是苯的同分异构体,其分子中的碳碳键角只有60度和90度两种,所以这种有机物的键线式结构为,它在核磁共振氢谱上会产生1个吸收峰。
(6)与环己烯互为同分异构体的炔烃共有CH≡CCH2CH2CH2CH3、CH3C≡CCH2CH2CH3、CH3CH2C≡CCH2CH3、CH≡CCH2CH(CH3)2、CH≡CCH(CH3)CH2CH3、CH≡CC(CH3)3、CH3C≡CCH(CH3)2,共计7种。
19. —COOH —CHO 羧酸 醛 3-甲基-2-乙基-1-戊烯 1, 2—二甲基—4—乙基苯
【解析】
【详解】
(1)有机物含有的官能团有羧基、酚羟基和醛基,所以这个化合物可看作羧酸类和醛类;
(2)①的最长碳链含有5个碳原子,为戊烯,在3号碳原子上有一个甲基,在2号碳原子上有一个乙基,命名为:3-甲基-2-乙基-1-戊烯;
②有苯环的,命名时可以依次编号命名,命名为:对甲基乙苯或4-甲基乙基苯;
③根据2,4-二甲基已烷的名称可知,在主链上有6个碳原子,在2号和4号碳上各有一个甲基,结构简式为。
20. BE AD 酚 醇 酯基、羟基、羧基 3,4,5—三甲基庚烷
【解析】
【分析】
【详解】
①B中,和都属于氨基酸,但分子式不同,二者属于同系物;E 中,和都属于二元饱和羧酸,但分子式不同,二者属于同系物,所以上述各组化合物属于同系物的是BE。A中,CH3CH2CH2CHO和的分子式相同、结构不同;D中,CH3CH2C≡CH和CH2=CH-CH=CH2的分子式相同、结构不同,所以属于同分异构体的是AD。答案为:BE;AD;
②根据官能团的特点,C中含有酚羟基,含有醇羟基,所以两化合物划分为酚类和醇类。答案为:酚;醇;
(2) 中含氧官能团为-OOC-、-OH、-COOH,名称分别为酯基、羟基、羧基。答案为:酯基、羟基、羧基;
(3)有机物的主链碳原子有7个,在3、4、5三个碳原子上各连有1个-CH3,所以名称为3,4,5—三甲基庚烷。
21. ③和⑥ ⑤和⑦ ①和②、④和⑧ 醛基 (醇)羟基 1 8 甲和丙 2,3—二甲基戊烷 1 5
【解析】
【分析】
【详解】
(1)互为同分异构体的化合物具有相同的分子式、不同结构,满足条件的有③和⑥;互为同素异形体的物质一定为同种元素形成的不同单质,满足条件的有⑤和⑦;互为同系物的物质必须满足结构相似,分子间相差一个或多个CH2原子团,满足该条件的为①和②、④和⑧;
(2) ①甲为,含有的含氧官能团为醛基和羟基;
②乙中羟基所连的C原子为饱和碳原子,故饱和碳原子只有一个;丙中苯环上的六个碳原子一定在一个平面上,苯环所连接的C原子在同一平面上,故一定在同一平面上的C原子有8个;
③互为同分异构体的化合物具有相同的分子式、不同结构,满足条件的有甲和丙;
(3)由结构简式可知,该烷烃的最长碳链由5个碳原子,支链为2个甲基,名称为2,3-二甲基戊烷;该烷烃中含有一个手性碳原子;连在同一个碳原子上的甲基形成的烯烃相同,根据碳原子成4键规律可知,能够生成该烷烃的烯烃有5种。
22.(1)AC
(2) 16 16 18 三 ⅥA
(3) C
【解析】
(1)
根据示意图不难看出①②③分别是H、D、T原子:
A.首先明确核素的定义,不同的原子即不同的核素,氕、氘、氚明显是三种不同的核素,A项正确;
B.质量数=质子数+中子数,氕、氘、氚的质量数分别为1、2、3,B项错误;
C.氕、氘、氚互为氢元素的同位素,C项正确;
D.同位素的化学性质几乎完全一样,物理性质有差别,D项错误;
答案选AC;
(2)
的质子数为16,质量数为32,中子数为32-16=16,电子数为16+2=18,该元素在元素周期表中的位置是第三周期ⅥA族,该元素的最高价氧化物对应水化物的化学式是;
(3)
①氰酸铵和尿素的分子式相同,结构不同,所以它们之间的关系为同分异构体;
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为;
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为。
一、选择题(共16题)
1.下列各组物质,不互为同分异构体的是
A.CH3CH2CH2CH3和CH3CH(CH3)2 B.CH3CH=CH2CH2=CHCH3
C.CH≡CCH2CH3和CH2=CH-CH=CH2 D.CH3CH2OH和CH3OCH3
2.分子式为C8H8O2的芳香族化合物,能发生水解反应的结构有
A.4种 B.5种 C.6种 D.7种
3.如图是几种常见高度对称烷烃的分子碳架结构,这三种烷烃的一氯取代产物的同分异构体数目分别是
A.1种,1种,1种 B.1种,1种,2种 C.2种,3种,6种 D.2种,3种,8种
4.下列各组物质不互为同分异构体的是
A.和 B.和
C.和 D. 和
5.金刚烷(C10H16)是一种重要的脂肪烷烃,其结构高度对称,如图所示。金刚烷能与卤素发生取代反应,其中二氯金刚烷(C10H14Cl2)的同分异构体数目是
A.4种 B.6种
C.8种 D.10种
6.三位分别来自法国、美国、荷兰的科学家因研究“分子机器的设计与合成”而获得2016年诺贝尔化学奖。纳米分子机器日益受到关注,机器的“车轮”常用组件如图。
下列说法不正确的是
A.①②③④均属于烃
B.②与苯是同分异构体
C.③和金刚石是同素异形体
D.①②④的一氯代物分别为3种、1种、2种
7.下列说法正确的是
A.和互为同位素
B.CH2O与C2H4O互为同系物
C.NH4CNO与CO(NH2)2互为同分异构体
D.PCl3和PCl5互为同素异形体
8.分子式为的有机物共有(不含立体异构)
A.5种 B.6种 C.7种 D.8种
9.化合物M是某种药物合成的中间体,其结构简式如图所示,下列关于化合物M的说法不正确的是
A.属于芳香烃
B.不溶于水,且密度比水小
C.既能发生加成反应,又能发生取代反应
D.能使酸性溶液褪色
10.下列化学用语正确的是
A.丙烷分子的分子式:CH3CH2CH3
B.对硝基甲苯的结构简式:
C.2-乙基-1,3-丁二烯分子的键线式:
D.聚丙烯的结构简式:
11.分子式C4H10O的同分异构体有
A.6种 B.7种 C.8种 D.9种
12.下列说法正确的是
A.和互为同位素
B.金刚石和富勒烯互为同素异形体
C.乙醚和乙醇互为同分异构体
D.和互为同系物
13.下列说法不正确的是
A.CH2=CH—CHO、CH≡C—CH2OH互为同分异构体,与足量H2加成后为同一物质
B.CH3CH2NO2与H2NCH2COOH互为同分异构体
C.符合通式CnH2n+2的不同烃一定属于同系物
D.C5H12同分异构体中新戊烷沸点最低
14.下列说法不正确的是
A.乙苯和对二甲苯互为同分异构体
B.石墨烯和C60互为同素异形体
C.H+、H-、D属于同种元素
D.Na2O、Na2O2互为同系物
15.通过电解催化还原CO2可得到碳酸二甲酯DMC()。下列说法错误的是
A.通入CO2、CH3OH的电极为阳极
B.Br-的物质的量在催化循环前后不变
C.过程⑤的副产物可能含有乙二酸二甲酯()
D.该电解催化过程的总反应方程式为:CO2+2CH3OH+H2O
16.NA为阿伏加德罗常数的值,下列有关说法正确的是
A.500mL2mol·L-1FeCl3溶液中含有的Fe3+的数目为NA
B.室温下pH=11的Na2CO3溶液,由水电离出的OH-数目为0.001NA
C.0.25molZn与一定量浓硫酸反应后完全溶解,生成气体的分子数为0.25NA
D.46g有机物C2H6O中含有的极性共价键的数目一定为7NA
二、综合题(共6题)
17.按要求回答问题
(1)给有机物命名, 名称________________________。
(2) 写出符合分子式C3H8O的有机物的结构简式(如乙酸结构简式为CH3COOH):CH3CH2CH2OH,__________________________________________________。
(3)配平下列反应离子方程式:
As2S3 + H2O + NO3- AsO + SO + NO↑ + (未配平)
___________________________________________________________
(4)某地污水中的有机污染物主要成分是三氯乙烯(C2HCl3),向污水中加入KMnO4(其还原产物为MnO2)可将三氯乙烯除去,其生成物不污染环境,写出该反应的化学方程式:_____。
(5)根据氧化还原反应:2 Fe3+ + Cu = 2Fe2+ +Cu2+ ,设计一个盐桥原电池。画出原电池结构图(需注明电极、电解质溶液、盐桥)。___
18.乙苯(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是:
C8H10(g) C8H8(g)+H2(g) ΔH=+125 kJ·mol-1
Ⅰ.某温度下,将0.40 mol乙苯充入1 L真空密闭容器中发生上述反应,测定不同时间该容器内物质的物质的量,得到数据见下表:
时间/min 0 10 20 30 40
n(C8H10)/mol 0.40 0.30 0.26 n2 n3
n(C8H8)/mol 0.00 0.10 n1 0.16 0.16
(1)当反应进行到20 min时,该段时间内H2的平均生成速率是__________。
(2)该温度下,反应从开始到平衡的过程中共从环境吸收__________kJ热量。
(3)若保持反应条件不变,用0.40 mol H2(g)和0.40 mol C8H8(g)合成C8H10(g),当有25 kJ热量放出时,该反应中H2的转化率是______,此时该反应的方向是________(填“正向” 或“ 逆向”)。
Ⅱ.氢化热是指在一定条件下,1 mol不饱和化合物加氢时放出的热量,表中是环己烯(g)、1,3- 环己二烯(g)和苯的氢化热数据:
物质 +H2 +2H2 +3H2
氢化热(kJ/mol) 119.7 232.7 208.4
(4)1,3 -环己二烯的稳定性________(填“大于”“小于”或“等于”)苯。
(5)某有机物是苯的同分异构体,其分子中的碳碳键角只有60度和90度两种。请写出这种有机物的键线式结构________,它在核磁共振氢谱上会产生________个吸收峰 。
(6)与环己烯互为同分异构体的炔烃共有________种(不考虑立体异构)。
19.有机化学基础填空题:
⑴具有复合官能团的复杂有机物中官能团具有各自的独立性,在不同条件下所发生的化学反应可分别从各官能团讨论。根据上图回答:该物质具有的官能团是_______________、_____________(填化学式),所以该物质即可以归为_____________类又可以归为____________类(填有机物的类别)。
⑵写出下列化合物的名称或结构简式:
①结构简式为
此烃的名称为__________________
②结构简式为此烃的名称为_______________
③2,4-二甲基已烷的结构简式为_________________
20.(1)现有下列各化合物:
A.CH3CH2CH2CHO和;B.和;C.和;D.CH3CH2C≡CH和CH2=CH-CH=CH2;E.和;F.戊烯和环戊烷
①上述各组化合物属于同系物的是____,属于同分异构体的是_____填入编号。
②根据官能团的特点可将C中两化合物划分为____类和____类。
(2)写出下列有机化合物含氧官能团的名称____。
(3)用系统命名法命名 __。
21.(1)在下列物质中互为同分异构体的有___;互为同素异形体的有___;互为同系物的是___(填序号)。
①2—甲基丁烷②CH3—CH2—CH3③CH3CH2CH2OH④CH3—Cl⑤白磷⑥CH3—O—CH2CH3⑦红磷⑧CH3CH2—Cl
(2)已知有机物:甲:,乙:,丙:。
①请写出甲中含氧官能团的名称:___、___。
②乙中饱和碳原子有___个;丙中一定在同一个平面上的碳原子有___个;
③请判别上述哪些化合物互为同分异构体:___。
(3)某有机物A的结构简式为,该烃用系统命名法命名为:___;有机物A中共有__个手性碳原子;若该有机物A是由烯烃和1molH2加成得到的,则原烯烃的结构有___种。
22.请按要求填空:
(1)简单原子的原子结构如图:
① ② ③
其中“●”表示质子或电子,“○”表示中子。则下列有关①②③的叙述正确的是___________(填标号)。
A.①②③是三种不同的核素 B.①②③具有相同的质量数
C.①②③互为同位素 D.①②③是三种化学性质不同的粒子
(2)的质子数为___________,中子数为___________,电子数为___________,该元素在元素周期表中的位置是第___________周期___________族,该元素的最高价氧化物对应水化物的化学式是___________
(3)1828年,德国化学家维勒通过蒸发氰酸铵()水溶液得到尿素[]。
①氰酸铵和尿素之间的关系是___________(填标号)。
A.同位素B.同素异形体C.同分异构体D.同系物
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为___________。
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为___________。
试卷第页,共页
参考答案:
1.B
【解析】
【分析】
【详解】
A.CH3CH2CH2CH3和CH3CH(CH3)2分子式均为C4H10,分子式相同,结构不同,互为同分异构体,A不符题意;
B.CH3CH=CH2和CH2=CHCH3均为丙烯,为同一种物质,B不符题意;
C.CH≡CCH2CH3和CH2=CH-CH=CH2分子式均为C4H6,分子式相同,结构不同,互为同分异构体,C不符题意;
D.CH3CH2OH和CH3OCH3分子式均为C2H6O,分子式相同,结构不同,互为同分异构体,D不符题意;
答案选B。
2.C
【解析】
【分析】
【详解】
含酯基能发生水解反应,属于芳香族化合物说明含有苯环,则取代基为-C2H3O2,符合条件的有:、、、共6种,故选:C。
3.B
【解析】
【分析】
【详解】
正四面体烷分子中氢原子完全等同,一氯代物只有1种;立方烷分子中氢原子完全等同,一氯代物只有1种;金刚烷分子中氢原子有两种类型,其一氯代物有2种,B项正确。
故选B。
4.C
【解析】
【分析】
同分异构体是指分子式相同,但结构不同的化合物,同分异构体包含碳链异构、官能团异构、位置异构等,据此解答。
【详解】
A.和的分子式都为CH4N2O,二者结构不同,属于同分异构体,故A不选;
B.和的分子式都为C2H6O,二者结构不同,属于同分异构体,故B不选;
C.的分子式为C3H6O2,的分子式为C3H4O2,二者分子式不同,不互为同分异构体,故C选;
D. 和的分子式都为C7H8O,二者结构不同,属于同分异构体,故D不选;
答案选C。
5.B
【解析】
【详解】
金刚烷有2种等效氢,一氯取代物有2种:和,有3种等效氢:,对应二氯代物有3种;有4种等效氢:,对应的二氯代物有4种;两种情况中Cl位于邻位的情况重复,因此共有3+4-1=6种;
选B。
6.A
【解析】
【分析】
【详解】
A.③为富勒烯只含有碳原子,不属于烃,A项错误;
B.②的分子式为C6H6,与苯的分子式相同,结构不同,二者互为同分异构体,B项正确;
C.③和金刚石均为C元素的单质,二者互为同素异形体,C项正确;
D.①中有3种氢原子,一氯代物有3种,②中有1种氢原子,一氯代物有1种,④中含有2种氢原子,一氯代物有2种,D项正确;
答案选A。
7.C
【解析】
【详解】
A.是原子,而是离子,因此二者不能互为同位素,A错误;
B.CH2O表示甲醛,C2H4O表示的物质可能表示乙醛CH3CHO,也可能为乙烯醇CH2=CH-OH,因此二者不一定是同系物,B错误;
C.NH4CNO与CO(NH2)2分子式相同,结构不同,故二者互为同分异构体,C正确;
D.PCl3和PCl5是P与Cl两种元素形成的两种不同的化合物,二者不是单质,因此它们不能互为同素异形体,D错误;
故合理选项是C。
8.C
【解析】
【分析】
【详解】
分子式为的有机物有Cl2C=CHCH3、ClCH=CClCH3、ClCH=CHCH2Cl、CH2=CClCH2Cl、CH2=CHCHCl2、、,共7种,故选C;
9.A
【解析】
【详解】
A.化合物M除了碳、氢元素外还含有氧元素,属于烃的衍生物,A错误;
B.由化合物M的结构可知含有酯基,其不溶于水,且密度比水小,B正确;
C.化合物M中含碳碳双键和酯基,所以既能发生加成反应。又能发生取代反应,C正确;
D.化合物M中含碳碳双键,所以能使酸性溶液褪色,D正确;
答案选A。
10.C
【解析】
【详解】
A.CH3CH2CH3为丙烷的结构简式,分子式为C3H8,故A错误;
B.对硝基甲苯中硝基和甲基处于对位的位置,且硝基的N原子与苯环相连,其结构简式是,故B错误;
C.2-乙基-1,3-丁二烯的结构简式为,键线式中用短线“-”表示化学键,端点、交点表示碳原子,C、H原子不标出,则2-乙基-1,3-丁二烯的键线式为,故C正确;
D.丙烯发生加聚反应生成聚丙烯,其结构简式为,故D错误;
故选C。
11.B
【解析】
【分析】
【详解】
分子式C4H10O的同分异构体有醇类和醚类,醇类有CH3CH2CH2CH2OH、CH3CH2CH(CH3)OH、(CH3)2CHCH2OH、C(CH3)3OH,醚类有CH3OCH2CH2CH3,CH3CH2OCH2CH3,CH3OCH(CH3)2,共7种,选B。
12.B
【解析】
【分析】
【详解】
A.和是由同位素原子构成的分子,而不是原子,因此二者不能互为同位素,A错误;
B.金刚石和富勒烯是C元素形成的不同性质的单质,二者互为同素异形体,B正确;
C.乙醚结构简式是C2H5OC2H5,分子式是C4H10O;乙醇结构简式是CH3CH2OH,分子式是C2H6O,二者的分子式不相同,因此不能互为同分异构体,C错误;
D.羟基直接连接在苯环上,属于酚;羟基连接在侧链上,属于芳香醇,因此二者是不同类别的物质,不能互为同系物,D错误;
故合理选项是B。
13.C
【解析】
【详解】
A.CH2=CH-CHO、CH≡C-CH2OH的分子式相同而结构不同,故互为同分异构体,而加成后均生成CH3CH2CH2OH,是同一种物质,故A正确;
B.分子式相同而结构不同的化合物间互为同分异构体,故CH3CH2NO2与H2NCH2COOH互为同分异构体,故B正确;
C.符合通式CnH2n+2的不同烃,若n相同时属同分异构体,不属于同系物,故C错误;
D.互为同分异构体的烷烃,支链越多,则熔沸点越低,故新戊烷的沸点最低,故D正确;
故选:C。
14.D
【解析】
【分析】
【详解】
A.乙苯和对二甲苯只是甲基位置不相同,分子式相同互为同分异构体,A正确;
B.石墨烯和C60均为单质,且组成元素均为C元素,故互为同素异形体,B正确;
C.H+、H-、D属于同种元素都是氢元素,C正确;
D.Na2O、Na2O2结构不相似,且不相差n个-CH2,故不互为同系物,D错误;
答案选D。
15.A
【解析】
【分析】
【详解】
A.通入的CO2得到电子生成CO,发生还原反应,所以通入CO2、CH3OH的电极为阴极,故A错误;
B.Br-在阳极失去电子生成Br2,Br2参与反应,反应过程中Br2又转化为Br-,所以Br-的物质的量在催化循环前后不变,故B正确;
C.过程⑤中的 在连有碳氧双键的碳原子和Pb之间断键生成DMC,断键后生成的-COOCH3可以两两结合生成乙二酸二甲酯,故C正确;
D.该电解过程是CO2和甲醇反应最终生成DMC和水的反应,总反应方程式为:CO2+2CH3OH +H2O,故D正确;
故选A。
16.C
【解析】
【分析】
【详解】
A.500mL2mol·L-1FeCl3溶液中溶质的物质的量为1mol,但由于Fe3+发生水解,所以溶液中含有的Fe3+的数目小于NA,A错误;
B.溶液体积未知,无法计算由水电离出的OH-数目,B错误;
C.1mol锌和浓硫酸反应生成1mol二氧化硫,1molZn和稀硫酸反应生成1mol氢气,因此0.25molZn与一定量浓硫酸反应后完全溶解,生成气体的分子数为0.25NA,C正确;
D.C2H6O不一定是乙醇,也可能是二甲醚,所以46g有机物C2H6O中含有极性共价键的数目不一定为7NA,D错误;
答案选C。
17. 2-甲基-2丁烯 CH3CH (OH)CH3,CH3-O-CH2CH3 3As2S3+4H2O+28NO3-=6AsO43-+ 9SO42-+28NO↑ +8H+ C2HCl3+2KMnO4 =2CO2↑+2MnO2+HCl+KCl (或其他合理答案)
【解析】
【详解】
(1) 名称2-甲基-2丁烯;
(2) CH3CH2CH2OH可能的结构简式有CH3CH (OH)CH3,CH3-O-CH2CH3;
(3)反应中 ,As元素化合价由+3价升高为+5价,S元素化合价由 2价升高为+6价,化合价共升高2×(5 3)+3×[6 ( 2)]=28, ,N元素化合价由+5价降低为+2价,化合价共降低3价,故化合价升降最小公倍数为84,故 系数为3, 系数为4,根据原子守恒可知, 系数为6, 系数为9,NO系数为28,根据电荷守恒可知,缺项为H+,故H+系数为8,由原子守恒可知,故H2O的系数为4,配平后离子方程式为:3As2S3+4H2O+28NO3-=6AsO43-+ 9SO42-+28NO↑ +8H+;
(4)由题意可知:KMnO4溶液与三氯乙烯反应,产物有 , ,依据原子个数守恒可知其余产物为:KCl,HCl,该反应为氧化还原反应, ,Mn元素由+7价→+4价,一个KMnO4得3个电子;C2HCl3→CO2,C元素由+1价→+4价,一个C2HCl3失去6个电子,依据得失电子守恒可知反应的方程式为:C2HCl3+2KMnO4 =2CO2↑+2MnO2+HCl+KCl;
(5)根据氧化还原反应:2 Fe3+ + Cu = 2Fe2+ +Cu2+ ,依据原电池原理负极失去电子发生氧化反应,正极得到电子发生还原反应,画出结构图如下:
。
18. 0.007 mol·L-1·min-1 20 50% 正向 小于 1 7
【解析】
【详解】
(1)当反应进行到20 min时消耗乙苯0.40mol-0.26mol=0.14mol,根据方程式可知生成氢气是0.14mol,浓度是0.14mol/L,所以该段时间内H2的平均生成速率是0.14mol/L÷20min=0.007 mol·L-1·min-1。
(2)根据表中数据可知平衡时生成苯乙烯是0.16mol,所以该温度下,反应从开始到平衡的过程中共从环境吸收0.16mol×125 kJ·mol-1=20kJ热量。
(3)当有25 kJ热量放出时,消耗氢气是25 kJ÷125 kJ·mol-1=0.2mol,所以氢气的转化率是0.2/0.4×100%=50%,此时该反应的方向是正向;
(4)根据题干信息可知①C6H8+2H2→C6H12 △H=-232.7kJ/mol,②C6H6+3H2→C6H12 △H=-208.4kJ/mol,依据盖斯定律②-①得到:C6H6+H2→C6H8 △H=+24.3kJ/mol,即苯转化为1,3 环己二烯吸热,因此苯的能量低于1,3 环己二烯,所以苯的稳定性强;
(5)某有机物是苯的同分异构体,其分子中的碳碳键角只有60度和90度两种,所以这种有机物的键线式结构为,它在核磁共振氢谱上会产生1个吸收峰。
(6)与环己烯互为同分异构体的炔烃共有CH≡CCH2CH2CH2CH3、CH3C≡CCH2CH2CH3、CH3CH2C≡CCH2CH3、CH≡CCH2CH(CH3)2、CH≡CCH(CH3)CH2CH3、CH≡CC(CH3)3、CH3C≡CCH(CH3)2,共计7种。
19. —COOH —CHO 羧酸 醛 3-甲基-2-乙基-1-戊烯 1, 2—二甲基—4—乙基苯
【解析】
【详解】
(1)有机物含有的官能团有羧基、酚羟基和醛基,所以这个化合物可看作羧酸类和醛类;
(2)①的最长碳链含有5个碳原子,为戊烯,在3号碳原子上有一个甲基,在2号碳原子上有一个乙基,命名为:3-甲基-2-乙基-1-戊烯;
②有苯环的,命名时可以依次编号命名,命名为:对甲基乙苯或4-甲基乙基苯;
③根据2,4-二甲基已烷的名称可知,在主链上有6个碳原子,在2号和4号碳上各有一个甲基,结构简式为。
20. BE AD 酚 醇 酯基、羟基、羧基 3,4,5—三甲基庚烷
【解析】
【分析】
【详解】
①B中,和都属于氨基酸,但分子式不同,二者属于同系物;E 中,和都属于二元饱和羧酸,但分子式不同,二者属于同系物,所以上述各组化合物属于同系物的是BE。A中,CH3CH2CH2CHO和的分子式相同、结构不同;D中,CH3CH2C≡CH和CH2=CH-CH=CH2的分子式相同、结构不同,所以属于同分异构体的是AD。答案为:BE;AD;
②根据官能团的特点,C中含有酚羟基,含有醇羟基,所以两化合物划分为酚类和醇类。答案为:酚;醇;
(2) 中含氧官能团为-OOC-、-OH、-COOH,名称分别为酯基、羟基、羧基。答案为:酯基、羟基、羧基;
(3)有机物的主链碳原子有7个,在3、4、5三个碳原子上各连有1个-CH3,所以名称为3,4,5—三甲基庚烷。
21. ③和⑥ ⑤和⑦ ①和②、④和⑧ 醛基 (醇)羟基 1 8 甲和丙 2,3—二甲基戊烷 1 5
【解析】
【分析】
【详解】
(1)互为同分异构体的化合物具有相同的分子式、不同结构,满足条件的有③和⑥;互为同素异形体的物质一定为同种元素形成的不同单质,满足条件的有⑤和⑦;互为同系物的物质必须满足结构相似,分子间相差一个或多个CH2原子团,满足该条件的为①和②、④和⑧;
(2) ①甲为,含有的含氧官能团为醛基和羟基;
②乙中羟基所连的C原子为饱和碳原子,故饱和碳原子只有一个;丙中苯环上的六个碳原子一定在一个平面上,苯环所连接的C原子在同一平面上,故一定在同一平面上的C原子有8个;
③互为同分异构体的化合物具有相同的分子式、不同结构,满足条件的有甲和丙;
(3)由结构简式可知,该烷烃的最长碳链由5个碳原子,支链为2个甲基,名称为2,3-二甲基戊烷;该烷烃中含有一个手性碳原子;连在同一个碳原子上的甲基形成的烯烃相同,根据碳原子成4键规律可知,能够生成该烷烃的烯烃有5种。
22.(1)AC
(2) 16 16 18 三 ⅥA
(3) C
【解析】
(1)
根据示意图不难看出①②③分别是H、D、T原子:
A.首先明确核素的定义,不同的原子即不同的核素,氕、氘、氚明显是三种不同的核素,A项正确;
B.质量数=质子数+中子数,氕、氘、氚的质量数分别为1、2、3,B项错误;
C.氕、氘、氚互为氢元素的同位素,C项正确;
D.同位素的化学性质几乎完全一样,物理性质有差别,D项错误;
答案选AC;
(2)
的质子数为16,质量数为32,中子数为32-16=16,电子数为16+2=18,该元素在元素周期表中的位置是第三周期ⅥA族,该元素的最高价氧化物对应水化物的化学式是;
(3)
①氰酸铵和尿素的分子式相同,结构不同,所以它们之间的关系为同分异构体;
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为;
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为。
