2.2 气体的等温变化 教案
文档属性
| 名称 | 2.2 气体的等温变化 教案 |

|
|
| 格式 | doc | ||
| 文件大小 | 513.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2022-02-12 00:00:00 | ||
图片预览


文档简介
2.2 气体的等温变化
〖教材分析〗
本节是本章的重难点内容之一。教材通过探究实验的得出玻意耳定律的内容及其数表达式。玻意耳定律是学生学习的第一个气体实验定律,第一次分析气体状态参量的定量变化,对学生后面进一步学习另外两个气体实验定律都有重要作用,同时也能培养学生通过观察来研究物理问题的思想方法。本节教材的内容是初中没有接触过的,学习起来比较陌生,所以要适当安排练习及时巩固所学的知识。
〖教学目标与核心素养〗
物理观念∶知道玻意耳定律的内容,具有将玻意耳定律与实际相联系的意识。
科学思维∶从具体事物入手分析和解决问题。
科学探究:能在他人指导下独立完成探究气体等温变化的规律的实验,知道基本的实验原理。
科学态度与责任∶培养学生从具体事物入手的分析方法,提高学生综合运用知识来分析和解决实际问题的能力。
〖教学重难点〗
教学重点:通过实验探究得出玻意耳定律的内容,并能进行简单运算。
教学难点:玻意耳定律的实际应用。
〖教学准备〗
多媒体课件、探究气体等温变化的规律的实验装置等。
〖教学过程〗
一、新课引入
在庆典活动中放飞的气球,会飞到我们看不见的地方。随着气球的升空,大气压在减小,温度在降低,气球在膨胀…看来,一定质量的气体的压强、体积和温度三个状态参量之间是有联系的。那么,它们会有怎样的联系呢
二、新课教学
(一)气体的等温变化
描述气体的状态变化的状态参量:
体积V,确定气体的空间大小。
压强P,确定气体与容器壁之间的作用力的大小。
温度T,确定气体的热运动剧烈程度大小。
对一定质量的气体而言,如果这三个状态参量都不变,就可以说气体的状态不变,但如果有参量变了,那气体的状态就会发生改变。
问题:那这三者间会不会存在一定的关系呢?
于一定质量的气体,在温度保持不变时,其压强与体积变化时就存在一定的关系,可以称之为等温变化。
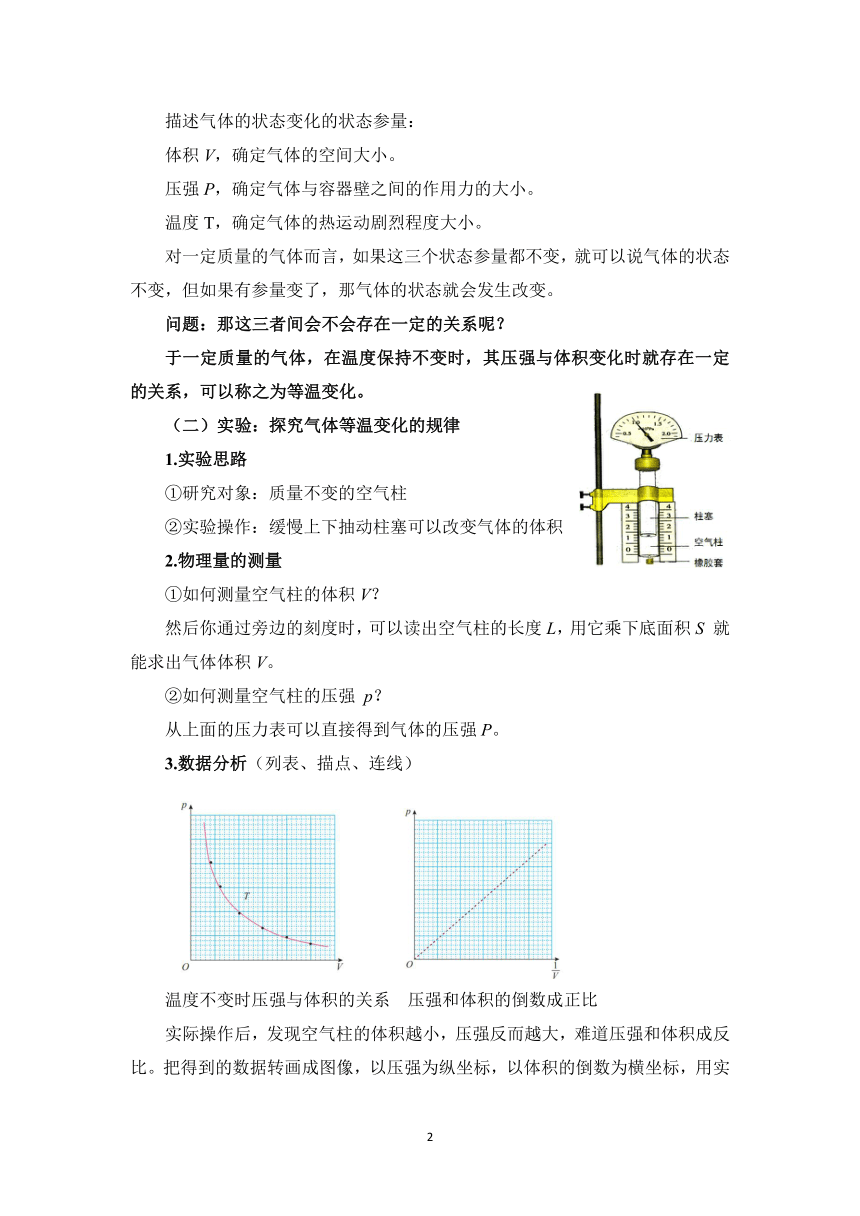
(二)实验:探究气体等温变化的规律
1.实验思路
①研究对象:质量不变的空气柱
②实验操作:缓慢上下抽动柱塞可以改变气体的体积
2.物理量的测量
①如何测量空气柱的体积V?
然后你通过旁边的刻度时,可以读出空气柱的长度L,用它乘下底面积S 就能求出气体体积V。
②如何测量空气柱的压强 p?
从上面的压力表可以直接得到气体的压强P。
3.数据分析(列表、描点、连线)
温度不变时压强与体积的关系 压强和体积的倒数成正比
实际操作后,发现空气柱的体积越小,压强反而越大,难道压强和体积成反比。把得到的数据转画成图像,以压强为纵坐标,以体积的倒数为横坐标,用实验数据描点,发现他们都位于过原点的同一条直线上,看来压强和体积的倒数成正比,也就是和体积成反比。
结论:一定质量的某种气体在温度不变的情况下,压强P与体积V成反比。
4.实验注意事项:
第一、为保证温度不变,气体体积的改变要缓慢进行,如果操作太快,就不是等温变化会影响结果的准确性。
第二、柱塞,事先要涂好润滑油,来保证装置的气密性。
第三,实验过程中,不要用手接触注射器的圆筒,如果你用手握着它,那其中的气体,就会从你温暖的手中吸收热量,温度升高,那就不是等温变化。
第四、读取空气柱长度时,视线要与刻度线相平,以减小读数误差。
(三)玻意耳定律
1.玻意耳定律的内容
用实验探究了气体的等温变化规律,得出:一定质量的某种气体在温度不变的情况下,压强与体积成反比。用公式可以表示
PV=C
还可以写成
P1V1=P2V2
左右两边分别表示气体在一、二两个状态下了压强和体积,这个式子可是非常有用。这个规律最早是由英国科学家玻意耳发现,所以被称为玻意耳定律。
适用范围:温度不太低,压强不太大。
2.等温变化的图像
①等温线是双曲线的一支。
②图中温度越高,C值也就越大,其等温线离原点越远。
课堂练习
例1:如图所示是一定质量的某气体状态变化的p-V图象,则下列说法正确的是( BCD )
A.气体做的是等温变化
B.气体的压强从A到B一直减小
C.气的体积从A 到B一直增大
D.气体的三个状态参量一直都在变
解析:注意压强与体积的关系是曲线。
例2:一定质量的气体,不同温度下的等温线是不同的。有两条等温线,哪条等温线表示的是温度比较高时的情形吗 请你尝试给出判断,并说明理由。
解析:图线温度越高,其等温线离原点越远。所以T2>T1。
例3:氧气瓶在储存过程中,由于密封不严,其瓶内氧气的压强和体积变化如图从A到B所示,则瓶内氧气的温度( )
A.一直升高
B.一直降低
C.先升高后降低
D.不变
解析:如果咱补上等温线比较温度,显然A点所在的等温线位置更高,温度就更高,也就是T2>T1 所以从A到B温度一直降低,看看选项,应该选B。你要是这么说,可就挂了,认真读题,这里的氧气瓶密封不严,等于说在漏气,还记得等温变化规律的前提吗?是对于一定质量的某种气体才行。所以题目中的情况根本不满足等温变化的规律,换个思路的来解答。你想了密封不严导致的漏气,咱可以看做是一个缓慢的过程,那瓶内的气体就可以与外界环境进行充分的热交换,所以和外界温度相等,所以无论从从A到B体积怎么变,温度却保持不变,所以正确答案应该选D。
例4:一个足球的容积是2.5L。用打气筒给这个足球打气,每打一次都把体积为125mL、压强与大气压强相同的气体打进球内。如果在打气前足球就已经是球形并且里面的压强与大气压强相同。打了20次后,足球内部空气的压强是大气压的多少倍?你在得出结论时考虑到了什么前提?实际打气时的情况能够满足你的前提吗?
解析:研究对象:打完20次气后足球内的气体,假设气体的温度和球的体积均不发生变化,设大气压强为p0,则
初态:p1=p0 V1=2.5+0.125×20=5L
末态:p2=? 体积为打气后V2=2.5L
据玻意耳定律有:p1V1=p2V2
代入数据解得:p2=2p0
例5:水银气压计中混入了一个气泡,上升到水银柱的上方,使水银柱上方不再是真空。当实际大气压相当于768mm高的水银柱产生的压强时,这个水银气压计的读数只有750mm,此时管中的水银面到管顶的距离为80mm。当这个气压计的读数为740mm水银柱时,实际的大气压相当于多高水银柱产生的压强 设温度保持不变。
解析:一管中封闭气体为研究对象,设玻璃管的横截面积为S,前后为等温变化。
初态:P1=(768-750)mmHg=18mmHg
V1=80S
末态:P2=(P-740)mmHg
V2=80S+(750-740)S
=90S
等温变化,根据p1V1=p2V2
代入得:18×80S=(P-740)×90S
解得:P=756mmHg
〖板书设计〗
2.2 气体的等温变化
1.等温变化∶一定量的气体在温度不变的状态下,发生的变化。
2.玻意耳定律∶ 一定质量的气体,在温度不变的情况下,它的压强跟体积成反比
pV=C 或p1V1=p2V2
3.适用范围∶温度不太低,压强不太大。
4.气体等温变化的图像,是一条以纵轴和横轴为渐近线的双曲线,称等温线
5.等温线的特点 ∶温度越高,其等温线离原点越远。
〖教学反思〗
本课属于实验探究课,实验探究课学生一般都会感觉到比较放松,觉得这个内容不重要,所以就有轻视心理,导致本课的基础知识不扎实。所以这节课的一般做法还是要先把实验讲解一遍,然后演示一遍给学生看,最后才让学生做实验。数据的处理要积极引导他们严格按照列表、描点、连线的方法进行。这样才能又快又好的得出相应的实验结论。增强学习的自信心。 (
1
)
〖教材分析〗
本节是本章的重难点内容之一。教材通过探究实验的得出玻意耳定律的内容及其数表达式。玻意耳定律是学生学习的第一个气体实验定律,第一次分析气体状态参量的定量变化,对学生后面进一步学习另外两个气体实验定律都有重要作用,同时也能培养学生通过观察来研究物理问题的思想方法。本节教材的内容是初中没有接触过的,学习起来比较陌生,所以要适当安排练习及时巩固所学的知识。
〖教学目标与核心素养〗
物理观念∶知道玻意耳定律的内容,具有将玻意耳定律与实际相联系的意识。
科学思维∶从具体事物入手分析和解决问题。
科学探究:能在他人指导下独立完成探究气体等温变化的规律的实验,知道基本的实验原理。
科学态度与责任∶培养学生从具体事物入手的分析方法,提高学生综合运用知识来分析和解决实际问题的能力。
〖教学重难点〗
教学重点:通过实验探究得出玻意耳定律的内容,并能进行简单运算。
教学难点:玻意耳定律的实际应用。
〖教学准备〗
多媒体课件、探究气体等温变化的规律的实验装置等。
〖教学过程〗
一、新课引入
在庆典活动中放飞的气球,会飞到我们看不见的地方。随着气球的升空,大气压在减小,温度在降低,气球在膨胀…看来,一定质量的气体的压强、体积和温度三个状态参量之间是有联系的。那么,它们会有怎样的联系呢
二、新课教学
(一)气体的等温变化
描述气体的状态变化的状态参量:
体积V,确定气体的空间大小。
压强P,确定气体与容器壁之间的作用力的大小。
温度T,确定气体的热运动剧烈程度大小。
对一定质量的气体而言,如果这三个状态参量都不变,就可以说气体的状态不变,但如果有参量变了,那气体的状态就会发生改变。
问题:那这三者间会不会存在一定的关系呢?
于一定质量的气体,在温度保持不变时,其压强与体积变化时就存在一定的关系,可以称之为等温变化。
(二)实验:探究气体等温变化的规律
1.实验思路
①研究对象:质量不变的空气柱
②实验操作:缓慢上下抽动柱塞可以改变气体的体积
2.物理量的测量
①如何测量空气柱的体积V?
然后你通过旁边的刻度时,可以读出空气柱的长度L,用它乘下底面积S 就能求出气体体积V。
②如何测量空气柱的压强 p?
从上面的压力表可以直接得到气体的压强P。
3.数据分析(列表、描点、连线)
温度不变时压强与体积的关系 压强和体积的倒数成正比
实际操作后,发现空气柱的体积越小,压强反而越大,难道压强和体积成反比。把得到的数据转画成图像,以压强为纵坐标,以体积的倒数为横坐标,用实验数据描点,发现他们都位于过原点的同一条直线上,看来压强和体积的倒数成正比,也就是和体积成反比。
结论:一定质量的某种气体在温度不变的情况下,压强P与体积V成反比。
4.实验注意事项:
第一、为保证温度不变,气体体积的改变要缓慢进行,如果操作太快,就不是等温变化会影响结果的准确性。
第二、柱塞,事先要涂好润滑油,来保证装置的气密性。
第三,实验过程中,不要用手接触注射器的圆筒,如果你用手握着它,那其中的气体,就会从你温暖的手中吸收热量,温度升高,那就不是等温变化。
第四、读取空气柱长度时,视线要与刻度线相平,以减小读数误差。
(三)玻意耳定律
1.玻意耳定律的内容
用实验探究了气体的等温变化规律,得出:一定质量的某种气体在温度不变的情况下,压强与体积成反比。用公式可以表示
PV=C
还可以写成
P1V1=P2V2
左右两边分别表示气体在一、二两个状态下了压强和体积,这个式子可是非常有用。这个规律最早是由英国科学家玻意耳发现,所以被称为玻意耳定律。
适用范围:温度不太低,压强不太大。
2.等温变化的图像
①等温线是双曲线的一支。
②图中温度越高,C值也就越大,其等温线离原点越远。
课堂练习
例1:如图所示是一定质量的某气体状态变化的p-V图象,则下列说法正确的是( BCD )
A.气体做的是等温变化
B.气体的压强从A到B一直减小
C.气的体积从A 到B一直增大
D.气体的三个状态参量一直都在变
解析:注意压强与体积的关系是曲线。
例2:一定质量的气体,不同温度下的等温线是不同的。有两条等温线,哪条等温线表示的是温度比较高时的情形吗 请你尝试给出判断,并说明理由。
解析:图线温度越高,其等温线离原点越远。所以T2>T1。
例3:氧气瓶在储存过程中,由于密封不严,其瓶内氧气的压强和体积变化如图从A到B所示,则瓶内氧气的温度( )
A.一直升高
B.一直降低
C.先升高后降低
D.不变
解析:如果咱补上等温线比较温度,显然A点所在的等温线位置更高,温度就更高,也就是T2>T1 所以从A到B温度一直降低,看看选项,应该选B。你要是这么说,可就挂了,认真读题,这里的氧气瓶密封不严,等于说在漏气,还记得等温变化规律的前提吗?是对于一定质量的某种气体才行。所以题目中的情况根本不满足等温变化的规律,换个思路的来解答。你想了密封不严导致的漏气,咱可以看做是一个缓慢的过程,那瓶内的气体就可以与外界环境进行充分的热交换,所以和外界温度相等,所以无论从从A到B体积怎么变,温度却保持不变,所以正确答案应该选D。
例4:一个足球的容积是2.5L。用打气筒给这个足球打气,每打一次都把体积为125mL、压强与大气压强相同的气体打进球内。如果在打气前足球就已经是球形并且里面的压强与大气压强相同。打了20次后,足球内部空气的压强是大气压的多少倍?你在得出结论时考虑到了什么前提?实际打气时的情况能够满足你的前提吗?
解析:研究对象:打完20次气后足球内的气体,假设气体的温度和球的体积均不发生变化,设大气压强为p0,则
初态:p1=p0 V1=2.5+0.125×20=5L
末态:p2=? 体积为打气后V2=2.5L
据玻意耳定律有:p1V1=p2V2
代入数据解得:p2=2p0
例5:水银气压计中混入了一个气泡,上升到水银柱的上方,使水银柱上方不再是真空。当实际大气压相当于768mm高的水银柱产生的压强时,这个水银气压计的读数只有750mm,此时管中的水银面到管顶的距离为80mm。当这个气压计的读数为740mm水银柱时,实际的大气压相当于多高水银柱产生的压强 设温度保持不变。
解析:一管中封闭气体为研究对象,设玻璃管的横截面积为S,前后为等温变化。
初态:P1=(768-750)mmHg=18mmHg
V1=80S
末态:P2=(P-740)mmHg
V2=80S+(750-740)S
=90S
等温变化,根据p1V1=p2V2
代入得:18×80S=(P-740)×90S
解得:P=756mmHg
〖板书设计〗
2.2 气体的等温变化
1.等温变化∶一定量的气体在温度不变的状态下,发生的变化。
2.玻意耳定律∶ 一定质量的气体,在温度不变的情况下,它的压强跟体积成反比
pV=C 或p1V1=p2V2
3.适用范围∶温度不太低,压强不太大。
4.气体等温变化的图像,是一条以纵轴和横轴为渐近线的双曲线,称等温线
5.等温线的特点 ∶温度越高,其等温线离原点越远。
〖教学反思〗
本课属于实验探究课,实验探究课学生一般都会感觉到比较放松,觉得这个内容不重要,所以就有轻视心理,导致本课的基础知识不扎实。所以这节课的一般做法还是要先把实验讲解一遍,然后演示一遍给学生看,最后才让学生做实验。数据的处理要积极引导他们严格按照列表、描点、连线的方法进行。这样才能又快又好的得出相应的实验结论。增强学习的自信心。 (
1
)
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
