第九单元实验活动5一定溶质质量分数的氯化钠溶液的配制课后练习-2021-2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 第九单元实验活动5一定溶质质量分数的氯化钠溶液的配制课后练习-2021-2022学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 265.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-15 00:00:00 | ||
图片预览



文档简介
实验活动5一定溶质质量分数的氯化钠溶液的配制 课后练习
一、选择题
1.下列关于配制溶液的操作中,可导致所配制的溶液浓度偏小的是
A.用固体氯化钠配制6%的氯化钠溶液,量取水时俯视读数
B.用固体氯化钠配制6%的氯化钠溶液,所称氯化钠固体不纯
C.用固体氯化钠配制6%的氯化钠溶液,配好的溶液装瓶后,烧杯内有溶液残留
D.用6%的氯化钠溶液配制3%的氯化钠溶液,量取6%氯化钠溶液时仰视读数
2.某学生用量筒量取液体时,量筒平稳地放置在实验台上,使视线与凹液面的最低处保持水平,读数为18mL;倒出部分液体后,俯视凹液面的最低处,读数为12mL。则该学生实际倒出的液体体积
A.大于6mL B.小于6mL C.等于6mL D.无法确定
3.下列实验操作错误的是( )
A.溶解固体 B.滴加液体
C.检验氢气的纯度 D.检查蜡烛燃烧生成水
4.下列知识整理的内容中三条都正确的选项是( )
A.物质构成 B.实验操作
①构成物质的微粒有分子、原子或离子 ②空气、液氧、过氧化氢中都含有氧分子 ③氯化钠是由离子构成的化合物 ①制取气体:先加药品后检查装置气密性 ②配制一定浓度溶液;量取水时仰视度数 ③称量一定质量药品,先加药品后加砝码
C.性质与用途 D.物质鉴别
①氢气密度小——填充探空气球 ②氧气具有助燃性——可作燃料 ③活性炭具有吸附性——除去色素和异味 ①鉴别空气、二氧化碳——用燃着的小木条 ②鉴别双氧水、水——用二氧化锰 ③鉴别硬水和软水——用肥皂水
A.A B.B C.C D.D
5.下列有关实验操作或现象记录中正确的是
A.用铁钉与硫酸铜溶液在敞口的容器中反应验证质量守恒
B.配制50g溶质质量分数为15%的氯化钠溶液,用100mL量筒量取水
C.向鸡蛋清溶液中加乙酸铅溶液,产生白色沉淀,再向其中加水,白色沉淀溶解
D.将点燃的木炭放入装有氧气的集气瓶中,木炭燃烧发白光,烧杯内壁有水雾
6.下列实验方法不正确的是( )
A.可以用铁钉和硫酸铜溶液的反应验证质量守恒定律
B.用KClO3制氧气通常加入MnO2作催化剂
C.氢气可以燃烧,在点燃氢气前一定要检验其纯度
D.配制50克5%的NaCl溶液时,把称好的固体倒入到量好水的量筒中进行溶解
7.实验室用氯化钠固体配制 100g 溶质质量分数为 8%的氯化钠溶液,下列说法中正确的是( )
A.经计算,所需氯化钠的质量为 0.8g B.将氯化钠直接放在托盘天平的右盘称量
C.量筒量水时仰视读数会使配得的溶液溶质质量分数偏小 D.配制溶液时,所需玻璃仪器有烧杯、玻璃棒、酒精灯
8.小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的称量氯化钠、量取水的操作规程进行操作(图示为小芳操作时的读数,其他操作都正确),小芳实际配制的氯化钠溶液的溶质质量分数约为(水的密度为lg/cm-3)
A.12.4% B.12.5% C.16.9% D.7.2%
9.实验室用氯化钠和水配制50g质量分数为6%的氯化钠溶液。下列说法正确的是
A.实验步骤:计算、量取、溶解、装瓶、贴签
B.量取水时,用规格为100mL的量筒
C.若在量取水时俯视读数量取,则配制溶液的溶质质量分数大于6%
D.实验过程中玻璃棒搅拌的作用是散热
10.配制好的生理盐水装瓶时不小心溅出少量溶液,剩余溶液溶质的质量分数( )
A.偏小 B.偏大 C.不变 D.无法判断
11.在2021年邵阳市化学实验操作考查中,小阳同学抽到的考题是“配制50g质量分数为6%的氯化钠溶液”,小阳的实验操作与目的分析均正确的一组是( )
选项 实验操作 目的分析
A 称取氯化钠时,在两边托盘上各放一张相同的纸张 整洁美观
B 称取氯化钠时,将剩余的氯化钠放回原瓶 节约药品
C 量取水时,视线与量筒内凹液面的最低处保持水平 准确读数
D 溶解氯化钠时,用玻璃棒搅拌 增大氯化钠的溶解度
A.A B.B C.C D.D
12.将20g溶质质量分数为98%的浓硫酸稀释为25%的稀硫酸。下列说法错误的是( )
A.实验步骤:计算、量取、稀释、装瓶存放
B.实验仪器:量筒、胶头滴管、烧杯、玻璃棒、细口瓶
C.溶液稀释:稀释浓硫酸时将水沿烧杯内壁慢慢注入浓硫酸中,并不断搅拌
D.事故处理:浓硫酸不慎沾到皮肤上,立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
13.下列选项中,仅利用选项中提供的实验仪器( 规格和数量不限,药品试剂省略)能够完成相应实验的是( )
选项 实验仪器 相应实验
A 铁架台、大试管、水槽、集气瓶、玻璃片 用高锰酸钾固体制取氧气
B 托盘天平、烧杯、玻璃棒、药匙、量筒、胶头滴管 用氯化钠固体配制20.0g质量分数为 6.0%的氯化钠溶液
C 集气瓶、橡胶塞、烧杯、弹簧夹 用红磷测定空气里氧气的含量
D 锥形瓶、长颈漏斗、集气瓶、导气管、单孔橡胶塞 用锌粒与稀硫酸制取氢气
A.A B.B C.C D.D
14.净化水的方法有:①过滤②加明矾吸附沉降③蒸馏④消毒杀菌⑤活性炭吸附。要将混有泥沙的天然水净化成生活用的自来水,应选用的方法和顺序为
A.②①⑤④ B.②④①③⑤ C.①②③④⑤ D.①⑤③④
二、填空题
15.请回答下列问题。
(1)正确量取20 mL液体,应选用下列____(填序号)量筒和胶头滴管。①10 mL;②25 mL;③100 mL
(2)小明想要称量3.5 g(1 g以下用游码)的食盐做实验,称量时药品和砝码放错了盘,小明同学实际称得食盐的质量为______g。
(3)小明经过纠正,正确称量3.5 g的食盐,称量过程中,指针偏向左边,他应该__________;
A.增加砝码 B.继续加药品 C.减少砝码 D.减少药品
16.配制50g质量分数为6%的氯化钠溶液,结合下列操作步骤,回答有关问题:
(1)计算:需氯化钠3g,水47mL;
(2)称量所需的氯化钠时,先调节天平平衡,然后___(选填“添加药品”或“移动游码”);
(3)量取所需的水时,应选用50mL的量筒;
(4)将称得的氯化钠倒入烧杯里,再倒入量取的水,用玻璃棒搅拌,使氯化钠溶解。在量取水时,若俯视读数,则所得氯化钠溶液中溶质的质量分数___6%(选填“大于”或“等于”或“小于”)。
17.如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
(1)用图中序号表示配制溶液的正确操作顺序是________________。
(2)图中②用来取用NaCl的仪器是________。
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示位置见图,则称取的NaCl质量为________g。
(4)若用量筒取水时仰视读数,其它操作正确,则配得NaCl溶液的质量分数__(填“大于”“小于”或“等于”)10%。
18.下表是KNO3在不同温度时的溶解度,回答问题。
温度/℃ 30 40 50 60 70 80 90
溶解度/g 45.8 63.9 85.5 110 138 169 202
⑴影响固体物质溶解度大小的因素有______、______、______。
⑵30℃时KNO3溶液的溶质质量分数的最大值是 _____(只列出表达式)。
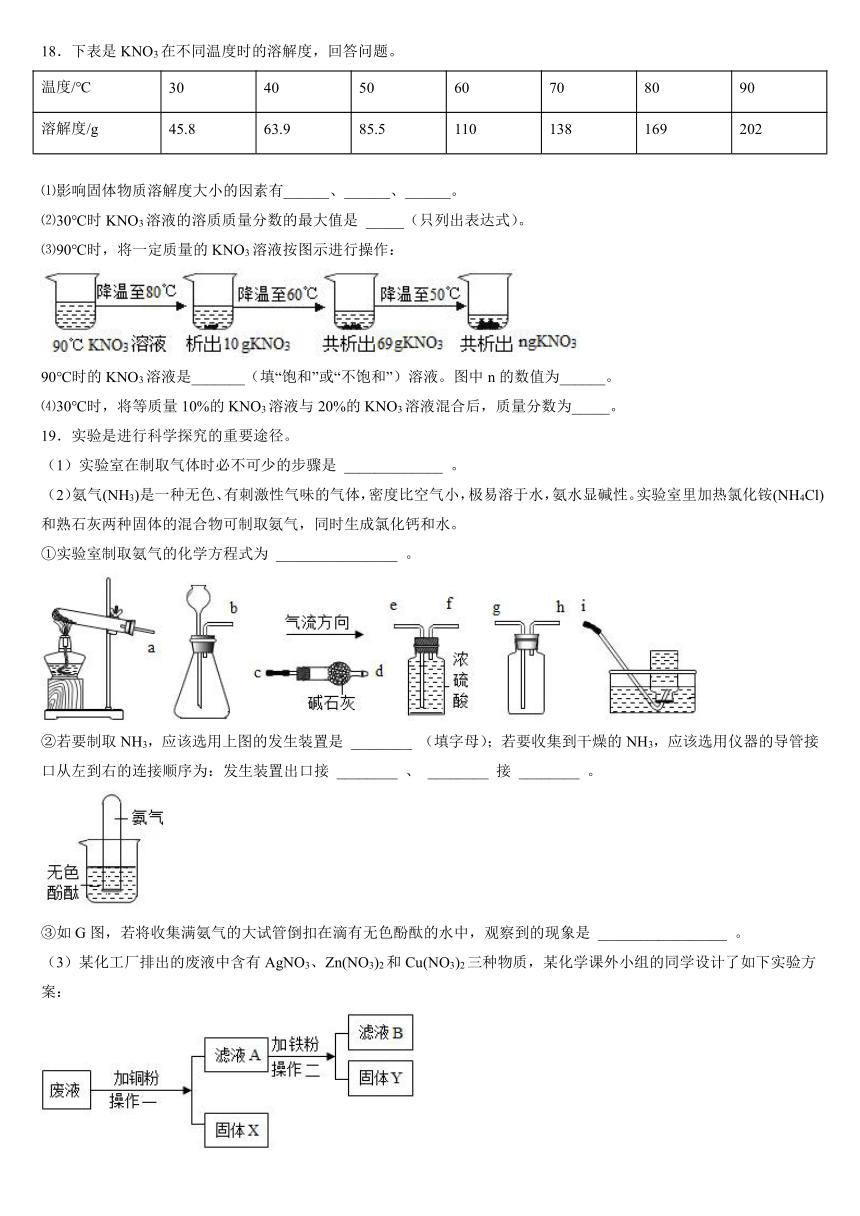
⑶90℃时,将一定质量的KNO3溶液按图示进行操作:
90℃时的KNO3溶液是_______(填“饱和”或“不饱和”)溶液。图中n的数值为______。
⑷30℃时,将等质量10%的KNO3溶液与20%的KNO3溶液混合后,质量分数为_____。
19.实验是进行科学探究的重要途径。
(1)实验室在制取气体时必不可少的步骤是 _____________ 。
(2)氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,氨水显碱性。实验室里加热氯化铵(NH4Cl)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水。
①实验室制取氨气的化学方程式为 ________________ 。
②若要制取NH3,应该选用上图的发生装置是 ________ (填字母);若要收集到干燥的NH3,应该选用仪器的导管接口从左到右的连接顺序为:发生装置出口接 ________ 、 ________ 接 ________ 。
③如G图,若将收集满氨气的大试管倒扣在滴有无色酚酞的水中,观察到的现象是 _________________ 。
(3)某化工厂排出的废液中含有AgNO3、Zn(NO3)2和Cu(NO3)2三种物质,某化学课外小组的同学设计了如下实验方案:
①写出操作一的化学方程式: _______________ ;
②若固体Y加稀硫酸无气泡产生,滤液B中的溶质最多有 ______ 种。
③滤液A的质量 _________ (填“>”、“<”或“=”)废液的质量。
(4)小华实验操作考试的题目是:配制一定溶质质量分数的碳酸钠溶液并测定其酸碱度。考试时,小华进行了如下图所示的操作:(已知碳酸钠溶液呈碱性)
①请填写标号仪器的名称:a. ___________ ;b. __________ 。
②以上实验的正确操作顺序为 ________________ (用序号字母表示)。
③上图所示操作中,若C中砝码为12g,游码的读数为2.5g,则碳酸钠实际质量为 ______ g。
④小华在测定所配制溶液的酸碱度时,先将pH试纸用蒸馏水湿润,再进行测定,则测的溶液的pH值 _________ (选填“偏大”、“偏小”或“不受影响”)。
20.如图所示是甲、乙两种固体物质的溶解度曲线。
(1)t1℃时,乙溶液中溶质与溶剂的质量比是3:13,那么乙溶液_______。(填“是”或“不是”)饱和溶液。
(2)将t2℃时等质量的甲、乙饱和溶液分别降温到t1,此时甲溶液中的溶剂质量_______(填“>”“=”或“<”)乙溶液中的。
(3)t2℃,将75g甲的饱和溶液稀释为10%,需加水_______g;若其它操作都正确,用量筒量取水时仰视读数,那么实际配制的溶液中溶质的质量分数_______(填“>””=”或“ <”)10%。
三、简答题
21.结合配制100g质量分数为6%的溶液的实验,回答下列问题。
(1)计算:需要质量分数为30%的溶液________g;
(2)量取:量取所需水时俯视读数,其他操作均正确,则配制出的稀溶液的质量分数________6%(选填“大于”、“等于”或“小于”);
(3)混匀:将准确量取的溶液和水倒入________(填写一种仪器名称)中,用玻璃棒搅拌,使溶液混合均匀;
(4)装入棕色瓶中贴好标签(标签中包括过氧化氢溶液和________),密封保存在阴凉处。
22.(1)已知:水的密度为1.0g/mL。实验室能制50g溶质质量分数为5%的氯化钠溶液,需要量取水的体积______ 。
(2)配制的操作示意图如下,该实验的正确操作顺序为______(填字母序号)。
(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是______(填序号)。
①氯化钠固体不纯 ②称量时,砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,先用蒸馏水清洗细口瓶
(4)将与水混合溶解。装瓶贴标签放置,若装瓶过程中有溶液外溅,不会影响所配制溶液的溶质质量分数,原因是______。
【参考答案】
1.B 2.D 3.D 4.D 5.A 6.B 7.C 8.C 9.C 10.C 11.A 12.D 13.D 14.B
15.(1)②(2)2.5(3)D
16.移动游码 大于
17.②⑤①④③ 药匙 18.2 小于
【解析】
(1)用图中序号表示配制溶液的正确操作顺序是②⑤①④③。(2)图中②用来取用NaCl的仪器是药匙。(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示位置见图,则称取的NaCl质量为10g+5g+3.2g=18.2g。 (4)若用量筒取水时仰视读数,其它操作正确,则配得NaCl溶液的质量分数小于10%。
18.溶质性质(或种类) 溶剂性质(或种类) 温度 不饱和 93.5 15%
【详解】
(1)影响固体物质溶解度大小的因素有温度、溶质性质(或种类)、溶剂性质(或种类);
(2)30℃时,硝酸钾的溶解度是45.8g,所以KNO3溶液的溶质质量分数的最大值是: ×100%
(3)80℃降温到60℃,析出硝酸钾质量59g,所以溶液中的溶剂质量为100g,90℃降到80℃时,应该析出33g,所以90℃时的KNO3溶液是不饱和溶液;80℃KNO3的溶解度为169g,故图中n的数值为169g+10g-85.5g=93.5g;
(4)设两种溶液的质量为mg
mg10%的KNO3溶液中硝酸钾的质量为:mg×10%,mg 20%的KNO3溶液中溶质的质量为:mg×20%,混合后溶液的总质量为2m,其中溶质的质量为mg×10%+ mg×20%,故 后溶液中溶质的质量分数为: ×100%=15%
19.【答题空1】检查装置的气密性 2NH4Cl+Ca(OH)2△CaCl2+2NH3↑+2H2O A c d h 试管内液面上升且溶液逐渐变成红色 Cu+2AgSO4=CuSO4+2Ag 4 ﹤ 玻璃棒 药匙 ECADB 9.5 偏小
【详解】
根据所学知识和题中信息知,(1)实验室在制取气体时必不可少的步骤是检查装置的气密性。(2)氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,氨水显碱性。实验室里加热氯化铵(NH4Cl)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水。①实验室制取氨气的化学方程式为NH4Cl+Ca(OH)2 CaCl2+NH3↑+H2O。②若要制取NH3,应该选用上图的发生装置是A。若要收集到干燥的NH3,应该选用仪器的导管接口从左到右的连接顺序为:发生装置出口接c、d接h。③如G图,若将收集满氨气的大试管倒扣在滴有无色酚酞的水中,观察到的现象是试管内液面上升且溶液逐渐变成红色。(3)某化工厂排出的废液中含有AgNO3、Zn(NO3)2和Cu(NO3)2三种物质,①操作一的化学方程式:Cu+2AgNO3=Cu﹙NO3﹚2+2Ag. ②若固体Y加稀硫酸无气泡产生,滤液B中的溶质最多有Zn(NO3)2和Cu(NO3)2, AgNO3, Fe(NO3)2 共4种。③滤液A的质量<废液的质量。(4)配制一定溶质质量分数的碳酸钠溶液并测定其酸碱度。①仪器的名称a. 玻璃棒。b. 药匙。②实验的正确操作顺序为ECADB。③操作中,若C中砝码为12g,游码的读数为2.5g,则碳酸钠实际质量为12g-2.5g=9.5 g. ④小华在测定所配制溶液的酸碱度时,先将pH试纸用蒸馏水湿润,再进行测定,则测的溶液的pH值偏小。
20.不是 < 175 <
21.20 大于 烧杯 溶质质量分数6%
22.47.5 CBDEA ①②③④ 溶液具有均一性
一、选择题
1.下列关于配制溶液的操作中,可导致所配制的溶液浓度偏小的是
A.用固体氯化钠配制6%的氯化钠溶液,量取水时俯视读数
B.用固体氯化钠配制6%的氯化钠溶液,所称氯化钠固体不纯
C.用固体氯化钠配制6%的氯化钠溶液,配好的溶液装瓶后,烧杯内有溶液残留
D.用6%的氯化钠溶液配制3%的氯化钠溶液,量取6%氯化钠溶液时仰视读数
2.某学生用量筒量取液体时,量筒平稳地放置在实验台上,使视线与凹液面的最低处保持水平,读数为18mL;倒出部分液体后,俯视凹液面的最低处,读数为12mL。则该学生实际倒出的液体体积
A.大于6mL B.小于6mL C.等于6mL D.无法确定
3.下列实验操作错误的是( )
A.溶解固体 B.滴加液体
C.检验氢气的纯度 D.检查蜡烛燃烧生成水
4.下列知识整理的内容中三条都正确的选项是( )
A.物质构成 B.实验操作
①构成物质的微粒有分子、原子或离子 ②空气、液氧、过氧化氢中都含有氧分子 ③氯化钠是由离子构成的化合物 ①制取气体:先加药品后检查装置气密性 ②配制一定浓度溶液;量取水时仰视度数 ③称量一定质量药品,先加药品后加砝码
C.性质与用途 D.物质鉴别
①氢气密度小——填充探空气球 ②氧气具有助燃性——可作燃料 ③活性炭具有吸附性——除去色素和异味 ①鉴别空气、二氧化碳——用燃着的小木条 ②鉴别双氧水、水——用二氧化锰 ③鉴别硬水和软水——用肥皂水
A.A B.B C.C D.D
5.下列有关实验操作或现象记录中正确的是
A.用铁钉与硫酸铜溶液在敞口的容器中反应验证质量守恒
B.配制50g溶质质量分数为15%的氯化钠溶液,用100mL量筒量取水
C.向鸡蛋清溶液中加乙酸铅溶液,产生白色沉淀,再向其中加水,白色沉淀溶解
D.将点燃的木炭放入装有氧气的集气瓶中,木炭燃烧发白光,烧杯内壁有水雾
6.下列实验方法不正确的是( )
A.可以用铁钉和硫酸铜溶液的反应验证质量守恒定律
B.用KClO3制氧气通常加入MnO2作催化剂
C.氢气可以燃烧,在点燃氢气前一定要检验其纯度
D.配制50克5%的NaCl溶液时,把称好的固体倒入到量好水的量筒中进行溶解
7.实验室用氯化钠固体配制 100g 溶质质量分数为 8%的氯化钠溶液,下列说法中正确的是( )
A.经计算,所需氯化钠的质量为 0.8g B.将氯化钠直接放在托盘天平的右盘称量
C.量筒量水时仰视读数会使配得的溶液溶质质量分数偏小 D.配制溶液时,所需玻璃仪器有烧杯、玻璃棒、酒精灯
8.小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的称量氯化钠、量取水的操作规程进行操作(图示为小芳操作时的读数,其他操作都正确),小芳实际配制的氯化钠溶液的溶质质量分数约为(水的密度为lg/cm-3)
A.12.4% B.12.5% C.16.9% D.7.2%
9.实验室用氯化钠和水配制50g质量分数为6%的氯化钠溶液。下列说法正确的是
A.实验步骤:计算、量取、溶解、装瓶、贴签
B.量取水时,用规格为100mL的量筒
C.若在量取水时俯视读数量取,则配制溶液的溶质质量分数大于6%
D.实验过程中玻璃棒搅拌的作用是散热
10.配制好的生理盐水装瓶时不小心溅出少量溶液,剩余溶液溶质的质量分数( )
A.偏小 B.偏大 C.不变 D.无法判断
11.在2021年邵阳市化学实验操作考查中,小阳同学抽到的考题是“配制50g质量分数为6%的氯化钠溶液”,小阳的实验操作与目的分析均正确的一组是( )
选项 实验操作 目的分析
A 称取氯化钠时,在两边托盘上各放一张相同的纸张 整洁美观
B 称取氯化钠时,将剩余的氯化钠放回原瓶 节约药品
C 量取水时,视线与量筒内凹液面的最低处保持水平 准确读数
D 溶解氯化钠时,用玻璃棒搅拌 增大氯化钠的溶解度
A.A B.B C.C D.D
12.将20g溶质质量分数为98%的浓硫酸稀释为25%的稀硫酸。下列说法错误的是( )
A.实验步骤:计算、量取、稀释、装瓶存放
B.实验仪器:量筒、胶头滴管、烧杯、玻璃棒、细口瓶
C.溶液稀释:稀释浓硫酸时将水沿烧杯内壁慢慢注入浓硫酸中,并不断搅拌
D.事故处理:浓硫酸不慎沾到皮肤上,立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
13.下列选项中,仅利用选项中提供的实验仪器( 规格和数量不限,药品试剂省略)能够完成相应实验的是( )
选项 实验仪器 相应实验
A 铁架台、大试管、水槽、集气瓶、玻璃片 用高锰酸钾固体制取氧气
B 托盘天平、烧杯、玻璃棒、药匙、量筒、胶头滴管 用氯化钠固体配制20.0g质量分数为 6.0%的氯化钠溶液
C 集气瓶、橡胶塞、烧杯、弹簧夹 用红磷测定空气里氧气的含量
D 锥形瓶、长颈漏斗、集气瓶、导气管、单孔橡胶塞 用锌粒与稀硫酸制取氢气
A.A B.B C.C D.D
14.净化水的方法有:①过滤②加明矾吸附沉降③蒸馏④消毒杀菌⑤活性炭吸附。要将混有泥沙的天然水净化成生活用的自来水,应选用的方法和顺序为
A.②①⑤④ B.②④①③⑤ C.①②③④⑤ D.①⑤③④
二、填空题
15.请回答下列问题。
(1)正确量取20 mL液体,应选用下列____(填序号)量筒和胶头滴管。①10 mL;②25 mL;③100 mL
(2)小明想要称量3.5 g(1 g以下用游码)的食盐做实验,称量时药品和砝码放错了盘,小明同学实际称得食盐的质量为______g。
(3)小明经过纠正,正确称量3.5 g的食盐,称量过程中,指针偏向左边,他应该__________;
A.增加砝码 B.继续加药品 C.减少砝码 D.减少药品
16.配制50g质量分数为6%的氯化钠溶液,结合下列操作步骤,回答有关问题:
(1)计算:需氯化钠3g,水47mL;
(2)称量所需的氯化钠时,先调节天平平衡,然后___(选填“添加药品”或“移动游码”);
(3)量取所需的水时,应选用50mL的量筒;
(4)将称得的氯化钠倒入烧杯里,再倒入量取的水,用玻璃棒搅拌,使氯化钠溶解。在量取水时,若俯视读数,则所得氯化钠溶液中溶质的质量分数___6%(选填“大于”或“等于”或“小于”)。
17.如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
(1)用图中序号表示配制溶液的正确操作顺序是________________。
(2)图中②用来取用NaCl的仪器是________。
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示位置见图,则称取的NaCl质量为________g。
(4)若用量筒取水时仰视读数,其它操作正确,则配得NaCl溶液的质量分数__(填“大于”“小于”或“等于”)10%。
18.下表是KNO3在不同温度时的溶解度,回答问题。
温度/℃ 30 40 50 60 70 80 90
溶解度/g 45.8 63.9 85.5 110 138 169 202
⑴影响固体物质溶解度大小的因素有______、______、______。
⑵30℃时KNO3溶液的溶质质量分数的最大值是 _____(只列出表达式)。
⑶90℃时,将一定质量的KNO3溶液按图示进行操作:
90℃时的KNO3溶液是_______(填“饱和”或“不饱和”)溶液。图中n的数值为______。
⑷30℃时,将等质量10%的KNO3溶液与20%的KNO3溶液混合后,质量分数为_____。
19.实验是进行科学探究的重要途径。
(1)实验室在制取气体时必不可少的步骤是 _____________ 。
(2)氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,氨水显碱性。实验室里加热氯化铵(NH4Cl)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水。
①实验室制取氨气的化学方程式为 ________________ 。
②若要制取NH3,应该选用上图的发生装置是 ________ (填字母);若要收集到干燥的NH3,应该选用仪器的导管接口从左到右的连接顺序为:发生装置出口接 ________ 、 ________ 接 ________ 。
③如G图,若将收集满氨气的大试管倒扣在滴有无色酚酞的水中,观察到的现象是 _________________ 。
(3)某化工厂排出的废液中含有AgNO3、Zn(NO3)2和Cu(NO3)2三种物质,某化学课外小组的同学设计了如下实验方案:
①写出操作一的化学方程式: _______________ ;
②若固体Y加稀硫酸无气泡产生,滤液B中的溶质最多有 ______ 种。
③滤液A的质量 _________ (填“>”、“<”或“=”)废液的质量。
(4)小华实验操作考试的题目是:配制一定溶质质量分数的碳酸钠溶液并测定其酸碱度。考试时,小华进行了如下图所示的操作:(已知碳酸钠溶液呈碱性)
①请填写标号仪器的名称:a. ___________ ;b. __________ 。
②以上实验的正确操作顺序为 ________________ (用序号字母表示)。
③上图所示操作中,若C中砝码为12g,游码的读数为2.5g,则碳酸钠实际质量为 ______ g。
④小华在测定所配制溶液的酸碱度时,先将pH试纸用蒸馏水湿润,再进行测定,则测的溶液的pH值 _________ (选填“偏大”、“偏小”或“不受影响”)。
20.如图所示是甲、乙两种固体物质的溶解度曲线。
(1)t1℃时,乙溶液中溶质与溶剂的质量比是3:13,那么乙溶液_______。(填“是”或“不是”)饱和溶液。
(2)将t2℃时等质量的甲、乙饱和溶液分别降温到t1,此时甲溶液中的溶剂质量_______(填“>”“=”或“<”)乙溶液中的。
(3)t2℃,将75g甲的饱和溶液稀释为10%,需加水_______g;若其它操作都正确,用量筒量取水时仰视读数,那么实际配制的溶液中溶质的质量分数_______(填“>””=”或“ <”)10%。
三、简答题
21.结合配制100g质量分数为6%的溶液的实验,回答下列问题。
(1)计算:需要质量分数为30%的溶液________g;
(2)量取:量取所需水时俯视读数,其他操作均正确,则配制出的稀溶液的质量分数________6%(选填“大于”、“等于”或“小于”);
(3)混匀:将准确量取的溶液和水倒入________(填写一种仪器名称)中,用玻璃棒搅拌,使溶液混合均匀;
(4)装入棕色瓶中贴好标签(标签中包括过氧化氢溶液和________),密封保存在阴凉处。
22.(1)已知:水的密度为1.0g/mL。实验室能制50g溶质质量分数为5%的氯化钠溶液,需要量取水的体积______ 。
(2)配制的操作示意图如下,该实验的正确操作顺序为______(填字母序号)。
(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是______(填序号)。
①氯化钠固体不纯 ②称量时,砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,先用蒸馏水清洗细口瓶
(4)将与水混合溶解。装瓶贴标签放置,若装瓶过程中有溶液外溅,不会影响所配制溶液的溶质质量分数,原因是______。
【参考答案】
1.B 2.D 3.D 4.D 5.A 6.B 7.C 8.C 9.C 10.C 11.A 12.D 13.D 14.B
15.(1)②(2)2.5(3)D
16.移动游码 大于
17.②⑤①④③ 药匙 18.2 小于
【解析】
(1)用图中序号表示配制溶液的正确操作顺序是②⑤①④③。(2)图中②用来取用NaCl的仪器是药匙。(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示位置见图,则称取的NaCl质量为10g+5g+3.2g=18.2g。 (4)若用量筒取水时仰视读数,其它操作正确,则配得NaCl溶液的质量分数小于10%。
18.溶质性质(或种类) 溶剂性质(或种类) 温度 不饱和 93.5 15%
【详解】
(1)影响固体物质溶解度大小的因素有温度、溶质性质(或种类)、溶剂性质(或种类);
(2)30℃时,硝酸钾的溶解度是45.8g,所以KNO3溶液的溶质质量分数的最大值是: ×100%
(3)80℃降温到60℃,析出硝酸钾质量59g,所以溶液中的溶剂质量为100g,90℃降到80℃时,应该析出33g,所以90℃时的KNO3溶液是不饱和溶液;80℃KNO3的溶解度为169g,故图中n的数值为169g+10g-85.5g=93.5g;
(4)设两种溶液的质量为mg
mg10%的KNO3溶液中硝酸钾的质量为:mg×10%,mg 20%的KNO3溶液中溶质的质量为:mg×20%,混合后溶液的总质量为2m,其中溶质的质量为mg×10%+ mg×20%,故 后溶液中溶质的质量分数为: ×100%=15%
19.【答题空1】检查装置的气密性 2NH4Cl+Ca(OH)2△CaCl2+2NH3↑+2H2O A c d h 试管内液面上升且溶液逐渐变成红色 Cu+2AgSO4=CuSO4+2Ag 4 ﹤ 玻璃棒 药匙 ECADB 9.5 偏小
【详解】
根据所学知识和题中信息知,(1)实验室在制取气体时必不可少的步骤是检查装置的气密性。(2)氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,氨水显碱性。实验室里加热氯化铵(NH4Cl)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水。①实验室制取氨气的化学方程式为NH4Cl+Ca(OH)2 CaCl2+NH3↑+H2O。②若要制取NH3,应该选用上图的发生装置是A。若要收集到干燥的NH3,应该选用仪器的导管接口从左到右的连接顺序为:发生装置出口接c、d接h。③如G图,若将收集满氨气的大试管倒扣在滴有无色酚酞的水中,观察到的现象是试管内液面上升且溶液逐渐变成红色。(3)某化工厂排出的废液中含有AgNO3、Zn(NO3)2和Cu(NO3)2三种物质,①操作一的化学方程式:Cu+2AgNO3=Cu﹙NO3﹚2+2Ag. ②若固体Y加稀硫酸无气泡产生,滤液B中的溶质最多有Zn(NO3)2和Cu(NO3)2, AgNO3, Fe(NO3)2 共4种。③滤液A的质量<废液的质量。(4)配制一定溶质质量分数的碳酸钠溶液并测定其酸碱度。①仪器的名称a. 玻璃棒。b. 药匙。②实验的正确操作顺序为ECADB。③操作中,若C中砝码为12g,游码的读数为2.5g,则碳酸钠实际质量为12g-2.5g=9.5 g. ④小华在测定所配制溶液的酸碱度时,先将pH试纸用蒸馏水湿润,再进行测定,则测的溶液的pH值偏小。
20.不是 < 175 <
21.20 大于 烧杯 溶质质量分数6%
22.47.5 CBDEA ①②③④ 溶液具有均一性
同课章节目录
