2022年人教版九年级化学下册-第九单元 溶液 测试题 (word版 含答案)
文档属性
| 名称 | 2022年人教版九年级化学下册-第九单元 溶液 测试题 (word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 182.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-15 00:00:00 | ||
图片预览



文档简介
第九单元《溶液》测试题
一、单选题
1.把少量下列物质分别放入水中,充分搅拌,可以得到有色溶液的是
A.面粉 B.蔗糖 C.汽油 D.高锰酸钾
2.下列物质的用途主要由其化学性质决定的是
A.用汽油清洗衣服上的油污 B.用氧气急救病人
C.钨用于制作白炽灯的灯丝 D.活性炭用于冰箱除味剂
3.下列有关水与溶液的说法错误的是
A.电解水实验说明水是由氢元素和氧元素组成的
B.农药、化肥不合理使用,会造成水体污染
C.饱和溶液就是不能再溶解任何物质的溶液
D.天然淡水生产自来水需要经过沉降、过滤、吸附、杀菌消毒等净化过程
4.下列排序正确的是
A.溶解时放出的热量: B.氮元素的化合价:
C.地壳中元素含量: D.金属活动性顺序:
5.下列实验操作不能达到实验目的的是
选项 物质 目的 主要实验操作
A 铜粉中混有少量炭粉 除杂 在空气中灼烧
B NaCl和NH4NO3固体 鉴别 取样,分别加适量水溶解
C CO中是否混有CH4 检验 点燃,火焰上方罩干冷烧杯
D KCl和MnO2固体 分离 溶解、过滤、洗涤、干燥、蒸发
A.A B.B C.C D.D
6.下列有关溶液的说法,正确的是
A.一杯溶液中只可能有一种溶质
B.饱和溶液一定比不饱和溶液浓度大
C.20℃时,100g水中最多能溶解36gNaCl。则NaCl 的溶解度为36g
D.海水晒盐后剩下的母液一定是氯化钠的饱和溶液
7.下列有关化学知识的表述,不正确的是
A.用洗涤剂清洗油污与用汽油清洗油污所用的原理是不同的
B.用水分别溶解测温的方法可以区分氢氧化钠 氯化钠 硝酸铵三种白色固体
C.过滤可以使硬水转化为软水
D.不同种元素之间最本质的不同是质子数不同
8.下列说法正确的是
A.2gH2跟32gO2完全反应,可得到34gH2O
B.用含Fe2O385%的赤铁矿160t,理论上可生产100t含杂质4.8%的生铁
C.等质量镁和锌分别与足量盐酸完全反应,镁产生的H2多说明镁金属活动性比锌强
D.10g固体A与90g水混合,固体完全消失,所得溶液中溶质质量分数一定为10%
9.某小组对铁钉锈蚀的条件进行了如图探究,一周后观察,下列说法错误的是
A.①和②中的铁钉无明显变化,③中铁钉生锈
B.②中的蒸馏水要先煮沸,目的是除去水中溶解的氧气
C.③中的铁钉甲、乙、丙三处,甲处锈蚀得最严重
D.铁生锈与氧气、水有关
10.在相同温度下,将50g和100g饱和的KNO3溶液分别蒸发掉10g水和20g水,分别析出ag和bg溶质。则a和b的关系是
A.2a=b B.a=b C.a=2b D.a11.实验室提纯含少量泥沙的粗盐,一般操作流程如下。下列说法正确的是
A.操作①的作用是增大食盐的溶解度 B.操作②中可通过升高温度加速溶解
C.操作③中可用玻璃棒搅拌加速过滤 D.操作④中要将液体蒸干后停止加热
12.将60℃时的硝酸钾饱和溶液降温至20℃,下列说法中正确的是
A.饱和溶液变为不饱和溶液
B.溶液中溶质、溶剂的质量都发生改变
C.溶液中溶质的质量分数不变
D.溶液中有晶体析出
13.溶液在生产与生活中应用广泛。下列有关溶液的说法正确的是
A.搅拌或将固体溶质碾成粉末都可增大溶解速率
B.溶液中不能同时存在两种溶质
C.只有固体和液体才可以作为溶质
D.西瓜汁、冰水、可乐都是溶液
14.向16.8g铁粉中先加入200g稀硫酸,充分反应后再逐滴加入一定量的硫酸铜溶液,反应过程中所得剩余固体质量与加入物质的质量关系如图所示,下列说法正确的是
A.稀硫酸中硫酸质量分数为9.8%
B.a点和b点溶液中的溶质种类相同
C.m=12
D.向c点中固体中加入稀硫酸,有气泡产生
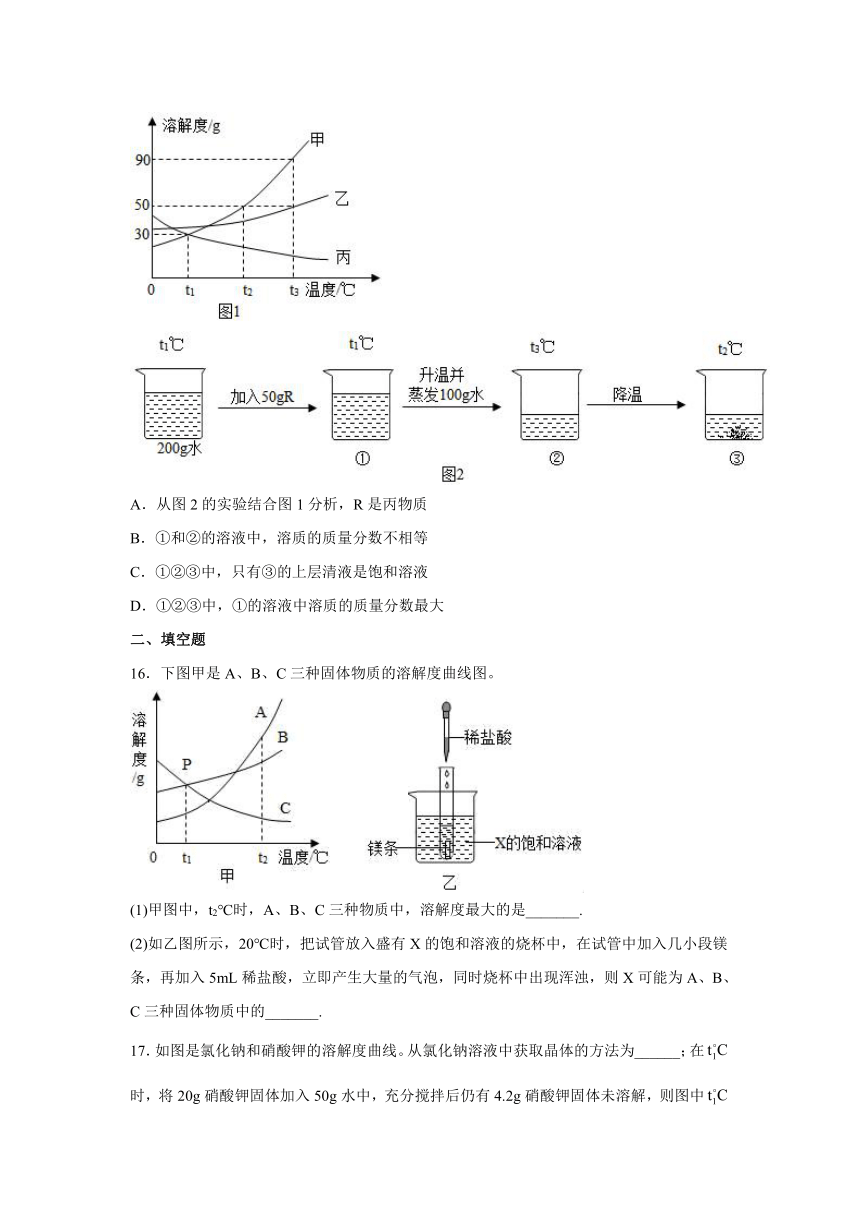
15.图1是甲,乙、丙三种物质的溶解度曲线,R是其中一种物质。现取50gR如图2进行有关实验,观察到①②中没有固体析出,③中有固体析出。下列说法正确的是
A.从图2的实验结合图1分析,R是丙物质
B.①和②的溶液中,溶质的质量分数不相等
C.①②③中,只有③的上层清液是饱和溶液
D.①②③中,①的溶液中溶质的质量分数最大
二、填空题
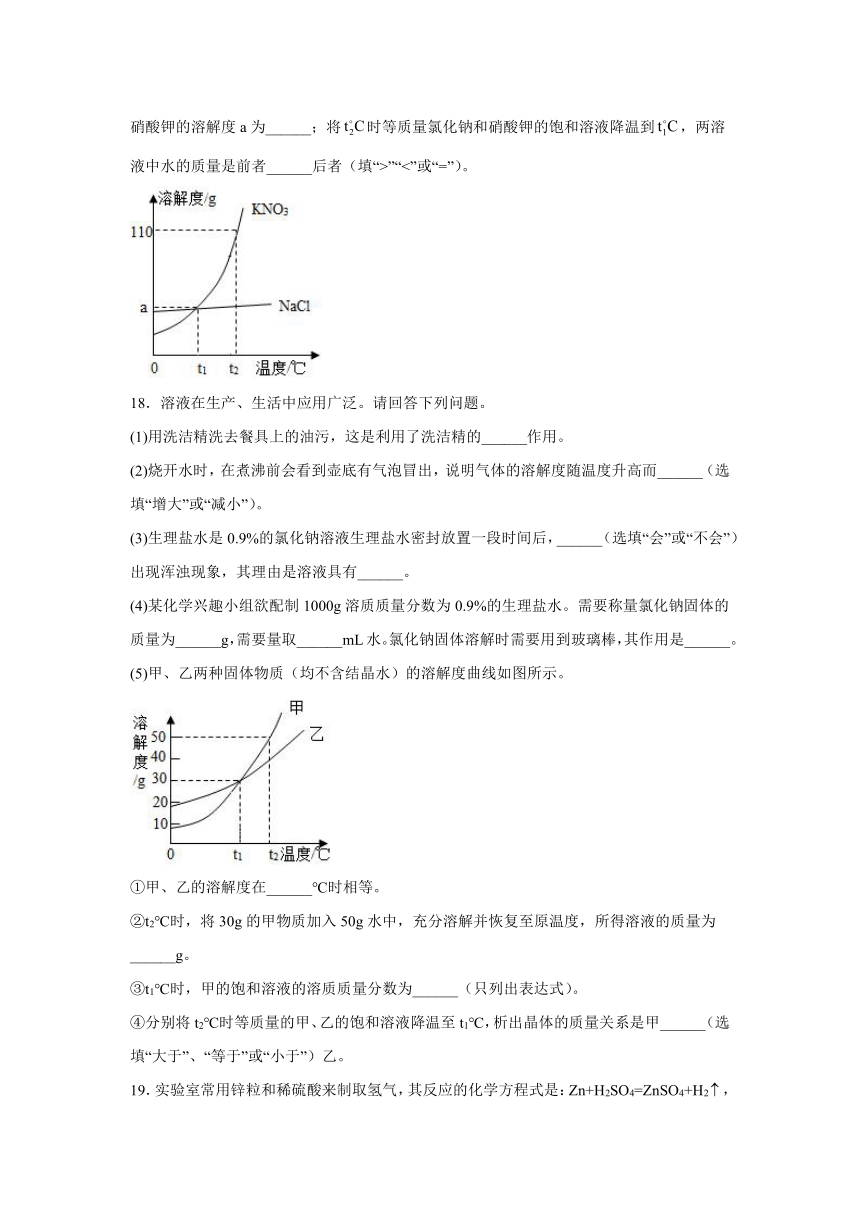
16.下图甲是A、B、C三种固体物质的溶解度曲线图。
(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是_______.
(2)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的_______.
17.如图是氯化钠和硝酸钾的溶解度曲线。从氯化钠溶液中获取晶体的方法为______;在时,将20g硝酸钾固体加入50g水中,充分搅拌后仍有4.2g硝酸钾固体未溶解,则图中硝酸钾的溶解度a为______;将时等质量氯化钠和硝酸钾的饱和溶液降温到,两溶液中水的质量是前者______后者(填“>”“<”或“=”)。
18.溶液在生产、生活中应用广泛。请回答下列问题。
(1)用洗洁精洗去餐具上的油污,这是利用了洗洁精的______作用。
(2)烧开水时,在煮沸前会看到壶底有气泡冒出,说明气体的溶解度随温度升高而______(选填“增大”或“减小”)。
(3)生理盐水是0.9%的氯化钠溶液生理盐水密封放置一段时间后,______(选填“会”或“不会”)出现浑浊现象,其理由是溶液具有______。
(4)某化学兴趣小组欲配制1000g溶质质量分数为0.9%的生理盐水。需要称量氯化钠固体的质量为______g,需要量取______mL水。氯化钠固体溶解时需要用到玻璃棒,其作用是______。
(5)甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示。
①甲、乙的溶解度在______℃时相等。
②t2℃时,将30g的甲物质加入50g水中,充分溶解并恢复至原温度,所得溶液的质量为______g。
③t1℃时,甲的饱和溶液的溶质质量分数为______(只列出表达式)。
④分别将t2℃时等质量的甲、乙的饱和溶液降温至t1℃,析出晶体的质量关系是甲______(选填“大于”、“等于”或“小于”)乙。
19.实验室常用锌粒和稀硫酸来制取氢气,其反应的化学方程式是:Zn+H2SO4=ZnSO4+H2,生成氢气的质量和加入锌粒的质量关系如下图所示,完成下列各小题:
(1)P点对应的溶液中溶质的成分是___________。
A.H2SO4 B.ZnSO4 C.H2SO4和ZnSO4
(2)为了验证Q点溶液是否是该温度下溶质的饱和溶液,以下方法可行的是___________。
A.加入少量该溶质,看是否溶解
B.蒸发溶剂看是否有晶体析出
C.加入少量食盐颗粒,看是否溶解
(3)Q点溶液中溶质的质量分数___________(填“大于”、“小于”或“等于”)M点溶液中溶质的质量分数。
20.水是人及一切生物生存所必需的,我们应该了解有关水的一些知识。
(1)水是由______组成的。
(2)硬水给生活和生产带来很多麻烦,含有______(填一种离子符号)较多的水称为硬水。我们通常用______来区分软水和硬水,生活中通过______的方法可以降低水的硬度。
(3)下列物质分别加入蒸馏水中,不断搅拌后,能形成无色溶液的是______(填序号)。
A.面粉 B.硫酸铜 C.蔗糖 D.食用油
(4)如图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,该反应的化学方程式为______。
三、推断题
21.A、B、C、D、E、F均是初中化学中的常见物质,其中A、D为单质,其余均为化合物,B、C由两种相同元素组成。
(1)若A在完全燃烧和不完全燃烧时,生成不同的气体。则A完全燃烧时反应的化学方程式为 ___________________________ ,该反应属于基本反应类型中的 _____________ 反应。
(2)B溶液在一定条件下可反应生成C和无色气体D,C和D都与生命活动息息相关。B溶液中的溶质是(用化学式表示),D物质的一种用途是 _____________ 。
(3)如图所示将固体E放入大烧杯中的水里,小烧杯中F的饱和溶液变浑浊。
则E的化学式可能为 _____________ ,产生此现象的原因是 _____________ 。
22.A、B、C、D和甲、乙均为初中化学中常见的物质,物质间存在着如图所示的相互转化关系(部分生成物未标出).请回答下列问题:
(1)若A为气体氧化物,与溶液甲和溶液乙反应均生成盐和水.则A的化学式为______;取溶液D少量于试管中,加入碳酸钠溶液,有白色沉淀生成,则溶液D中溶质为______(写化学式);③反应的化学方程式为______.
(2)若向一定质量的碳酸钠溶液中加入足量的氯化钙溶液,所得沉淀质量等于原碳酸钠溶液质量的,则原碳酸钠溶液中溶质的质量分数为______.
四、实验题
23.小明要用 100g 质量分数为 10%的氢氧化钠溶液来制作“叶脉书签”,如图是他配制氢氧化钠溶液的实验操作示意图。
(1)量取所需要的水应选择___________ (选填“10”、“50”或“100”)mL 量筒。
(2)指出图中的一处操作错误:___________ 。
(3)用如图图示的序号表示配制溶液的操作顺序 ___________。
(4)要将此溶液稀释成 4%的溶液,需加水多少克?(写出计算过程)
五、计算题
24.某化学兴趣小组同学在清理实验室时发现一瓶浓盐酸,标签如图。报据标签计算:
(1)HC1中氢元素和氯元素的质量比为____________(最简整数比表示)
(2)要配制3700g溶质质量分数为10%的稀盐酸,需要用到这种浓盐酸和水,其中需要用水的质量为_______g(配制过程中不考虑浓盐酸的挥发)。
25.某品牌钙片的部分信息:①钙片主要成分为碳酸钙;②每片钙片的质量为1g。某科学学习小组同学用该品牌钙片做了如下实验:把100g稀盐酸分成五等份,分次将稀盐酸添加到放有12片钙片的烧杯中,充分反应(钙片中其它成分不溶于水且不与盐酸反应)。剩余固体的质量为2g。
(1)钙片中所含的“钙”是指______(填序号)。
A.元素 B.单质 C.原子
(2)计算该实验中所用稀盐酸的溶质质量分数(写出计算过程)
参考答案:
1.D 2.B 3.C 4.B 5.A 6.D 7.C 8.B 9.C 10.A 11.B 12.D 13.A 14.B 15.B 16.(1)A
(2)C
17. 蒸发结晶 31.6 >
18.(1)乳化
(2)减小
(3) 不会 均一性、稳定性
(4) 9 991 加速溶解
(5) t1 75 大于
19.(1)C
(2)A
(3)等于
20.(1)氢元素和氧元素
(2) Ca2+##Mg2+ 肥皂水 煮沸
(3)C
(4)
21. C+O2CO2;化合反应 H2O2;潜水(答案合理给分) NaOH(或CaO); 溶于水或与水反应放出热量,F溶液温度升高; 氢氧化钙的溶解度随温度的升高而降低,有固体析出。
22. CO2 NaOH、Ca(OH)2 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 53%
23.(1)100
(2)氢氧化钠放在右盘(或读取量筒读数时仰视)
(3)④①③⑤②
(4)设需加水的质量为 x
100g×10%=(100g+x)×4%
x=150g
答:稀释成 4%的溶液,需加水 150 克。
24.(1)2:71
(2)2700
25.(1)A
(2)解:参加反应的碳酸钙的质量为1g×12-2g=10g
设参与反应的氯化氢的质量为x
所以使用的稀盐酸的溶质质量分数为
答:所以使用的稀盐酸的溶质质量分数为7.3%。
一、单选题
1.把少量下列物质分别放入水中,充分搅拌,可以得到有色溶液的是
A.面粉 B.蔗糖 C.汽油 D.高锰酸钾
2.下列物质的用途主要由其化学性质决定的是
A.用汽油清洗衣服上的油污 B.用氧气急救病人
C.钨用于制作白炽灯的灯丝 D.活性炭用于冰箱除味剂
3.下列有关水与溶液的说法错误的是
A.电解水实验说明水是由氢元素和氧元素组成的
B.农药、化肥不合理使用,会造成水体污染
C.饱和溶液就是不能再溶解任何物质的溶液
D.天然淡水生产自来水需要经过沉降、过滤、吸附、杀菌消毒等净化过程
4.下列排序正确的是
A.溶解时放出的热量: B.氮元素的化合价:
C.地壳中元素含量: D.金属活动性顺序:
5.下列实验操作不能达到实验目的的是
选项 物质 目的 主要实验操作
A 铜粉中混有少量炭粉 除杂 在空气中灼烧
B NaCl和NH4NO3固体 鉴别 取样,分别加适量水溶解
C CO中是否混有CH4 检验 点燃,火焰上方罩干冷烧杯
D KCl和MnO2固体 分离 溶解、过滤、洗涤、干燥、蒸发
A.A B.B C.C D.D
6.下列有关溶液的说法,正确的是
A.一杯溶液中只可能有一种溶质
B.饱和溶液一定比不饱和溶液浓度大
C.20℃时,100g水中最多能溶解36gNaCl。则NaCl 的溶解度为36g
D.海水晒盐后剩下的母液一定是氯化钠的饱和溶液
7.下列有关化学知识的表述,不正确的是
A.用洗涤剂清洗油污与用汽油清洗油污所用的原理是不同的
B.用水分别溶解测温的方法可以区分氢氧化钠 氯化钠 硝酸铵三种白色固体
C.过滤可以使硬水转化为软水
D.不同种元素之间最本质的不同是质子数不同
8.下列说法正确的是
A.2gH2跟32gO2完全反应,可得到34gH2O
B.用含Fe2O385%的赤铁矿160t,理论上可生产100t含杂质4.8%的生铁
C.等质量镁和锌分别与足量盐酸完全反应,镁产生的H2多说明镁金属活动性比锌强
D.10g固体A与90g水混合,固体完全消失,所得溶液中溶质质量分数一定为10%
9.某小组对铁钉锈蚀的条件进行了如图探究,一周后观察,下列说法错误的是
A.①和②中的铁钉无明显变化,③中铁钉生锈
B.②中的蒸馏水要先煮沸,目的是除去水中溶解的氧气
C.③中的铁钉甲、乙、丙三处,甲处锈蚀得最严重
D.铁生锈与氧气、水有关
10.在相同温度下,将50g和100g饱和的KNO3溶液分别蒸发掉10g水和20g水,分别析出ag和bg溶质。则a和b的关系是
A.2a=b B.a=b C.a=2b D.a
A.操作①的作用是增大食盐的溶解度 B.操作②中可通过升高温度加速溶解
C.操作③中可用玻璃棒搅拌加速过滤 D.操作④中要将液体蒸干后停止加热
12.将60℃时的硝酸钾饱和溶液降温至20℃,下列说法中正确的是
A.饱和溶液变为不饱和溶液
B.溶液中溶质、溶剂的质量都发生改变
C.溶液中溶质的质量分数不变
D.溶液中有晶体析出
13.溶液在生产与生活中应用广泛。下列有关溶液的说法正确的是
A.搅拌或将固体溶质碾成粉末都可增大溶解速率
B.溶液中不能同时存在两种溶质
C.只有固体和液体才可以作为溶质
D.西瓜汁、冰水、可乐都是溶液
14.向16.8g铁粉中先加入200g稀硫酸,充分反应后再逐滴加入一定量的硫酸铜溶液,反应过程中所得剩余固体质量与加入物质的质量关系如图所示,下列说法正确的是
A.稀硫酸中硫酸质量分数为9.8%
B.a点和b点溶液中的溶质种类相同
C.m=12
D.向c点中固体中加入稀硫酸,有气泡产生
15.图1是甲,乙、丙三种物质的溶解度曲线,R是其中一种物质。现取50gR如图2进行有关实验,观察到①②中没有固体析出,③中有固体析出。下列说法正确的是
A.从图2的实验结合图1分析,R是丙物质
B.①和②的溶液中,溶质的质量分数不相等
C.①②③中,只有③的上层清液是饱和溶液
D.①②③中,①的溶液中溶质的质量分数最大
二、填空题
16.下图甲是A、B、C三种固体物质的溶解度曲线图。
(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是_______.
(2)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的_______.
17.如图是氯化钠和硝酸钾的溶解度曲线。从氯化钠溶液中获取晶体的方法为______;在时,将20g硝酸钾固体加入50g水中,充分搅拌后仍有4.2g硝酸钾固体未溶解,则图中硝酸钾的溶解度a为______;将时等质量氯化钠和硝酸钾的饱和溶液降温到,两溶液中水的质量是前者______后者(填“>”“<”或“=”)。
18.溶液在生产、生活中应用广泛。请回答下列问题。
(1)用洗洁精洗去餐具上的油污,这是利用了洗洁精的______作用。
(2)烧开水时,在煮沸前会看到壶底有气泡冒出,说明气体的溶解度随温度升高而______(选填“增大”或“减小”)。
(3)生理盐水是0.9%的氯化钠溶液生理盐水密封放置一段时间后,______(选填“会”或“不会”)出现浑浊现象,其理由是溶液具有______。
(4)某化学兴趣小组欲配制1000g溶质质量分数为0.9%的生理盐水。需要称量氯化钠固体的质量为______g,需要量取______mL水。氯化钠固体溶解时需要用到玻璃棒,其作用是______。
(5)甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示。
①甲、乙的溶解度在______℃时相等。
②t2℃时,将30g的甲物质加入50g水中,充分溶解并恢复至原温度,所得溶液的质量为______g。
③t1℃时,甲的饱和溶液的溶质质量分数为______(只列出表达式)。
④分别将t2℃时等质量的甲、乙的饱和溶液降温至t1℃,析出晶体的质量关系是甲______(选填“大于”、“等于”或“小于”)乙。
19.实验室常用锌粒和稀硫酸来制取氢气,其反应的化学方程式是:Zn+H2SO4=ZnSO4+H2,生成氢气的质量和加入锌粒的质量关系如下图所示,完成下列各小题:
(1)P点对应的溶液中溶质的成分是___________。
A.H2SO4 B.ZnSO4 C.H2SO4和ZnSO4
(2)为了验证Q点溶液是否是该温度下溶质的饱和溶液,以下方法可行的是___________。
A.加入少量该溶质,看是否溶解
B.蒸发溶剂看是否有晶体析出
C.加入少量食盐颗粒,看是否溶解
(3)Q点溶液中溶质的质量分数___________(填“大于”、“小于”或“等于”)M点溶液中溶质的质量分数。
20.水是人及一切生物生存所必需的,我们应该了解有关水的一些知识。
(1)水是由______组成的。
(2)硬水给生活和生产带来很多麻烦,含有______(填一种离子符号)较多的水称为硬水。我们通常用______来区分软水和硬水,生活中通过______的方法可以降低水的硬度。
(3)下列物质分别加入蒸馏水中,不断搅拌后,能形成无色溶液的是______(填序号)。
A.面粉 B.硫酸铜 C.蔗糖 D.食用油
(4)如图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,该反应的化学方程式为______。
三、推断题
21.A、B、C、D、E、F均是初中化学中的常见物质,其中A、D为单质,其余均为化合物,B、C由两种相同元素组成。
(1)若A在完全燃烧和不完全燃烧时,生成不同的气体。则A完全燃烧时反应的化学方程式为 ___________________________ ,该反应属于基本反应类型中的 _____________ 反应。
(2)B溶液在一定条件下可反应生成C和无色气体D,C和D都与生命活动息息相关。B溶液中的溶质是(用化学式表示),D物质的一种用途是 _____________ 。
(3)如图所示将固体E放入大烧杯中的水里,小烧杯中F的饱和溶液变浑浊。
则E的化学式可能为 _____________ ,产生此现象的原因是 _____________ 。
22.A、B、C、D和甲、乙均为初中化学中常见的物质,物质间存在着如图所示的相互转化关系(部分生成物未标出).请回答下列问题:
(1)若A为气体氧化物,与溶液甲和溶液乙反应均生成盐和水.则A的化学式为______;取溶液D少量于试管中,加入碳酸钠溶液,有白色沉淀生成,则溶液D中溶质为______(写化学式);③反应的化学方程式为______.
(2)若向一定质量的碳酸钠溶液中加入足量的氯化钙溶液,所得沉淀质量等于原碳酸钠溶液质量的,则原碳酸钠溶液中溶质的质量分数为______.
四、实验题
23.小明要用 100g 质量分数为 10%的氢氧化钠溶液来制作“叶脉书签”,如图是他配制氢氧化钠溶液的实验操作示意图。
(1)量取所需要的水应选择___________ (选填“10”、“50”或“100”)mL 量筒。
(2)指出图中的一处操作错误:___________ 。
(3)用如图图示的序号表示配制溶液的操作顺序 ___________。
(4)要将此溶液稀释成 4%的溶液,需加水多少克?(写出计算过程)
五、计算题
24.某化学兴趣小组同学在清理实验室时发现一瓶浓盐酸,标签如图。报据标签计算:
(1)HC1中氢元素和氯元素的质量比为____________(最简整数比表示)
(2)要配制3700g溶质质量分数为10%的稀盐酸,需要用到这种浓盐酸和水,其中需要用水的质量为_______g(配制过程中不考虑浓盐酸的挥发)。
25.某品牌钙片的部分信息:①钙片主要成分为碳酸钙;②每片钙片的质量为1g。某科学学习小组同学用该品牌钙片做了如下实验:把100g稀盐酸分成五等份,分次将稀盐酸添加到放有12片钙片的烧杯中,充分反应(钙片中其它成分不溶于水且不与盐酸反应)。剩余固体的质量为2g。
(1)钙片中所含的“钙”是指______(填序号)。
A.元素 B.单质 C.原子
(2)计算该实验中所用稀盐酸的溶质质量分数(写出计算过程)
参考答案:
1.D 2.B 3.C 4.B 5.A 6.D 7.C 8.B 9.C 10.A 11.B 12.D 13.A 14.B 15.B 16.(1)A
(2)C
17. 蒸发结晶 31.6 >
18.(1)乳化
(2)减小
(3) 不会 均一性、稳定性
(4) 9 991 加速溶解
(5) t1 75 大于
19.(1)C
(2)A
(3)等于
20.(1)氢元素和氧元素
(2) Ca2+##Mg2+ 肥皂水 煮沸
(3)C
(4)
21. C+O2CO2;化合反应 H2O2;潜水(答案合理给分) NaOH(或CaO); 溶于水或与水反应放出热量,F溶液温度升高; 氢氧化钙的溶解度随温度的升高而降低,有固体析出。
22. CO2 NaOH、Ca(OH)2 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 53%
23.(1)100
(2)氢氧化钠放在右盘(或读取量筒读数时仰视)
(3)④①③⑤②
(4)设需加水的质量为 x
100g×10%=(100g+x)×4%
x=150g
答:稀释成 4%的溶液,需加水 150 克。
24.(1)2:71
(2)2700
25.(1)A
(2)解:参加反应的碳酸钙的质量为1g×12-2g=10g
设参与反应的氯化氢的质量为x
所以使用的稀盐酸的溶质质量分数为
答:所以使用的稀盐酸的溶质质量分数为7.3%。
同课章节目录
