2022年人教版九年级化学下册9.3 溶液的浓度 第1课时同步练习(word版 含答案)
文档属性
| 名称 | 2022年人教版九年级化学下册9.3 溶液的浓度 第1课时同步练习(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 346.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-15 00:00:00 | ||
图片预览


文档简介
第1课时 溶质的质量分数
一 选择题
1.下列关于“10%的硝酸钾溶液”含义的说法中,错误的是( )
A.100 g水中溶解了10 g硝酸钾
B.100 g硝酸钾溶液中有10 g硝酸钾
C.将10 g硝酸钾溶于90 g水中所得的溶液
D.将硝酸钾与水按1:9的质量比配制的溶液
2.向100 g质量分数为10%的NaOH溶液中加入12.5 g NaOH固体,完全溶解后,所得溶液溶质质量分数为( )
A.12.5% B.20% C.22.5% D.25%
3.将100 g 98%的浓硫酸注入900 g水中,所得稀硫酸中溶质的质量分数为( )
A.9.8% B.10.0% C.10.9% D.11.1%
4.将200 g溶质质量分数为10%的氯化钠溶液与300 g溶质质量分数为15%的氯化钠溶液相互混合,所得溶液溶质质量分数为( )
A.8% B.12% C.15% D.13%
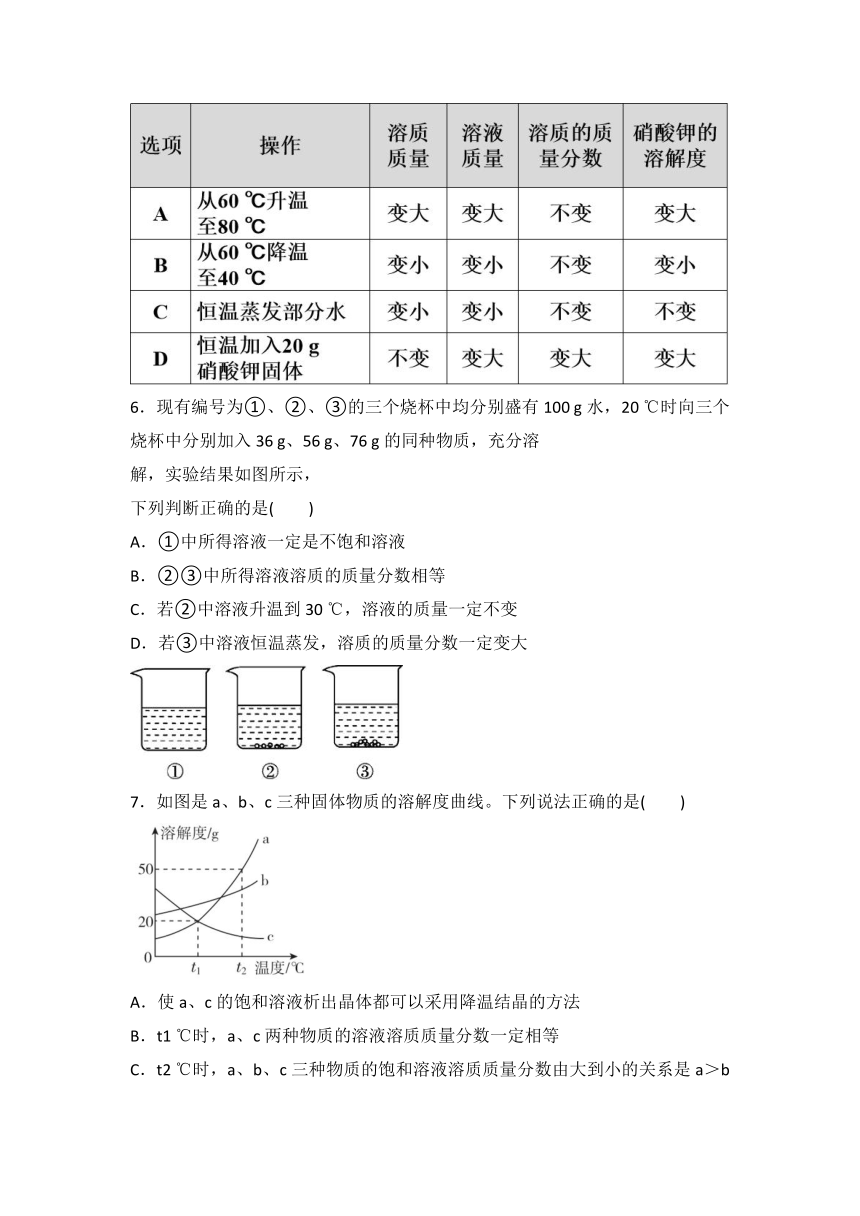
5.硝酸钾的溶解度曲线如图所示,将100 g 60 ℃的硝酸钾饱和溶液分别进行如下操作,所得溶液与原溶液相比,变化结果全部正确的是( )
6.现有编号为①、②、③的三个烧杯中均分别盛有100 g水,20 ℃时向三个烧杯中分别加入36 g、56 g、76 g的同种物质,充分溶
解,实验结果如图所示,
下列判断正确的是( )
A.①中所得溶液一定是不饱和溶液
B.②③中所得溶液溶质的质量分数相等
C.若②中溶液升温到30 ℃,溶液的质量一定不变
D.若③中溶液恒温蒸发,溶质的质量分数一定变大
7.如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是( )
A.使a、c的饱和溶液析出晶体都可以采用降温结晶的方法
B.t1 ℃时,a、c两种物质的溶液溶质质量分数一定相等
C.t2 ℃时,a、b、c三种物质的饱和溶液溶质质量分数由大到小的关系是a>b>c
D.在t2 ℃时,将30 g a物质加入50 g水中充分溶解,所得溶液质量为80 g
二 非选择题
1.生理盐水是0.9%的氯化钠溶液。200 g生理盐水中含有氯化钠________ g(直接写出结果)。
2.在农业生产中,常用溶质质量分数为3%的KNO3溶液作无土栽培的营养液,配制100 kg该营养液需要水的质量是________kg。
3.为了做好疫情防控,公共场所可用0.5%的过氧乙酸(化学式为C2H4O3)溶液来消毒。请计算(直接写出结果):
(1)过氧乙酸中碳、氢、氧三种元素的原子个数比为________。
(2)现要配制溶质质量分数为0.5%的过氧乙酸溶液2 000 g,需要过氧乙酸的质量是________。
4.已知KNO3在20 ℃时的溶解度是31.6 g,此温度下将15.8 g KNO3固体溶于水配成饱和溶液,需加水______g,所得溶液的溶质质量分数是_______(保留到1%)。
5.20 ℃时,向50 g水中加入20 g氯化钠,充分溶解后,得到溶液的质量为68 g,则20 ℃时氯化钠的溶解度为________g,所得溶液溶质的质量分数为________(结果保留一位小数)。
6.解答溶液的稀释、浓缩、混合问题的计算时应注意:
(1)溶液在稀释前后,____________________保持不变。
(2)溶液的浓缩是指将溶液蒸发水分(无晶体析出),使其浓度变大,浓缩前后,__________________保持不变。
(3)将两种溶液混合时,混合前两种溶液中溶质的质量之和,等于_________________________的质量。
7.将90 g溶质质量分数为10%的硝酸钾溶液恒温蒸发掉10 g水(无晶体析出),所得溶液溶质的质量分数为________。
8.新冠肺炎疫情期间,可用体积分数为75%的乙醇(C2H5OH)消毒液进行手和其他皮肤的消毒。如图为某品牌乙醇消毒液的标签。(纯乙醇的密度约为0.8 g/mL,水的密度约为1.0 g/mL)
请回答下列问题:
(1)乙醇由__________元素组成,配制乙醇消毒液需要乙醇和水的体积比为________。
(2)乙醇消毒液中乙醇的质量分数约为多少?(要求写出计算过程,结果精确到0.1%)
9..农业生产中通常用溶质质量分数为10%~20%的食盐溶液来选种。
(1)现要配制120 kg溶质质量分数为20%的食盐溶液,需要取用固体食盐________kg。
(2)用60 kg溶质质量分数为20%的食盐溶液,可稀释成12%的食盐溶液________kg。
10.现有80 g溶质质量分数为10%的硝酸钠溶液,试回答下列问题:
(1)上述溶液中含溶质的质量为________g,溶剂的质量为________g。
(2)若向上述溶液中加入20 g水,则所得溶液中溶质的质量分数为________。
(3)若向上述溶液中加入20 g硝酸钠,完全溶解后所得溶液中溶质的质量分数为________。
(4)若使上述溶液中溶质的质量分数变为20%,则应加入硝酸钠________g;或蒸发掉________g水。
(5)若使上述溶液中溶质的质量分数变为5%,则应加水________g。
(6)将该溶液倒出一半,所剩溶液的溶质质量分数为________。
11.下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
(1)10 ℃时,100 g水中最多可溶解硝酸钾的质量为_____g。
(2)20 ℃时,将10 g硝酸钾加入40 g水中,所得溶液溶质质量分数为________。
(3)如图是硝酸钾溶液的变化情况,请写出一种可采用的操作方法。(写出计算过程)
参考答案
一 选择题
ABADCBC
二 非选择题
1.1.8
2.97
3.1)2:4:3
2)10 g
4.50 24%
5.36;26.5%
6.1)溶质的质量
2)溶质质量
3)混合后溶液中溶质
7.11.25%
8.1)C、H、O 3:1
2)70.6%
9.1)24
2)100
10.1)8 72
2)8%
3)28%
4)10 40
80
6)10%
11.1)20.9
2)20%
3)可加入20 g KNO3或恒温蒸发60 g水。
一 选择题
1.下列关于“10%的硝酸钾溶液”含义的说法中,错误的是( )
A.100 g水中溶解了10 g硝酸钾
B.100 g硝酸钾溶液中有10 g硝酸钾
C.将10 g硝酸钾溶于90 g水中所得的溶液
D.将硝酸钾与水按1:9的质量比配制的溶液
2.向100 g质量分数为10%的NaOH溶液中加入12.5 g NaOH固体,完全溶解后,所得溶液溶质质量分数为( )
A.12.5% B.20% C.22.5% D.25%
3.将100 g 98%的浓硫酸注入900 g水中,所得稀硫酸中溶质的质量分数为( )
A.9.8% B.10.0% C.10.9% D.11.1%
4.将200 g溶质质量分数为10%的氯化钠溶液与300 g溶质质量分数为15%的氯化钠溶液相互混合,所得溶液溶质质量分数为( )
A.8% B.12% C.15% D.13%
5.硝酸钾的溶解度曲线如图所示,将100 g 60 ℃的硝酸钾饱和溶液分别进行如下操作,所得溶液与原溶液相比,变化结果全部正确的是( )
6.现有编号为①、②、③的三个烧杯中均分别盛有100 g水,20 ℃时向三个烧杯中分别加入36 g、56 g、76 g的同种物质,充分溶
解,实验结果如图所示,
下列判断正确的是( )
A.①中所得溶液一定是不饱和溶液
B.②③中所得溶液溶质的质量分数相等
C.若②中溶液升温到30 ℃,溶液的质量一定不变
D.若③中溶液恒温蒸发,溶质的质量分数一定变大
7.如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是( )
A.使a、c的饱和溶液析出晶体都可以采用降温结晶的方法
B.t1 ℃时,a、c两种物质的溶液溶质质量分数一定相等
C.t2 ℃时,a、b、c三种物质的饱和溶液溶质质量分数由大到小的关系是a>b>c
D.在t2 ℃时,将30 g a物质加入50 g水中充分溶解,所得溶液质量为80 g
二 非选择题
1.生理盐水是0.9%的氯化钠溶液。200 g生理盐水中含有氯化钠________ g(直接写出结果)。
2.在农业生产中,常用溶质质量分数为3%的KNO3溶液作无土栽培的营养液,配制100 kg该营养液需要水的质量是________kg。
3.为了做好疫情防控,公共场所可用0.5%的过氧乙酸(化学式为C2H4O3)溶液来消毒。请计算(直接写出结果):
(1)过氧乙酸中碳、氢、氧三种元素的原子个数比为________。
(2)现要配制溶质质量分数为0.5%的过氧乙酸溶液2 000 g,需要过氧乙酸的质量是________。
4.已知KNO3在20 ℃时的溶解度是31.6 g,此温度下将15.8 g KNO3固体溶于水配成饱和溶液,需加水______g,所得溶液的溶质质量分数是_______(保留到1%)。
5.20 ℃时,向50 g水中加入20 g氯化钠,充分溶解后,得到溶液的质量为68 g,则20 ℃时氯化钠的溶解度为________g,所得溶液溶质的质量分数为________(结果保留一位小数)。
6.解答溶液的稀释、浓缩、混合问题的计算时应注意:
(1)溶液在稀释前后,____________________保持不变。
(2)溶液的浓缩是指将溶液蒸发水分(无晶体析出),使其浓度变大,浓缩前后,__________________保持不变。
(3)将两种溶液混合时,混合前两种溶液中溶质的质量之和,等于_________________________的质量。
7.将90 g溶质质量分数为10%的硝酸钾溶液恒温蒸发掉10 g水(无晶体析出),所得溶液溶质的质量分数为________。
8.新冠肺炎疫情期间,可用体积分数为75%的乙醇(C2H5OH)消毒液进行手和其他皮肤的消毒。如图为某品牌乙醇消毒液的标签。(纯乙醇的密度约为0.8 g/mL,水的密度约为1.0 g/mL)
请回答下列问题:
(1)乙醇由__________元素组成,配制乙醇消毒液需要乙醇和水的体积比为________。
(2)乙醇消毒液中乙醇的质量分数约为多少?(要求写出计算过程,结果精确到0.1%)
9..农业生产中通常用溶质质量分数为10%~20%的食盐溶液来选种。
(1)现要配制120 kg溶质质量分数为20%的食盐溶液,需要取用固体食盐________kg。
(2)用60 kg溶质质量分数为20%的食盐溶液,可稀释成12%的食盐溶液________kg。
10.现有80 g溶质质量分数为10%的硝酸钠溶液,试回答下列问题:
(1)上述溶液中含溶质的质量为________g,溶剂的质量为________g。
(2)若向上述溶液中加入20 g水,则所得溶液中溶质的质量分数为________。
(3)若向上述溶液中加入20 g硝酸钠,完全溶解后所得溶液中溶质的质量分数为________。
(4)若使上述溶液中溶质的质量分数变为20%,则应加入硝酸钠________g;或蒸发掉________g水。
(5)若使上述溶液中溶质的质量分数变为5%,则应加水________g。
(6)将该溶液倒出一半,所剩溶液的溶质质量分数为________。
11.下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
(1)10 ℃时,100 g水中最多可溶解硝酸钾的质量为_____g。
(2)20 ℃时,将10 g硝酸钾加入40 g水中,所得溶液溶质质量分数为________。
(3)如图是硝酸钾溶液的变化情况,请写出一种可采用的操作方法。(写出计算过程)
参考答案
一 选择题
ABADCBC
二 非选择题
1.1.8
2.97
3.1)2:4:3
2)10 g
4.50 24%
5.36;26.5%
6.1)溶质的质量
2)溶质质量
3)混合后溶液中溶质
7.11.25%
8.1)C、H、O 3:1
2)70.6%
9.1)24
2)100
10.1)8 72
2)8%
3)28%
4)10 40
80
6)10%
11.1)20.9
2)20%
3)可加入20 g KNO3或恒温蒸发60 g水。
同课章节目录
