2022年人教版九年级化学下册第十一、十二单元单元检测题(word版有答案)
文档属性
| 名称 | 2022年人教版九年级化学下册第十一、十二单元单元检测题(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 503.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-16 00:00:00 | ||
图片预览




文档简介
第十一、十二单元检测题
班级 姓名
可能用到的相对原子质量:H—1、C—12、O—16、Na— 23、Cl— 35.5
一、选择题(每小题四个选项中均只有一个正确,每小题2分,共40分)
1.分类和归纳是行之有效、简单易行的科学方法,下列说法错误的是 ( )
A.锂、汞都属于金属元素
B.锌、碘都属于人体必需的微量元素
C.尿素、硝酸钾都属于复合肥
D.塑料、合成纤维都属于合成材料
2. 新冠肺炎疫情防控期间,有医学专家建议大家早餐以鸡蛋、瘦肉、牛奶等食物为主,提高身体抵抗力。这三种食物提供的基本营养素主要是 ( )
A.糖类 B.油脂 C.蛋白质 D.维生素
3.下列有关化肥和农药的说法错误的是 ( )
A.氯化钾可用作钾肥
B.化肥能有效提高农作物产量
C.农药施用后,不会通过农作物转移到人体
D.农药应根据农作物、虫害和农药的特点合理施用
4. 下列说法正确的是 ( )
A.石油是可再生能源
B.高炉炼铁炼出的是纯铁
C.医用口罩过滤层使用了有机合成材料
D.易拉罐和矿泉水瓶属于不可回收垃圾
5. 化学与我们的生活密切相关。下列有关说法错误的是( )
A.如果人体缺乏维生素C,会引起坏血病
B.可用甲醛溶液浸泡海产品,以确保长期食用
C.酱油中加入铁元素,可以预防缺铁性贫血
D.如果人体内缺乏碘元素会导致甲状腺肿大
6.某些劣质食品中常添加过量的“甜蜜素”,有害人体健康。工业上由环己胺(化学式是C6H11NH2)与氢氧化钠反应合成“甜蜜素”。下列对环己胺的叙述不正确的是 ( )
A.从类别上看:环己胺属于有机化合物
B.从性质上看:环己胺可以与碱反应
C.从组成上看:环己胺中碳元素和氮元素的质量比为36∶7
D.从结构上看:环己胺由6个碳原子、13个氢原子、1个氮原子构成
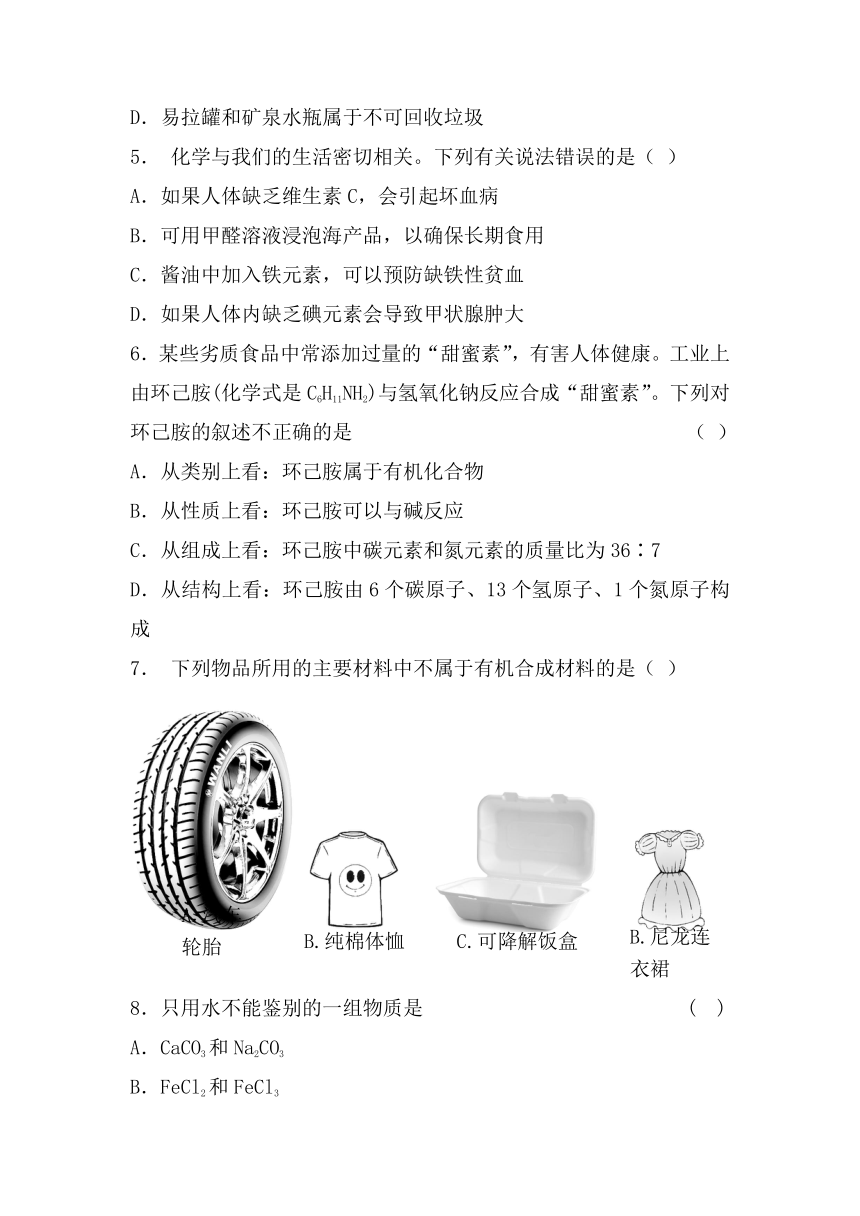
7. 下列物品所用的主要材料中不属于有机合成材料的是( )
8.只用水不能鉴别的一组物质是 ( )
A.CaCO3和Na2CO3
B.FeCl2和FeCl3
C.NaCl和Na2SO4
D.固体NaOH和固体NH4NO3
9.现有氧化铁、稀硫酸、氢氧化钠溶液、氯化钡溶液和碳酸钾溶液五种物质,在常温下它们两两相互发生的化学反应共有 ( )
A.4个 B.5个 C.6个 D.7个
10. 下列各组离子在水中能大量共存且形成无色溶液的是 ( )
A.Fe2+ Na+ SO42- Cl-
B.K+ Na+ OH- NO3-
C.Ba2+ Cl- SO42- OH-
D.H+ K+ NO3- CO32-
11. 去除难溶性杂质后的食盐样品中还含有可溶性杂质:CaCl2、MgCl2和Na2SO4。为除去可溶性杂质,将食盐样品溶于水,依次加入稍过量的三种溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反应后过滤,得滤渣X,向滤液中加入过量的稀盐酸,搅拌、煮沸,得氯化钠溶液。下列说法正确的是 ( )
A.滤渣X中有三种成分
B.“向滤液中加入过量的稀盐酸”。目的只是为了除去过量的NaOH
C.除杂过程中有Na2CO3参加的化学反应为复分解反应
D.将氯化钠溶液用如图装置加热蒸发,至水分完全蒸干时停止加热
12. 为鉴别氯化钠、氢氧化钠、碳酸钠和硫酸钠四种物质的溶液,设计如下实验:
下面对试剂①、试剂②和试剂③的选择,合理的是 ( )
A.①酚酞 ②稀盐酸 ③氯化钡
B.①酚酞 ②稀盐酸 ③稀盐酸
C.①石蕊 ②氯化钡 ③稀盐酸
D.①石蕊 ②氯化钡 ③碳酸钠
河道两旁有甲、乙两厂,它们排放的工业废水中共含H+、Na+、Ba2+、Cl-、SO42-、CO32-六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,则甲厂废水中的离子是 ( )
A.H+、Na+、Ba2+ B.H+、Ba2+、Cl-
C.Na+、SO42-、CO32- D.H+、SO42-、CO32-
14.已知在一定条件下发生反应:甲+乙―→丙+丁,下列判断正确的是 ( )
A.甲、乙、丙、丁不可能含有同一种元素
B.丙为盐、丁为水,则该反应一定为复分解反应
C.甲、乙为化合物,则该反应一定为复分解反应
D.丙为Cu(NO3)2,则甲可能为单质、氧化物、碱或盐
15.下列关于化学实验中“操作—现象—结论”的描述正确的是( )
A.在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐
B.在某溶液中加入氯化钡溶液和稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子
C.某溶液用pH试纸测试,试纸变蓝色(pH约为10),该溶液一定是碱性溶液
D.在稀盐酸与氢氧化钠反应后的溶液中滴加无色酚酞溶液不变色,可以断定两者恰好反应完全
16.有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种。取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,沉淀完全溶解并有气体产生。由此推断白色固体中 ( )
A.可能存在NaOH
B.可能存在Na2SO4
C.肯定不存在BaCl2
D.肯定存在Na2CO3和Na2SO4
17.下列实验方案能达成实验目的的是 ( )
A.鉴别KCl和NH4Cl两种化肥:取样,加入适量熟石灰研磨
B.检验NaOH溶液部分变质:取样,加入少量BaCl2溶液
C.除去CaCl2溶液中混有的少量盐酸:加入过量的Ca(OH)2溶液
D.配制溶质质量分数为5%的KCl溶液:称取5 g KCl,放入100 mL水中搅拌溶解
18. 向一定量的硫酸铜和稀硫酸的混合溶液中滴加氢氧化钠溶液,反应过程中产生的沉淀质量与加入的氢氧化钠溶液质量关系如图所示。下列说法不正确的是 ( )
A.a点溶液中的溶质有2种
B.c点溶液中的溶质有3种
C.ab(不包括a点)段有沉淀生成
D.d点溶液的pH>7
19.除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是 ( )
选项 物质 杂质 除杂试剂及操作方法
A Cu Fe 加入过量的CuCl2溶液,过滤、洗涤、干燥
B KCl MnO2 加入足量的水溶解,过滤、洗涤、干燥
C NaCl NaNO3 加入适量的硝酸银溶液至不再产生沉淀
D Cu C 在空气中灼烧
20. 向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤。不可能存在的情况是 ( )
A.滤纸上有Ag,滤液中有Ag+、Cu2+、 Zn2+、Mg2+
B.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+
C.滤纸上有Ag、Cu、Zn、Mg,滤液中有Zn2+
D.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
二、填空题(化学方程式每空2分,其余每空1分,共30分)
21.化学与我们的生活有着密切的联系。现有①氮气,②盐酸,③淀粉,④熟石灰,⑤金刚石,
⑥氯化钾。选择适当物质填空(填序号)。
(1)可用作钾肥的是__ __;
(2)可用来裁玻璃的是__ __;
(3)人体胃液中含有的酸是__ __;
(4)可用来改良酸性土壤的碱是__ __;
(5)焊接金属时常用作保护气的是__ __;
(6)米和面中含有的糖类物质主要是__ __。
22.清明时节,同学们相约外出踏青野炊。请用化学知识分析下列问题:
(1)野炊食谱如表所示:从合理膳食角度来看,你认为食谱中还应添加__ __(填字母)。
主食 馒头
配菜 红烧肉、豆腐汤、牛肉干
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)野炊后同学们准备将垃圾分类处理,其中属于不可回收垃圾的是__ __(填字母)。
A.废纸 B.果皮 C.易拉罐 D.塑料桶
(3)小滨用洗涤剂洗去手上的油迹,是利用了洗涤剂的__ __作用。
(4)大家在田边看到农民正在使用化肥NH4NO3,于是联想到NH4NO3不能和熟石灰混合施用,请用化学方程式解释原理__ __。
23. 在抗击新冠肺炎疫情期间,我国采取了一系列有效的防控措施。 请用所学化学知识回答下列问题:
(1)进入人群密集或封闭场所应佩戴合格口罩,生产口罩的关键材料熔喷布是一种链状结构高分子材料,具有 (选填“热塑性”或“热固性”),口罩贴合鼻梁部位的铝条很柔软,属于 (选填“纯金属”或“合金”)。
(2)人们回家常用75%乙醇溶液擦拭随身物品消毒,乙醇也常用作燃料。写出乙醇完全燃烧的化学方程式: 。
(3)适当运动和合理膳食可增强人体抵抗力,专家建议早餐用牛奶代替传统的白粥,是为了增加营养物质中的 摄入。
(4) 84消毒液常用于环境消毒,某次使用的消毒液pH为13,该溶液呈 (选填“酸”“中”或“碱”)性。其有效成分是一种盐,化学式为NaClO, 其阴离子符号为 。
24. 2020年5月22日,国务院总理李克强在政府工作报告中强调:着力抓好农业生产,稳定粮食播种面积和产量,大力防治重大病虫害。恢复生猪生产,落实“米袋子”省长负责制和“菜篮子”市长负责制。请用所学的化学知识回答下列问题。
(1)“米袋子”中的大米主要含有的基本营养素是 “菜篮子”中包含多种蔬菜和水果,它们富含维生素C,人体缺乏维生素C,会引起 ;
(2)食盐几乎是每道菜不可或缺的调味品,加碘食盐中的“碘”指的是碘 (选填 “单质”“原子”或“元素”);
(3) 为提高粮食产量,农业生产中要合理使用化肥, (选填“氮肥”“磷肥”或“钾肥”)能增强抗病虫害和抗倒伏能力;
(4)下列有关饮食安全的说法正确的是 。
A.甲醛有防腐作用,可以用来浸泡食材
B.青少年多喝牛奶能补充钙元素
C.脂肪、蛋白质是人体必需的营养素,吃得越多越好
D.恢复生猪生产,为提高产量和瘦肉率,在饲料中添加瘦肉精
25.A~N是初中学过的物质。D是相对分子质量为40的氧化物,A是不溶于稀硝酸的白色沉淀,E是难溶于水的白色沉淀,实验室通常用N制取CO2。如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。
(注:难溶性碱加热分解生成对应的氧化物)
(1)写出化学式:
A__ __,
N__ __。
(2)写出E→B的化学反应方程式:
__ _。
(3)由F生成E需加入的物质是__ _。
(4)C在空气中燃烧生成D的实验现象是__ 。C在空气中燃烧除了生成D之外,也可能与空气中的氮气生成氮化物(氮元素化合价为-3价),该氮化物的化学式是__ __。
三、实验探究题(每空2分,共22分)
26.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50 g 5%的氯化钠溶液。
实验一:如图是同学们做粗盐提纯实验的操作示意图。
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是__ __。
(2)操作⑥中的错误是__ __。
(3)粗盐提纯实验的操作顺序为__ __(填操作序号)、称量精盐并计算产率。
(4)操作④中,当观察到__ __时,停止加热。
实验二:用提纯得到的精盐配制了50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有__ __(填序号)。
①氯化钠固体仍然不纯
②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
27.(青岛中考)化学课堂上,同学们分小组合作探究碳酸钠的性质,请你参与探究并填空。
【实验记录与分析】
实验一 实验二 实验三 实验四
实验 操作
实验 现象 溶液由无色变为红色 生成白色沉淀 生成白色沉淀
实验 结论 碳酸钠溶液显 性 碳酸钠能与盐酸发生反应 碳酸钠能与氢氧化钙发生反应
【反思与拓展】
(1)甲同学分析实验得出:盐溶液 (选填“一定”或“不一定”)显中性。
(2)乙同学用稀硫酸代替实验二中的稀盐酸进行探究,发现实验现象相同。从微观角度分析,这是因为稀盐酸和稀硫酸中都含有 。
(3 )丙同学对比实验三和实验四的现象,从微观角度分析,两个反应的实质相同,溶液中相互结合的离子都是_ _。
四、计算题(共8分)
28. 洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0 g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
第一次 第二次 第三次 第四次 第五次
加入Na2CO3溶液的质量/g 20.0 20.0 20.0 20.0 20.0
反应后溶液的总质量/g 118.9 137.8 M 175.6 195.6
请根据实验数据分析解答下列问题。
(1)表格中M的数值为 ;
(2)恰好完全反应时消耗Na2CO3的质量是多少?
(3)该洁厕灵中HCl的质量分数是多少?
参考答案
一、选择题(每小题四个选项中均只有一个正确,每小题2分,共40分)
1.分类和归纳是行之有效、简单易行的科学方法,下列说法错误的是 (C)
A.锂、汞都属于金属元素
B.锌、碘都属于人体必需的微量元素
C.尿素、硝酸钾都属于复合肥
D.塑料、合成纤维都属于合成材料
2. 新冠肺炎疫情防控期间,有医学专家建议大家早餐以鸡蛋、瘦肉、牛奶等食物为主,提高身体抵抗力。这三种食物提供的基本营养素主要是 (C)
A.糖类 B.油脂 C.蛋白质 D.维生素
3.下列有关化肥和农药的说法错误的是 (C)
A.氯化钾可用作钾肥
B.化肥能有效提高农作物产量
C.农药施用后,不会通过农作物转移到人体
D.农药应根据农作物、虫害和农药的特点合理施用
4. 下列说法正确的是 (C)
A.石油是可再生能源
B.高炉炼铁炼出的是纯铁
C.医用口罩过滤层使用了有机合成材料
D.易拉罐和矿泉水瓶属于不可回收垃圾
5. 化学与我们的生活密切相关。下列有关说法错误的是(B)
A.如果人体缺乏维生素C,会引起坏血病
B.可用甲醛溶液浸泡海产品,以确保长期食用
C.酱油中加入铁元素,可以预防缺铁性贫血
D.如果人体内缺乏碘元素会导致甲状腺肿大
6.某些劣质食品中常添加过量的“甜蜜素”,有害人体健康。工业上由环己胺(化学式是C6H11NH2)与氢氧化钠反应合成“甜蜜素”。下列对环己胺的叙述不正确的是 (D)
A.从类别上看:环己胺属于有机化合物
B.从性质上看:环己胺可以与碱反应
C.从组成上看:环己胺中碳元素和氮元素的质量比为36∶7
D.从结构上看:环己胺由6个碳原子、13个氢原子、1个氮原子构成
7. 下列物品所用的主要材料中不属于有机合成材料的是(B)
8.只用水不能鉴别的一组物质是 (C)
A.CaCO3和Na2CO3
B.FeCl2和FeCl3
C.NaCl和Na2SO4
D.固体NaOH和固体NH4NO3
9.现有氧化铁、稀硫酸、氢氧化钠溶液、氯化钡溶液和碳酸钾溶液五种物质,在常温下它们两两相互发生的化学反应共有 (B)
A.4个 B.5个 C.6个 D.7个
10. 下列各组离子在水中能大量共存且形成无色溶液的是(B)
A.Fe2+ Na+ SO42- Cl-
B.K+ Na+ OH- NO
C.Ba2+ Cl- SO42- OH-
D.H+ K+ NO32- CO32-
11. 去除难溶性杂质后的食盐样品中还含有可溶性杂质:CaCl2、MgCl2和Na2SO4。为除去可溶性杂质,将食盐样品溶于水,依次加入稍过量的三种溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反应后过滤,得滤渣X,向滤液中加入过量的稀盐酸,搅拌、煮沸,得氯化钠溶液。下列说法正确的是 (C)
A.滤渣X中有三种成分
B.“向滤液中加入过量的稀盐酸”。目的只是为了除去过量的NaOH
C.除杂过程中有Na2CO3参加的化学反应为复分解反应
D.将氯化钠溶液用如图装置加热蒸发,至水分完全蒸干时停止加热
12. 为鉴别氯化钠、氢氧化钠、碳酸钠和硫酸钠四种物质的溶液,设计如下实验:
下面对试剂①、试剂②和试剂③的选择,合理的是 (A)
A.①酚酞 ②稀盐酸 ③氯化钡
B.①酚酞 ②稀盐酸 ③稀盐酸
C.①石蕊 ②氯化钡 ③稀盐酸
D.①石蕊 ②氯化钡 ③碳酸钠
河道两旁有甲、乙两厂,它们排放的工业废水中共含H+、Na+、
Ba2+、Cl-、SO42-、CO32-六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,则甲厂废水中的离子是 (B)
A.H+、Na+、Ba2+ B.H+、Ba2+、Cl-
C.Na+、SO42-、CO32- D.H+、SO42-、CO32-
14.已知在一定条件下发生反应:甲+乙―→丙+丁,下列判断正确的是 (D)
A.甲、乙、丙、丁不可能含有同一种元素
B.丙为盐、丁为水,则该反应一定为复分解反应
C.甲、乙为化合物,则该反应一定为复分解反应
D.丙为Cu(NO3)2,则甲可能为单质、氧化物、碱或盐
15.下列关于化学实验中“操作—现象—结论”的描述正确的是(C)
A.在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐
B.在某溶液中加入氯化钡溶液和稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子
C.某溶液用pH试纸测试,试纸变蓝色(pH约为10),该溶液一定是碱性溶液
D.在稀盐酸与氢氧化钠反应后的溶液中滴加无色酚酞溶液不变色,可以断定两者恰好反应完全
16.有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种。取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,沉淀完全溶解并有气体产生。由此推断白色固体中 (A)
A.可能存在NaOH
B.可能存在Na2SO4
C.肯定不存在BaCl2
D.肯定存在Na2CO3和Na2SO4
17.下列实验方案能达成实验目的的是 (A)
A.鉴别KCl和NH4Cl两种化肥:取样,加入适量熟石灰研磨
B.检验NaOH溶液部分变质:取样,加入少量BaCl2溶液
C.除去CaCl2溶液中混有的少量盐酸:加入过量的Ca(OH)2溶液
D.配制溶质质量分数为5%的KCl溶液:称取5 g KCl,放入100 mL水中搅拌溶解
18. 向一定量的硫酸铜和稀硫酸的混合溶液中滴加氢氧化钠溶液,反应过程中产生的沉淀质量与加入的氢氧化钠溶液质量关系如图所示。下列说法不正确的是 (B)
A.a点溶液中的溶质有2种
B.c点溶液中的溶质有3种
C.ab(不包括a点)段有沉淀生成
D.d点溶液的pH>7
19.除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是 (A)
选项 物质 杂质 除杂试剂及操作方法
A Cu Fe 加入过量的CuCl2溶液,过滤、洗涤、干燥
B KCl MnO2 加入足量的水溶解,过滤、洗涤、干燥
C NaCl NaNO3 加入适量的硝酸银溶液至不再产生沉淀
D Cu C 在空气中灼烧
20. 向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤。不可能存在的情况是 (C)
A.滤纸上有Ag,滤液中有Ag+、Cu2+、 Zn2+、Mg2+
B.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+
C.滤纸上有Ag、Cu、Zn、Mg,滤液中有Zn2+
D.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
二、填空题(化学方程式每空2分,其余每空1分,共30分)
21.化学与我们的生活有着密切的联系。现有①氮气,②盐酸,③淀粉,④熟石灰,⑤金刚石,
⑥氯化钾。选择适当物质填空(填序号)。
(1)可用作钾肥的是__⑥__;
(2)可用来裁玻璃的是__⑤__;
(3)人体胃液中含有的酸是__②__;
(4)可用来改良酸性土壤的碱是__④__;
(5)焊接金属时常用作保护气的是__①__;
(6)米和面中含有的糖类物质主要是__③__。
22.清明时节,同学们相约外出踏青野炊。请用化学知识分析下列问题:
(1)野炊食谱如表所示:从合理膳食角度来看,你认为食谱中还应添加__C__(填字母)。
主食 馒头
配菜 红烧肉、豆腐汤、牛肉干
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)野炊后同学们准备将垃圾分类处理,其中属于不可回收垃圾的是__B__(填字母)。
A.废纸 B.果皮 C.易拉罐 D.塑料桶
(3)小滨用洗涤剂洗去手上的油迹,是利用了洗涤剂的__乳化__作用。
(4)大家在田边看到农民正在使用化肥NH4NO3,于是联想到NH4NO3不能和熟石灰混合施用,请用化学方程式解释原理__2NH4NO3+Ca(OH)2===Ca(NO3)2+2H2O+2NH3↑__。
23. 在抗击新冠肺炎疫情期间,我国采取了一系列有效的防控措施。 请用所学化学知识回答下列问题:
(1)进入人群密集或封闭场所应佩戴合格口罩,生产口罩的关键材料熔喷布是一种链状结构高分子材料,具有热塑性(选填“热塑性”或“热固性”),口罩贴合鼻梁部位的铝条很柔软,属于纯金属(选填“纯金属”或“合金”)。
(2)人们回家常用75%乙醇溶液擦拭随身物品消毒,乙醇也常用作燃料。写出乙醇完全燃烧的化学方程式:C2H5OH+3O22CO2+ 3H2O。
(3)适当运动和合理膳食可增强人体抵抗力,专家建议早餐用牛奶代替传统的白粥,是为了增加营养物质中的蛋白质摄入。
(4) 84消毒液常用于环境消毒,某次使用的消毒液pH为13,该溶液呈碱(选填“酸”“中”或“碱”)性。其有效成分是一种盐,化学式为NaClO, 其阴离子符号为ClO-。
24. 2020年5月22日,国务院总理李克强在政府工作报告中强调:着力抓好农业生产,稳定粮食播种面积和产量,大力防治重大病虫害。恢复生猪生产,落实“米袋子”省长负责制和“菜篮子”市长负责制。请用所学的化学知识回答下列问题。
(1)“米袋子”中的大米主要含有的基本营养素是糖类 “菜篮子”中包含多种蔬菜和水果,它们富含维生素C,人体缺乏维生素C,会引起坏血病;
(2)食盐几乎是每道菜不可或缺的调味品,加碘食盐中的“碘”指的是碘元素(选填 “单质”“原子”或“元素”);
(3) 为提高粮食产量,农业生产中要合理使用化肥, 钾肥(选填“氮肥”“磷肥”或“钾肥”)能增强抗病虫害和抗倒伏能力;
(4)下列有关饮食安全的说法正确的是B。
A.甲醛有防腐作用,可以用来浸泡食材
B.青少年多喝牛奶能补充钙元素
C.脂肪、蛋白质是人体必需的营养素,吃得越多越好
D.恢复生猪生产,为提高产量和瘦肉率,在饲料中添加瘦肉精
25.A~N是初中学过的物质。D是相对分子质量为40的氧化物,A是不溶于稀硝酸的白色沉淀,E是难溶于水的白色沉淀,实验室通常用N制取CO2。如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。
(注:难溶性碱加热分解生成对应的氧化物)
(1)写出化学式:
A__BaSO4__,
N__HCl__。
(2)写出E→B的化学反应方程式:
__Mg(OH)2+H2SO4===MgSO4+2H2O__。
(3)由F生成E需加入的物质是__NaOH或KOH等__。
(4)C在空气中燃烧生成D的实验现象是__发出耀眼的白光,产生白烟,生成白色固体。C在空气中燃烧除了生成D之外,也可能与空气中的氮气生成氮化物(氮元素化合价为-3价),该氮化物的化学式是__Mg3N2__。
三、实验探究题(每空2分,共22分)
26.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50 g 5%的氯化钠溶液。
实验一:如图是同学们做粗盐提纯实验的操作示意图。
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是__加速溶解__。
(2)操作⑥中的错误是__未用玻璃棒引流__。
(3)粗盐提纯实验的操作顺序为__①⑤②③⑥④__(填操作序号)、称量精盐并计算产率。
(4)操作④中,当观察到__出现较多固体__时,停止加热。
实验二:用提纯得到的精盐配制了50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有__①②③__(填序号)。
①氯化钠固体仍然不纯
②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
27. 化学课堂上,同学们分小组合作探究碳酸钠的性质,请你参与探究并填空。
【实验记录与分析】
实验一 实验二 实验三 实验四
实验 操作
实验 现象 溶液由无色变为红色 有气泡产生 生成白色沉淀 生成白色沉淀
实验 结论 碳酸钠溶液显碱性 碳酸钠能与盐酸发生反应 碳酸钠能与氢氧化钙发生反应 氯化钙能与碳酸钠反应
【反思与拓展】
(1)甲同学分析实验得出:盐溶液不一定(选填“一定”或“不一定”)显中性。
(2)乙同学用稀硫酸代替实验二中的稀盐酸进行探究,发现实验现象相同。从微观角度分析,这是因为稀盐酸和稀硫酸中都含有H+(或氢离子)。
(3 )丙同学对比实验三和实验四的现象,从微观角度分析,两个反应的实质相同,溶液中相互结合的离子都是__Ca2+和CO__。
四、计算题(共8分)
28. 洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0 g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
第一次 第二次 第三次 第四次 第五次
加入Na2CO3溶液的质量/g 20.0 20.0 20.0 20.0 20.0
反应后溶液的总质量/g 118.9 137.8 M 175.6 195.6
请根据实验数据分析解答下列问题。
(1)表格中M的数值为156.7;
(2)恰好完全反应时消耗Na2CO3的质量是多少?
(3)该洁厕灵中HCl的质量分数是多少?
解:(2)由表格数据可知,前四次中每次加入20 g Na2CO3溶液都恰好生成1.1 g CO2,第五次加入后总质量无变化,可知第四次加入碳酸钠溶液后,恰好完全反应,生成CO2的质量为100 g+20 g+20 g+20 g+20 g+20 g-195.6 g=4.4 g,
设恰好反应时消耗Na2CO3的质量为x,HCl的质量为y。
Na2CO3+2HCl===2NaCl+H2O+CO2↑
106 73 44
x y 4.4 g
= x=10.6 g
= y=7.3 g
(3)该洁厕灵中HCl的质量分数为×100%=7.3%。
班级 姓名
可能用到的相对原子质量:H—1、C—12、O—16、Na— 23、Cl— 35.5
一、选择题(每小题四个选项中均只有一个正确,每小题2分,共40分)
1.分类和归纳是行之有效、简单易行的科学方法,下列说法错误的是 ( )
A.锂、汞都属于金属元素
B.锌、碘都属于人体必需的微量元素
C.尿素、硝酸钾都属于复合肥
D.塑料、合成纤维都属于合成材料
2. 新冠肺炎疫情防控期间,有医学专家建议大家早餐以鸡蛋、瘦肉、牛奶等食物为主,提高身体抵抗力。这三种食物提供的基本营养素主要是 ( )
A.糖类 B.油脂 C.蛋白质 D.维生素
3.下列有关化肥和农药的说法错误的是 ( )
A.氯化钾可用作钾肥
B.化肥能有效提高农作物产量
C.农药施用后,不会通过农作物转移到人体
D.农药应根据农作物、虫害和农药的特点合理施用
4. 下列说法正确的是 ( )
A.石油是可再生能源
B.高炉炼铁炼出的是纯铁
C.医用口罩过滤层使用了有机合成材料
D.易拉罐和矿泉水瓶属于不可回收垃圾
5. 化学与我们的生活密切相关。下列有关说法错误的是( )
A.如果人体缺乏维生素C,会引起坏血病
B.可用甲醛溶液浸泡海产品,以确保长期食用
C.酱油中加入铁元素,可以预防缺铁性贫血
D.如果人体内缺乏碘元素会导致甲状腺肿大
6.某些劣质食品中常添加过量的“甜蜜素”,有害人体健康。工业上由环己胺(化学式是C6H11NH2)与氢氧化钠反应合成“甜蜜素”。下列对环己胺的叙述不正确的是 ( )
A.从类别上看:环己胺属于有机化合物
B.从性质上看:环己胺可以与碱反应
C.从组成上看:环己胺中碳元素和氮元素的质量比为36∶7
D.从结构上看:环己胺由6个碳原子、13个氢原子、1个氮原子构成
7. 下列物品所用的主要材料中不属于有机合成材料的是( )
8.只用水不能鉴别的一组物质是 ( )
A.CaCO3和Na2CO3
B.FeCl2和FeCl3
C.NaCl和Na2SO4
D.固体NaOH和固体NH4NO3
9.现有氧化铁、稀硫酸、氢氧化钠溶液、氯化钡溶液和碳酸钾溶液五种物质,在常温下它们两两相互发生的化学反应共有 ( )
A.4个 B.5个 C.6个 D.7个
10. 下列各组离子在水中能大量共存且形成无色溶液的是 ( )
A.Fe2+ Na+ SO42- Cl-
B.K+ Na+ OH- NO3-
C.Ba2+ Cl- SO42- OH-
D.H+ K+ NO3- CO32-
11. 去除难溶性杂质后的食盐样品中还含有可溶性杂质:CaCl2、MgCl2和Na2SO4。为除去可溶性杂质,将食盐样品溶于水,依次加入稍过量的三种溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反应后过滤,得滤渣X,向滤液中加入过量的稀盐酸,搅拌、煮沸,得氯化钠溶液。下列说法正确的是 ( )
A.滤渣X中有三种成分
B.“向滤液中加入过量的稀盐酸”。目的只是为了除去过量的NaOH
C.除杂过程中有Na2CO3参加的化学反应为复分解反应
D.将氯化钠溶液用如图装置加热蒸发,至水分完全蒸干时停止加热
12. 为鉴别氯化钠、氢氧化钠、碳酸钠和硫酸钠四种物质的溶液,设计如下实验:
下面对试剂①、试剂②和试剂③的选择,合理的是 ( )
A.①酚酞 ②稀盐酸 ③氯化钡
B.①酚酞 ②稀盐酸 ③稀盐酸
C.①石蕊 ②氯化钡 ③稀盐酸
D.①石蕊 ②氯化钡 ③碳酸钠
河道两旁有甲、乙两厂,它们排放的工业废水中共含H+、Na+、Ba2+、Cl-、SO42-、CO32-六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,则甲厂废水中的离子是 ( )
A.H+、Na+、Ba2+ B.H+、Ba2+、Cl-
C.Na+、SO42-、CO32- D.H+、SO42-、CO32-
14.已知在一定条件下发生反应:甲+乙―→丙+丁,下列判断正确的是 ( )
A.甲、乙、丙、丁不可能含有同一种元素
B.丙为盐、丁为水,则该反应一定为复分解反应
C.甲、乙为化合物,则该反应一定为复分解反应
D.丙为Cu(NO3)2,则甲可能为单质、氧化物、碱或盐
15.下列关于化学实验中“操作—现象—结论”的描述正确的是( )
A.在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐
B.在某溶液中加入氯化钡溶液和稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子
C.某溶液用pH试纸测试,试纸变蓝色(pH约为10),该溶液一定是碱性溶液
D.在稀盐酸与氢氧化钠反应后的溶液中滴加无色酚酞溶液不变色,可以断定两者恰好反应完全
16.有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种。取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,沉淀完全溶解并有气体产生。由此推断白色固体中 ( )
A.可能存在NaOH
B.可能存在Na2SO4
C.肯定不存在BaCl2
D.肯定存在Na2CO3和Na2SO4
17.下列实验方案能达成实验目的的是 ( )
A.鉴别KCl和NH4Cl两种化肥:取样,加入适量熟石灰研磨
B.检验NaOH溶液部分变质:取样,加入少量BaCl2溶液
C.除去CaCl2溶液中混有的少量盐酸:加入过量的Ca(OH)2溶液
D.配制溶质质量分数为5%的KCl溶液:称取5 g KCl,放入100 mL水中搅拌溶解
18. 向一定量的硫酸铜和稀硫酸的混合溶液中滴加氢氧化钠溶液,反应过程中产生的沉淀质量与加入的氢氧化钠溶液质量关系如图所示。下列说法不正确的是 ( )
A.a点溶液中的溶质有2种
B.c点溶液中的溶质有3种
C.ab(不包括a点)段有沉淀生成
D.d点溶液的pH>7
19.除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是 ( )
选项 物质 杂质 除杂试剂及操作方法
A Cu Fe 加入过量的CuCl2溶液,过滤、洗涤、干燥
B KCl MnO2 加入足量的水溶解,过滤、洗涤、干燥
C NaCl NaNO3 加入适量的硝酸银溶液至不再产生沉淀
D Cu C 在空气中灼烧
20. 向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤。不可能存在的情况是 ( )
A.滤纸上有Ag,滤液中有Ag+、Cu2+、 Zn2+、Mg2+
B.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+
C.滤纸上有Ag、Cu、Zn、Mg,滤液中有Zn2+
D.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
二、填空题(化学方程式每空2分,其余每空1分,共30分)
21.化学与我们的生活有着密切的联系。现有①氮气,②盐酸,③淀粉,④熟石灰,⑤金刚石,
⑥氯化钾。选择适当物质填空(填序号)。
(1)可用作钾肥的是__ __;
(2)可用来裁玻璃的是__ __;
(3)人体胃液中含有的酸是__ __;
(4)可用来改良酸性土壤的碱是__ __;
(5)焊接金属时常用作保护气的是__ __;
(6)米和面中含有的糖类物质主要是__ __。
22.清明时节,同学们相约外出踏青野炊。请用化学知识分析下列问题:
(1)野炊食谱如表所示:从合理膳食角度来看,你认为食谱中还应添加__ __(填字母)。
主食 馒头
配菜 红烧肉、豆腐汤、牛肉干
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)野炊后同学们准备将垃圾分类处理,其中属于不可回收垃圾的是__ __(填字母)。
A.废纸 B.果皮 C.易拉罐 D.塑料桶
(3)小滨用洗涤剂洗去手上的油迹,是利用了洗涤剂的__ __作用。
(4)大家在田边看到农民正在使用化肥NH4NO3,于是联想到NH4NO3不能和熟石灰混合施用,请用化学方程式解释原理__ __。
23. 在抗击新冠肺炎疫情期间,我国采取了一系列有效的防控措施。 请用所学化学知识回答下列问题:
(1)进入人群密集或封闭场所应佩戴合格口罩,生产口罩的关键材料熔喷布是一种链状结构高分子材料,具有 (选填“热塑性”或“热固性”),口罩贴合鼻梁部位的铝条很柔软,属于 (选填“纯金属”或“合金”)。
(2)人们回家常用75%乙醇溶液擦拭随身物品消毒,乙醇也常用作燃料。写出乙醇完全燃烧的化学方程式: 。
(3)适当运动和合理膳食可增强人体抵抗力,专家建议早餐用牛奶代替传统的白粥,是为了增加营养物质中的 摄入。
(4) 84消毒液常用于环境消毒,某次使用的消毒液pH为13,该溶液呈 (选填“酸”“中”或“碱”)性。其有效成分是一种盐,化学式为NaClO, 其阴离子符号为 。
24. 2020年5月22日,国务院总理李克强在政府工作报告中强调:着力抓好农业生产,稳定粮食播种面积和产量,大力防治重大病虫害。恢复生猪生产,落实“米袋子”省长负责制和“菜篮子”市长负责制。请用所学的化学知识回答下列问题。
(1)“米袋子”中的大米主要含有的基本营养素是 “菜篮子”中包含多种蔬菜和水果,它们富含维生素C,人体缺乏维生素C,会引起 ;
(2)食盐几乎是每道菜不可或缺的调味品,加碘食盐中的“碘”指的是碘 (选填 “单质”“原子”或“元素”);
(3) 为提高粮食产量,农业生产中要合理使用化肥, (选填“氮肥”“磷肥”或“钾肥”)能增强抗病虫害和抗倒伏能力;
(4)下列有关饮食安全的说法正确的是 。
A.甲醛有防腐作用,可以用来浸泡食材
B.青少年多喝牛奶能补充钙元素
C.脂肪、蛋白质是人体必需的营养素,吃得越多越好
D.恢复生猪生产,为提高产量和瘦肉率,在饲料中添加瘦肉精
25.A~N是初中学过的物质。D是相对分子质量为40的氧化物,A是不溶于稀硝酸的白色沉淀,E是难溶于水的白色沉淀,实验室通常用N制取CO2。如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。
(注:难溶性碱加热分解生成对应的氧化物)
(1)写出化学式:
A__ __,
N__ __。
(2)写出E→B的化学反应方程式:
__ _。
(3)由F生成E需加入的物质是__ _。
(4)C在空气中燃烧生成D的实验现象是__ 。C在空气中燃烧除了生成D之外,也可能与空气中的氮气生成氮化物(氮元素化合价为-3价),该氮化物的化学式是__ __。
三、实验探究题(每空2分,共22分)
26.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50 g 5%的氯化钠溶液。
实验一:如图是同学们做粗盐提纯实验的操作示意图。
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是__ __。
(2)操作⑥中的错误是__ __。
(3)粗盐提纯实验的操作顺序为__ __(填操作序号)、称量精盐并计算产率。
(4)操作④中,当观察到__ __时,停止加热。
实验二:用提纯得到的精盐配制了50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有__ __(填序号)。
①氯化钠固体仍然不纯
②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
27.(青岛中考)化学课堂上,同学们分小组合作探究碳酸钠的性质,请你参与探究并填空。
【实验记录与分析】
实验一 实验二 实验三 实验四
实验 操作
实验 现象 溶液由无色变为红色 生成白色沉淀 生成白色沉淀
实验 结论 碳酸钠溶液显 性 碳酸钠能与盐酸发生反应 碳酸钠能与氢氧化钙发生反应
【反思与拓展】
(1)甲同学分析实验得出:盐溶液 (选填“一定”或“不一定”)显中性。
(2)乙同学用稀硫酸代替实验二中的稀盐酸进行探究,发现实验现象相同。从微观角度分析,这是因为稀盐酸和稀硫酸中都含有 。
(3 )丙同学对比实验三和实验四的现象,从微观角度分析,两个反应的实质相同,溶液中相互结合的离子都是_ _。
四、计算题(共8分)
28. 洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0 g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
第一次 第二次 第三次 第四次 第五次
加入Na2CO3溶液的质量/g 20.0 20.0 20.0 20.0 20.0
反应后溶液的总质量/g 118.9 137.8 M 175.6 195.6
请根据实验数据分析解答下列问题。
(1)表格中M的数值为 ;
(2)恰好完全反应时消耗Na2CO3的质量是多少?
(3)该洁厕灵中HCl的质量分数是多少?
参考答案
一、选择题(每小题四个选项中均只有一个正确,每小题2分,共40分)
1.分类和归纳是行之有效、简单易行的科学方法,下列说法错误的是 (C)
A.锂、汞都属于金属元素
B.锌、碘都属于人体必需的微量元素
C.尿素、硝酸钾都属于复合肥
D.塑料、合成纤维都属于合成材料
2. 新冠肺炎疫情防控期间,有医学专家建议大家早餐以鸡蛋、瘦肉、牛奶等食物为主,提高身体抵抗力。这三种食物提供的基本营养素主要是 (C)
A.糖类 B.油脂 C.蛋白质 D.维生素
3.下列有关化肥和农药的说法错误的是 (C)
A.氯化钾可用作钾肥
B.化肥能有效提高农作物产量
C.农药施用后,不会通过农作物转移到人体
D.农药应根据农作物、虫害和农药的特点合理施用
4. 下列说法正确的是 (C)
A.石油是可再生能源
B.高炉炼铁炼出的是纯铁
C.医用口罩过滤层使用了有机合成材料
D.易拉罐和矿泉水瓶属于不可回收垃圾
5. 化学与我们的生活密切相关。下列有关说法错误的是(B)
A.如果人体缺乏维生素C,会引起坏血病
B.可用甲醛溶液浸泡海产品,以确保长期食用
C.酱油中加入铁元素,可以预防缺铁性贫血
D.如果人体内缺乏碘元素会导致甲状腺肿大
6.某些劣质食品中常添加过量的“甜蜜素”,有害人体健康。工业上由环己胺(化学式是C6H11NH2)与氢氧化钠反应合成“甜蜜素”。下列对环己胺的叙述不正确的是 (D)
A.从类别上看:环己胺属于有机化合物
B.从性质上看:环己胺可以与碱反应
C.从组成上看:环己胺中碳元素和氮元素的质量比为36∶7
D.从结构上看:环己胺由6个碳原子、13个氢原子、1个氮原子构成
7. 下列物品所用的主要材料中不属于有机合成材料的是(B)
8.只用水不能鉴别的一组物质是 (C)
A.CaCO3和Na2CO3
B.FeCl2和FeCl3
C.NaCl和Na2SO4
D.固体NaOH和固体NH4NO3
9.现有氧化铁、稀硫酸、氢氧化钠溶液、氯化钡溶液和碳酸钾溶液五种物质,在常温下它们两两相互发生的化学反应共有 (B)
A.4个 B.5个 C.6个 D.7个
10. 下列各组离子在水中能大量共存且形成无色溶液的是(B)
A.Fe2+ Na+ SO42- Cl-
B.K+ Na+ OH- NO
C.Ba2+ Cl- SO42- OH-
D.H+ K+ NO32- CO32-
11. 去除难溶性杂质后的食盐样品中还含有可溶性杂质:CaCl2、MgCl2和Na2SO4。为除去可溶性杂质,将食盐样品溶于水,依次加入稍过量的三种溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反应后过滤,得滤渣X,向滤液中加入过量的稀盐酸,搅拌、煮沸,得氯化钠溶液。下列说法正确的是 (C)
A.滤渣X中有三种成分
B.“向滤液中加入过量的稀盐酸”。目的只是为了除去过量的NaOH
C.除杂过程中有Na2CO3参加的化学反应为复分解反应
D.将氯化钠溶液用如图装置加热蒸发,至水分完全蒸干时停止加热
12. 为鉴别氯化钠、氢氧化钠、碳酸钠和硫酸钠四种物质的溶液,设计如下实验:
下面对试剂①、试剂②和试剂③的选择,合理的是 (A)
A.①酚酞 ②稀盐酸 ③氯化钡
B.①酚酞 ②稀盐酸 ③稀盐酸
C.①石蕊 ②氯化钡 ③稀盐酸
D.①石蕊 ②氯化钡 ③碳酸钠
河道两旁有甲、乙两厂,它们排放的工业废水中共含H+、Na+、
Ba2+、Cl-、SO42-、CO32-六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,则甲厂废水中的离子是 (B)
A.H+、Na+、Ba2+ B.H+、Ba2+、Cl-
C.Na+、SO42-、CO32- D.H+、SO42-、CO32-
14.已知在一定条件下发生反应:甲+乙―→丙+丁,下列判断正确的是 (D)
A.甲、乙、丙、丁不可能含有同一种元素
B.丙为盐、丁为水,则该反应一定为复分解反应
C.甲、乙为化合物,则该反应一定为复分解反应
D.丙为Cu(NO3)2,则甲可能为单质、氧化物、碱或盐
15.下列关于化学实验中“操作—现象—结论”的描述正确的是(C)
A.在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐
B.在某溶液中加入氯化钡溶液和稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子
C.某溶液用pH试纸测试,试纸变蓝色(pH约为10),该溶液一定是碱性溶液
D.在稀盐酸与氢氧化钠反应后的溶液中滴加无色酚酞溶液不变色,可以断定两者恰好反应完全
16.有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种。取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,沉淀完全溶解并有气体产生。由此推断白色固体中 (A)
A.可能存在NaOH
B.可能存在Na2SO4
C.肯定不存在BaCl2
D.肯定存在Na2CO3和Na2SO4
17.下列实验方案能达成实验目的的是 (A)
A.鉴别KCl和NH4Cl两种化肥:取样,加入适量熟石灰研磨
B.检验NaOH溶液部分变质:取样,加入少量BaCl2溶液
C.除去CaCl2溶液中混有的少量盐酸:加入过量的Ca(OH)2溶液
D.配制溶质质量分数为5%的KCl溶液:称取5 g KCl,放入100 mL水中搅拌溶解
18. 向一定量的硫酸铜和稀硫酸的混合溶液中滴加氢氧化钠溶液,反应过程中产生的沉淀质量与加入的氢氧化钠溶液质量关系如图所示。下列说法不正确的是 (B)
A.a点溶液中的溶质有2种
B.c点溶液中的溶质有3种
C.ab(不包括a点)段有沉淀生成
D.d点溶液的pH>7
19.除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是 (A)
选项 物质 杂质 除杂试剂及操作方法
A Cu Fe 加入过量的CuCl2溶液,过滤、洗涤、干燥
B KCl MnO2 加入足量的水溶解,过滤、洗涤、干燥
C NaCl NaNO3 加入适量的硝酸银溶液至不再产生沉淀
D Cu C 在空气中灼烧
20. 向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤。不可能存在的情况是 (C)
A.滤纸上有Ag,滤液中有Ag+、Cu2+、 Zn2+、Mg2+
B.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+
C.滤纸上有Ag、Cu、Zn、Mg,滤液中有Zn2+
D.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
二、填空题(化学方程式每空2分,其余每空1分,共30分)
21.化学与我们的生活有着密切的联系。现有①氮气,②盐酸,③淀粉,④熟石灰,⑤金刚石,
⑥氯化钾。选择适当物质填空(填序号)。
(1)可用作钾肥的是__⑥__;
(2)可用来裁玻璃的是__⑤__;
(3)人体胃液中含有的酸是__②__;
(4)可用来改良酸性土壤的碱是__④__;
(5)焊接金属时常用作保护气的是__①__;
(6)米和面中含有的糖类物质主要是__③__。
22.清明时节,同学们相约外出踏青野炊。请用化学知识分析下列问题:
(1)野炊食谱如表所示:从合理膳食角度来看,你认为食谱中还应添加__C__(填字母)。
主食 馒头
配菜 红烧肉、豆腐汤、牛肉干
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)野炊后同学们准备将垃圾分类处理,其中属于不可回收垃圾的是__B__(填字母)。
A.废纸 B.果皮 C.易拉罐 D.塑料桶
(3)小滨用洗涤剂洗去手上的油迹,是利用了洗涤剂的__乳化__作用。
(4)大家在田边看到农民正在使用化肥NH4NO3,于是联想到NH4NO3不能和熟石灰混合施用,请用化学方程式解释原理__2NH4NO3+Ca(OH)2===Ca(NO3)2+2H2O+2NH3↑__。
23. 在抗击新冠肺炎疫情期间,我国采取了一系列有效的防控措施。 请用所学化学知识回答下列问题:
(1)进入人群密集或封闭场所应佩戴合格口罩,生产口罩的关键材料熔喷布是一种链状结构高分子材料,具有热塑性(选填“热塑性”或“热固性”),口罩贴合鼻梁部位的铝条很柔软,属于纯金属(选填“纯金属”或“合金”)。
(2)人们回家常用75%乙醇溶液擦拭随身物品消毒,乙醇也常用作燃料。写出乙醇完全燃烧的化学方程式:C2H5OH+3O22CO2+ 3H2O。
(3)适当运动和合理膳食可增强人体抵抗力,专家建议早餐用牛奶代替传统的白粥,是为了增加营养物质中的蛋白质摄入。
(4) 84消毒液常用于环境消毒,某次使用的消毒液pH为13,该溶液呈碱(选填“酸”“中”或“碱”)性。其有效成分是一种盐,化学式为NaClO, 其阴离子符号为ClO-。
24. 2020年5月22日,国务院总理李克强在政府工作报告中强调:着力抓好农业生产,稳定粮食播种面积和产量,大力防治重大病虫害。恢复生猪生产,落实“米袋子”省长负责制和“菜篮子”市长负责制。请用所学的化学知识回答下列问题。
(1)“米袋子”中的大米主要含有的基本营养素是糖类 “菜篮子”中包含多种蔬菜和水果,它们富含维生素C,人体缺乏维生素C,会引起坏血病;
(2)食盐几乎是每道菜不可或缺的调味品,加碘食盐中的“碘”指的是碘元素(选填 “单质”“原子”或“元素”);
(3) 为提高粮食产量,农业生产中要合理使用化肥, 钾肥(选填“氮肥”“磷肥”或“钾肥”)能增强抗病虫害和抗倒伏能力;
(4)下列有关饮食安全的说法正确的是B。
A.甲醛有防腐作用,可以用来浸泡食材
B.青少年多喝牛奶能补充钙元素
C.脂肪、蛋白质是人体必需的营养素,吃得越多越好
D.恢复生猪生产,为提高产量和瘦肉率,在饲料中添加瘦肉精
25.A~N是初中学过的物质。D是相对分子质量为40的氧化物,A是不溶于稀硝酸的白色沉淀,E是难溶于水的白色沉淀,实验室通常用N制取CO2。如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。
(注:难溶性碱加热分解生成对应的氧化物)
(1)写出化学式:
A__BaSO4__,
N__HCl__。
(2)写出E→B的化学反应方程式:
__Mg(OH)2+H2SO4===MgSO4+2H2O__。
(3)由F生成E需加入的物质是__NaOH或KOH等__。
(4)C在空气中燃烧生成D的实验现象是__发出耀眼的白光,产生白烟,生成白色固体。C在空气中燃烧除了生成D之外,也可能与空气中的氮气生成氮化物(氮元素化合价为-3价),该氮化物的化学式是__Mg3N2__。
三、实验探究题(每空2分,共22分)
26.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50 g 5%的氯化钠溶液。
实验一:如图是同学们做粗盐提纯实验的操作示意图。
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是__加速溶解__。
(2)操作⑥中的错误是__未用玻璃棒引流__。
(3)粗盐提纯实验的操作顺序为__①⑤②③⑥④__(填操作序号)、称量精盐并计算产率。
(4)操作④中,当观察到__出现较多固体__时,停止加热。
实验二:用提纯得到的精盐配制了50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有__①②③__(填序号)。
①氯化钠固体仍然不纯
②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
27. 化学课堂上,同学们分小组合作探究碳酸钠的性质,请你参与探究并填空。
【实验记录与分析】
实验一 实验二 实验三 实验四
实验 操作
实验 现象 溶液由无色变为红色 有气泡产生 生成白色沉淀 生成白色沉淀
实验 结论 碳酸钠溶液显碱性 碳酸钠能与盐酸发生反应 碳酸钠能与氢氧化钙发生反应 氯化钙能与碳酸钠反应
【反思与拓展】
(1)甲同学分析实验得出:盐溶液不一定(选填“一定”或“不一定”)显中性。
(2)乙同学用稀硫酸代替实验二中的稀盐酸进行探究,发现实验现象相同。从微观角度分析,这是因为稀盐酸和稀硫酸中都含有H+(或氢离子)。
(3 )丙同学对比实验三和实验四的现象,从微观角度分析,两个反应的实质相同,溶液中相互结合的离子都是__Ca2+和CO__。
四、计算题(共8分)
28. 洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0 g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
第一次 第二次 第三次 第四次 第五次
加入Na2CO3溶液的质量/g 20.0 20.0 20.0 20.0 20.0
反应后溶液的总质量/g 118.9 137.8 M 175.6 195.6
请根据实验数据分析解答下列问题。
(1)表格中M的数值为156.7;
(2)恰好完全反应时消耗Na2CO3的质量是多少?
(3)该洁厕灵中HCl的质量分数是多少?
解:(2)由表格数据可知,前四次中每次加入20 g Na2CO3溶液都恰好生成1.1 g CO2,第五次加入后总质量无变化,可知第四次加入碳酸钠溶液后,恰好完全反应,生成CO2的质量为100 g+20 g+20 g+20 g+20 g+20 g-195.6 g=4.4 g,
设恰好反应时消耗Na2CO3的质量为x,HCl的质量为y。
Na2CO3+2HCl===2NaCl+H2O+CO2↑
106 73 44
x y 4.4 g
= x=10.6 g
= y=7.3 g
(3)该洁厕灵中HCl的质量分数为×100%=7.3%。
同课章节目录
