8.3酸和碱的反应第二课时中和反应的应用-2021-2022学年九年级化学科粤版(2012)下册(23张PPT)
文档属性
| 名称 | 8.3酸和碱的反应第二课时中和反应的应用-2021-2022学年九年级化学科粤版(2012)下册(23张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-17 00:00:00 | ||
图片预览







文档简介
(共23张PPT)
第八章 常见的酸、碱、盐
8.3 酸和碱的反应
(第二课时)
中和反应的应用
8.3 酸和碱的反应
【教学目标】:
1. 理解中和反应的原理和实质。
2. 了解中和反应在实际生活中的应用。
二、【教学重点】:
理解酸和碱发生中和反应的本质。
三、【教学难点】:
中和反应的应用。
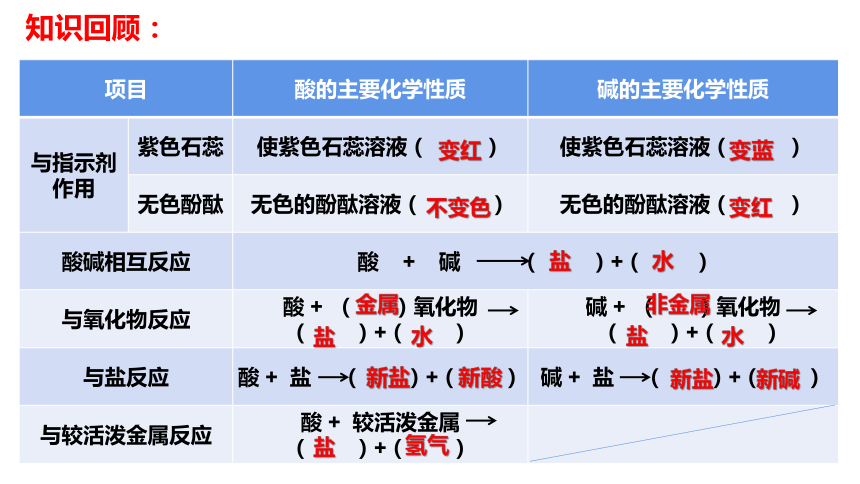
项目 酸的主要化学性质 碱的主要化学性质
与指示剂作用 紫色石蕊 使紫色石蕊溶液( ) 使紫色石蕊溶液( )
无色酚酞 无色的酚酞溶液( ) 无色的酚酞溶液( )
酸碱相互反应 酸 + 碱 ( )+( ) 与氧化物反应 酸 + ( )氧化物 ( )+( ) 碱 + ( )氧化物
( )+( )
与盐反应 酸 + 盐 ( )+( ) 碱 + 盐 ( )+( )
与较活泼金属反应 酸 + 较活泼金属 ( )+( )
知识回顾:
变红
变蓝
不变色
变红
盐
水
金属
非金属
盐
盐
水
水
新盐
新酸
新盐
新碱
盐
氢气
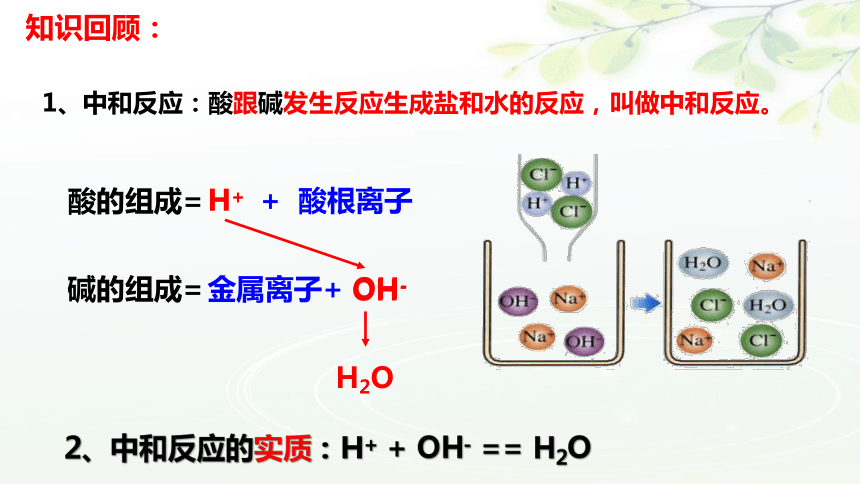
酸的组成=
H+ + 酸根离子
碱的组成=
金属离子+ OH-
H2O
2、中和反应的实质:H+ + OH- == H2O
H+
OH-
1、中和反应:酸跟碱发生反应生成盐和水的反应,叫做中和反应。
知识回顾:
知识回顾:
3、复分解反应:
4、通式:AB+CD → AD+CB
5、反应特点:
③中和反应属于复分解反应中的一种
①反应物和生成物都是化合物
②反应物之间一定要交换成分(化合价不变)
由两种化合物互相交换成分,生成另外两种化合物的反应。
一、中和反应的应用
1.改良酸性或碱性土壤
(2)向鱼塘撒熟石灰,中和鱼塘底泥中过多的有机酸,使鱼塘水达到适合鱼苗生长的pH。
(1)利用熟石灰的碱性中和土壤和某些水源的过多酸性
2.处理工厂的废水
酸性或碱性废水必须先进行处理,达标后才可以排放,否则会造成水体污染。
(1)如何处理硫酸厂生产中形成的含硫酸的污水?
熟石灰(Ca(OH)2)
(2)请写出有关反应的化学方程式:
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
(3)用生石灰(CaO)来中和污水行不行?
CaO + H2O =Ca(OH)2
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
3.医药应用
好多人给山药削完皮手奇痒难忍,怎么解
夏天蚊虫多,被叮了一下又疼又痒,怎么办?
3.医药应用
山药中含有植物碱,会引起皮肤的过敏反应而发痒。
被蚊虫叮咬,皮肤会出现红肿而疼痒,是因为它们向我们的皮肤“注射”了“蚁酸”——甲酸。
醋或柠檬中含有酸性物质,可以与山药中的植物碱发生中和反应就止痒啦。。。
这时用碱性的肥皂水可以中和“蚁酸”,达到止痒的目的。
3.医药应用
如不小心被黄蜂刺到,由于黄蜂的刺是碱性的。
可在皮肤上涂抹酸性物质如醋酸,以减轻痛痒。
3.医药应用
胃酸 (主要是HCl溶液)过多时可口服碱性“胃舒平”(主要成分为Al(OH)3)或小苏打片(主要成分是NaHCO3)
3HCl + Al(OH)3 == AlCl3 + 3H2O
科学实验需将溶液的ph控制在一定范围内。若溶液酸碱性太强或太弱,都可用适当的碱或酸调节溶液ph。
4.调节溶液的酸碱性
知识视窗:
部分非金属氧化物能跟水化合生成酸.
例如: SO2 + H2O = H2SO3 (亚硫酸)
SO3 + H2O = H2SO4
3NO2 + H2O = 2HNO3 + NO
SO2、NO2 是形成酸雨的主要物质。
雨水为显酸性的雨水,若其 pH 小于5.6 称为酸雨.
CO2 + H2O = H2CO3
小结:
部分酸、碱、盐的溶解性表P305
铵钾钠盐均可溶;
硝盐遇水影无踪;
氯银硫钡沉下去;
碳盐氢物多不溶。
巩固练习:
1.胃酸能帮助消化,但过多的胃酸会危害健康。可用于治疗胃酸过多的物质是 ( )
A.NaCl B.Al(OH)3
C.CaO D.NaOH
2.食用松花蛋时常感到有涩味,这是因为制作松花蛋的过程中用到了熟石灰和纯碱等原料。为了减轻涩味,可在食用松花蛋时添加某种调味品,这种调味品最好是 ( )
A、食盐 B、食醋
C、香油 D、味精
B
B
巩固练习:
3.一些物质的近似pH如下表,下列有关表中四种物质的说法中正确的是( )
A.只有胃液显酸性 B.只有胰液显碱性
C.正常雨水显中性 D.胃酸过多的人宜食用玉米粥
D
物质 胰液 胃液 正常雨水 玉米粥
pH 7.8~8.0 0.9~1.5 ≈5.6 6.9~8.0
巩固练习:
4.生活中一些常见物质的pH如下图所示:其中能使洗涤用苏打水(含Na2CO3)产生气泡的是( )
A.食盐水 B.矿泉水 C.柠檬水 D.含氨洗涤液
C
巩固练习:
5.某实验小组使用pH传感器探究稀盐酸和氢氧化钠溶液的反应,实验过程中测得溶液pH的变化如图所示。下列说法中,正确的是( )
A.图中a点时的溶液pH>7,显酸性
B.图中c点时的溶液里溶质只有氯化钠
C.该实验是将稀盐酸滴加到氢氧化钠溶液中
D.实验中可以观察到产生大量气泡
C
巩固练习:
6.室温下,将氢氧化钠溶液滴加到盛有一定量稀盐酸的容器中,边滴边搅拌,用数字pH仪连接电脑实时测得pH变化曲线如图。下列相关叙述错误的是( )
A.容器中发生的反应属于中和反应
B.a点溶液能使紫色石蕊溶液变红
C.b点表示HCl与NaOH等质量反应
D.c点溶液中的溶质是NaCl和NaOH
C
巩固练习:
7.某实验小组将Ba(OH)2溶液逐滴滴入硫酸溶液中,溶质的质量与加入的Ba(OH)2溶液的质量关系如图所示(提示BaSO4:不溶于水)。下列说法错误的是( )
A.a点溶液为酸性
B.b点恰好完全反应
C.c点溶液的溶质为硫酸
D.b、c两点沉淀质量相等
C
巩固练习:
8.室温下,将稀盐酸滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度与加入稀盐酸的质量关系如图所示,下列叙述错误的是( )
A.B点表示氢氧化钠完全反应
B.稀盐酸与氢氧化钠溶液发生的反应是放热反应
C.从A点到B点的过程中,烧杯中溶液的pH逐渐增大
D.C点时,溶液中的溶质是氯化钠和氯化氢
C
第八章 常见的酸、碱、盐
8.3 酸和碱的反应
(第二课时)
中和反应的应用
8.3 酸和碱的反应
【教学目标】:
1. 理解中和反应的原理和实质。
2. 了解中和反应在实际生活中的应用。
二、【教学重点】:
理解酸和碱发生中和反应的本质。
三、【教学难点】:
中和反应的应用。
项目 酸的主要化学性质 碱的主要化学性质
与指示剂作用 紫色石蕊 使紫色石蕊溶液( ) 使紫色石蕊溶液( )
无色酚酞 无色的酚酞溶液( ) 无色的酚酞溶液( )
酸碱相互反应 酸 + 碱 ( )+( ) 与氧化物反应 酸 + ( )氧化物 ( )+( ) 碱 + ( )氧化物
( )+( )
与盐反应 酸 + 盐 ( )+( ) 碱 + 盐 ( )+( )
与较活泼金属反应 酸 + 较活泼金属 ( )+( )
知识回顾:
变红
变蓝
不变色
变红
盐
水
金属
非金属
盐
盐
水
水
新盐
新酸
新盐
新碱
盐
氢气
酸的组成=
H+ + 酸根离子
碱的组成=
金属离子+ OH-
H2O
2、中和反应的实质:H+ + OH- == H2O
H+
OH-
1、中和反应:酸跟碱发生反应生成盐和水的反应,叫做中和反应。
知识回顾:
知识回顾:
3、复分解反应:
4、通式:AB+CD → AD+CB
5、反应特点:
③中和反应属于复分解反应中的一种
①反应物和生成物都是化合物
②反应物之间一定要交换成分(化合价不变)
由两种化合物互相交换成分,生成另外两种化合物的反应。
一、中和反应的应用
1.改良酸性或碱性土壤
(2)向鱼塘撒熟石灰,中和鱼塘底泥中过多的有机酸,使鱼塘水达到适合鱼苗生长的pH。
(1)利用熟石灰的碱性中和土壤和某些水源的过多酸性
2.处理工厂的废水
酸性或碱性废水必须先进行处理,达标后才可以排放,否则会造成水体污染。
(1)如何处理硫酸厂生产中形成的含硫酸的污水?
熟石灰(Ca(OH)2)
(2)请写出有关反应的化学方程式:
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
(3)用生石灰(CaO)来中和污水行不行?
CaO + H2O =Ca(OH)2
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
3.医药应用
好多人给山药削完皮手奇痒难忍,怎么解
夏天蚊虫多,被叮了一下又疼又痒,怎么办?
3.医药应用
山药中含有植物碱,会引起皮肤的过敏反应而发痒。
被蚊虫叮咬,皮肤会出现红肿而疼痒,是因为它们向我们的皮肤“注射”了“蚁酸”——甲酸。
醋或柠檬中含有酸性物质,可以与山药中的植物碱发生中和反应就止痒啦。。。
这时用碱性的肥皂水可以中和“蚁酸”,达到止痒的目的。
3.医药应用
如不小心被黄蜂刺到,由于黄蜂的刺是碱性的。
可在皮肤上涂抹酸性物质如醋酸,以减轻痛痒。
3.医药应用
胃酸 (主要是HCl溶液)过多时可口服碱性“胃舒平”(主要成分为Al(OH)3)或小苏打片(主要成分是NaHCO3)
3HCl + Al(OH)3 == AlCl3 + 3H2O
科学实验需将溶液的ph控制在一定范围内。若溶液酸碱性太强或太弱,都可用适当的碱或酸调节溶液ph。
4.调节溶液的酸碱性
知识视窗:
部分非金属氧化物能跟水化合生成酸.
例如: SO2 + H2O = H2SO3 (亚硫酸)
SO3 + H2O = H2SO4
3NO2 + H2O = 2HNO3 + NO
SO2、NO2 是形成酸雨的主要物质。
雨水为显酸性的雨水,若其 pH 小于5.6 称为酸雨.
CO2 + H2O = H2CO3
小结:
部分酸、碱、盐的溶解性表P305
铵钾钠盐均可溶;
硝盐遇水影无踪;
氯银硫钡沉下去;
碳盐氢物多不溶。
巩固练习:
1.胃酸能帮助消化,但过多的胃酸会危害健康。可用于治疗胃酸过多的物质是 ( )
A.NaCl B.Al(OH)3
C.CaO D.NaOH
2.食用松花蛋时常感到有涩味,这是因为制作松花蛋的过程中用到了熟石灰和纯碱等原料。为了减轻涩味,可在食用松花蛋时添加某种调味品,这种调味品最好是 ( )
A、食盐 B、食醋
C、香油 D、味精
B
B
巩固练习:
3.一些物质的近似pH如下表,下列有关表中四种物质的说法中正确的是( )
A.只有胃液显酸性 B.只有胰液显碱性
C.正常雨水显中性 D.胃酸过多的人宜食用玉米粥
D
物质 胰液 胃液 正常雨水 玉米粥
pH 7.8~8.0 0.9~1.5 ≈5.6 6.9~8.0
巩固练习:
4.生活中一些常见物质的pH如下图所示:其中能使洗涤用苏打水(含Na2CO3)产生气泡的是( )
A.食盐水 B.矿泉水 C.柠檬水 D.含氨洗涤液
C
巩固练习:
5.某实验小组使用pH传感器探究稀盐酸和氢氧化钠溶液的反应,实验过程中测得溶液pH的变化如图所示。下列说法中,正确的是( )
A.图中a点时的溶液pH>7,显酸性
B.图中c点时的溶液里溶质只有氯化钠
C.该实验是将稀盐酸滴加到氢氧化钠溶液中
D.实验中可以观察到产生大量气泡
C
巩固练习:
6.室温下,将氢氧化钠溶液滴加到盛有一定量稀盐酸的容器中,边滴边搅拌,用数字pH仪连接电脑实时测得pH变化曲线如图。下列相关叙述错误的是( )
A.容器中发生的反应属于中和反应
B.a点溶液能使紫色石蕊溶液变红
C.b点表示HCl与NaOH等质量反应
D.c点溶液中的溶质是NaCl和NaOH
C
巩固练习:
7.某实验小组将Ba(OH)2溶液逐滴滴入硫酸溶液中,溶质的质量与加入的Ba(OH)2溶液的质量关系如图所示(提示BaSO4:不溶于水)。下列说法错误的是( )
A.a点溶液为酸性
B.b点恰好完全反应
C.c点溶液的溶质为硫酸
D.b、c两点沉淀质量相等
C
巩固练习:
8.室温下,将稀盐酸滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度与加入稀盐酸的质量关系如图所示,下列叙述错误的是( )
A.B点表示氢氧化钠完全反应
B.稀盐酸与氢氧化钠溶液发生的反应是放热反应
C.从A点到B点的过程中,烧杯中溶液的pH逐渐增大
D.C点时,溶液中的溶质是氯化钠和氯化氢
C
同课章节目录
