第九单元第二节金属的化学性质课件—2021-2022学年九年级化学鲁教版下册(共19张PPT)
文档属性
| 名称 | 第九单元第二节金属的化学性质课件—2021-2022学年九年级化学鲁教版下册(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-18 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
第九单元 第二节第一课时
金属的化学性质
铝粉在氧气中燃烧
铁丝在氧气中燃烧
镁条在空气中燃烧
大多数的金属能与氧气发生反应,但是相同条件下反应的现象(剧烈程度)不同
一、金属与氧气的反应探究
反应现象 化学方程式
镁
锌
铁
铜
比较三种金属与酸反应的难易和剧烈程度,将三种金属的活动性按由强到弱的顺序为 。
结论:部分金属能与酸反应放出氢气
二、金属与酸的反应探究
镁条表面产生大量气泡
锌粒表面产生大量气泡
铁丝表面产生大量气泡,溶液由无色变为浅绿色
无明显变化
Fe + 2HCl = FeCl2 + 2H2
Zn + 2HCl = ZnCl2 + 2H2
Mg + 2HCl = MgCl2+ 2H2
金属活动性由强逐渐减弱
常见金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属与酸反应放出氢气的反应规律:
①排在氢前面的金属才能与酸反应生成氢气,金属越活泼,反应越剧烈,速度越快。
②这里的酸一般指 盐酸和稀硫酸,不能用浓硫酸和硝酸,否则反应不会生成氢气。
注意问题:铁跟酸反应时生成的是亚铁盐。
金属与酸的反应的一般规律
A. Fe+HCl
B. Cu+HCl
C. Zn+H2SO4
D. Fe+HNO3
E. Mg+H2SO4
F. Al+H2SO4(浓)
判断下列反应能否发生,不能反应的说明原因
下列方程式表示的是置换反应且正确的是:
A 2Al + 3H2SO4 = Al2(SO4)3 + 3H2
C 2Fe + 3H2SO4 = Fe2(SO4 )3+ 3H2
D NaCl + AgNO3 = NaNO3 + AgCl
B Cu + H2SO4 = CuSO4 + H2
反馈练习
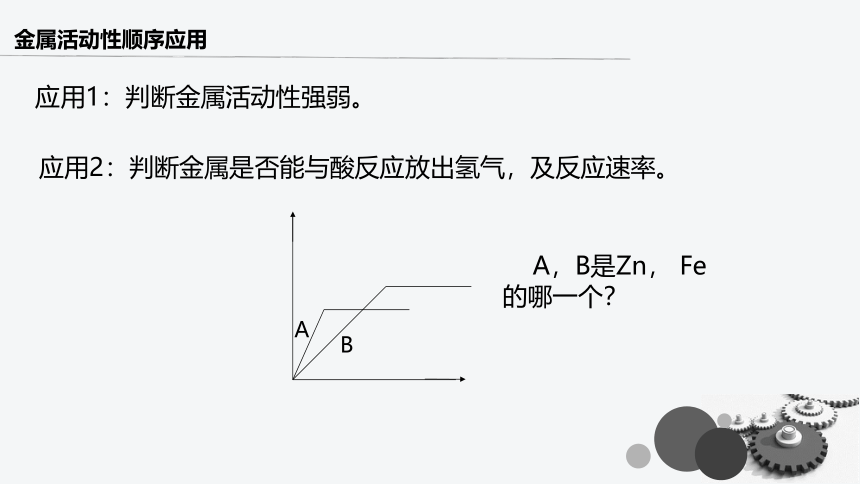
应用1:判断金属活动性强弱。
应用2:判断金属是否能与酸反应放出氢气,及反应速率。
A
B
A,B是Zn, Fe的哪一个?
金属活动性顺序应用
1.向装有铁丝的试管中加入少量的稀盐酸你会观察到的现象是:
铁丝表面产生大量气泡,溶液由无色变为浅绿色。
2.下列物质可以由相应的金属和酸发生置换反应制得
的是( )
A、Fe2(SO4)3 B、CuCl2
C、AgNO3 D、Al2(SO4)3
写出发生反应的化学方程式:
Fe + HCl + H2
2
FeCl2
金属与酸的反应常见题型
气泡
甲
乙
丙
丁
①.判断四种金属的活动性:
甲>
乙>
丙>
丁
在金属活动性顺序中甲乙丙排在氢的前面,丁 排在氢的后面。
Mg Zn Fe Cu
3.
②.除此之外你还可以得到哪些信息:
③.列举出一个符合图示现象的甲乙丙丁的金属组合
金属与酸的反应常见题型
A
B
m(H2)
t
0
C
A.金属活动性的强弱关系是A>B
B.反应结束后A放出的气体比B多
C.相对原子量的关系可能是A>B
4. 等质量的金属A, B 与足量的等质量等质量分数的稀盐酸反应,得到反应过程中氢气质量与时间的关系如图,请判断:
D. A,B,C依次可能是
,C
×
√
√
×
Mg,Zn,Fe
Zn,Fe,Mg
√
小结: ①金属活动性越强, 反应放出的气体速率越大,则斜线部分越陡;
②等质量的不同金属与等质量等质量分数的足量的酸发生置换反应,若在反应中表现的化合价相同,则相对原子质量小的产生氢气多。
金属与酸的反应常见题型
第九单元 第二节第二课时
金属的化学性质
CuSO4溶液 AgNO3溶液 NaCl溶液
Al
Fe
Cu
铝片表面附着有红色物质,溶液由蓝色变为无色
结论:某些金属和盐溶液之间会发生反应,生成另一种金属和另一种盐
三、金属盐溶液的反应探究
1.活动性强的金属置换活动性弱的;
2.盐必须是可溶性的;
3、金属K、Ca、Na除外。
Cu有可能把Ag从它的盐溶液中置换出来吗?
Cu和AgNO3,AgCl,Hg(NO3)2,中的哪些能反应?
Fe和ZnNO3能否反应?
金属K、Ca、Na的化学性质太活泼与水就会反应放出氢气
三、金属盐溶液的反应探究
3、下列物质可以由相应的金属和酸发生置换反应而制得的是( )
A、Fe2(SO4)3 B、CuCl2
C、AgNO3 D、Al2(SO4)3
1、下列金属中,金属活动性最强的是( )
A Zn B Mg C Fe D Cu
2、下列化学方程式中,正确的是( )
A、Cu + 2AgCl 2Ag + CuCl2
B、Zn + 2AgNO3 2Ag +Zn(NO3)2
C、2Na + CuSO4 Cu + Na2SO4
D、2Fe +3CuCl2 2FeCl3 + 3Cu
金属与盐溶液的反应常见题型练习
4、把一枚无锈铁钉放在硫酸铜溶液中,一段时间后,可出现的是( )
A. 溶液蓝色变浅直至无色 B. 铁钉表面析出红色物质
C. 产生大量气泡 D. 溶液质量增加
金属与盐溶液的反应常见题型练习
5、 有甲、乙、丙三种金属,如果将甲、乙、丙分别放入硫酸铜溶液中,
一段时间后,乙、丙表面出现红色物质,甲没有明显现象;再将大小相同
的乙、丙分别放入相同溶质质量分数的稀盐酸中,乙、丙均产生气泡,但
丙产生气泡的速度明显快于乙,则甲、乙、丙三种金属的活动性顺序是( )
A. 丙>乙>甲 B. 甲>丙>乙 C. 丙>甲>乙 D. 甲>乙>丙
金属与盐溶液的反应常见题型练习
6、将金属M的粉末放入盛有硝酸铜溶液的烧杯中,充分反应后,溶液呈无色,继续向烧杯中加入一定量的硝酸银溶液,充分反应后过滤,得到滤渣和蓝色滤液。根据上述实验分析,下列说法错误的是( )
A. 金属活动性强弱顺序:M>Cu>Ag
B. 滤渣中可能有金属M
C. 滤液中至少含有两种溶质
D. 滤渣中一定有Ag
金属与盐溶液的反应常见题型练习
7、金属在生产、生活中有广泛应用。
(1)写出用盐酸除去铁制品表面铁锈的化学方程式__________________。
(2)硫酸铜、硫酸亚铁的混合溶液中加入一定量镁粉,充分反应后过滤,得到滤渣和滤液。若滤液呈无色,则滤渣中一定含有的金属是__________。
金属与盐溶液的反应常见题型练习
A
B
C
D
8、将质量相等的镁粉和铁粉分别投入等质量等浓度的稀硫酸中,所得氢气质量与稀硫酸质量关系曲线正确的是
金属与盐溶液的反应常见题型练习
9、 置换反应是初中化学反应的基本类型之一。
已知化合物A+单质B→化合物C+单质D 。试回答下列问题:
(1)若D为氢气,A为稀硫酸,则B应满足的条件是_______________________。
(2)若D为铜,化合物A的化学式可能为______________________________。
第九单元 第二节第一课时
金属的化学性质
铝粉在氧气中燃烧
铁丝在氧气中燃烧
镁条在空气中燃烧
大多数的金属能与氧气发生反应,但是相同条件下反应的现象(剧烈程度)不同
一、金属与氧气的反应探究
反应现象 化学方程式
镁
锌
铁
铜
比较三种金属与酸反应的难易和剧烈程度,将三种金属的活动性按由强到弱的顺序为 。
结论:部分金属能与酸反应放出氢气
二、金属与酸的反应探究
镁条表面产生大量气泡
锌粒表面产生大量气泡
铁丝表面产生大量气泡,溶液由无色变为浅绿色
无明显变化
Fe + 2HCl = FeCl2 + 2H2
Zn + 2HCl = ZnCl2 + 2H2
Mg + 2HCl = MgCl2+ 2H2
金属活动性由强逐渐减弱
常见金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属与酸反应放出氢气的反应规律:
①排在氢前面的金属才能与酸反应生成氢气,金属越活泼,反应越剧烈,速度越快。
②这里的酸一般指 盐酸和稀硫酸,不能用浓硫酸和硝酸,否则反应不会生成氢气。
注意问题:铁跟酸反应时生成的是亚铁盐。
金属与酸的反应的一般规律
A. Fe+HCl
B. Cu+HCl
C. Zn+H2SO4
D. Fe+HNO3
E. Mg+H2SO4
F. Al+H2SO4(浓)
判断下列反应能否发生,不能反应的说明原因
下列方程式表示的是置换反应且正确的是:
A 2Al + 3H2SO4 = Al2(SO4)3 + 3H2
C 2Fe + 3H2SO4 = Fe2(SO4 )3+ 3H2
D NaCl + AgNO3 = NaNO3 + AgCl
B Cu + H2SO4 = CuSO4 + H2
反馈练习
应用1:判断金属活动性强弱。
应用2:判断金属是否能与酸反应放出氢气,及反应速率。
A
B
A,B是Zn, Fe的哪一个?
金属活动性顺序应用
1.向装有铁丝的试管中加入少量的稀盐酸你会观察到的现象是:
铁丝表面产生大量气泡,溶液由无色变为浅绿色。
2.下列物质可以由相应的金属和酸发生置换反应制得
的是( )
A、Fe2(SO4)3 B、CuCl2
C、AgNO3 D、Al2(SO4)3
写出发生反应的化学方程式:
Fe + HCl + H2
2
FeCl2
金属与酸的反应常见题型
气泡
甲
乙
丙
丁
①.判断四种金属的活动性:
甲>
乙>
丙>
丁
在金属活动性顺序中甲乙丙排在氢的前面,丁 排在氢的后面。
Mg Zn Fe Cu
3.
②.除此之外你还可以得到哪些信息:
③.列举出一个符合图示现象的甲乙丙丁的金属组合
金属与酸的反应常见题型
A
B
m(H2)
t
0
C
A.金属活动性的强弱关系是A>B
B.反应结束后A放出的气体比B多
C.相对原子量的关系可能是A>B
4. 等质量的金属A, B 与足量的等质量等质量分数的稀盐酸反应,得到反应过程中氢气质量与时间的关系如图,请判断:
D. A,B,C依次可能是
,C
×
√
√
×
Mg,Zn,Fe
Zn,Fe,Mg
√
小结: ①金属活动性越强, 反应放出的气体速率越大,则斜线部分越陡;
②等质量的不同金属与等质量等质量分数的足量的酸发生置换反应,若在反应中表现的化合价相同,则相对原子质量小的产生氢气多。
金属与酸的反应常见题型
第九单元 第二节第二课时
金属的化学性质
CuSO4溶液 AgNO3溶液 NaCl溶液
Al
Fe
Cu
铝片表面附着有红色物质,溶液由蓝色变为无色
结论:某些金属和盐溶液之间会发生反应,生成另一种金属和另一种盐
三、金属盐溶液的反应探究
1.活动性强的金属置换活动性弱的;
2.盐必须是可溶性的;
3、金属K、Ca、Na除外。
Cu有可能把Ag从它的盐溶液中置换出来吗?
Cu和AgNO3,AgCl,Hg(NO3)2,中的哪些能反应?
Fe和ZnNO3能否反应?
金属K、Ca、Na的化学性质太活泼与水就会反应放出氢气
三、金属盐溶液的反应探究
3、下列物质可以由相应的金属和酸发生置换反应而制得的是( )
A、Fe2(SO4)3 B、CuCl2
C、AgNO3 D、Al2(SO4)3
1、下列金属中,金属活动性最强的是( )
A Zn B Mg C Fe D Cu
2、下列化学方程式中,正确的是( )
A、Cu + 2AgCl 2Ag + CuCl2
B、Zn + 2AgNO3 2Ag +Zn(NO3)2
C、2Na + CuSO4 Cu + Na2SO4
D、2Fe +3CuCl2 2FeCl3 + 3Cu
金属与盐溶液的反应常见题型练习
4、把一枚无锈铁钉放在硫酸铜溶液中,一段时间后,可出现的是( )
A. 溶液蓝色变浅直至无色 B. 铁钉表面析出红色物质
C. 产生大量气泡 D. 溶液质量增加
金属与盐溶液的反应常见题型练习
5、 有甲、乙、丙三种金属,如果将甲、乙、丙分别放入硫酸铜溶液中,
一段时间后,乙、丙表面出现红色物质,甲没有明显现象;再将大小相同
的乙、丙分别放入相同溶质质量分数的稀盐酸中,乙、丙均产生气泡,但
丙产生气泡的速度明显快于乙,则甲、乙、丙三种金属的活动性顺序是( )
A. 丙>乙>甲 B. 甲>丙>乙 C. 丙>甲>乙 D. 甲>乙>丙
金属与盐溶液的反应常见题型练习
6、将金属M的粉末放入盛有硝酸铜溶液的烧杯中,充分反应后,溶液呈无色,继续向烧杯中加入一定量的硝酸银溶液,充分反应后过滤,得到滤渣和蓝色滤液。根据上述实验分析,下列说法错误的是( )
A. 金属活动性强弱顺序:M>Cu>Ag
B. 滤渣中可能有金属M
C. 滤液中至少含有两种溶质
D. 滤渣中一定有Ag
金属与盐溶液的反应常见题型练习
7、金属在生产、生活中有广泛应用。
(1)写出用盐酸除去铁制品表面铁锈的化学方程式__________________。
(2)硫酸铜、硫酸亚铁的混合溶液中加入一定量镁粉,充分反应后过滤,得到滤渣和滤液。若滤液呈无色,则滤渣中一定含有的金属是__________。
金属与盐溶液的反应常见题型练习
A
B
C
D
8、将质量相等的镁粉和铁粉分别投入等质量等浓度的稀硫酸中,所得氢气质量与稀硫酸质量关系曲线正确的是
金属与盐溶液的反应常见题型练习
9、 置换反应是初中化学反应的基本类型之一。
已知化合物A+单质B→化合物C+单质D 。试回答下列问题:
(1)若D为氢气,A为稀硫酸,则B应满足的条件是_______________________。
(2)若D为铜,化合物A的化学式可能为______________________________。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
