2021-2022学年八年级化学鲁教版(五四制)全一册 第四单元我们周围的空气质量监测试题(word版 含答案)
文档属性
| 名称 | 2021-2022学年八年级化学鲁教版(五四制)全一册 第四单元我们周围的空气质量监测试题(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 161.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-19 00:00:00 | ||
图片预览

文档简介
第四单元《我们周围的空气》质量监测试题
( 时间45分钟, 分值100分)
班级______________ 姓名______________ 成绩______________
可能用到的相对原子质量:C 12 H 1 O 16
一、选择题(本题包括10小题,每小题3分,共30分。请将正确答案的序号填写在下表相应空格内)
题号 1 2 3 4 5 6 7 8 9 10
答案
1.宁阳县某学校研究性学习活动小组的学生利用课余时间调查雾霾产生的原因,并提出可减少雾霾的说法正确的是
A.鼓励开私家车出行 B.鼓励燃煤火力发电
C.鼓动使用太阳能热水器 D.鼓励露天焚烧垃圾
2.空气是一种宝贵的自然资源。下列有关说法不正确的是
A.把空气中的其他成分分离出去,只留下氧气会更有益于生命活动
B.分离液态空气制取氧气属于物理变化
C.空气中的氮气常用作保护气
D.稀有气体都没有颜色、没有气味,在通电时能发出不同颜色的光
3.下列选项不属于氧气在大自然中消耗途径的是
A.生物的呼吸作用 B.绿色植物的光合作用
C.物质在空气中的燃烧 D.物质在空气中的缓慢氧化
4.下列有关氧气性质的叙述中,正确的是
A.氧气的密度比空气的略大
B.氧气极易溶于水
C.氧气是一种化学性质很活泼的气体,能与所有物质发生反应
D.氧气具有可燃性,是一种常用的燃料
5.用过氧化氢溶液制取氧气时,忘记加二氧化锰,其结果是
A.不放出氧气 B.放出氧气速率慢
C.放出氧气总量会减少 D.放出氧气总量会更多
6.一氧化氮在常温下是一种难溶于水的气体,密度比空气略大;它能跟空气里的氧气迅速反应,生成二氧化氮。先要收集一瓶一氧化氮气体,可采用的方法是8
A.向上排空气法 B.排水法
C.排水法或向上排空气法 D.排水法或向下排空气法
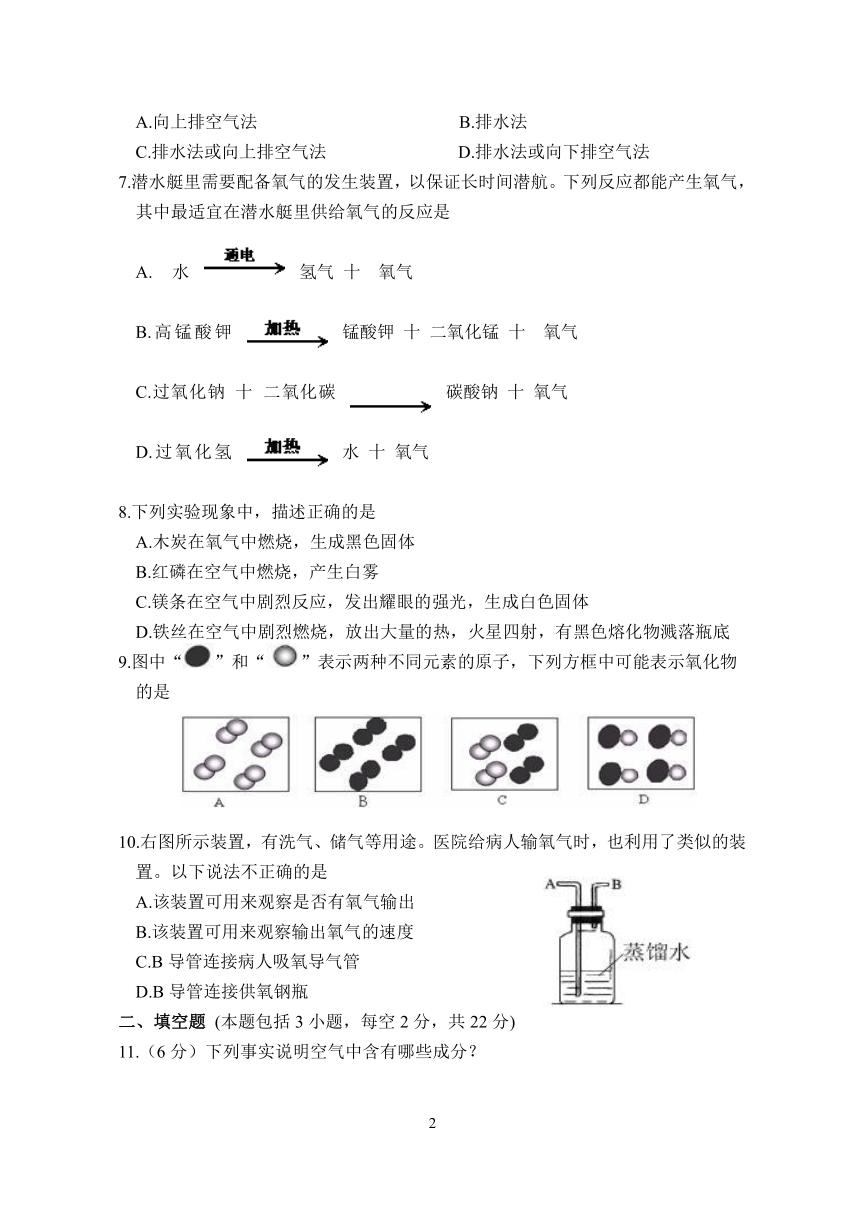
7.潜水艇里需要配备氧气的发生装置,以保证长时间潜航。下列反应都能产生氧气,其中最适宜在潜水艇里供给氧气的反应是
A. 水 氢气 十 氧气
B.高锰酸钾 锰酸钾 十 二氧化锰 十 氧气
C.过氧化钠 十 二氧化碳 碳酸钠 十 氧气
D.过氧化氢 水 十 氧气
8.下列实验现象中,描述正确的是
A.木炭在氧气中燃烧,生成黑色固体
B.红磷在空气中燃烧,产生白雾
C.镁条在空气中剧烈反应,发出耀眼的强光,生成白色固体
D.铁丝在空气中剧烈燃烧,放出大量的热,火星四射,有黑色熔化物溅落瓶底
9.图中“”和“”表示两种不同元素的原子,下列方框中可能表示氧化物
的是
10.右图所示装置,有洗气、储气等用途。医院给病人输氧气时,也利用了类似的装置。以下说法不正确的是
A.该装置可用来观察是否有氧气输出
B.该装置可用来观察输出氧气的速度
C.B导管连接病人吸氧导气管
D.B导管连接供氧钢瓶
二、填空题 (本题包括3小题,每空2分,共22分)
11.(6分)下列事实说明空气中含有哪些成分?
8
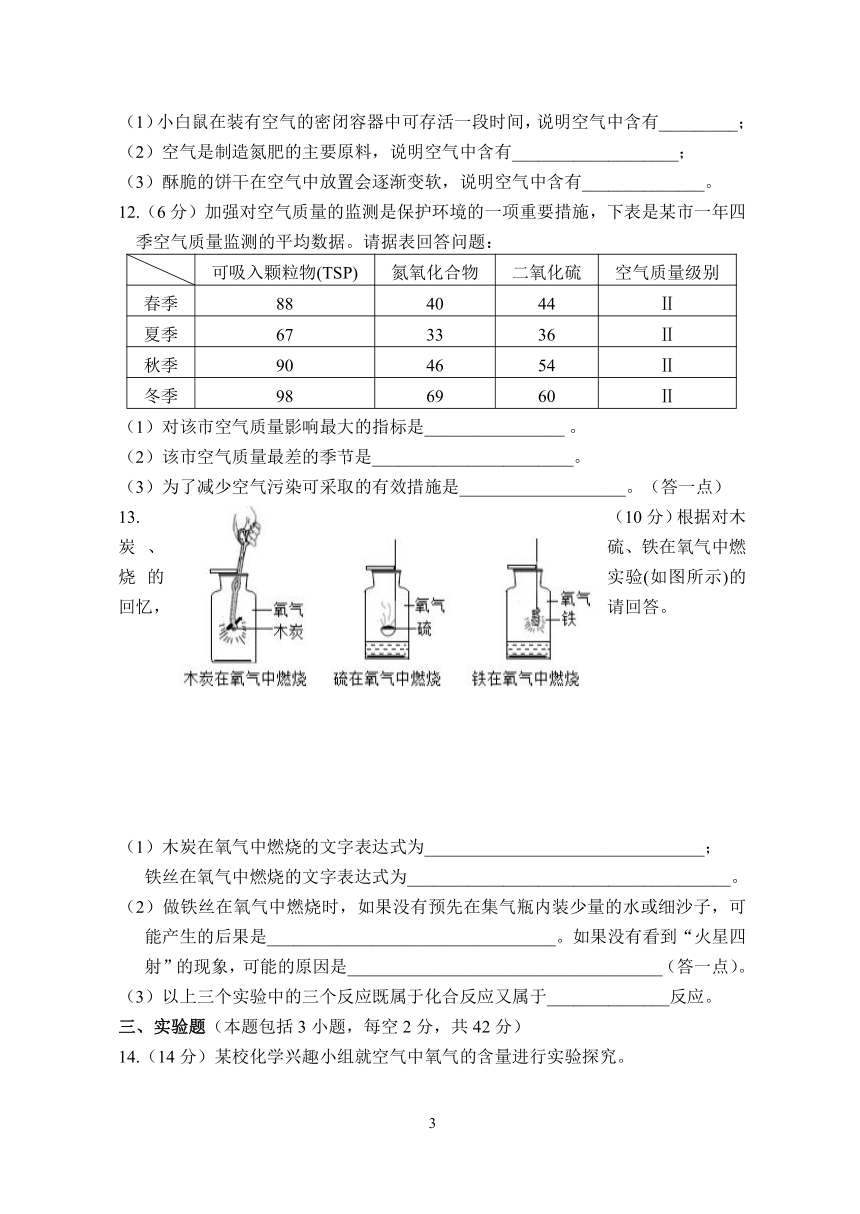
(1)小白鼠在装有空气的密闭容器中可存活一段时间,说明空气中含有_________;
(2)空气是制造氮肥的主要原料,说明空气中含有___________________;
(3)酥脆的饼干在空气中放置会逐渐变软,说明空气中含有______________。
12.(6分)加强对空气质量的监测是保护环境的一项重要措施,下表是某市一年四季空气质量监测的平均数据。请据表回答问题:
可吸入颗粒物(TSP) 氮氧化合物 二氧化硫 空气质量级别
春季 88 40 44 Ⅱ
夏季 67 33 36 Ⅱ
秋季 90 46 54 Ⅱ
冬季 98 69 60 Ⅱ
(1)对该市空气质量影响最大的指标是________________ 。
(2)该市空气质量最差的季节是_______________________。
(3)为了减少空气污染可采取的有效措施是___________________。(答一点)
13.(10分)根据对木炭、硫、铁在氧气中燃烧的实验(如图所示)的回忆,请回答。
(1)木炭在氧气中燃烧的文字表达式为________________________________;
铁丝在氧气中燃烧的文字表达式为_____________________________________。
(2)做铁丝在氧气中燃烧时,如果没有预先在集气瓶内装少量的水或细沙子,可能产生的后果是_________________________________。如果没有看到“火星四射”的现象,可能的原因是____________________________________(答一点)。
(3)以上三个实验中的三个反应既属于化合反应又属于______________反应。
三、实验题(本题包括3小题,每空2分,共42分)
14.(14分)某校化学兴趣小组就空气中氧气的含量进行实验探究。8
【小组讨论】(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体。他们应该选择(填序号)____________,为了充分消耗容器中的氧气,药品的用量应保证________________。
A.蜡烛 B.红磷 C.硫粉 D.木炭
(2)小组同学共同设计了下图的两套装置,你认为合理的是(填序号)________。为了确保实验成功,在装药品之前应该__________________________________。
【分组实验】在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100mL)
组别 1 2 3 4 5 6
进入集气瓶中水的体积(mL) 20 21 19 20 22 18
通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的____________。通过实验还可以推断集气瓶中剩余气体的物理性质是________________________,化学性质是______________________________________。
(18分)下图是实验室制取、收集有关气体的装置图,按要求回答下列问题。
(1)请写出图中标号仪器的名称:①________________;②________________。
(2)在实验室中常用过氧化氢溶液和二氧化锰混合制取氧气,写出该反应的表达式__________________________________,如需随时控制产生气体的量并节约药品,发生装置最好选用__________________(填编号)。
(3)制取一瓶纯净的氧气,应选用的收集装置为__________,检验该装置氧气是否收集满的方法是_____________________ __________________。
(4)如果用H装置收集氧气,预先装满水,气体应从____________(填“a”或8
“b”)进入。
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,其水溶液呈碱性。制取并收集氨气,应该从上图中选择的发生装置是______,收集装置是_______。
16.(10分)研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探险究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与催化剂的种类有关。
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量的MnO2和红砖粉,测量各收集一瓶(相同体积)O2所需要的时间。
【实验记录】
实验编号 1 2
反应物 6% H2O2 6% H2O2
催化剂 1g红砖粉 1g MnO2
时间 152s 35s
【结论】该探究过程得出的结论是______________________________________。
【反思】H2O2在常温下分角缓慢,别入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验证明它们在化学反应前后的_____________和__________________是否改变。
H2O2生成O2的快慢还与哪些因素有关?请你帮助他们继续探究。(只要求提出假设和实验方案)
【假设】______________________________________________________。
【实验方案】_________________________________________________________
_____________________________________________________________________。
四、计算题(本题共6分)
17.(6分)过氧乙酸在医药中常用作杀菌剂,也可用于食品的消毒。某市售过氧乙酸,其标签上的部分文字说明如图。请计算:
(1)过氧乙酸的化学式量__________________。
(2)过氧乙酸中碳元素、氢元素和氧元素的质量比_________________________(填最简整数比)。
(3)7.6g过氧乙酸中含有氧元素的质量是多少?
8
第四单元《我们周围的空气》质量监测试题
参考答案
一、选择题
1.C 2.A 3.B 4.A 5.B 6.B 7.C 8.C 9.D 10.D
二、填空题
11.(1)氧气 (2)氮气 (3)水蒸气
12.(1)可吸入颗粒物(TSP) (2)冬季
(3)使用清洁能源(合理即可)
点燃 点燃
(1)碳+氧气———→二氧化碳 铁+氧气———→四氧化三铁
(2)炸裂集气瓶底
铁丝没有打磨(或没有系上火柴头、没有绕成螺旋状、氧气不纯等)
(3)氧化
三、实验题
14.【小组讨论】(1)B 足量 (2)A 检查装置的气密性
【数据分析】1/5 难溶于水 不燃烧,不支持燃烧
15.(1)① 长颈漏斗 ② 试管
MnO2
(2)H2O2———→H2O+O2 B
(3)F 气泡从瓶口外冒出 (4)b (5)D G
16. 【结论】在相同条件下,H2O2生成O2的快慢与催化剂种类有关
【反思】质量 化学性质
【假设】过氧化氢溶液的浓度或温度等
【实验方案】在同温下,取二份质量相等的不同浓度的H2O2溶液,8
分别加入质量相等的同种催化剂,测量各收集一瓶(相同体积)气体所需的时间。
四、计算题
17.(1)76 (2)6:1:12 (3)4.8g
8
( 时间45分钟, 分值100分)
班级______________ 姓名______________ 成绩______________
可能用到的相对原子质量:C 12 H 1 O 16
一、选择题(本题包括10小题,每小题3分,共30分。请将正确答案的序号填写在下表相应空格内)
题号 1 2 3 4 5 6 7 8 9 10
答案
1.宁阳县某学校研究性学习活动小组的学生利用课余时间调查雾霾产生的原因,并提出可减少雾霾的说法正确的是
A.鼓励开私家车出行 B.鼓励燃煤火力发电
C.鼓动使用太阳能热水器 D.鼓励露天焚烧垃圾
2.空气是一种宝贵的自然资源。下列有关说法不正确的是
A.把空气中的其他成分分离出去,只留下氧气会更有益于生命活动
B.分离液态空气制取氧气属于物理变化
C.空气中的氮气常用作保护气
D.稀有气体都没有颜色、没有气味,在通电时能发出不同颜色的光
3.下列选项不属于氧气在大自然中消耗途径的是
A.生物的呼吸作用 B.绿色植物的光合作用
C.物质在空气中的燃烧 D.物质在空气中的缓慢氧化
4.下列有关氧气性质的叙述中,正确的是
A.氧气的密度比空气的略大
B.氧气极易溶于水
C.氧气是一种化学性质很活泼的气体,能与所有物质发生反应
D.氧气具有可燃性,是一种常用的燃料
5.用过氧化氢溶液制取氧气时,忘记加二氧化锰,其结果是
A.不放出氧气 B.放出氧气速率慢
C.放出氧气总量会减少 D.放出氧气总量会更多
6.一氧化氮在常温下是一种难溶于水的气体,密度比空气略大;它能跟空气里的氧气迅速反应,生成二氧化氮。先要收集一瓶一氧化氮气体,可采用的方法是8
A.向上排空气法 B.排水法
C.排水法或向上排空气法 D.排水法或向下排空气法
7.潜水艇里需要配备氧气的发生装置,以保证长时间潜航。下列反应都能产生氧气,其中最适宜在潜水艇里供给氧气的反应是
A. 水 氢气 十 氧气
B.高锰酸钾 锰酸钾 十 二氧化锰 十 氧气
C.过氧化钠 十 二氧化碳 碳酸钠 十 氧气
D.过氧化氢 水 十 氧气
8.下列实验现象中,描述正确的是
A.木炭在氧气中燃烧,生成黑色固体
B.红磷在空气中燃烧,产生白雾
C.镁条在空气中剧烈反应,发出耀眼的强光,生成白色固体
D.铁丝在空气中剧烈燃烧,放出大量的热,火星四射,有黑色熔化物溅落瓶底
9.图中“”和“”表示两种不同元素的原子,下列方框中可能表示氧化物
的是
10.右图所示装置,有洗气、储气等用途。医院给病人输氧气时,也利用了类似的装置。以下说法不正确的是
A.该装置可用来观察是否有氧气输出
B.该装置可用来观察输出氧气的速度
C.B导管连接病人吸氧导气管
D.B导管连接供氧钢瓶
二、填空题 (本题包括3小题,每空2分,共22分)
11.(6分)下列事实说明空气中含有哪些成分?
8
(1)小白鼠在装有空气的密闭容器中可存活一段时间,说明空气中含有_________;
(2)空气是制造氮肥的主要原料,说明空气中含有___________________;
(3)酥脆的饼干在空气中放置会逐渐变软,说明空气中含有______________。
12.(6分)加强对空气质量的监测是保护环境的一项重要措施,下表是某市一年四季空气质量监测的平均数据。请据表回答问题:
可吸入颗粒物(TSP) 氮氧化合物 二氧化硫 空气质量级别
春季 88 40 44 Ⅱ
夏季 67 33 36 Ⅱ
秋季 90 46 54 Ⅱ
冬季 98 69 60 Ⅱ
(1)对该市空气质量影响最大的指标是________________ 。
(2)该市空气质量最差的季节是_______________________。
(3)为了减少空气污染可采取的有效措施是___________________。(答一点)
13.(10分)根据对木炭、硫、铁在氧气中燃烧的实验(如图所示)的回忆,请回答。
(1)木炭在氧气中燃烧的文字表达式为________________________________;
铁丝在氧气中燃烧的文字表达式为_____________________________________。
(2)做铁丝在氧气中燃烧时,如果没有预先在集气瓶内装少量的水或细沙子,可能产生的后果是_________________________________。如果没有看到“火星四射”的现象,可能的原因是____________________________________(答一点)。
(3)以上三个实验中的三个反应既属于化合反应又属于______________反应。
三、实验题(本题包括3小题,每空2分,共42分)
14.(14分)某校化学兴趣小组就空气中氧气的含量进行实验探究。8
【小组讨论】(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体。他们应该选择(填序号)____________,为了充分消耗容器中的氧气,药品的用量应保证________________。
A.蜡烛 B.红磷 C.硫粉 D.木炭
(2)小组同学共同设计了下图的两套装置,你认为合理的是(填序号)________。为了确保实验成功,在装药品之前应该__________________________________。
【分组实验】在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100mL)
组别 1 2 3 4 5 6
进入集气瓶中水的体积(mL) 20 21 19 20 22 18
通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的____________。通过实验还可以推断集气瓶中剩余气体的物理性质是________________________,化学性质是______________________________________。
(18分)下图是实验室制取、收集有关气体的装置图,按要求回答下列问题。
(1)请写出图中标号仪器的名称:①________________;②________________。
(2)在实验室中常用过氧化氢溶液和二氧化锰混合制取氧气,写出该反应的表达式__________________________________,如需随时控制产生气体的量并节约药品,发生装置最好选用__________________(填编号)。
(3)制取一瓶纯净的氧气,应选用的收集装置为__________,检验该装置氧气是否收集满的方法是_____________________ __________________。
(4)如果用H装置收集氧气,预先装满水,气体应从____________(填“a”或8
“b”)进入。
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,其水溶液呈碱性。制取并收集氨气,应该从上图中选择的发生装置是______,收集装置是_______。
16.(10分)研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探险究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与催化剂的种类有关。
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量的MnO2和红砖粉,测量各收集一瓶(相同体积)O2所需要的时间。
【实验记录】
实验编号 1 2
反应物 6% H2O2 6% H2O2
催化剂 1g红砖粉 1g MnO2
时间 152s 35s
【结论】该探究过程得出的结论是______________________________________。
【反思】H2O2在常温下分角缓慢,别入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验证明它们在化学反应前后的_____________和__________________是否改变。
H2O2生成O2的快慢还与哪些因素有关?请你帮助他们继续探究。(只要求提出假设和实验方案)
【假设】______________________________________________________。
【实验方案】_________________________________________________________
_____________________________________________________________________。
四、计算题(本题共6分)
17.(6分)过氧乙酸在医药中常用作杀菌剂,也可用于食品的消毒。某市售过氧乙酸,其标签上的部分文字说明如图。请计算:
(1)过氧乙酸的化学式量__________________。
(2)过氧乙酸中碳元素、氢元素和氧元素的质量比_________________________(填最简整数比)。
(3)7.6g过氧乙酸中含有氧元素的质量是多少?
8
第四单元《我们周围的空气》质量监测试题
参考答案
一、选择题
1.C 2.A 3.B 4.A 5.B 6.B 7.C 8.C 9.D 10.D
二、填空题
11.(1)氧气 (2)氮气 (3)水蒸气
12.(1)可吸入颗粒物(TSP) (2)冬季
(3)使用清洁能源(合理即可)
点燃 点燃
(1)碳+氧气———→二氧化碳 铁+氧气———→四氧化三铁
(2)炸裂集气瓶底
铁丝没有打磨(或没有系上火柴头、没有绕成螺旋状、氧气不纯等)
(3)氧化
三、实验题
14.【小组讨论】(1)B 足量 (2)A 检查装置的气密性
【数据分析】1/5 难溶于水 不燃烧,不支持燃烧
15.(1)① 长颈漏斗 ② 试管
MnO2
(2)H2O2———→H2O+O2 B
(3)F 气泡从瓶口外冒出 (4)b (5)D G
16. 【结论】在相同条件下,H2O2生成O2的快慢与催化剂种类有关
【反思】质量 化学性质
【假设】过氧化氢溶液的浓度或温度等
【实验方案】在同温下,取二份质量相等的不同浓度的H2O2溶液,8
分别加入质量相等的同种催化剂,测量各收集一瓶(相同体积)气体所需的时间。
四、计算题
17.(1)76 (2)6:1:12 (3)4.8g
8
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
