人教版化学九上第5章化学方程式复习课件
文档属性
| 名称 | 人教版化学九上第5章化学方程式复习课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 286.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-12-04 00:00:00 | ||
图片预览










文档简介
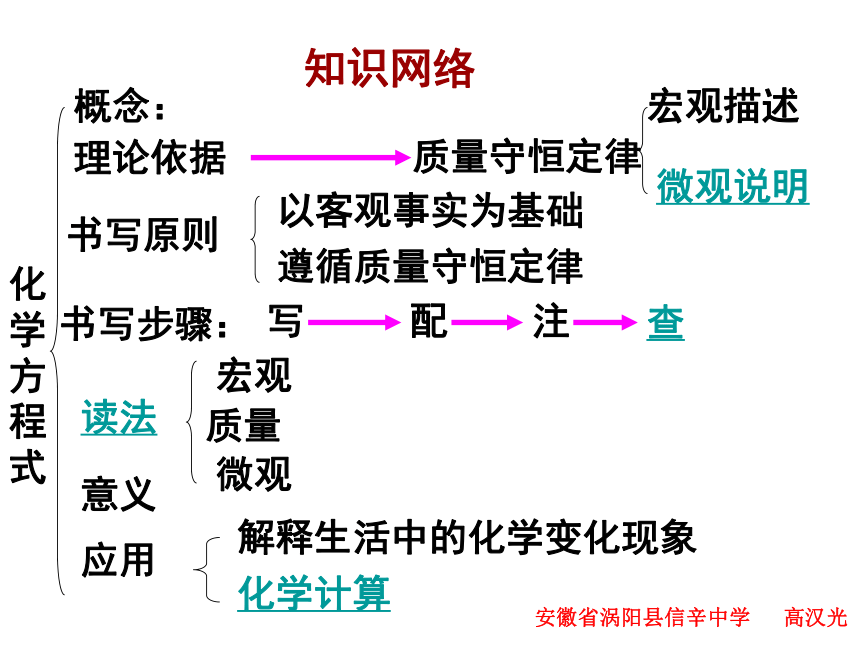
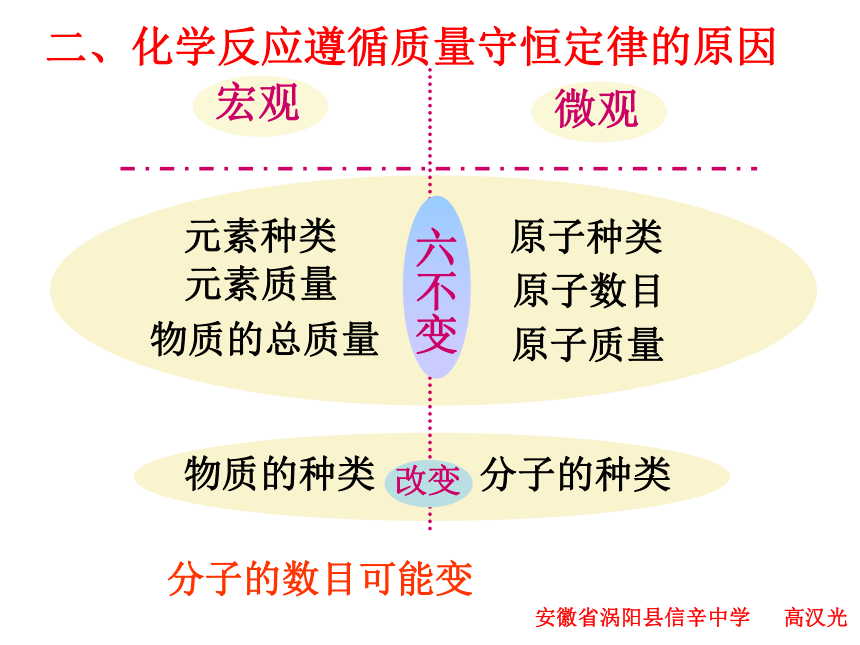
课件30张PPT。知识网络化学方程式写 安徽省涡阳县信辛中学 高汉光 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和一、质量守恒定律 安徽省涡阳县信辛中学 高汉光原子数目原子质量原子种类物质的总质量元素质量元素种类物质的种类分子的种类分子的数目可能变二、化学反应遵循质量守恒定律的原因 安徽省涡阳县信辛中学 高汉光1、氢气在氯中燃烧,下列说法符合质量守恒定律的是( )
A:2克H2和7克O2反应生成9克H2O
B:1克H2和8克O2反应生成9克H2O
C:4克H2和5克O2反应生成9克H2O
D:5克H2和4克O2反应生成9克H2O2、在A+B=C+2D的反应中,9.8克A和8克B完全反应生成
14.2克C,同时得到D的质量是( )
A:1.8克 B:3.6克 C:7.2克 D:14.4克3、某反应A+B=2C+D,已知3克A和5克B恰好完全反应,
生成2克C,若生成D的质量为9克,则参加反应的B的质量
为( )
A:1.1克 B:7.5克 C:1.5克 D:1.75克BBB练习 安徽省涡阳县信辛中学 高汉光4、由元素X,Y组成的两种物质经化合生成Z,化学方程式
为:3X2+2YX=2Z,则Z的化学式是( )
A:X3Y2 B:XY C:X4Y D:YX25、2.8克某有机物充分燃烧,生成8.8克CO2和3.6克H2O,
则有关该有机物的组成的说法正确的是( )
A:一定含有碳、氢、氧三种元素
B:一定含有碳、氢两种元素,可能含有氧元素
C:一定含有碳、氢两种元素,不含有氧元素
D:无法确定CC练习 安徽省涡阳县信辛中学 高汉光 简答题:
法轮功邪教组织的头目李洪志说,他发功能使铝发生化学反应,变成铜和金,使铝分子变成铜分子和金分子,请你根据所学化学知识,指出这种说法违反科学之处。答案:两个要点: (1)金属不是由分子而是由原了构成的;(2)化学变化中元素的种类不变。练习 安徽省涡阳县信辛中学 高汉光三、书写化学方程式要遵守两个原则:必须遵守质量守恒定律必须以客观事实为基础 安徽省涡阳县信辛中学 高汉光四、书写化学方程式的步骤(1)写根据实验事实,在式子两边写出反应物和生成物的化学式,并在两边之间画一条短线
(2)配配平化学方程式,将短线改为等号
(3)标标明化学反应发生的条件,短线改成等号。
安徽省涡阳县信辛中学 高汉光五、化学方程式的涵义(提供的信息)a. 哪些物质参加了反应(反应物)
b .生成了哪些物质(生成物)
c .反应条件
d .反应物与生成物之间的粒子数量比
e. 反应物与生成物之间的质量比
安徽省涡阳县信辛中学 高汉光
配平时,首先找出反应式左、右两边各出现一次,且原子个数即不相等,又相差较多的元素,求出最小公倍数。如:P+ O2—P2 O5中 ,O2和P2 O5中的O最小公倍数为2×5=10,用最小公倍数分别除以含有该元素的化学式中的原子个数,其商就是该化学式的化学计量数。如:P2 O5中有5个O原子,P2 O5的系数为10/5=2;O2中有2个O原子, O2的系数为10/2=5。 2.最小公倍数法:六、化学方程式的配平1.观察法 安徽省涡阳县信辛中学 高汉光化学方程式的读法是从左到右,先读反应物,后读生成物。如反应物和生成物不止一种,反应物之间的“+”号读作“跟”、“与”或“和”,生成物之间的“+”读作“和”,“=”读作“生成”。如反应是在一定的条件下发生的,还应读出反应条件。
例如:S+O2 SO2
①? 质的方面:硫与氧气在点燃的条件下生成二氧化硫。
②? 量的方面:每32份质量的硫跟32份质量的氧气完全反应生成64份质量的二氧化硫。
③粒子方面:每1个硫原子与1个氧分子反应生成1个二氧化硫分子。
七、化学方程式的读法八、根据化学方程式计算各物质的质量比各物质的质量比等于化学方程式中每种物质的相对分子质量乘以化学计量数的比2H2O 2 H2 + O218×2 : 2×2 : 3236: : 4 : 32 KClO3 KCl + O2232MnO2△122.5×2 :74.5×2 :32×3 245 : 149 :96
安徽省涡阳县信辛中学 高汉光 完成下列化学方程式的书写:①、加热氯酸钾与二氧化锰的混合物: .
②、加热高锰酸钾: .
③、锌与稀H2SO4制H2: .
④、氢氧化钠溶液与二氧化硫的反应:
.Zn+H2SO4=ZnSO4+H2↑2NaOH+SO2=Na2SO3+H2O 练习 安徽省涡阳县信辛中学 高汉光 点燃
(1)2Mg+O2===2MgO
点燃
(2)S+O2 ====SO2
点燃
(3)C+O2====CO2
点燃
(4)2C+O2=====2CO
高温
(5)CO2+C=====2CO
点燃
(6)4P+5O2====2P2O5 点燃
(7)3Fe+2O2=====Fe3O4
点燃
(8)2H2+O2====2H2O
点燃
(9)2CO+O2=====2CO2
(10)CO2+H2O==H2CO3
常见的化学方程式1、化合反应 安徽省涡阳县信辛中学 高汉光 MnO2
2KClO3=====2KCl+3O2↑
△
△
2KMnO4===K2MnO4+MnO2+O2↑
MnO2
2H2O2====2H2O+O2↑
通电
2H2O====2H2↑+O2↑
?
H2CO3===H2O+CO2↑
2、分解反应 安徽省涡阳县信辛中学 高汉光Zn+H2SO4==ZnSO4+H2↑
Mg+H2SO4==MgSO4+H2↑
Fe+H2SO4 ==FeSO4+H2↑
2Al+3H2SO4 ==Al2(SO4)3+3H2↑
Zn+2HCl==ZnCl2+H2↑
Mg+2HCl==MgCl2+H2↑
Fe+2HCl==FeCl2+H2↑
2Al+6HCl==2AlCl3+3H2
高温
C+2CuO=====2Cu+CO2↑
Fe+CuSO4==FeSO4+Cu
CuSO4+Zn==ZnSO4+Cu
Hg(NO3)2+Cu==Cu(NO3)2+Hg3、置换反应 安徽省涡阳县信辛中学 高汉光 加热
CuO+CO====Cu+CO2
高温
Fe2O3+3CO====2Fe+3CO2
Fe3O4+4CO====3Fe+4CO2
CaCO3+2HCl==CaCl2+H2O+CO2↑
Na2CO3+2HCl==2NaCl+H2O+CO2↑ Ca(OH)2+CO2===CaCO3↓+H2O
2NaOH+CO2==Na2CO3+H2O
点燃
CH4+2O2=====CO2+2H2O
点燃
C2H5OH+3O2=====2CO2+3H2O
4、其它反应碳、硫、磷、铝、铁、镁、氢气与氧气反应 4、 Al + O2 Al2O3 1. C + O2 CO2
2. S + O2 SO23. P + O2 P2O5 5. Fe + O2 Fe3O46. Mg + O2 MgO7. H2 + O2 H2O524324322222点燃点燃点燃点燃点燃点燃点燃 安徽省涡阳县信辛中学 高汉光8. H2O2 H2O + O2
9. KClO3 KCl + O2
10. KMnO4 K2MnO4 +MnO2 + O2
实验室制取氧气电解水: 11. H2O H2 + O2
22232222MnO2△△通电MnO2 安徽省涡阳县信辛中学 高汉光1.设未知量(求什么就设什么,将所求的问题一次设出)
2.写出化学方程式并配平(计算中所用到的化学方程式)
3.写出有关物质的相对分子质量和已知量、未知量(只写与已知和所求有关的物质,上写相对分子质量,下写物质的质量,已知的带单位)
4.列出比例式、求解(列正比例式,上下同种量,左右同一物质)
5.简明地写出答案
九、根据化学方程式计算的步骤 安徽省涡阳县信辛中学 高汉光练习1:高温煅烧含杂质10%的石灰石(主要成分为CaCO3)100吨,可得生石灰( CaO)多少吨? 我会计算:练习2:在一密闭容器内有A、B、C三种物质,在一定条件下充分反应,测得反应前后各物质质量如下:(1)表中m= 。
(2)该反应中各物质的质量比为 。
(3)若已知A、B、C的相对分子质量分别为:28、32、44,则该反应中A、B、C的化学计量数之比为 。
(4)用A、B、C表示这三种物质的化学式,试写出该反应的化学方程式 。该反应属于 反应。60+32+12=m+0+100m-56-32+8856g 32g 88g28 32 444A:B:C=7:4:112:1:22A+B=2C化合例3:4g氧气可与多少g氢气完全反应?同时生成水多少g?解:设4g氧气可与质量为X的氢气完全反应,同时生成水的质量 为Y2H2+ O2 2 H2O点燃4 32 36X 4g Y 4
32X
4gX=4×4g
32=0. 5g32
364g
yY=36 ×4g
32=4.5g答:4g氧气可与0.5g氢气完全反应,同时生成水4.5g。
安徽省涡阳县信辛中学 高汉光例4:150g稀盐酸跟一定量含少量杂质的石灰石恰好完全反应(杂质不溶解,也不参加反应),生成11g二氧化碳。回答下列问题:(1)写出盐酸跟石灰石反应的化学方程式。
(2)求反应后所得的溶液中溶质的质量分数(保留到0.1%)答:(1)2HCl+CaCO3=CaCl2 +H2O + CO2↑ (2)解:设生成11g二氧化碳气体需碳酸钙的质量为x,生成氯化钙的质量为y。∴ x=100*11/44=25 y=111*11/44=27.25150g+25g-11g=164g生成物溶液中溶质的质量分数为:反应后溶液的质量为:27.25/164g*100%=16.9%2HCl+CaCO3= CaCl2 +H2O +CO2↑ 安徽省涡阳县信辛中学 高汉光综合练习一:DC 安徽省涡阳县信辛中学 高汉光综合练习一:5、今有H2和O2的混合气体10克,点燃充分反应后,恢复到室温气体的质量减少了9克,则原混合气体中的成分不可能是( )
A:5克H2和5克O2 B:1克H2和9克O2
C:2克H2和8克O2 D:H2和O2的质量1∶46、在反应2A+3B=2C+3D中,已知2.3克A跟4.8克B恰好完全反应,生成4.4克C,已知D的式量为18,则A的式量为( )
A:46 B:23 C:96 D:43CBA 安徽省涡阳县信辛中学 高汉光综合练习一:7、在化学反应3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O中X的化学式是( )
A:N2O B:NO C:NO2 D:N2O38、天平两端分别放置一个盛有足量稀硫酸的烧杯,把天平调至平衡,现向其中一只烧杯投入5.3克Na2CO3,向另一只烧杯中投入适量的铁片,并使天平最终保持平衡,投入铁片的质量为( )
A:大于5.6克 B:5.3克 C:3.21克 D:3.1克9、天平两端分别放置一个盛有98克10%的稀硫酸的烧杯,把天平调至平衡,现向其中一只烧杯投入13克锌,向另一只烧杯中投入适量的铁片,要使天平平衡最终保持平衡,投入铁片的质量为( )
A:11.2克 B:13克 C:5.6克 D:6.5克BCB 安徽省涡阳县信辛中学 高汉光综合练习一:10、如图所示的杠杆两端分别挂着质量不等的实心铜球和铁球,此时杠杆平衡,将两球分别浸在硫酸铜溶液中,过一段时间,可以看到杠杆( )。(假设反应前后球的体积和溶液的密度不变)
A:向右端下沉
B:向左端下沉
C:保持平衡
D:无法确定答案分析:
铁球一端会发生反应,CuSO4+Fe=Cu+FeSO4,生成的Cu会覆盖在铁球表面,致使铁球的质量增大,而铜球不与CuSO4反应,故质量不变,根据杠杆原理,F1L1=F2L2,只要改变F1或F2平衡均可以打破。A 安徽省涡阳县信辛中学 高汉光 要点:1)认识质量守恒定律,并能说明常见化学反应中的质量关系。3)能正确书写常见的化学方程式。5)能进行化学方程式的简单计算。4)能够掌握化学方程式配平的一般方法和常用技巧6)认识定量研究对化学学科发展的重大作用。2)认识化学变化的基本特征,理解反应现象和本质的联系。 安徽省涡阳县信辛中学 高汉光
A:2克H2和7克O2反应生成9克H2O
B:1克H2和8克O2反应生成9克H2O
C:4克H2和5克O2反应生成9克H2O
D:5克H2和4克O2反应生成9克H2O2、在A+B=C+2D的反应中,9.8克A和8克B完全反应生成
14.2克C,同时得到D的质量是( )
A:1.8克 B:3.6克 C:7.2克 D:14.4克3、某反应A+B=2C+D,已知3克A和5克B恰好完全反应,
生成2克C,若生成D的质量为9克,则参加反应的B的质量
为( )
A:1.1克 B:7.5克 C:1.5克 D:1.75克BBB练习 安徽省涡阳县信辛中学 高汉光4、由元素X,Y组成的两种物质经化合生成Z,化学方程式
为:3X2+2YX=2Z,则Z的化学式是( )
A:X3Y2 B:XY C:X4Y D:YX25、2.8克某有机物充分燃烧,生成8.8克CO2和3.6克H2O,
则有关该有机物的组成的说法正确的是( )
A:一定含有碳、氢、氧三种元素
B:一定含有碳、氢两种元素,可能含有氧元素
C:一定含有碳、氢两种元素,不含有氧元素
D:无法确定CC练习 安徽省涡阳县信辛中学 高汉光 简答题:
法轮功邪教组织的头目李洪志说,他发功能使铝发生化学反应,变成铜和金,使铝分子变成铜分子和金分子,请你根据所学化学知识,指出这种说法违反科学之处。答案:两个要点: (1)金属不是由分子而是由原了构成的;(2)化学变化中元素的种类不变。练习 安徽省涡阳县信辛中学 高汉光三、书写化学方程式要遵守两个原则:必须遵守质量守恒定律必须以客观事实为基础 安徽省涡阳县信辛中学 高汉光四、书写化学方程式的步骤(1)写根据实验事实,在式子两边写出反应物和生成物的化学式,并在两边之间画一条短线
(2)配配平化学方程式,将短线改为等号
(3)标标明化学反应发生的条件,短线改成等号。
安徽省涡阳县信辛中学 高汉光五、化学方程式的涵义(提供的信息)a. 哪些物质参加了反应(反应物)
b .生成了哪些物质(生成物)
c .反应条件
d .反应物与生成物之间的粒子数量比
e. 反应物与生成物之间的质量比
安徽省涡阳县信辛中学 高汉光
配平时,首先找出反应式左、右两边各出现一次,且原子个数即不相等,又相差较多的元素,求出最小公倍数。如:P+ O2—P2 O5中 ,O2和P2 O5中的O最小公倍数为2×5=10,用最小公倍数分别除以含有该元素的化学式中的原子个数,其商就是该化学式的化学计量数。如:P2 O5中有5个O原子,P2 O5的系数为10/5=2;O2中有2个O原子, O2的系数为10/2=5。 2.最小公倍数法:六、化学方程式的配平1.观察法 安徽省涡阳县信辛中学 高汉光化学方程式的读法是从左到右,先读反应物,后读生成物。如反应物和生成物不止一种,反应物之间的“+”号读作“跟”、“与”或“和”,生成物之间的“+”读作“和”,“=”读作“生成”。如反应是在一定的条件下发生的,还应读出反应条件。
例如:S+O2 SO2
①? 质的方面:硫与氧气在点燃的条件下生成二氧化硫。
②? 量的方面:每32份质量的硫跟32份质量的氧气完全反应生成64份质量的二氧化硫。
③粒子方面:每1个硫原子与1个氧分子反应生成1个二氧化硫分子。
七、化学方程式的读法八、根据化学方程式计算各物质的质量比各物质的质量比等于化学方程式中每种物质的相对分子质量乘以化学计量数的比2H2O 2 H2 + O218×2 : 2×2 : 3236: : 4 : 32 KClO3 KCl + O2232MnO2△122.5×2 :74.5×2 :32×3 245 : 149 :96
安徽省涡阳县信辛中学 高汉光 完成下列化学方程式的书写:①、加热氯酸钾与二氧化锰的混合物: .
②、加热高锰酸钾: .
③、锌与稀H2SO4制H2: .
④、氢氧化钠溶液与二氧化硫的反应:
.Zn+H2SO4=ZnSO4+H2↑2NaOH+SO2=Na2SO3+H2O 练习 安徽省涡阳县信辛中学 高汉光 点燃
(1)2Mg+O2===2MgO
点燃
(2)S+O2 ====SO2
点燃
(3)C+O2====CO2
点燃
(4)2C+O2=====2CO
高温
(5)CO2+C=====2CO
点燃
(6)4P+5O2====2P2O5 点燃
(7)3Fe+2O2=====Fe3O4
点燃
(8)2H2+O2====2H2O
点燃
(9)2CO+O2=====2CO2
(10)CO2+H2O==H2CO3
常见的化学方程式1、化合反应 安徽省涡阳县信辛中学 高汉光 MnO2
2KClO3=====2KCl+3O2↑
△
△
2KMnO4===K2MnO4+MnO2+O2↑
MnO2
2H2O2====2H2O+O2↑
通电
2H2O====2H2↑+O2↑
?
H2CO3===H2O+CO2↑
2、分解反应 安徽省涡阳县信辛中学 高汉光Zn+H2SO4==ZnSO4+H2↑
Mg+H2SO4==MgSO4+H2↑
Fe+H2SO4 ==FeSO4+H2↑
2Al+3H2SO4 ==Al2(SO4)3+3H2↑
Zn+2HCl==ZnCl2+H2↑
Mg+2HCl==MgCl2+H2↑
Fe+2HCl==FeCl2+H2↑
2Al+6HCl==2AlCl3+3H2
高温
C+2CuO=====2Cu+CO2↑
Fe+CuSO4==FeSO4+Cu
CuSO4+Zn==ZnSO4+Cu
Hg(NO3)2+Cu==Cu(NO3)2+Hg3、置换反应 安徽省涡阳县信辛中学 高汉光 加热
CuO+CO====Cu+CO2
高温
Fe2O3+3CO====2Fe+3CO2
Fe3O4+4CO====3Fe+4CO2
CaCO3+2HCl==CaCl2+H2O+CO2↑
Na2CO3+2HCl==2NaCl+H2O+CO2↑ Ca(OH)2+CO2===CaCO3↓+H2O
2NaOH+CO2==Na2CO3+H2O
点燃
CH4+2O2=====CO2+2H2O
点燃
C2H5OH+3O2=====2CO2+3H2O
4、其它反应碳、硫、磷、铝、铁、镁、氢气与氧气反应 4、 Al + O2 Al2O3 1. C + O2 CO2
2. S + O2 SO23. P + O2 P2O5 5. Fe + O2 Fe3O46. Mg + O2 MgO7. H2 + O2 H2O524324322222点燃点燃点燃点燃点燃点燃点燃 安徽省涡阳县信辛中学 高汉光8. H2O2 H2O + O2
9. KClO3 KCl + O2
10. KMnO4 K2MnO4 +MnO2 + O2
实验室制取氧气电解水: 11. H2O H2 + O2
22232222MnO2△△通电MnO2 安徽省涡阳县信辛中学 高汉光1.设未知量(求什么就设什么,将所求的问题一次设出)
2.写出化学方程式并配平(计算中所用到的化学方程式)
3.写出有关物质的相对分子质量和已知量、未知量(只写与已知和所求有关的物质,上写相对分子质量,下写物质的质量,已知的带单位)
4.列出比例式、求解(列正比例式,上下同种量,左右同一物质)
5.简明地写出答案
九、根据化学方程式计算的步骤 安徽省涡阳县信辛中学 高汉光练习1:高温煅烧含杂质10%的石灰石(主要成分为CaCO3)100吨,可得生石灰( CaO)多少吨? 我会计算:练习2:在一密闭容器内有A、B、C三种物质,在一定条件下充分反应,测得反应前后各物质质量如下:(1)表中m= 。
(2)该反应中各物质的质量比为 。
(3)若已知A、B、C的相对分子质量分别为:28、32、44,则该反应中A、B、C的化学计量数之比为 。
(4)用A、B、C表示这三种物质的化学式,试写出该反应的化学方程式 。该反应属于 反应。60+32+12=m+0+100m-56-32+8856g 32g 88g28 32 444A:B:C=7:4:112:1:22A+B=2C化合例3:4g氧气可与多少g氢气完全反应?同时生成水多少g?解:设4g氧气可与质量为X的氢气完全反应,同时生成水的质量 为Y2H2+ O2 2 H2O点燃4 32 36X 4g Y 4
32X
4gX=4×4g
32=0. 5g32
364g
yY=36 ×4g
32=4.5g答:4g氧气可与0.5g氢气完全反应,同时生成水4.5g。
安徽省涡阳县信辛中学 高汉光例4:150g稀盐酸跟一定量含少量杂质的石灰石恰好完全反应(杂质不溶解,也不参加反应),生成11g二氧化碳。回答下列问题:(1)写出盐酸跟石灰石反应的化学方程式。
(2)求反应后所得的溶液中溶质的质量分数(保留到0.1%)答:(1)2HCl+CaCO3=CaCl2 +H2O + CO2↑ (2)解:设生成11g二氧化碳气体需碳酸钙的质量为x,生成氯化钙的质量为y。∴ x=100*11/44=25 y=111*11/44=27.25150g+25g-11g=164g生成物溶液中溶质的质量分数为:反应后溶液的质量为:27.25/164g*100%=16.9%2HCl+CaCO3= CaCl2 +H2O +CO2↑ 安徽省涡阳县信辛中学 高汉光综合练习一:DC 安徽省涡阳县信辛中学 高汉光综合练习一:5、今有H2和O2的混合气体10克,点燃充分反应后,恢复到室温气体的质量减少了9克,则原混合气体中的成分不可能是( )
A:5克H2和5克O2 B:1克H2和9克O2
C:2克H2和8克O2 D:H2和O2的质量1∶46、在反应2A+3B=2C+3D中,已知2.3克A跟4.8克B恰好完全反应,生成4.4克C,已知D的式量为18,则A的式量为( )
A:46 B:23 C:96 D:43CBA 安徽省涡阳县信辛中学 高汉光综合练习一:7、在化学反应3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O中X的化学式是( )
A:N2O B:NO C:NO2 D:N2O38、天平两端分别放置一个盛有足量稀硫酸的烧杯,把天平调至平衡,现向其中一只烧杯投入5.3克Na2CO3,向另一只烧杯中投入适量的铁片,并使天平最终保持平衡,投入铁片的质量为( )
A:大于5.6克 B:5.3克 C:3.21克 D:3.1克9、天平两端分别放置一个盛有98克10%的稀硫酸的烧杯,把天平调至平衡,现向其中一只烧杯投入13克锌,向另一只烧杯中投入适量的铁片,要使天平平衡最终保持平衡,投入铁片的质量为( )
A:11.2克 B:13克 C:5.6克 D:6.5克BCB 安徽省涡阳县信辛中学 高汉光综合练习一:10、如图所示的杠杆两端分别挂着质量不等的实心铜球和铁球,此时杠杆平衡,将两球分别浸在硫酸铜溶液中,过一段时间,可以看到杠杆( )。(假设反应前后球的体积和溶液的密度不变)
A:向右端下沉
B:向左端下沉
C:保持平衡
D:无法确定答案分析:
铁球一端会发生反应,CuSO4+Fe=Cu+FeSO4,生成的Cu会覆盖在铁球表面,致使铁球的质量增大,而铜球不与CuSO4反应,故质量不变,根据杠杆原理,F1L1=F2L2,只要改变F1或F2平衡均可以打破。A 安徽省涡阳县信辛中学 高汉光 要点:1)认识质量守恒定律,并能说明常见化学反应中的质量关系。3)能正确书写常见的化学方程式。5)能进行化学方程式的简单计算。4)能够掌握化学方程式配平的一般方法和常用技巧6)认识定量研究对化学学科发展的重大作用。2)认识化学变化的基本特征,理解反应现象和本质的联系。 安徽省涡阳县信辛中学 高汉光
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
