第十单元课题1常见的酸和碱第2课时常见的碱-2021-2022学年九年级化学人教版下册(99张PPT)
文档属性
| 名称 | 第十单元课题1常见的酸和碱第2课时常见的碱-2021-2022学年九年级化学人教版下册(99张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-20 00:00:00 | ||
图片预览








文档简介
常见的酸和碱
第二课时 常见的碱
CONTENTS
01
常见的碱
02
碱的化学性质
内容提要
03
溶液的导电性
认识几种常见碱的主要性质和用途
能够设计实验验证溶液的导电性
会用酸碱指示剂检验溶液的酸碱性
目标一
目标三
目标二
学习目标
人类社会除了需要酸,同样也离不开碱,你知道哪些碱?
它们在生产生活中有哪些应用?
新课引入
你知道生活中哪些物质含有碱吗?
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等。
“尝起来涩涩的”
“摸起来滑滑的”
新课导入
PART 1
01 常见的碱
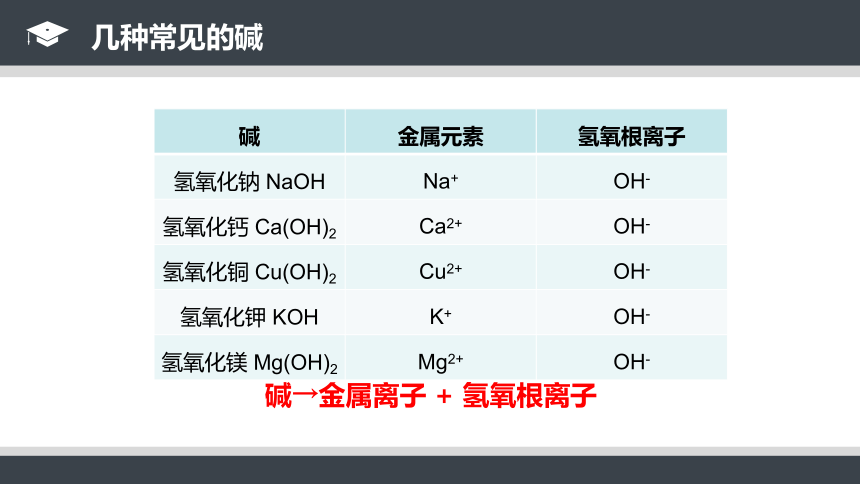
几种常见的碱
常见的碱:氢氧化钠(NaOH)、氢氧化钙[Ca(OH)2]、氢氧化钾(KOH)、氢氧化铜[Cu(OH)2] 、氨水(NH3.H2O)等。
观察这几种碱,从名称和组成上看你能发现什么?
碱→金属离子 + 氢氧根离子
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}碱
金属元素
氢氧根离子
氢氧化钠 NaOH
Na+
OH-
氢氧化钙 Ca(OH)2
Ca2+
OH-
氢氧化铜 Cu(OH)2
Cu2+
OH-
氢氧化钾 KOH
K+
OH-
氢氧化镁 Mg(OH)2
Mg2+
OH-
几种常见的碱
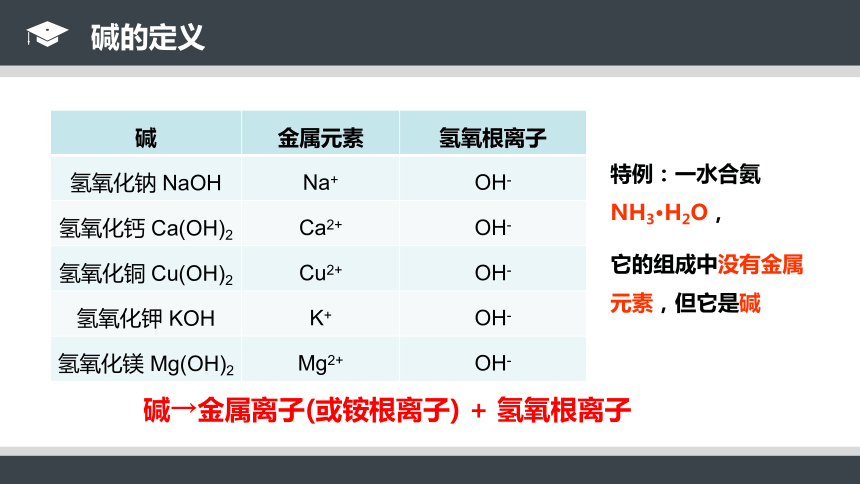
碱→金属离子(或铵根离子) + 氢氧根离子
特例:一水合氨NH3·H2O,
它的组成中没有金属元素,但它是碱
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}碱
金属元素
氢氧根离子
氢氧化钠 NaOH
Na+
OH-
氢氧化钙 Ca(OH)2
Ca2+
OH-
氢氧化铜 Cu(OH)2
Cu2+
OH-
氢氧化钾 KOH
K+
OH-
氢氧化镁 Mg(OH)2
Mg2+
OH-
碱的定义
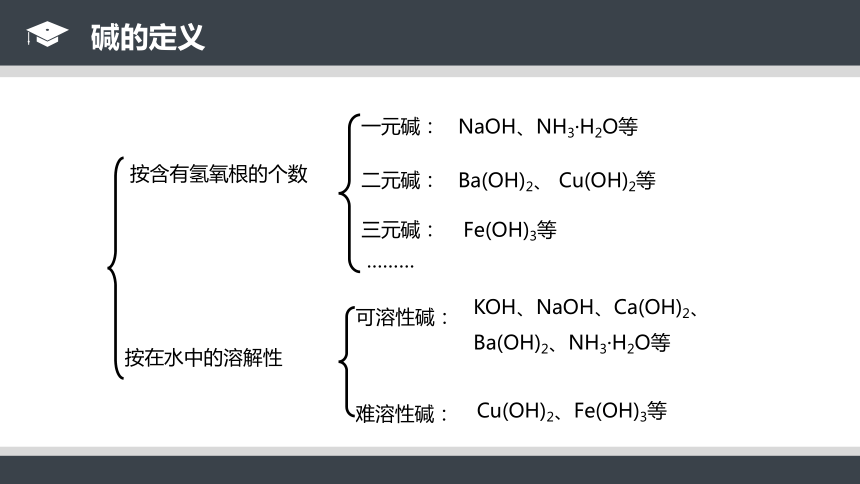
按含有氢氧根的个数
按在水中的溶解性
可溶性碱:
KOH、NaOH、Ca(OH)2、Ba(OH)2、NH3·H2O等
难溶性碱:
Cu(OH)2、Fe(OH)3等
一元碱:
NaOH、NH3·H2O等
二元碱:
Ba(OH)2、 Cu(OH)2等
三元碱:
Fe(OH)3等
………
碱的定义
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
根据在水中的溶解性
根据含有氢氧根的个数
可溶性碱
难溶性碱
一元碱
二元碱
三元碱
NaOH
Cu(OH)2
Ca(OH)2
NH3·H2O
Fe(OH)3
碱的分类
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
根据在水中的溶解性
根据含有氢氧根的个数
可溶性碱
难溶性碱
一元碱
二元碱
三元碱
NaOH
√
Cu(OH)2
√
Ca(OH)2
√
NH3·H2O
√
Fe(OH)3
√
碱的分类
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
根据在水中的溶解性
根据含有氢氧根的个数
可溶性碱
难溶性碱
一元碱
二元碱
三元碱
NaOH
√
√
Cu(OH)2
√
√
Ca(OH)2
√
√
NH3·H2O
√
√
Fe(OH)3
√
√
碱的分类
认识常见的碱
氢氧化钠
氢氧化钙
实验: 认识常见的碱
氢氧化钠(NaOH)
颜色、状态:白色固体
俗名:苛性钠、火碱、烧碱
溶解性:易溶于水,溶解时放出大量的热
吸水性:易吸水潮解
用途:广泛用于制取肥皂,以及石油、造纸、纺织等工业;生活中
用来去除油污;实验室可用作某些气体的干燥剂。
与油脂反应
汽油→溶解,洗涤剂→乳化
氢氧化钠
1.氢氧化钠曝露在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫潮解。
2.氢氧化钠有强烈的腐蚀性,使用时必须十分小心,防止眼睛、皮肤、衣服等被腐蚀。实验时最好戴防护眼镜。
物理变化
拓展提升
氢氧化钙[Ca(OH)2]
颜色、状态:白色粉末状固体
俗名:熟石灰、消石灰
溶解性:微溶于水,溶解度随温度升高而减小
吸水性:不易吸水
用途:建筑上用熟石灰和沙子混合来砌砖,用石灰浆粉刷墙壁;涂刷含硫磺粉等的石灰浆,可保护树木;可用石灰乳和硫酸铜等配制农药波尔多液,熟石灰还可用来改良酸性土壤;实验室中用澄清石灰水检验二氧化碳。
氢氧化钙
氢氧化钙微溶于水,其水溶液俗称石灰水,当石灰水中存在较多未溶解的氢氧化钙时,就称为石灰乳或石灰浆。
氢氧化钙
氢氧化钙的制取:
CaO + H2O == Ca(OH)2
hhh,说到氢氧化钙,我还要偷偷告诉大家个小知识!!!
竖起耳朵听!!!
从化学角度解释《石灰吟》
“千锤万凿出深山”
“烈火焚烧若等闲”
“粉身碎骨全不怕”
“要留清白在人间”
小知识
从化学角度解释《石灰吟》
“千锤万凿出深山” 此过程是物理变化
“烈火焚烧若等闲”
CaCO3 ?CaO + CO2↑
?
“粉骨碎身浑不怕”
CaO + H2O == Ca(OH)2
“要留清白在人间”
Ca(OH)2+CO2=CaCO3↓+H2O
?
小知识
1.氢氧化钠易潮解,且易与空气中的CO2发生反应而变质,必须密封保存。
2.保存氢氧化钠溶液的试剂瓶要用橡胶塞,不能用玻璃塞。(玻璃中含有二氧化硅,能与碱反应)。
3.氢氧化钠固体通常用来干燥O2、H2、O2、 CH4、 NH3等碱性或中性气体,但不能干燥CO2、SO2、HCl等酸性气体。
4. CaO俗称生石灰,具有吸水性,生石灰固体常用作干燥剂,检验CO2时常用Ca(OH)2溶液。
拓展提升
除了NaOH、Ca(OH)2外,
常见的碱还有氢氧化钾(KOH)、氨水(NH3.H2O)
其他的碱
1.下列关于氢氧化钠和氢氧化钙的性质和用途说法不正确的是( )
A.氢氧化钠是一种白色固体,溶于水时放出热量
B.氢氧化钙是白色粉末状固体,微溶于水
C.氢氧化钙可用作某些气体的干燥剂
D.氢氧化钠易潮解,可作某些气体的干燥剂
课堂达标
2.(2019·滨州中考)下列物质露置在空气中一段时间后,因发生化学变化而质量增加的是( )
A. 浓硫酸 B. 浓盐酸 C. 氢氧化钠 D. 石灰石
1.下列关于氢氧化钠和氢氧化钙的性质和用途说法不正确的是( )
C
A.氢氧化钠是一种白色固体,溶于水时放出热量
B.氢氧化钙是白色粉末状固体,微溶于水
C.氢氧化钙可用作某些气体的干燥剂
D.氢氧化钠易潮解,可作某些气体的干燥剂
不能吸收水分,不可作干燥剂
课堂达标
2.(2019·滨州中考)下列物质露置在空气中一段时间后,因发生化学变化而质量增加的是( )
A. 浓硫酸 B. 浓盐酸 C. 氢氧化钠 D. 石灰石
C
4. (2019·苏州中考)运输下列物质时,应张贴“腐蚀品”标识的是( )
3.下列说法中错误的是( )
A.氢氧化钠俗称烧碱 B.实验室中用熟石灰作干燥剂
C.氢氧化钠可去除油污 D.氢氧化钙微溶于水
课堂达标
A.氢氧化钠 B.汽油
C.铁矿石 D.大理石
3.下列说法中错误的是( )
A.氢氧化钠俗称烧碱 B.实验室中用熟石灰作干燥剂
C.氢氧化钠可去除油污 D.氢氧化钙微溶于水
B
课堂达标
A
4. (2019·苏州中考)运输下列物质时,应张贴“腐蚀品”标识的是( )
A.氢氧化钠 B.汽油
C.铁矿石 D.大理石
PART 2
02 碱的化学性质
碱的化学性质
碱的化学性质
2、碱的化学性质
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
氢氧化钠溶液
氢氧化钙溶液
紫色石蕊溶液
无色酚酞溶液
(1)碱与指示剂作用
碱的化学性质
2、碱的化学性质
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
氢氧化钠溶液
氢氧化钙溶液
紫色石蕊溶液
变蓝
变蓝
无色酚酞溶液
变红
变红
(1)碱与指示剂作用
【实验结论】紫色石蕊溶液遇碱变蓝,无色酚酞溶液遇碱变红
(2)碱与酸性氧化物反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
氢氧化钠(NaOH)溶液
氢氧化钙 [Ca(OH)2]溶液
CO2
SO2
2NaOH+CO2 Na2CO3+H2O
2NaOH+SO2 Na2SO3+H2O
Ca(OH)2+CO2 CaCO3 ↓+H2O
Ca(OH)2+SO2 CaSO3 ↓+H2O
碱的化学性质
(2)碱与酸性氧化物反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
氢氧化钠(NaOH)溶液
氢氧化钙 [Ca(OH)2]溶液
CO2
SO2
2NaOH+CO2 Na2CO3+H2O
2NaOH+SO2 Na2SO3+H2O
Ca(OH)2+CO2 CaCO3 ↓+H2O
Ca(OH)2+SO2 CaSO3 ↓+H2O
【实验结论】碱能与某些非金属氧化物反应,生成盐和水。
大家可以写出SO3与NaOH 的反应吗?
碱的化学性质
碱与非金属氧化物反应时,有两点必须注意:
SO3与NaOH 的反应:
2NaOH+SO3 Na2SO4 + H2O
碱的化学性质
碱与非金属氧化物反应时,有两点必须注意:
① 碱必须可溶 ② CO、NO等非金属氧化物不能与碱反应
SO3与NaOH 的反应:
2NaOH+SO3 Na2SO4 + H2O
碱的化学性质
碱的化学性质(拓展延伸)
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}碱与酸的反应
碱 + 酸 → 盐 + 水
H2SO4+Ca(OH)2=CaSO4↓+2H2O
?
H2SO4+Ba(OH)2=BaSO4+2H2O
?
(3)碱与酸的反应
碱的化学性质(拓展延伸)
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}碱与盐的反应
碱 + 盐 → 新碱 + 新盐
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
?
2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
?
(4)碱与盐的反应
碱有一些相似的化学性质
1、碱能使紫色石蕊溶液变蓝,使无色酚酞溶液变红。
2、碱可以与某些酸性氧化物反应生成盐和水。
3、碱可以与酸反应生成盐和水。
4、碱可以与某些盐反应生成新碱和新盐。
归纳总结
氢氧化钠:白色固体,易潮解
物理性质
几种常
见的碱
氢氧化钙:白色粉末、微溶于水
化学性质
用途
碱能使紫色石蕊溶液变蓝,使无色酚酞溶液变红
阶段小结
碱+酸性氧化物 盐+水
碱+酸 盐+水
碱+盐 新盐+新碱
课堂达标
1.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( ? ?)
A. 紫色石蕊试液??? B. 氯化钠溶液????????
C. 铁粉??????? D. pH试纸
课堂达标
1.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( ? ?)
A. 紫色石蕊试液??? B. 氯化钠溶液????????
C. 铁粉??????? D. pH试纸
B
课堂达标
2.下列四种物质中,能与其它三种物质都能发生化学反应的是( )
A.氯化铜
B.三氧化硫
C.氢氧化钠溶液
D.稀盐酸
课堂达标
2.下列四种物质中,能与其它三种物质都能发生化学反应的是( )
A.氯化铜
B.三氧化硫
C.氢氧化钠溶液
D.稀盐酸
C
课堂达标
3.某品牌牙膏中的摩擦剂是经过一系列加工而制得的极细小的碳酸钙粉末,它的生产过程如下:
????
?????????????????????
(1)请写出A物质的名称????????????????(化学式),俗名_________。?
(2) 写出反应②的化学方程式?????? ????? ?????。?
(3)二氧化碳有许多用途,请举出一例?????????????????????????。
课堂达标
3.某品牌牙膏中的摩擦剂是经过一系列加工而制得的极细小的碳酸钙粉末,它的生产过程如下:
????
?????????????????????
(1)请写出A物质的名称????????????????(化学式),俗名_________。?
(2) 写出反应②的化学方程式?????? ????? ?????。?
(3)二氧化碳有许多用途,请举出一例?????????????????????????。
作灭火剂
Ca(OH)2
熟石灰
CaO + H2O===Ca(OH)2
03 溶液的导电性
PART 3
思考与讨论
通过实验和讨论,我们知道盐酸、硫酸等酸有一些相似的化学性质,而氢氧化钠、氢氧化钙等碱也有一些相似的化学性质。这是为什么呢?通过这个实验我们来探究一下!
实验 :溶液的导电性
溶液的导电性
【实验现象和结论】
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}待测液
盐酸
稀硫酸
氢氧化钠溶液
氢氧化钙溶液
蒸馏水
乙醇
灯泡是否亮
亮
亮
亮
亮
不亮
不亮
结论
溶液的导电性
【实验现象和结论】
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}待测液
盐酸
稀硫酸
氢氧化钠溶液
氢氧化钙溶液
蒸馏水
乙醇
灯泡是否亮
亮
亮
亮
亮
不亮
不亮
结论
导电
导电
导电
导电
不导电
不导电
溶液的导电性
为什么酸和碱的溶液可以导电,蒸馏水和乙醇不导电???
能导电,说明在这些溶液中存在带电的粒子,即溶液中含有自由移动的离子,通电后,阴阳离子定向移动,形成电流。
思考分析
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}物质
离子种类
HCl
H2SO4
NaOH
Ca(OH)2
能导电,说明在这些溶液中存在带电的粒子,即溶液中含有自由移动的离子,通电后,阴阳离子定向移动,形成电流。
进一步说明,盐酸、硫酸、氢氧化钠溶液和氢氧化钙溶液在溶于水时解离出能自由移动的离子,即上述溶液在水中解离出的离子种类如表所示。
思考分析
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}物质
离子种类
HCl
H+ Cl-
H2SO4
H+ SO42-
NaOH
Na+ OH-
Ca(OH)2
Ca2+ OH-
分析表格,我们发现什么?
酸或碱化学性质相似的原因
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}物质
离子种类
HCl
H+ Cl-
H2SO4
H+ SO42-
NaOH
Na+ OH-
Ca(OH)2
Ca2+ OH-
(1)酸在溶液中能解离出自由移动的H+和酸根离子,不同的酸溶液中都含有H+,故酸具有一些相似的化学性质。
(2)碱溶于水后,能解离出自由移动的金属离子(或NH4+)和OH-,不同的碱溶液中都含有OH-,故碱具有一些相似的化学性质。
酸或碱化学性质相似的原因
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}物质
离子种类
HCl
H+ Cl-
H2SO4
H+ SO42-
NaOH
Na+ OH-
Ca(OH)2
Ca2+ OH-
通过实验和讨论,我们知道了酸具有一些相似的化学性质,和碱也具有有一些相似的化学性质的原因了,那么酸和碱的具体定义是什么?
思考讨论
HCl → H+ + Cl-
H2SO4→ 2H+ + SO42-
NaOH → Na+ + OH-
Ca(OH)2→ Ca2+ + 2OH-
碱:溶于水时产生的阴离子全部是氢氧根离子( OH- )的化合物
酸:溶于水时产生的阳离子全部是氢离子(H+ )的化合物。
酸碱的定义
自由移动的离子
溶液导电原因
溶液的导电性
酸:溶于水时产生的阳离子全部是氢离子
(H+ )的化合物
酸或碱化学性质相似的原因
阶段小结
酸:H+ 碱:OH-
酸碱的
定义
碱:溶于水时产生的阴离子全部是氢氧根
离子( OH- )的化合物
课堂达标
1.酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不属于酸的共同性质的是 ( )
A 能使紫色石蕊溶液变为红色
B 能与氢氧化钠反应生成水
C 能与硝酸银溶液反应生成白色沉淀
D 能与锌反应生成氢气
课堂达标
1.酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不属于酸的共同性质的是 ( )
A 能使紫色石蕊溶液变为红色
B 能与氢氧化钠反应生成水
C 能与硝酸银溶液反应生成白色沉淀
D 能与锌反应生成氢气
C
课堂达标
2.稀盐酸和稀硫酸具有相似的化学性质,其本质原因是( )
A.都能与指示剂作用
B. 都能解离出酸根离子
C. 都能解离出氢离子
D. 都含有氢元素
课堂达标
2.稀盐酸和稀硫酸具有相似的化学性质,其本质原因是( )
A.都能与指示剂作用
B. 都能解离出酸根离子
C. 都能解离出氢离子
D. 都含有氢元素
C
课堂达标
3. (2019·成都中考节选)氢氧化钠、氢氧化钙是两种常见的碱。
(1)它们有一些相似的化学性质,其原因是溶液中都含有___________。
(2)可作某些气体的干燥剂的是 。
课堂达标
3. (2019·成都中考节选)氢氧化钠、氢氧化钙是两种常见的碱。
(1)它们有一些相似的化学性质,其原因是溶液中都含有___________。
(2)可作某些气体的干燥剂的是 。
OH-
氢氧化钠固体
PART 1
常见的酸和碱练习题
1.某地曾发生一起泼硫酸事件,一位老人被泼瞬间毁容,并导致右眼失明。下列关于硫酸的说法中,不正确的是( )
A.浓硫酸有很强的腐蚀性,使用时要特别小心
B.把水直接倒入盛有浓硫酸的烧杯中稀释
C.浓硫酸的脱水性是化学性质
D.浓硫酸有吸水性,可用作干燥剂
1.某地曾发生一起泼硫酸事件,一位老人被泼瞬间毁容,并导致右眼失明。下列关于硫酸的说法中,不正确的是( )
A.浓硫酸有很强的腐蚀性,使用时要特别小心
B.把水直接倒入盛有浓硫酸的烧杯中稀释
C.浓硫酸的脱水性是化学性质
D.浓硫酸有吸水性,可用作干燥剂
B
酸入水
2.下列溶液曝露在空气中,一段时间后溶液质量增大的是( )
A.蔗糖溶液 B.浓盐酸
C.浓硫酸 D.饱和食盐水
2.下列溶液曝露在空气中,一段时间后溶液质量增大的是( )
A.蔗糖溶液 B.浓盐酸
C.浓硫酸 D.饱和食盐水
C
3.化学晚会上小豆把一张白纸的正反两面向大家展示清楚,然后把白纸用电吹风的热风吹片刻,不一会儿,白纸上出现了一只小黑猫,大家惊奇不已,你知道这是怎么回事吗?请你用学过的化学知识来解释。
(1)小豆事先用 画了一只小猫。
(2)使白纸出现黑猫的物质是 ;表现该物质具有 性。
3.化学晚会上小豆把一张白纸的正反两面向大家展示清楚,然后把白纸用电吹风的热风吹片刻,不一会儿,白纸上出现了一只小黑猫,大家惊奇不已,你知道这是怎么回事吗?请你用学过的化学知识来解释。
(1)小豆事先用 画了一只小猫。
(2)使白纸出现黑猫的物质是 ;表现该物质具有 性。
稀硫酸
浓硫酸
脱水
4.(双选题)用酒精灯和水浸泡蝴蝶兰花可得到紫色溶液,该溶液遇酸溶液显蓝色,遇碱溶液显黄色。下列说法不正确的是( )
A 蝴蝶兰花的溶液与酸作用显红色是物理变化
B 能使蝴蝶兰花的溶液显黄色的一定是碱溶液
C 将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色
D 蝴蝶兰花的溶液可用作酸碱指示剂
4.(双选题)用酒精灯和水浸泡蝴蝶兰花可得到紫色溶液,该溶液遇酸溶液显蓝色,遇碱溶液显黄色。下列说法不正确的是( )
A 蝴蝶兰花的溶液与酸作用显红色是物理变化
B 能使蝴蝶兰花的溶液显黄色的一定是碱溶液
C 将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色
D 蝴蝶兰花的溶液可用作酸碱指示剂
A B
5.某同学在化学晚会上用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四字.该同学所用的两种无色液体可能是( )
A. NaOH溶液、酚酞溶液
B. CuSO4溶液、NaOH溶液
C. 紫色石蕊溶液、酚酞溶液
D. 酚酞溶液、“雪碧”饮料
5.某同学在化学晚会上用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四字.该同学所用的两种无色液体可能是( )
A. NaOH溶液、酚酞溶液
B. CuSO4溶液、NaOH溶液
C. 紫色石蕊溶液、酚酞溶液
D. 酚酞溶液、“雪碧”饮料
A
(1)紫薯汁 (填“能”或”不能”)作酸碱指示剂。
(2)草木灰溶液显 (填“酸性” ”中性”或”碱性”)。
(3)“向蒸馏水中滴加紫薯汁”的目的是 。
6.实验小组同学分别向下列试剂中滴加自制紫薯汁,现象记录如下:
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}试剂
稀盐酸
氢氧化钠溶液
蒸馏水
白醋
草木灰溶液
现象
红色
绿色
紫色
红色
绿色
(1)紫薯汁 (填“能”或”不能”)作酸碱指示剂。
(2)草木灰溶液显 (填“酸性” ”中性”或”碱性”)。
(3)“向蒸馏水中滴加紫薯汁”的目的是 。
6.实验小组同学分别向下列试剂中滴加自制紫薯汁,现象记录如下:
能
碱性
作空白对照
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}试剂
稀盐酸
氢氧化钠溶液
蒸馏水
白醋
草木灰溶液
现象
红色
绿色
紫色
红色
绿色
7.将一根生锈的铁钉放入稀硫酸中,下列对发生变化的预测错的是( )
A.铁钉表面的铁锈将消失
B.一段时间后铁钉表面将产生气泡
C. 溶液的颜色由无色变为黄色
D.溶液的质量将会减少
7.将一根生锈的铁钉放入稀硫酸中,下列对发生变化的预测错的是( )
A.铁钉表面的铁锈将消失
B.一段时间后铁钉表面将产生气泡
C. 溶液的颜色由无色变为黄色
D.溶液的质量将会减少
D
8. (2019·广东中考)取一定量打磨后的铝片于某容器中,再逐渐加入稀盐酸。加入稀盐酸的质量与有关量的变化关系图错误的是( )
8. (2019·广东中考)取一定量打磨后的铝片于某容器中,再逐渐加入稀盐酸。加入稀盐酸的质量与有关量的变化关系图错误的是( )
B
9. 生锈的铁钉放入足量的稀盐酸中,片刻后观察到的现象
是 ,发生反应的化学方程式为 ;反应一段时间后,又观察到铁钉表面 ,发生反应的化学方程式为 。
9. 生锈的铁钉放入足量的稀盐酸中,片刻后观察到的现象
是 ,发生反应的化学方程式为 ;反应一段时间后,又观察到铁钉表面 ,发生反应的化学方程式为 。
铁锈消失,溶液由无色变为黄色
有气泡产生
Fe2O3+6HCl 2FeCl3+3H2O
Fe+2HCl FeCl2+H2↑
10.将一套如图所示的密闭装置放在天平上,使天平平衡,经过一段时间后出现的情况是( )
A.指针偏左,食盐溶液一定变稀,烧碱潮解
B.指针偏左,食盐溶液一定变浓,烧碱潮解
C.指针偏右,食盐溶液一定变浓,烧碱潮解
D.指针偏右,食盐溶液一定饱和,烧碱潮解
10.将一套如图所示的密闭装置放在天平上,使天平平衡,经过一段时间后出现的情况是( )
A.指针偏左,食盐溶液一定变稀,烧碱潮解
B.指针偏左,食盐溶液一定变浓,烧碱潮解
C.指针偏右,食盐溶液一定变浓,烧碱潮解
D.指针偏右,食盐溶液一定饱和,烧碱潮解
C
11、盛有饱和氢氧化钠溶液的烧杯在空气中放置较长一段时间后,该溶液中的(??? )
A.氧氧化钠的质量减小
B.氧氧化钠的质量保持不变
C.氧氧化钠的质量分数增大
D.氧氧化钠的质量分数保持不变
11、盛有饱和氢氧化钠溶液的烧杯在空气中放置较长一段时间后,该溶液中的(??? )
A.氧氧化钠的质量减小
B.氧氧化钠的质量保持不变
C.氧氧化钠的质量分数增大
D.氧氧化钠的质量分数保持不变
A
12.如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起。气体X和液体Y不可能是( )
A. X: HCl; Y: 水 B. X: CO2; Y: 石灰水
C. X: SO2 ;Y: NaOH D. X: CO ; Y: NaOH
D
12.如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起。气体X和液体Y不可能是( )
A. X: HCl; Y: 水 B. X: CO2; Y: 石灰水
C. X: SO2 ;Y: NaOH D. X: CO ; Y: NaOH
D
13.在四支试管中分别加入2mL稀盐酸,并滴入几滴酚酞试液,如果分别不断加入下列物质直至过量,其中能使溶液显红色的是( )
A.CuO B.CaCO3
C.NaOH D.Fe
13.在四支试管中分别加入2mL稀盐酸,并滴入几滴酚酞试液,如果分别不断加入下列物质直至过量,其中能使溶液显红色的是( )
A.CuO B.CaCO3
C.NaOH D.Fe
C
14.下列4个坐标图分别表示4个实验过程中某些物质质量的变化,其中正确的是( )
14.下列4个坐标图分别表示4个实验过程中某些物质质量的变化,其中正确的是( )
C
15.构建知识网络,理清物质间的相互关系,是化学学习中的一种重要方法。下图中连线两端的物质可以相互反应。下列四组选项中,符合该图要求的是( )(多选)
A.①Na2CO3 ② SO2 ③ K2CO3
B.①NaHCO3 ②CO2 ③BaCl2
C.①Fe2O3 ②CO ③Ba(NO3)2
D.①MgCO3 ② SO2 ③Na2CO3
15.构建知识网络,理清物质间的相互关系,是化学学习中的一种重要方法。下图中连线两端的物质可以相互反应。下列四组选项中,符合该图要求的是( )(多选)
A.①Na2CO3 ② SO2 ③ K2CO3
B.①NaHCO3 ②CO2 ③BaCl2
C.①Fe2O3 ②CO ③Ba(NO3)2
D.①MgCO3 ② SO2 ③Na2CO3
AD
16.酸具有酸的通性的原因是( )
A.酸都能电离出H+
B.酸都含有酸根
C.酸中都含有氢元素
D.酸中都含有氧元素
16.酸具有酸的通性的原因是( )
A.酸都能电离出H+
B.酸都含有酸根
C.酸中都含有氢元素
D.酸中都含有氧元素
A
17.氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是( )
A 都能与指示剂 作用
B 都能解离出氢氧根离子
C 都能解离出金属阳离子
D 都含有氢元素和氧元素
17.氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是( )
A 都能与指示剂 作用
B 都能解离出氢氧根离子
C 都能解离出金属阳离子
D 都含有氢元素和氧元素
B
18.在稀硫酸中加入下列溶液后,其导电性几乎消失的是( )
A.KOH
B.BaCl2
C.MgCl2
D.Ba(OH)2
18.在稀硫酸中加入下列溶液后,其导电性几乎消失的是( )
A.KOH
B.BaCl2
C.MgCl2
D.Ba(OH)2
D
谢谢观看
第二课时 常见的碱
CONTENTS
01
常见的碱
02
碱的化学性质
内容提要
03
溶液的导电性
认识几种常见碱的主要性质和用途
能够设计实验验证溶液的导电性
会用酸碱指示剂检验溶液的酸碱性
目标一
目标三
目标二
学习目标
人类社会除了需要酸,同样也离不开碱,你知道哪些碱?
它们在生产生活中有哪些应用?
新课引入
你知道生活中哪些物质含有碱吗?
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等。
“尝起来涩涩的”
“摸起来滑滑的”
新课导入
PART 1
01 常见的碱
几种常见的碱
常见的碱:氢氧化钠(NaOH)、氢氧化钙[Ca(OH)2]、氢氧化钾(KOH)、氢氧化铜[Cu(OH)2] 、氨水(NH3.H2O)等。
观察这几种碱,从名称和组成上看你能发现什么?
碱→金属离子 + 氢氧根离子
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}碱
金属元素
氢氧根离子
氢氧化钠 NaOH
Na+
OH-
氢氧化钙 Ca(OH)2
Ca2+
OH-
氢氧化铜 Cu(OH)2
Cu2+
OH-
氢氧化钾 KOH
K+
OH-
氢氧化镁 Mg(OH)2
Mg2+
OH-
几种常见的碱
碱→金属离子(或铵根离子) + 氢氧根离子
特例:一水合氨NH3·H2O,
它的组成中没有金属元素,但它是碱
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}碱
金属元素
氢氧根离子
氢氧化钠 NaOH
Na+
OH-
氢氧化钙 Ca(OH)2
Ca2+
OH-
氢氧化铜 Cu(OH)2
Cu2+
OH-
氢氧化钾 KOH
K+
OH-
氢氧化镁 Mg(OH)2
Mg2+
OH-
碱的定义
按含有氢氧根的个数
按在水中的溶解性
可溶性碱:
KOH、NaOH、Ca(OH)2、Ba(OH)2、NH3·H2O等
难溶性碱:
Cu(OH)2、Fe(OH)3等
一元碱:
NaOH、NH3·H2O等
二元碱:
Ba(OH)2、 Cu(OH)2等
三元碱:
Fe(OH)3等
………
碱的定义
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
根据在水中的溶解性
根据含有氢氧根的个数
可溶性碱
难溶性碱
一元碱
二元碱
三元碱
NaOH
Cu(OH)2
Ca(OH)2
NH3·H2O
Fe(OH)3
碱的分类
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
根据在水中的溶解性
根据含有氢氧根的个数
可溶性碱
难溶性碱
一元碱
二元碱
三元碱
NaOH
√
Cu(OH)2
√
Ca(OH)2
√
NH3·H2O
√
Fe(OH)3
√
碱的分类
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
根据在水中的溶解性
根据含有氢氧根的个数
可溶性碱
难溶性碱
一元碱
二元碱
三元碱
NaOH
√
√
Cu(OH)2
√
√
Ca(OH)2
√
√
NH3·H2O
√
√
Fe(OH)3
√
√
碱的分类
认识常见的碱
氢氧化钠
氢氧化钙
实验: 认识常见的碱
氢氧化钠(NaOH)
颜色、状态:白色固体
俗名:苛性钠、火碱、烧碱
溶解性:易溶于水,溶解时放出大量的热
吸水性:易吸水潮解
用途:广泛用于制取肥皂,以及石油、造纸、纺织等工业;生活中
用来去除油污;实验室可用作某些气体的干燥剂。
与油脂反应
汽油→溶解,洗涤剂→乳化
氢氧化钠
1.氢氧化钠曝露在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫潮解。
2.氢氧化钠有强烈的腐蚀性,使用时必须十分小心,防止眼睛、皮肤、衣服等被腐蚀。实验时最好戴防护眼镜。
物理变化
拓展提升
氢氧化钙[Ca(OH)2]
颜色、状态:白色粉末状固体
俗名:熟石灰、消石灰
溶解性:微溶于水,溶解度随温度升高而减小
吸水性:不易吸水
用途:建筑上用熟石灰和沙子混合来砌砖,用石灰浆粉刷墙壁;涂刷含硫磺粉等的石灰浆,可保护树木;可用石灰乳和硫酸铜等配制农药波尔多液,熟石灰还可用来改良酸性土壤;实验室中用澄清石灰水检验二氧化碳。
氢氧化钙
氢氧化钙微溶于水,其水溶液俗称石灰水,当石灰水中存在较多未溶解的氢氧化钙时,就称为石灰乳或石灰浆。
氢氧化钙
氢氧化钙的制取:
CaO + H2O == Ca(OH)2
hhh,说到氢氧化钙,我还要偷偷告诉大家个小知识!!!
竖起耳朵听!!!
从化学角度解释《石灰吟》
“千锤万凿出深山”
“烈火焚烧若等闲”
“粉身碎骨全不怕”
“要留清白在人间”
小知识
从化学角度解释《石灰吟》
“千锤万凿出深山” 此过程是物理变化
“烈火焚烧若等闲”
CaCO3 ?CaO + CO2↑
?
“粉骨碎身浑不怕”
CaO + H2O == Ca(OH)2
“要留清白在人间”
Ca(OH)2+CO2=CaCO3↓+H2O
?
小知识
1.氢氧化钠易潮解,且易与空气中的CO2发生反应而变质,必须密封保存。
2.保存氢氧化钠溶液的试剂瓶要用橡胶塞,不能用玻璃塞。(玻璃中含有二氧化硅,能与碱反应)。
3.氢氧化钠固体通常用来干燥O2、H2、O2、 CH4、 NH3等碱性或中性气体,但不能干燥CO2、SO2、HCl等酸性气体。
4. CaO俗称生石灰,具有吸水性,生石灰固体常用作干燥剂,检验CO2时常用Ca(OH)2溶液。
拓展提升
除了NaOH、Ca(OH)2外,
常见的碱还有氢氧化钾(KOH)、氨水(NH3.H2O)
其他的碱
1.下列关于氢氧化钠和氢氧化钙的性质和用途说法不正确的是( )
A.氢氧化钠是一种白色固体,溶于水时放出热量
B.氢氧化钙是白色粉末状固体,微溶于水
C.氢氧化钙可用作某些气体的干燥剂
D.氢氧化钠易潮解,可作某些气体的干燥剂
课堂达标
2.(2019·滨州中考)下列物质露置在空气中一段时间后,因发生化学变化而质量增加的是( )
A. 浓硫酸 B. 浓盐酸 C. 氢氧化钠 D. 石灰石
1.下列关于氢氧化钠和氢氧化钙的性质和用途说法不正确的是( )
C
A.氢氧化钠是一种白色固体,溶于水时放出热量
B.氢氧化钙是白色粉末状固体,微溶于水
C.氢氧化钙可用作某些气体的干燥剂
D.氢氧化钠易潮解,可作某些气体的干燥剂
不能吸收水分,不可作干燥剂
课堂达标
2.(2019·滨州中考)下列物质露置在空气中一段时间后,因发生化学变化而质量增加的是( )
A. 浓硫酸 B. 浓盐酸 C. 氢氧化钠 D. 石灰石
C
4. (2019·苏州中考)运输下列物质时,应张贴“腐蚀品”标识的是( )
3.下列说法中错误的是( )
A.氢氧化钠俗称烧碱 B.实验室中用熟石灰作干燥剂
C.氢氧化钠可去除油污 D.氢氧化钙微溶于水
课堂达标
A.氢氧化钠 B.汽油
C.铁矿石 D.大理石
3.下列说法中错误的是( )
A.氢氧化钠俗称烧碱 B.实验室中用熟石灰作干燥剂
C.氢氧化钠可去除油污 D.氢氧化钙微溶于水
B
课堂达标
A
4. (2019·苏州中考)运输下列物质时,应张贴“腐蚀品”标识的是( )
A.氢氧化钠 B.汽油
C.铁矿石 D.大理石
PART 2
02 碱的化学性质
碱的化学性质
碱的化学性质
2、碱的化学性质
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
氢氧化钠溶液
氢氧化钙溶液
紫色石蕊溶液
无色酚酞溶液
(1)碱与指示剂作用
碱的化学性质
2、碱的化学性质
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}
氢氧化钠溶液
氢氧化钙溶液
紫色石蕊溶液
变蓝
变蓝
无色酚酞溶液
变红
变红
(1)碱与指示剂作用
【实验结论】紫色石蕊溶液遇碱变蓝,无色酚酞溶液遇碱变红
(2)碱与酸性氧化物反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
氢氧化钠(NaOH)溶液
氢氧化钙 [Ca(OH)2]溶液
CO2
SO2
2NaOH+CO2 Na2CO3+H2O
2NaOH+SO2 Na2SO3+H2O
Ca(OH)2+CO2 CaCO3 ↓+H2O
Ca(OH)2+SO2 CaSO3 ↓+H2O
碱的化学性质
(2)碱与酸性氧化物反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
氢氧化钠(NaOH)溶液
氢氧化钙 [Ca(OH)2]溶液
CO2
SO2
2NaOH+CO2 Na2CO3+H2O
2NaOH+SO2 Na2SO3+H2O
Ca(OH)2+CO2 CaCO3 ↓+H2O
Ca(OH)2+SO2 CaSO3 ↓+H2O
【实验结论】碱能与某些非金属氧化物反应,生成盐和水。
大家可以写出SO3与NaOH 的反应吗?
碱的化学性质
碱与非金属氧化物反应时,有两点必须注意:
SO3与NaOH 的反应:
2NaOH+SO3 Na2SO4 + H2O
碱的化学性质
碱与非金属氧化物反应时,有两点必须注意:
① 碱必须可溶 ② CO、NO等非金属氧化物不能与碱反应
SO3与NaOH 的反应:
2NaOH+SO3 Na2SO4 + H2O
碱的化学性质
碱的化学性质(拓展延伸)
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}碱与酸的反应
碱 + 酸 → 盐 + 水
H2SO4+Ca(OH)2=CaSO4↓+2H2O
?
H2SO4+Ba(OH)2=BaSO4+2H2O
?
(3)碱与酸的反应
碱的化学性质(拓展延伸)
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}碱与盐的反应
碱 + 盐 → 新碱 + 新盐
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
?
2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
?
(4)碱与盐的反应
碱有一些相似的化学性质
1、碱能使紫色石蕊溶液变蓝,使无色酚酞溶液变红。
2、碱可以与某些酸性氧化物反应生成盐和水。
3、碱可以与酸反应生成盐和水。
4、碱可以与某些盐反应生成新碱和新盐。
归纳总结
氢氧化钠:白色固体,易潮解
物理性质
几种常
见的碱
氢氧化钙:白色粉末、微溶于水
化学性质
用途
碱能使紫色石蕊溶液变蓝,使无色酚酞溶液变红
阶段小结
碱+酸性氧化物 盐+水
碱+酸 盐+水
碱+盐 新盐+新碱
课堂达标
1.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( ? ?)
A. 紫色石蕊试液??? B. 氯化钠溶液????????
C. 铁粉??????? D. pH试纸
课堂达标
1.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( ? ?)
A. 紫色石蕊试液??? B. 氯化钠溶液????????
C. 铁粉??????? D. pH试纸
B
课堂达标
2.下列四种物质中,能与其它三种物质都能发生化学反应的是( )
A.氯化铜
B.三氧化硫
C.氢氧化钠溶液
D.稀盐酸
课堂达标
2.下列四种物质中,能与其它三种物质都能发生化学反应的是( )
A.氯化铜
B.三氧化硫
C.氢氧化钠溶液
D.稀盐酸
C
课堂达标
3.某品牌牙膏中的摩擦剂是经过一系列加工而制得的极细小的碳酸钙粉末,它的生产过程如下:
????
?????????????????????
(1)请写出A物质的名称????????????????(化学式),俗名_________。?
(2) 写出反应②的化学方程式?????? ????? ?????。?
(3)二氧化碳有许多用途,请举出一例?????????????????????????。
课堂达标
3.某品牌牙膏中的摩擦剂是经过一系列加工而制得的极细小的碳酸钙粉末,它的生产过程如下:
????
?????????????????????
(1)请写出A物质的名称????????????????(化学式),俗名_________。?
(2) 写出反应②的化学方程式?????? ????? ?????。?
(3)二氧化碳有许多用途,请举出一例?????????????????????????。
作灭火剂
Ca(OH)2
熟石灰
CaO + H2O===Ca(OH)2
03 溶液的导电性
PART 3
思考与讨论
通过实验和讨论,我们知道盐酸、硫酸等酸有一些相似的化学性质,而氢氧化钠、氢氧化钙等碱也有一些相似的化学性质。这是为什么呢?通过这个实验我们来探究一下!
实验 :溶液的导电性
溶液的导电性
【实验现象和结论】
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}待测液
盐酸
稀硫酸
氢氧化钠溶液
氢氧化钙溶液
蒸馏水
乙醇
灯泡是否亮
亮
亮
亮
亮
不亮
不亮
结论
溶液的导电性
【实验现象和结论】
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}待测液
盐酸
稀硫酸
氢氧化钠溶液
氢氧化钙溶液
蒸馏水
乙醇
灯泡是否亮
亮
亮
亮
亮
不亮
不亮
结论
导电
导电
导电
导电
不导电
不导电
溶液的导电性
为什么酸和碱的溶液可以导电,蒸馏水和乙醇不导电???
能导电,说明在这些溶液中存在带电的粒子,即溶液中含有自由移动的离子,通电后,阴阳离子定向移动,形成电流。
思考分析
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}物质
离子种类
HCl
H2SO4
NaOH
Ca(OH)2
能导电,说明在这些溶液中存在带电的粒子,即溶液中含有自由移动的离子,通电后,阴阳离子定向移动,形成电流。
进一步说明,盐酸、硫酸、氢氧化钠溶液和氢氧化钙溶液在溶于水时解离出能自由移动的离子,即上述溶液在水中解离出的离子种类如表所示。
思考分析
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}物质
离子种类
HCl
H+ Cl-
H2SO4
H+ SO42-
NaOH
Na+ OH-
Ca(OH)2
Ca2+ OH-
分析表格,我们发现什么?
酸或碱化学性质相似的原因
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}物质
离子种类
HCl
H+ Cl-
H2SO4
H+ SO42-
NaOH
Na+ OH-
Ca(OH)2
Ca2+ OH-
(1)酸在溶液中能解离出自由移动的H+和酸根离子,不同的酸溶液中都含有H+,故酸具有一些相似的化学性质。
(2)碱溶于水后,能解离出自由移动的金属离子(或NH4+)和OH-,不同的碱溶液中都含有OH-,故碱具有一些相似的化学性质。
酸或碱化学性质相似的原因
{93296810-A885-4BE3-A3E7-6D5BEEA58F35}物质
离子种类
HCl
H+ Cl-
H2SO4
H+ SO42-
NaOH
Na+ OH-
Ca(OH)2
Ca2+ OH-
通过实验和讨论,我们知道了酸具有一些相似的化学性质,和碱也具有有一些相似的化学性质的原因了,那么酸和碱的具体定义是什么?
思考讨论
HCl → H+ + Cl-
H2SO4→ 2H+ + SO42-
NaOH → Na+ + OH-
Ca(OH)2→ Ca2+ + 2OH-
碱:溶于水时产生的阴离子全部是氢氧根离子( OH- )的化合物
酸:溶于水时产生的阳离子全部是氢离子(H+ )的化合物。
酸碱的定义
自由移动的离子
溶液导电原因
溶液的导电性
酸:溶于水时产生的阳离子全部是氢离子
(H+ )的化合物
酸或碱化学性质相似的原因
阶段小结
酸:H+ 碱:OH-
酸碱的
定义
碱:溶于水时产生的阴离子全部是氢氧根
离子( OH- )的化合物
课堂达标
1.酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不属于酸的共同性质的是 ( )
A 能使紫色石蕊溶液变为红色
B 能与氢氧化钠反应生成水
C 能与硝酸银溶液反应生成白色沉淀
D 能与锌反应生成氢气
课堂达标
1.酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不属于酸的共同性质的是 ( )
A 能使紫色石蕊溶液变为红色
B 能与氢氧化钠反应生成水
C 能与硝酸银溶液反应生成白色沉淀
D 能与锌反应生成氢气
C
课堂达标
2.稀盐酸和稀硫酸具有相似的化学性质,其本质原因是( )
A.都能与指示剂作用
B. 都能解离出酸根离子
C. 都能解离出氢离子
D. 都含有氢元素
课堂达标
2.稀盐酸和稀硫酸具有相似的化学性质,其本质原因是( )
A.都能与指示剂作用
B. 都能解离出酸根离子
C. 都能解离出氢离子
D. 都含有氢元素
C
课堂达标
3. (2019·成都中考节选)氢氧化钠、氢氧化钙是两种常见的碱。
(1)它们有一些相似的化学性质,其原因是溶液中都含有___________。
(2)可作某些气体的干燥剂的是 。
课堂达标
3. (2019·成都中考节选)氢氧化钠、氢氧化钙是两种常见的碱。
(1)它们有一些相似的化学性质,其原因是溶液中都含有___________。
(2)可作某些气体的干燥剂的是 。
OH-
氢氧化钠固体
PART 1
常见的酸和碱练习题
1.某地曾发生一起泼硫酸事件,一位老人被泼瞬间毁容,并导致右眼失明。下列关于硫酸的说法中,不正确的是( )
A.浓硫酸有很强的腐蚀性,使用时要特别小心
B.把水直接倒入盛有浓硫酸的烧杯中稀释
C.浓硫酸的脱水性是化学性质
D.浓硫酸有吸水性,可用作干燥剂
1.某地曾发生一起泼硫酸事件,一位老人被泼瞬间毁容,并导致右眼失明。下列关于硫酸的说法中,不正确的是( )
A.浓硫酸有很强的腐蚀性,使用时要特别小心
B.把水直接倒入盛有浓硫酸的烧杯中稀释
C.浓硫酸的脱水性是化学性质
D.浓硫酸有吸水性,可用作干燥剂
B
酸入水
2.下列溶液曝露在空气中,一段时间后溶液质量增大的是( )
A.蔗糖溶液 B.浓盐酸
C.浓硫酸 D.饱和食盐水
2.下列溶液曝露在空气中,一段时间后溶液质量增大的是( )
A.蔗糖溶液 B.浓盐酸
C.浓硫酸 D.饱和食盐水
C
3.化学晚会上小豆把一张白纸的正反两面向大家展示清楚,然后把白纸用电吹风的热风吹片刻,不一会儿,白纸上出现了一只小黑猫,大家惊奇不已,你知道这是怎么回事吗?请你用学过的化学知识来解释。
(1)小豆事先用 画了一只小猫。
(2)使白纸出现黑猫的物质是 ;表现该物质具有 性。
3.化学晚会上小豆把一张白纸的正反两面向大家展示清楚,然后把白纸用电吹风的热风吹片刻,不一会儿,白纸上出现了一只小黑猫,大家惊奇不已,你知道这是怎么回事吗?请你用学过的化学知识来解释。
(1)小豆事先用 画了一只小猫。
(2)使白纸出现黑猫的物质是 ;表现该物质具有 性。
稀硫酸
浓硫酸
脱水
4.(双选题)用酒精灯和水浸泡蝴蝶兰花可得到紫色溶液,该溶液遇酸溶液显蓝色,遇碱溶液显黄色。下列说法不正确的是( )
A 蝴蝶兰花的溶液与酸作用显红色是物理变化
B 能使蝴蝶兰花的溶液显黄色的一定是碱溶液
C 将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色
D 蝴蝶兰花的溶液可用作酸碱指示剂
4.(双选题)用酒精灯和水浸泡蝴蝶兰花可得到紫色溶液,该溶液遇酸溶液显蓝色,遇碱溶液显黄色。下列说法不正确的是( )
A 蝴蝶兰花的溶液与酸作用显红色是物理变化
B 能使蝴蝶兰花的溶液显黄色的一定是碱溶液
C 将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色
D 蝴蝶兰花的溶液可用作酸碱指示剂
A B
5.某同学在化学晚会上用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四字.该同学所用的两种无色液体可能是( )
A. NaOH溶液、酚酞溶液
B. CuSO4溶液、NaOH溶液
C. 紫色石蕊溶液、酚酞溶液
D. 酚酞溶液、“雪碧”饮料
5.某同学在化学晚会上用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四字.该同学所用的两种无色液体可能是( )
A. NaOH溶液、酚酞溶液
B. CuSO4溶液、NaOH溶液
C. 紫色石蕊溶液、酚酞溶液
D. 酚酞溶液、“雪碧”饮料
A
(1)紫薯汁 (填“能”或”不能”)作酸碱指示剂。
(2)草木灰溶液显 (填“酸性” ”中性”或”碱性”)。
(3)“向蒸馏水中滴加紫薯汁”的目的是 。
6.实验小组同学分别向下列试剂中滴加自制紫薯汁,现象记录如下:
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}试剂
稀盐酸
氢氧化钠溶液
蒸馏水
白醋
草木灰溶液
现象
红色
绿色
紫色
红色
绿色
(1)紫薯汁 (填“能”或”不能”)作酸碱指示剂。
(2)草木灰溶液显 (填“酸性” ”中性”或”碱性”)。
(3)“向蒸馏水中滴加紫薯汁”的目的是 。
6.实验小组同学分别向下列试剂中滴加自制紫薯汁,现象记录如下:
能
碱性
作空白对照
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}试剂
稀盐酸
氢氧化钠溶液
蒸馏水
白醋
草木灰溶液
现象
红色
绿色
紫色
红色
绿色
7.将一根生锈的铁钉放入稀硫酸中,下列对发生变化的预测错的是( )
A.铁钉表面的铁锈将消失
B.一段时间后铁钉表面将产生气泡
C. 溶液的颜色由无色变为黄色
D.溶液的质量将会减少
7.将一根生锈的铁钉放入稀硫酸中,下列对发生变化的预测错的是( )
A.铁钉表面的铁锈将消失
B.一段时间后铁钉表面将产生气泡
C. 溶液的颜色由无色变为黄色
D.溶液的质量将会减少
D
8. (2019·广东中考)取一定量打磨后的铝片于某容器中,再逐渐加入稀盐酸。加入稀盐酸的质量与有关量的变化关系图错误的是( )
8. (2019·广东中考)取一定量打磨后的铝片于某容器中,再逐渐加入稀盐酸。加入稀盐酸的质量与有关量的变化关系图错误的是( )
B
9. 生锈的铁钉放入足量的稀盐酸中,片刻后观察到的现象
是 ,发生反应的化学方程式为 ;反应一段时间后,又观察到铁钉表面 ,发生反应的化学方程式为 。
9. 生锈的铁钉放入足量的稀盐酸中,片刻后观察到的现象
是 ,发生反应的化学方程式为 ;反应一段时间后,又观察到铁钉表面 ,发生反应的化学方程式为 。
铁锈消失,溶液由无色变为黄色
有气泡产生
Fe2O3+6HCl 2FeCl3+3H2O
Fe+2HCl FeCl2+H2↑
10.将一套如图所示的密闭装置放在天平上,使天平平衡,经过一段时间后出现的情况是( )
A.指针偏左,食盐溶液一定变稀,烧碱潮解
B.指针偏左,食盐溶液一定变浓,烧碱潮解
C.指针偏右,食盐溶液一定变浓,烧碱潮解
D.指针偏右,食盐溶液一定饱和,烧碱潮解
10.将一套如图所示的密闭装置放在天平上,使天平平衡,经过一段时间后出现的情况是( )
A.指针偏左,食盐溶液一定变稀,烧碱潮解
B.指针偏左,食盐溶液一定变浓,烧碱潮解
C.指针偏右,食盐溶液一定变浓,烧碱潮解
D.指针偏右,食盐溶液一定饱和,烧碱潮解
C
11、盛有饱和氢氧化钠溶液的烧杯在空气中放置较长一段时间后,该溶液中的(??? )
A.氧氧化钠的质量减小
B.氧氧化钠的质量保持不变
C.氧氧化钠的质量分数增大
D.氧氧化钠的质量分数保持不变
11、盛有饱和氢氧化钠溶液的烧杯在空气中放置较长一段时间后,该溶液中的(??? )
A.氧氧化钠的质量减小
B.氧氧化钠的质量保持不变
C.氧氧化钠的质量分数增大
D.氧氧化钠的质量分数保持不变
A
12.如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起。气体X和液体Y不可能是( )
A. X: HCl; Y: 水 B. X: CO2; Y: 石灰水
C. X: SO2 ;Y: NaOH D. X: CO ; Y: NaOH
D
12.如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起。气体X和液体Y不可能是( )
A. X: HCl; Y: 水 B. X: CO2; Y: 石灰水
C. X: SO2 ;Y: NaOH D. X: CO ; Y: NaOH
D
13.在四支试管中分别加入2mL稀盐酸,并滴入几滴酚酞试液,如果分别不断加入下列物质直至过量,其中能使溶液显红色的是( )
A.CuO B.CaCO3
C.NaOH D.Fe
13.在四支试管中分别加入2mL稀盐酸,并滴入几滴酚酞试液,如果分别不断加入下列物质直至过量,其中能使溶液显红色的是( )
A.CuO B.CaCO3
C.NaOH D.Fe
C
14.下列4个坐标图分别表示4个实验过程中某些物质质量的变化,其中正确的是( )
14.下列4个坐标图分别表示4个实验过程中某些物质质量的变化,其中正确的是( )
C
15.构建知识网络,理清物质间的相互关系,是化学学习中的一种重要方法。下图中连线两端的物质可以相互反应。下列四组选项中,符合该图要求的是( )(多选)
A.①Na2CO3 ② SO2 ③ K2CO3
B.①NaHCO3 ②CO2 ③BaCl2
C.①Fe2O3 ②CO ③Ba(NO3)2
D.①MgCO3 ② SO2 ③Na2CO3
15.构建知识网络,理清物质间的相互关系,是化学学习中的一种重要方法。下图中连线两端的物质可以相互反应。下列四组选项中,符合该图要求的是( )(多选)
A.①Na2CO3 ② SO2 ③ K2CO3
B.①NaHCO3 ②CO2 ③BaCl2
C.①Fe2O3 ②CO ③Ba(NO3)2
D.①MgCO3 ② SO2 ③Na2CO3
AD
16.酸具有酸的通性的原因是( )
A.酸都能电离出H+
B.酸都含有酸根
C.酸中都含有氢元素
D.酸中都含有氧元素
16.酸具有酸的通性的原因是( )
A.酸都能电离出H+
B.酸都含有酸根
C.酸中都含有氢元素
D.酸中都含有氧元素
A
17.氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是( )
A 都能与指示剂 作用
B 都能解离出氢氧根离子
C 都能解离出金属阳离子
D 都含有氢元素和氧元素
17.氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是( )
A 都能与指示剂 作用
B 都能解离出氢氧根离子
C 都能解离出金属阳离子
D 都含有氢元素和氧元素
B
18.在稀硫酸中加入下列溶液后,其导电性几乎消失的是( )
A.KOH
B.BaCl2
C.MgCl2
D.Ba(OH)2
18.在稀硫酸中加入下列溶液后,其导电性几乎消失的是( )
A.KOH
B.BaCl2
C.MgCl2
D.Ba(OH)2
D
谢谢观看
同课章节目录
