(人教版)8.2金属的化学性质——趣味运动会 九年级化学下册同步课件(13页ppt)
文档属性
| 名称 | (人教版)8.2金属的化学性质——趣味运动会 九年级化学下册同步课件(13页ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 69.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-21 00:00:00 | ||
图片预览




文档简介
(共13张PPT)
金属村趣味运动会
经安中学 刘馨元
入场仪式
各组入场介绍代表金属
九年级第一届金属趣味运动会
项目一:有氧竞速
参赛小组
项目一:有氧竞速
以上反应体现了金属的什么化学性质?
能与氧气发生反应
Mg、Fe、Cu、Au谁的化学性质更活泼?为什么?
如何比较金属活动性的强弱?
Mg
根据金属与氧气反应的难易程度和剧烈程度
项目二:酸中速游
参赛小组
盐酸(HCl)
硫酸(H2SO4)
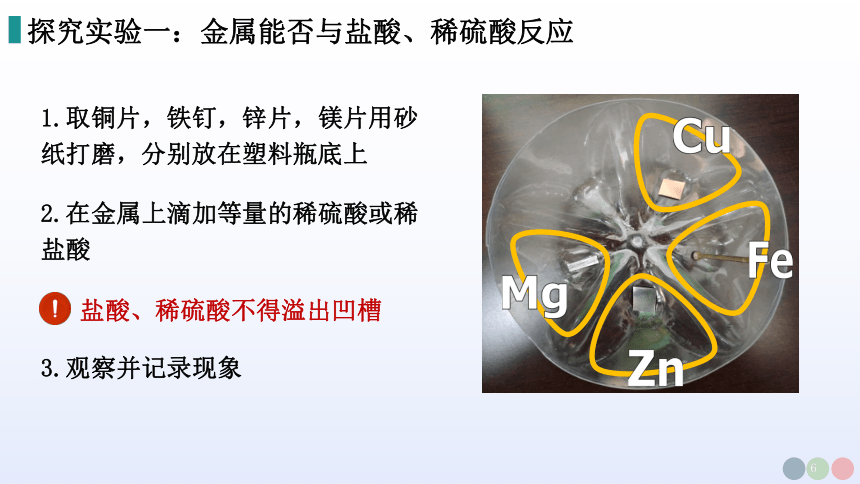
探究实验一:金属能否与盐酸、稀硫酸反应
2.在金属上滴加等量的稀硫酸或稀盐酸
1.取铜片,铁钉,锌片,镁片用砂纸打磨,分别放在塑料瓶底上
3.观察并记录现象
盐酸、稀硫酸不得溢出凹槽
金属 与盐酸,稀硫酸反应
现象
镁
锌
铁
铜
固体消失,产生大量气体,放出热量
部分固体消失,产生气体,放出热量
产生少量气体,溶液变为浅绿色
无明显现象
探究实验一:金属能否与盐酸、稀硫酸反应
书写锌与稀硫酸的化学方程式
书写余下的的化学方程式
项目二:酸中速游
以上反应体现了金属的什么化学性质?
能与盐酸、稀硫酸发生反应
Mg、Zn、Fe、Cu中谁的活动性强?为什么
如何比较金属活动性的强弱?
根据金属能否与盐酸、稀硫酸发生反应
项目三:盐滩登陆
参赛选手
探究实验二:金属能否与金属化合物溶液反应
1.取一块铝,两块铜分别放在点滴板上
2.向铝中加入硫酸铜溶液,铜中加入硝酸银溶液,铜中加入硫酸铝溶液
加入的液体不能溢出凹槽
3.观察并记录现象
探究实验二:金属能否与金属化合物溶液反应
实验 现象 化学方程式
Al CuSO4
Cu AgNO3
Cu Al2(SO4)3
铝片表面有红色物质析出,溶液由蓝色逐渐变为无色
铜片表面有银白色的物质析出,溶液由无色变为蓝色
无明显现象
不反应
Cu+2AgNO3 Cu(NO3)2+2Ag
2Al+3CuSO4 Al2(SO4)3+3Cu
项目二:酸中速游
以上反应体现了金属的什么化学性质?
能与金属化合物溶液发生反应
根据这条性质,能否总结出判定金属活动性的方法?
如何比较金属活动性的强弱?
活动性强的金属能把活动性弱的金属从它的化合物溶液中置换出来
课堂总结
金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb ( H ) Cu Hg Ag Pt Au
金 属 活 动 性 由 强 逐 渐 减 弱
1.在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2.在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
3.在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
金属村趣味运动会
经安中学 刘馨元
入场仪式
各组入场介绍代表金属
九年级第一届金属趣味运动会
项目一:有氧竞速
参赛小组
项目一:有氧竞速
以上反应体现了金属的什么化学性质?
能与氧气发生反应
Mg、Fe、Cu、Au谁的化学性质更活泼?为什么?
如何比较金属活动性的强弱?
Mg
根据金属与氧气反应的难易程度和剧烈程度
项目二:酸中速游
参赛小组
盐酸(HCl)
硫酸(H2SO4)
探究实验一:金属能否与盐酸、稀硫酸反应
2.在金属上滴加等量的稀硫酸或稀盐酸
1.取铜片,铁钉,锌片,镁片用砂纸打磨,分别放在塑料瓶底上
3.观察并记录现象
盐酸、稀硫酸不得溢出凹槽
金属 与盐酸,稀硫酸反应
现象
镁
锌
铁
铜
固体消失,产生大量气体,放出热量
部分固体消失,产生气体,放出热量
产生少量气体,溶液变为浅绿色
无明显现象
探究实验一:金属能否与盐酸、稀硫酸反应
书写锌与稀硫酸的化学方程式
书写余下的的化学方程式
项目二:酸中速游
以上反应体现了金属的什么化学性质?
能与盐酸、稀硫酸发生反应
Mg、Zn、Fe、Cu中谁的活动性强?为什么
如何比较金属活动性的强弱?
根据金属能否与盐酸、稀硫酸发生反应
项目三:盐滩登陆
参赛选手
探究实验二:金属能否与金属化合物溶液反应
1.取一块铝,两块铜分别放在点滴板上
2.向铝中加入硫酸铜溶液,铜中加入硝酸银溶液,铜中加入硫酸铝溶液
加入的液体不能溢出凹槽
3.观察并记录现象
探究实验二:金属能否与金属化合物溶液反应
实验 现象 化学方程式
Al CuSO4
Cu AgNO3
Cu Al2(SO4)3
铝片表面有红色物质析出,溶液由蓝色逐渐变为无色
铜片表面有银白色的物质析出,溶液由无色变为蓝色
无明显现象
不反应
Cu+2AgNO3 Cu(NO3)2+2Ag
2Al+3CuSO4 Al2(SO4)3+3Cu
项目二:酸中速游
以上反应体现了金属的什么化学性质?
能与金属化合物溶液发生反应
根据这条性质,能否总结出判定金属活动性的方法?
如何比较金属活动性的强弱?
活动性强的金属能把活动性弱的金属从它的化合物溶液中置换出来
课堂总结
金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb ( H ) Cu Hg Ag Pt Au
金 属 活 动 性 由 强 逐 渐 减 弱
1.在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2.在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
3.在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
同课章节目录
