高二化学化学反应中的热效应
图片预览









文档简介
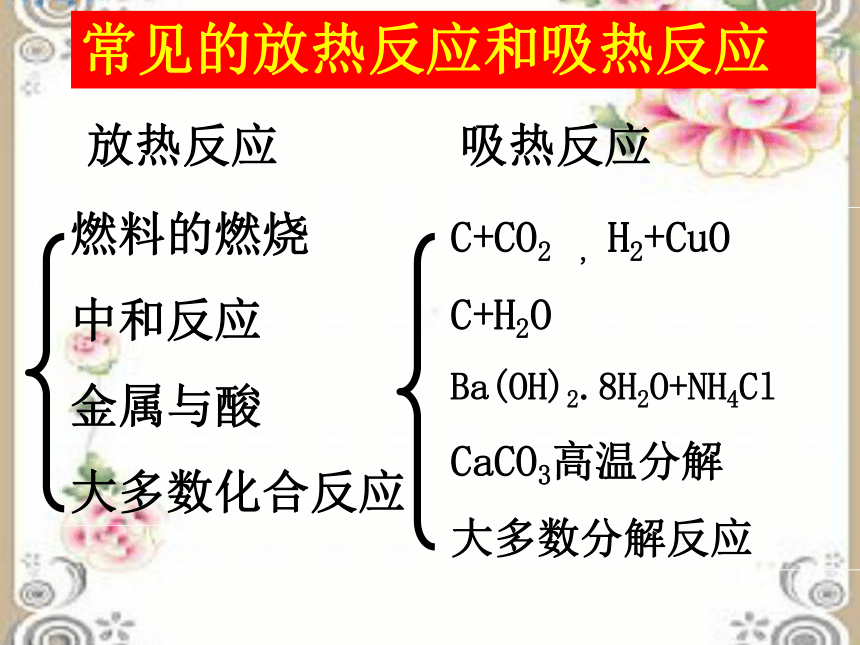
课件64张PPT。化学反应的焓变专题一:化学反应与能量变化第一单元:化学反应中的热效应李德昌吸热反应放热反应化学反应中 热量的反应化学反应中 热量的反应一、放热反应和吸热反应吸收放出常见的放热反应和吸热反应放热反应吸热反应燃料的燃烧
中和反应
金属与酸
大多数化合反应C+CO2 , H2+CuO
C+H2O
Ba(OH)2.8H2O+NH4Cl
CaCO3高温分解
大多数分解反应 为什么有的反应会放出热量有的需要吸收热量呢? 一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于
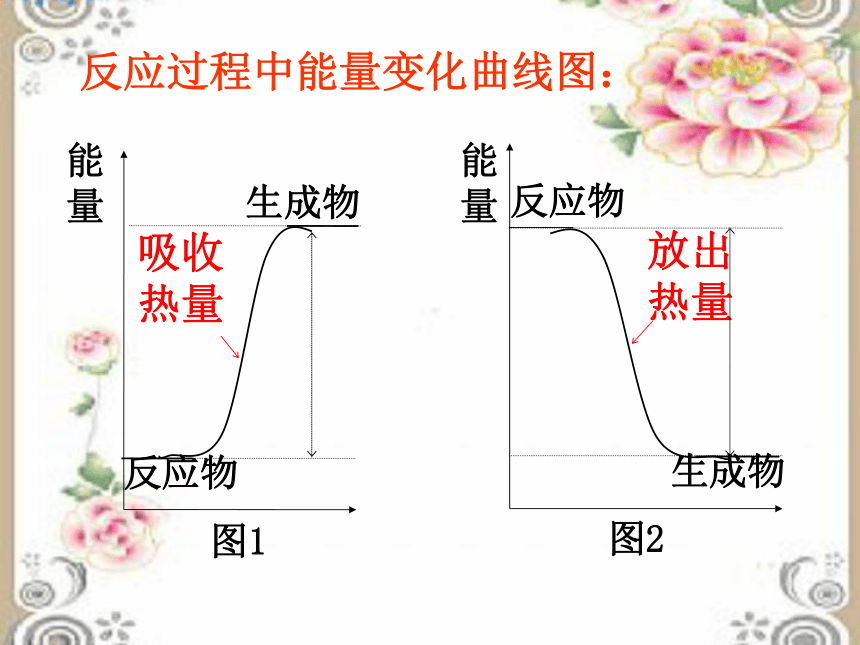
。 反应物的总能量与生成物的总能量的相对大小。问题探究一生成物反应过程中能量变化曲线图:生成物反应物的能量之和
E反生成物的能量之和
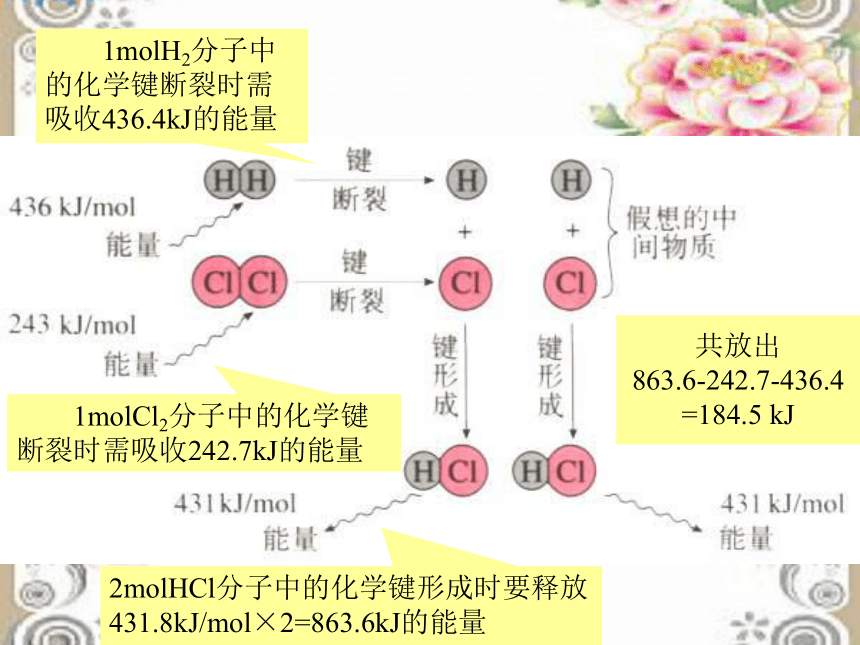
E生(1)若E反> E生,(2)若E反< E生,放出能量吸收能量放热反应吸热反应规 律问题探究二化学反应的本质是什么?化学键的断裂和形成旧键断裂需要 能量,新键形成会 能量。放 出吸 收 1molH2分子中的化学键断裂时需吸收436.4kJ的能量 1molCl2分子中的化学键断裂时需吸收242.7kJ的能量2molHCl分子中的化学键形成时要释放431.8kJ/mol×2=863.6kJ的能量共放出
863.6-242.7-436.4
=184.5 kJ所以:一个化学反应是放热还是吸热取决于取决于所有断键吸收的总能量与所有
形成新键放出的总能量的相对大小二、反应热 焓变1、定义:2、符号:△H3、单位:KJ·mol-1 在恒温、恒压的条件下,化学反应过程中所吸收或释放的热量称为反应的焓变。 化学反应过程中放出或吸收的热量叫做化学反应的反应热.4、规定:吸热反应:△H > 0 或者值为“+”
正号不省略
放热反应:△H < 0 或者值为“-” 表示化学反应中放出或吸收的热量的化学方程式三、热化学方程式问题探究三H2(g)+Cl2(g)=2HCl(g);△H=-184.6KJ/mol H2(g)+ Cl2(g)=HCl(g);△H=-92.3KJ/mol 2H2(g)+O2(g)=2H2O(l);△H=-571.6KJ/mol H2(g)+ O2(g)=H2O(l);△H=-285.8KJ/mol 请观察下列表示氢气在氧气中燃烧生成水的反应热效应的化学方程式,分析其在书写上与化学方程式有何不同。问题探究三 在热化学方程式中,物质前的计量数为什么可以用分数或小数表示呢?它们表示的含义是什么?表示物质的量热化学方程式的意义2H2(g)+O2(g)=2H2O(l) △H=-571.6KJ/mol据此,你能得到什么结论? H2(g)+ O2(g)=H2O(l) △H=-285.8KJ/mol(1)反应热与物质前的计量数有关
(2) 同一化学反应,热化学方程式中同一物质的化学计量数和△H成正比问题探究四 在热化学方程式中,物质的后面为什么要标明该物质的聚集状态呢?2H2(g)+O2(g)=2H2O(l) △H=-571.6KJ/mol2H2(g)+O2(g)=2H2O(g) △H=-483.6KJ/mol 据此,你能得到什么结论?反应热与反应物及生成物的状态有关
反应热还与温度、压强有关课本第3页交流与讨论书写热化学方程式注意事项:
(1)反应物和生成物要标明其聚集状态,用g、l、s分别代表气态、液态、固态。
(2)方程式右端用△H 标明恒压条件下反应放出或吸收的热量,放热为负,吸热为正。
(3)热化学方程式中各物质前的化学计量数不表示分子个数,只表示物质的量,因此可以是整数或分数。
(4)对于相同物质的反应,当化学计量数不同时,其△H 也不同,即△H 的值与计量数成正比。 书写步骤1、写出化学方程式
2、注明反应物和生成物的状态
3、标明反应热△H(注意单位和+、-)
4、注明反应的温度和压强(中学一般不注明)
5、检查写出下列反应的热化学方程式:
1、N2 (g)与H2 (g)反应生成1molNH3 (g) ,放出46.1KJ热量。
2、1molC2H5OH (l)完全 燃烧生成CO2 (g) 和H2O (l) ,放出1366.8KJ热量。
3、2molC2H2 (g)在O2 (g)中完全燃烧生成CO2 (g)和H2O (l) ,放出2598.8KJ热量
4、1molC(石墨)与适量H2O (g)反应生成CO (g)和H2 (g) ,吸收131.3KJ热量。1、下列说法不正确的是 ( )
A、化学反应除了生成新物质外,还伴随着能量的变化
B、放热反应不需要加热即可发生
C、需要加热条件的化学反应都是吸热反应
D、化学反应是吸热还是放热决定于生成物具有的总能量和反应物具有的总能量
E、分解反应肯定是吸热反应
F、物质燃烧放出热量BCE课堂练习2、氢气在氧气中燃烧产生蓝色火焰,已知
破坏1molH-H键消耗的能量为Q1kJ,
破坏1molO = O键消耗的能量为Q2kJ,
形成1molH-O键释放的能量为Q3kJ。
下列关系式中正确的是( )
A. 2Q1 + Q2 > 4Q3
B. 2Q1 + Q2 < 4Q3
C. Q1 + Q2 < Q3
D. Q1 + Q2 = Q3B课堂练习B例1、已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
( )A. H2O(g)=H2(g)+1/2O2(g);ΔH=+242kJ·mol-1
B. 2H2(g)+O2(g)=2H2O(l);ΔH=-484kJ·mol-1
C. H2(g)+1/2O2(g)=H2O(g);ΔH=+242kJ·mol-1
D. 2H2(g)+O2(g)=2H2O(g);ΔH=+484kJ·mol-1 热化学方程式的书写及正误判断课堂复习例2(2003·江苏)已知在25℃、101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ 热量。表示上述反应的热化学方程式正确的是 ( )
A、C8H18(l)+25/2O2(g)=8CO2(g) +9H2O(g)
△H= - 48.40kJ·mol -1
B、C8H18(l)+25/2O2(g)=8CO2 (g) +9H2O(l)
△H= - 5518kJ·mol -1
C、C8H18(l)+25/2O2(g)=8CO2(g) + 9H2O(l)
△H= + 5518kJ·mol -1
D、C8H18(l)+25/2O2(g)=8CO2 (g)+ 9H2O(l)
△H= - 48.40kJ·mol -1B3、已知
(1)H2( g )+1/2O2 ( g ) = H2O ( g ) ΔH1 = a kJ/mol
(2)2H2( g )+O2 ( g ) =2H2O ( g ) ΔH2 = b kJ/mol
(3) H2( g )+1/2O2 ( g ) = H2O ( l ) ΔH3 = c kJ/mol
(4) 2H2( g )+O2 ( g ) =2H2O ( l ) ΔH4 = d kJ/mol
则a、b、c、d的关系正确的是 。
A、ad>0 C、2a=b< 0 D、2c=d>0
C反应热的测量与计算第一单元 化学反应中的热效应第二课时 中和热的测定:H+(aq)+OH-(aq)=H2O(l); △H=?
实验目的: 测定强酸、强碱反应的中和热。
实验原理:
Q=mcΔt ①
Q:中和反应放出的热量。
m:反应混合液的质量。
c:反应混合液的比热容。
Δt:反应前后溶液温度的差值。
Q=(V酸ρ酸+V碱ρ碱)·c·(t2-t1)②
V酸=V碱=50 mL。
c酸=0.50 mol/L c碱=0.55 mol/L
ρ酸=ρ碱=1 g/cm3
c=4.18 J/(g·℃)
Q=0.418(t2-t1)kJ ③
实验步骤
误差分析活动与探究简易测定方法:
大烧杯(500 mL)、小烧杯(100 mL)
温度计、量筒(50 mL)两个、泡沫塑料 或纸条、泡沫塑料板或硬纸板(中心有两个小孔)、环形玻璃搅拌棒。
0.50 mol/L 盐酸、0.55 mol/L NaOH溶液 我们取一定量的盐酸和氢氧化钠溶液发生中和反应,哪些数据可以帮助我们测出它们的反应热呢?请大家讨论回答。Q =m c Δt? ①
Q:中和反应放出的热量。
m:反应混合液的质量。
c:反应混合液的比热容。
Δt:反应前后溶液温度的差值。我们如何得到上述数据呢?m的质量为所用酸、碱的质量和,测出参加反应的酸、碱质量相加即可;c 需要查阅,Δt可用温度计测出反应前后的温度相减得到。[问]酸、碱反应时,我们用的是它的稀溶液,它们的质量应怎样得到?量出它们的体积,再乘以它们的密度即可。 Q =(V酸ρ酸+V碱ρ碱)·c·(t2-t1) ② 本实验中,我们所用一元酸、一元碱的体积均为50 mL,它 们的浓度分别为0.50 mol/L和0.55 mol/L。由于是稀溶液,且为了计算简便,我们近似地认为,所用酸、碱溶液的密度均为1 g/cm3,且中和后所得溶液的比热容为 4.18 J/(g·℃)已知 V酸=V碱=50 mL。
c酸=0.50 mol/L c碱=0.55 mol/L。
ρ酸=ρ碱=1 g/cm3
c=4.18 J/(g·℃)
请把以上数据代入式②,得出Q的表示式。其中热量的单位用kJ。 得出结果。 Q = 0.418(t2-t1)kJ ③思考:③式表示的是不是该反应的反应热?是中和热吗?为什么?③式不是该反应的反应热,因为反应热是有正负的,中和反应放热,故其ΔH为“-”。中和热是稀的酸、碱中和生成 1 mol水的反应热,而50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L 氢氧化钠反应后生成的水只有0.025 mol,故③式表示的也不是中和热。 [问题]该反应的中和热应怎样表示呢?实验步骤:1.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,如下图所示。 中和热的测定
大、小烧杯放置时,为何要使两杯口相平?填碎纸条的作用是什么?对此装置,你有何更好的建议?答案:.两杯口相平,可使盖板把杯口尽量盖严,从而减少热量损失;填碎纸条的作用是为了达到保温隔热、减少实验过程中热量损失的目的。若换用隔热、密封性能更好的装置(如保温杯)会使实验结果更准确。2.用一个量筒最取50 mL 0.50 mol/L盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记入下表。然后把温度计上的酸用水冲洗干净。 温度计上的酸为何要用水冲洗干净?冲洗后的溶液能否倒入小烧杯?为什么? 因为该温度计还要用来测碱液的温度,若不冲洗,温度计上的酸会和碱发生中和反应而使热量散失,故要冲洗干净;冲洗后的溶液不能倒入小烧杯,若倒入,会使总溶液的质量增加,而导致实验结果误差。3.用另一个量筒量取50 mL 0.55 mol/L NaOH溶液,并用温度计测量NaOH溶液的温度,记入下表。.酸、碱混合时,为何要把量筒中的NaOH溶液一次倒入小烧杯而不能缓缓倒入?. 因为本实验的关键是测反应的反应热,若动作迟缓,将会使热量损失而使误差增大。4.把温度计和环形玻璃搅拌棒放入小烧杯的盐酸中,并把量筒中的NaOH溶液一次倒入小烧杯(注意不要洒到外面)。用环形玻璃搅拌棒轻轻搅动溶液,并准确读取混合溶液的最高温度,记为终止温度,记入下表。 实验中所用HCl和NaOH的物质的量比为何不是1∶1而是NaOH过量?若用HCl过量行吗? 为了保证0.50 mol/L的盐酸完全被NaOH中和,采用0.55 mol/L NaOH溶液,使碱稍稍过量。若使盐酸过量,亦可。5.重复实验两次,取测量所得数据的平均值作为计算依据。 [议一议]你所测得的数据是否为57.3 kJ/mol,若不是,分析产生误差的原因。可能的原因有:
1.量取溶液的体积有误差(测量结果是按50 mL的酸、碱进行计算,若实际量取时,多于50 mL或小于50 mL都会造成误差)
2.温度计的读数有误。
3.实验过程中有液体洒在外面。
4.混合酸、碱溶液时,动作缓慢,导致实验误差。
5.隔热操作不到位,致使实验过程中热量损失而导致误差。
6.测了酸后的温度计未用水清洗而便立即去测碱的温度,致使热量损失而引起误差。 讨论下列问题 1.本实验中若把50 mL 0.50 mol/L的盐酸改为50 mL 0.50 mol/L醋酸,所测结果是否会有所变化?为什么?
2.若改用100 mL 0.50 mol/L的盐酸和100 mL 0.55 mol/L的NaOH溶液,所测中和热的数值是否约为本实验结果的二倍(假定各步操作没有失误)?答案:1.会有所变化。因为醋酸为弱电解质,其电离时要吸热,故将使测得结果偏小。
2.否。因中和热是指酸与碱发生中和反应生成1 mol H2O时放出的热量,其数值与反应物的量的多少无关,故所测结果应基本和本次实验结果相同(若所有操作都准确无误,且无热量损失,则二者结果相同)。[练习]50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L-1 NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”“偏小”“无影响”)。
(4)实验中改用60 mL 0.50 mol/L盐酸跟50 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”“不相等”),所求中和热 (填“相等”“不相等”),简述理由: 。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会 ;用50 mL 0.50mol/L NaOH溶液进行上述实验,测得的中和热的数值会 。(均填“偏大”“偏小”“无影响”)环形玻璃搅拌棒减少实验过程中的热量损失偏小不等相等 因为中和热是指酸跟碱发生中和反应生成1 mol H2O所放出的能量,与酸碱的用量无关)偏小)偏小 ①C(s)+1/2O2(g)==CO(g) ΔH1=?
②CO(g)+1/2O2(g)== CO2(g) ΔH2=-283.0kJ/mol
③C(s)+O2(g)==CO2(g) ΔH3=-393.5kJ/mol
① + ② = ③ ,
则 ΔH1 + ΔH2 =ΔH3
ΔH1 =ΔH3 -ΔH2 = - 393.5kJ/mol + 283.0kJ/mol
= - 110.5kJ/mol如何测出这个反应的反应热:
(1)C(s)+1/2O2(g) = CO(g) ΔH1=?盖斯定律 不管化学反应是分一步完成或分几步完成,其反应热是相同的。
化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。如何理解盖斯定律?ΔH、ΔH1、ΔH2之间有何关系?ΔH=ΔH1+ΔH2BΔH 若多步化学反应相加可得到新的化学反应,则新反应的反应热即为上述多步反应的反应热之和。总结规律:注意:
1、计量数的变化与反应热数值的变化要对应
2、反应方向发生改变反应热的符号也要改变总结思考:
在用方程式叠加计算反应热时要注意哪些问题?有关热化学方程式的计算在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g)+O2(g)=2CO2(g); △H=-566KJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890KJ/mol
由1摩尔CO和3摩尔CH4组成的混和气在上述条件下完全燃烧时,释放的热量为( )
A.2912KJ B.2953KJ
C.3236KJ D.3867KJB0.5×566+3×890=2953 为什么要讨论反应热的计算?
1、有些反应热无法或很难精确测量
2、工业生产的需要
(1)燃料的燃烧
(2)反应条件的控制
(3)“废热”的利用如何计算C燃烧生成CO的燃烧热?反应热计算的常见题型:
1、化学反应中物质的量的变化与反应能量变化的定量计算。
2、理论推算反应热:
依据:物质变化决定能量变化
(1)盖斯定律
(2)通过已知热化学方程式的相加,得出新的热化学方程式:
设计合理路径
路径1总能量变化等于路径2总能量变化物质的叠加,反应热的叠加阅读课本P7,总结用盖斯定律进行计算的过程,并仿照课本的计算过程做以下练习:例1、已知: H2O(g)==H2O(l) △H2=-44kJ/mol
H2(g)+1/2O2(g)==H2O(g) △H1=-241.8kJ/mol
那么,H2的燃烧热△H是多少?H2(g)+1/2O2(g)==H2O(l) △H=?kJ/mol△H=△H1+△H2=-285.8kJ/mol你知道神六的火箭燃料是什么吗?例2、某次发射火箭,用N2H4(肼)在NO2中燃烧,生成N2、液态H2O。已知:
N2(g)+2O2(g)==2NO2(g) △H1=+67.2kJ/mol
N2H4(g)+O2(g)==N2(g)+2H2O(l) △H2=-534kJ/mol
假如都在相同状态下,请写出发射火箭反应的热化学方程式。2 N2H4(g)+ 2NO2(g)= 3N2(g)+4H2O(l)
△H=-1135.2kJ/mol
你写对了吗?例3、同素异形体相互转化但反应热相当小而且转化速率慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的观点“不管化学反应是一步完成或分几步完成,这个总过程的热效应是相同的”。已知:P4(s、白磷)+5O2(g)=P4O10(s); = -2983.2 kJ/molP(s、红磷)+5/4O2(g)=1/4P4O10(s); = -738.5 kJ/mol试写出白磷转化为红磷的热化学方程式
。 盖斯定律的应用根据下列反应的焓变,计算C(石墨)与H2(g)反应生成1molC2H2(g)的焓变:
C(石墨)+O2(g)=CO2(g) △H=-393.5KJ/mol
2H2(g)+O2(g)=2H2O(l) △H=-571.6KJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2599.2KJ/mol问题解决二:若某一化学反应可分为多步进行,则其总反应热为各步反应的反应热之和。
即△H= △H1+ △H2+ △H3+……一: 若某化学反应从始态(S)到终态(L)其反应热为△H,而从终态(L)到始态(S)的反应热为△H ’,这两者和为0。
即△H+ △H ’ = 0三:若多步化学反应相加可得到新的化学反应,则新反应的反应热即为上述多步反应的反应热之和。小结:请预习第三部分:能源的充分利用化学选修4 第一单元 化学反应与能量变化能源的充分利用第三课时
复习:若2.6 g 乙炔(C2H2,气态)完全燃烧生成液态水和CO2(g)时放热130 kJ。则乙炔燃烧的热化学方程式为: C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l)ΔH=-1300 kJ/mol或:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)
ΔH=-2600 kJ/mol
看看:你写对了吗?一、标准燃烧热与热值 在101 kPa下,1 mol 物质完全燃烧的反应热,叫做该物质的标准燃烧热。在101KPa下,1g物质完全燃烧的反应热叫做该物质的热值。关于燃烧热的理解:
①研究条件: 25℃ ,101 kPa
②反应程度:完全燃烧
③燃烧物的物质的量:1 mol
④研究内容:放出的热量。(ΔH<0,单位kJ/mol)
⑤在未有特别说明的情况下,外界压强一般指25℃ ,101 kPa.所谓完全燃烧也是完全氧化,它是指物质中的下列元素完全转变成对应的稳定物
如:C→CO2(g);H→H2O(l);S→SO2(g);Cl→HCl(g);N→N2(g)H2(g)+ O2(g)== H2O(l);ΔH= -285.8kJ/mol 由于计算燃烧热时,可燃物质是以1 mol 作为标准来计算的,所以热化学方程式的化学计量系数常出现分数。二、燃烧热的计算及应用
[例题]1.在101 kPa时,1 mol CH4 完全燃烧生成CO2和液态H2O,放出890.3 kJ的热量,试写出CH4燃烧的热化学方程式。1000 L CH4(标准状况)燃烧后所产生的热量为多少? 解析:根据题意,在101 kPa时,1 mol CH4完全燃烧的热化学方程式为:
CH4(g)+2O2(g)==CO2(g)+2H2O(l)ΔH=-890.3 kJ/mol
即CH4的燃烧热为890.3 kJ/mol。
1 000 L CH4(标准状况)的物质的量为:
n(CH4)=1000L÷22.4L·mol-1=44.6 mol
1 mol CH4 完全燃烧放出890.3 kJ的热量,
44.6 mol CH4 完全燃烧放出的热量为:
44.6 mol×890.3 kJ/mol=3.97×104 kJ
答案:CH4的燃烧热为890.3 kJ/mol,1 000 L CH4(标准状况)完全燃烧产生的热量为3.97×104 kJ。将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一。C+H2O=CO+H2
已知:C(s)+O2(g)=CO2(g) △H1=-393.5KJ/mol
H2(g)+1/2O2(g)=H2O(g) △H2=-241.8KJ/mol
CO(g)+1/2O2(g)=CO2(g) △H3=-283.0KJ/mol
甲同学认为:“煤燃烧时加少量的水,可以使煤炭燃烧放出更多的热量。”
乙同学认为:“将煤转化为水煤气再燃烧放出的热量与直接燃烧煤放出的热量一样,而将煤转化为水煤气会增加消耗,因此,将煤转化为水煤气得不偿失。”
你认为他们说得有道理吗?交流与讨论三、能源利用与节能措施 能源就是能提供能量的自然资源,包括化石燃料(煤、石油、天然气)、阳光、风力、流水、潮汐以及柴草等。能源的开发和利用可以用来衡量一个国家或地区的经济发展和科学技术水平。
煤、石油、天然气是当今世界上重要的化石燃料。 但它们的蕴藏有限,且不可再生。解决的办法 :开源节流。即开发新能源,节约现有能源,提高能源的利用率。 节约能源的重要措施:
科学地控制燃烧反应,使燃料充分燃烧,提高能源的利用率。资料卡通过降低反应温度的节能措施——P10阅读材料[问题探讨]1.燃料充分燃烧的条件是什么? 2.燃料燃烧时,若空气过量或不足,会造 成什么后果?3.为什么固体燃料要粉碎后使用?1.使燃料充分燃烧的措施:
(1)通入充足且适量的空气;
(2)固体燃料粉碎、液体燃料喷雾以增大燃料与空气的接触面。四、新能源的开发 1.燃料电池,2.氢能, 3.太阳能, 4.风能,生物能、核能、地热能、潮汐能等 讨论:有一种观点认为:与燃烧化石燃料相比,以乙醇为燃料不会增加大气中二氧化碳的含量。你认为这种观点是否正确?请根据乙醇的来源说明理由。谢谢!
中和反应
金属与酸
大多数化合反应C+CO2 , H2+CuO
C+H2O
Ba(OH)2.8H2O+NH4Cl
CaCO3高温分解
大多数分解反应 为什么有的反应会放出热量有的需要吸收热量呢? 一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于
。 反应物的总能量与生成物的总能量的相对大小。问题探究一生成物反应过程中能量变化曲线图:生成物反应物的能量之和
E反生成物的能量之和
E生(1)若E反> E生,(2)若E反< E生,放出能量吸收能量放热反应吸热反应规 律问题探究二化学反应的本质是什么?化学键的断裂和形成旧键断裂需要 能量,新键形成会 能量。放 出吸 收 1molH2分子中的化学键断裂时需吸收436.4kJ的能量 1molCl2分子中的化学键断裂时需吸收242.7kJ的能量2molHCl分子中的化学键形成时要释放431.8kJ/mol×2=863.6kJ的能量共放出
863.6-242.7-436.4
=184.5 kJ所以:一个化学反应是放热还是吸热取决于取决于所有断键吸收的总能量与所有
形成新键放出的总能量的相对大小二、反应热 焓变1、定义:2、符号:△H3、单位:KJ·mol-1 在恒温、恒压的条件下,化学反应过程中所吸收或释放的热量称为反应的焓变。 化学反应过程中放出或吸收的热量叫做化学反应的反应热.4、规定:吸热反应:△H > 0 或者值为“+”
正号不省略
放热反应:△H < 0 或者值为“-” 表示化学反应中放出或吸收的热量的化学方程式三、热化学方程式问题探究三H2(g)+Cl2(g)=2HCl(g);△H=-184.6KJ/mol H2(g)+ Cl2(g)=HCl(g);△H=-92.3KJ/mol 2H2(g)+O2(g)=2H2O(l);△H=-571.6KJ/mol H2(g)+ O2(g)=H2O(l);△H=-285.8KJ/mol 请观察下列表示氢气在氧气中燃烧生成水的反应热效应的化学方程式,分析其在书写上与化学方程式有何不同。问题探究三 在热化学方程式中,物质前的计量数为什么可以用分数或小数表示呢?它们表示的含义是什么?表示物质的量热化学方程式的意义2H2(g)+O2(g)=2H2O(l) △H=-571.6KJ/mol据此,你能得到什么结论? H2(g)+ O2(g)=H2O(l) △H=-285.8KJ/mol(1)反应热与物质前的计量数有关
(2) 同一化学反应,热化学方程式中同一物质的化学计量数和△H成正比问题探究四 在热化学方程式中,物质的后面为什么要标明该物质的聚集状态呢?2H2(g)+O2(g)=2H2O(l) △H=-571.6KJ/mol2H2(g)+O2(g)=2H2O(g) △H=-483.6KJ/mol 据此,你能得到什么结论?反应热与反应物及生成物的状态有关
反应热还与温度、压强有关课本第3页交流与讨论书写热化学方程式注意事项:
(1)反应物和生成物要标明其聚集状态,用g、l、s分别代表气态、液态、固态。
(2)方程式右端用△H 标明恒压条件下反应放出或吸收的热量,放热为负,吸热为正。
(3)热化学方程式中各物质前的化学计量数不表示分子个数,只表示物质的量,因此可以是整数或分数。
(4)对于相同物质的反应,当化学计量数不同时,其△H 也不同,即△H 的值与计量数成正比。 书写步骤1、写出化学方程式
2、注明反应物和生成物的状态
3、标明反应热△H(注意单位和+、-)
4、注明反应的温度和压强(中学一般不注明)
5、检查写出下列反应的热化学方程式:
1、N2 (g)与H2 (g)反应生成1molNH3 (g) ,放出46.1KJ热量。
2、1molC2H5OH (l)完全 燃烧生成CO2 (g) 和H2O (l) ,放出1366.8KJ热量。
3、2molC2H2 (g)在O2 (g)中完全燃烧生成CO2 (g)和H2O (l) ,放出2598.8KJ热量
4、1molC(石墨)与适量H2O (g)反应生成CO (g)和H2 (g) ,吸收131.3KJ热量。1、下列说法不正确的是 ( )
A、化学反应除了生成新物质外,还伴随着能量的变化
B、放热反应不需要加热即可发生
C、需要加热条件的化学反应都是吸热反应
D、化学反应是吸热还是放热决定于生成物具有的总能量和反应物具有的总能量
E、分解反应肯定是吸热反应
F、物质燃烧放出热量BCE课堂练习2、氢气在氧气中燃烧产生蓝色火焰,已知
破坏1molH-H键消耗的能量为Q1kJ,
破坏1molO = O键消耗的能量为Q2kJ,
形成1molH-O键释放的能量为Q3kJ。
下列关系式中正确的是( )
A. 2Q1 + Q2 > 4Q3
B. 2Q1 + Q2 < 4Q3
C. Q1 + Q2 < Q3
D. Q1 + Q2 = Q3B课堂练习B例1、已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
( )A. H2O(g)=H2(g)+1/2O2(g);ΔH=+242kJ·mol-1
B. 2H2(g)+O2(g)=2H2O(l);ΔH=-484kJ·mol-1
C. H2(g)+1/2O2(g)=H2O(g);ΔH=+242kJ·mol-1
D. 2H2(g)+O2(g)=2H2O(g);ΔH=+484kJ·mol-1 热化学方程式的书写及正误判断课堂复习例2(2003·江苏)已知在25℃、101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ 热量。表示上述反应的热化学方程式正确的是 ( )
A、C8H18(l)+25/2O2(g)=8CO2(g) +9H2O(g)
△H= - 48.40kJ·mol -1
B、C8H18(l)+25/2O2(g)=8CO2 (g) +9H2O(l)
△H= - 5518kJ·mol -1
C、C8H18(l)+25/2O2(g)=8CO2(g) + 9H2O(l)
△H= + 5518kJ·mol -1
D、C8H18(l)+25/2O2(g)=8CO2 (g)+ 9H2O(l)
△H= - 48.40kJ·mol -1B3、已知
(1)H2( g )+1/2O2 ( g ) = H2O ( g ) ΔH1 = a kJ/mol
(2)2H2( g )+O2 ( g ) =2H2O ( g ) ΔH2 = b kJ/mol
(3) H2( g )+1/2O2 ( g ) = H2O ( l ) ΔH3 = c kJ/mol
(4) 2H2( g )+O2 ( g ) =2H2O ( l ) ΔH4 = d kJ/mol
则a、b、c、d的关系正确的是 。
A、a
C反应热的测量与计算第一单元 化学反应中的热效应第二课时 中和热的测定:H+(aq)+OH-(aq)=H2O(l); △H=?
实验目的: 测定强酸、强碱反应的中和热。
实验原理:
Q=mcΔt ①
Q:中和反应放出的热量。
m:反应混合液的质量。
c:反应混合液的比热容。
Δt:反应前后溶液温度的差值。
Q=(V酸ρ酸+V碱ρ碱)·c·(t2-t1)②
V酸=V碱=50 mL。
c酸=0.50 mol/L c碱=0.55 mol/L
ρ酸=ρ碱=1 g/cm3
c=4.18 J/(g·℃)
Q=0.418(t2-t1)kJ ③
实验步骤
误差分析活动与探究简易测定方法:
大烧杯(500 mL)、小烧杯(100 mL)
温度计、量筒(50 mL)两个、泡沫塑料 或纸条、泡沫塑料板或硬纸板(中心有两个小孔)、环形玻璃搅拌棒。
0.50 mol/L 盐酸、0.55 mol/L NaOH溶液 我们取一定量的盐酸和氢氧化钠溶液发生中和反应,哪些数据可以帮助我们测出它们的反应热呢?请大家讨论回答。Q =m c Δt? ①
Q:中和反应放出的热量。
m:反应混合液的质量。
c:反应混合液的比热容。
Δt:反应前后溶液温度的差值。我们如何得到上述数据呢?m的质量为所用酸、碱的质量和,测出参加反应的酸、碱质量相加即可;c 需要查阅,Δt可用温度计测出反应前后的温度相减得到。[问]酸、碱反应时,我们用的是它的稀溶液,它们的质量应怎样得到?量出它们的体积,再乘以它们的密度即可。 Q =(V酸ρ酸+V碱ρ碱)·c·(t2-t1) ② 本实验中,我们所用一元酸、一元碱的体积均为50 mL,它 们的浓度分别为0.50 mol/L和0.55 mol/L。由于是稀溶液,且为了计算简便,我们近似地认为,所用酸、碱溶液的密度均为1 g/cm3,且中和后所得溶液的比热容为 4.18 J/(g·℃)已知 V酸=V碱=50 mL。
c酸=0.50 mol/L c碱=0.55 mol/L。
ρ酸=ρ碱=1 g/cm3
c=4.18 J/(g·℃)
请把以上数据代入式②,得出Q的表示式。其中热量的单位用kJ。 得出结果。 Q = 0.418(t2-t1)kJ ③思考:③式表示的是不是该反应的反应热?是中和热吗?为什么?③式不是该反应的反应热,因为反应热是有正负的,中和反应放热,故其ΔH为“-”。中和热是稀的酸、碱中和生成 1 mol水的反应热,而50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L 氢氧化钠反应后生成的水只有0.025 mol,故③式表示的也不是中和热。 [问题]该反应的中和热应怎样表示呢?实验步骤:1.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,如下图所示。 中和热的测定
大、小烧杯放置时,为何要使两杯口相平?填碎纸条的作用是什么?对此装置,你有何更好的建议?答案:.两杯口相平,可使盖板把杯口尽量盖严,从而减少热量损失;填碎纸条的作用是为了达到保温隔热、减少实验过程中热量损失的目的。若换用隔热、密封性能更好的装置(如保温杯)会使实验结果更准确。2.用一个量筒最取50 mL 0.50 mol/L盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记入下表。然后把温度计上的酸用水冲洗干净。 温度计上的酸为何要用水冲洗干净?冲洗后的溶液能否倒入小烧杯?为什么? 因为该温度计还要用来测碱液的温度,若不冲洗,温度计上的酸会和碱发生中和反应而使热量散失,故要冲洗干净;冲洗后的溶液不能倒入小烧杯,若倒入,会使总溶液的质量增加,而导致实验结果误差。3.用另一个量筒量取50 mL 0.55 mol/L NaOH溶液,并用温度计测量NaOH溶液的温度,记入下表。.酸、碱混合时,为何要把量筒中的NaOH溶液一次倒入小烧杯而不能缓缓倒入?. 因为本实验的关键是测反应的反应热,若动作迟缓,将会使热量损失而使误差增大。4.把温度计和环形玻璃搅拌棒放入小烧杯的盐酸中,并把量筒中的NaOH溶液一次倒入小烧杯(注意不要洒到外面)。用环形玻璃搅拌棒轻轻搅动溶液,并准确读取混合溶液的最高温度,记为终止温度,记入下表。 实验中所用HCl和NaOH的物质的量比为何不是1∶1而是NaOH过量?若用HCl过量行吗? 为了保证0.50 mol/L的盐酸完全被NaOH中和,采用0.55 mol/L NaOH溶液,使碱稍稍过量。若使盐酸过量,亦可。5.重复实验两次,取测量所得数据的平均值作为计算依据。 [议一议]你所测得的数据是否为57.3 kJ/mol,若不是,分析产生误差的原因。可能的原因有:
1.量取溶液的体积有误差(测量结果是按50 mL的酸、碱进行计算,若实际量取时,多于50 mL或小于50 mL都会造成误差)
2.温度计的读数有误。
3.实验过程中有液体洒在外面。
4.混合酸、碱溶液时,动作缓慢,导致实验误差。
5.隔热操作不到位,致使实验过程中热量损失而导致误差。
6.测了酸后的温度计未用水清洗而便立即去测碱的温度,致使热量损失而引起误差。 讨论下列问题 1.本实验中若把50 mL 0.50 mol/L的盐酸改为50 mL 0.50 mol/L醋酸,所测结果是否会有所变化?为什么?
2.若改用100 mL 0.50 mol/L的盐酸和100 mL 0.55 mol/L的NaOH溶液,所测中和热的数值是否约为本实验结果的二倍(假定各步操作没有失误)?答案:1.会有所变化。因为醋酸为弱电解质,其电离时要吸热,故将使测得结果偏小。
2.否。因中和热是指酸与碱发生中和反应生成1 mol H2O时放出的热量,其数值与反应物的量的多少无关,故所测结果应基本和本次实验结果相同(若所有操作都准确无误,且无热量损失,则二者结果相同)。[练习]50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L-1 NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”“偏小”“无影响”)。
(4)实验中改用60 mL 0.50 mol/L盐酸跟50 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”“不相等”),所求中和热 (填“相等”“不相等”),简述理由: 。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会 ;用50 mL 0.50mol/L NaOH溶液进行上述实验,测得的中和热的数值会 。(均填“偏大”“偏小”“无影响”)环形玻璃搅拌棒减少实验过程中的热量损失偏小不等相等 因为中和热是指酸跟碱发生中和反应生成1 mol H2O所放出的能量,与酸碱的用量无关)偏小)偏小 ①C(s)+1/2O2(g)==CO(g) ΔH1=?
②CO(g)+1/2O2(g)== CO2(g) ΔH2=-283.0kJ/mol
③C(s)+O2(g)==CO2(g) ΔH3=-393.5kJ/mol
① + ② = ③ ,
则 ΔH1 + ΔH2 =ΔH3
ΔH1 =ΔH3 -ΔH2 = - 393.5kJ/mol + 283.0kJ/mol
= - 110.5kJ/mol如何测出这个反应的反应热:
(1)C(s)+1/2O2(g) = CO(g) ΔH1=?盖斯定律 不管化学反应是分一步完成或分几步完成,其反应热是相同的。
化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。如何理解盖斯定律?ΔH、ΔH1、ΔH2之间有何关系?ΔH=ΔH1+ΔH2BΔH 若多步化学反应相加可得到新的化学反应,则新反应的反应热即为上述多步反应的反应热之和。总结规律:注意:
1、计量数的变化与反应热数值的变化要对应
2、反应方向发生改变反应热的符号也要改变总结思考:
在用方程式叠加计算反应热时要注意哪些问题?有关热化学方程式的计算在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g)+O2(g)=2CO2(g); △H=-566KJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890KJ/mol
由1摩尔CO和3摩尔CH4组成的混和气在上述条件下完全燃烧时,释放的热量为( )
A.2912KJ B.2953KJ
C.3236KJ D.3867KJB0.5×566+3×890=2953 为什么要讨论反应热的计算?
1、有些反应热无法或很难精确测量
2、工业生产的需要
(1)燃料的燃烧
(2)反应条件的控制
(3)“废热”的利用如何计算C燃烧生成CO的燃烧热?反应热计算的常见题型:
1、化学反应中物质的量的变化与反应能量变化的定量计算。
2、理论推算反应热:
依据:物质变化决定能量变化
(1)盖斯定律
(2)通过已知热化学方程式的相加,得出新的热化学方程式:
设计合理路径
路径1总能量变化等于路径2总能量变化物质的叠加,反应热的叠加阅读课本P7,总结用盖斯定律进行计算的过程,并仿照课本的计算过程做以下练习:例1、已知: H2O(g)==H2O(l) △H2=-44kJ/mol
H2(g)+1/2O2(g)==H2O(g) △H1=-241.8kJ/mol
那么,H2的燃烧热△H是多少?H2(g)+1/2O2(g)==H2O(l) △H=?kJ/mol△H=△H1+△H2=-285.8kJ/mol你知道神六的火箭燃料是什么吗?例2、某次发射火箭,用N2H4(肼)在NO2中燃烧,生成N2、液态H2O。已知:
N2(g)+2O2(g)==2NO2(g) △H1=+67.2kJ/mol
N2H4(g)+O2(g)==N2(g)+2H2O(l) △H2=-534kJ/mol
假如都在相同状态下,请写出发射火箭反应的热化学方程式。2 N2H4(g)+ 2NO2(g)= 3N2(g)+4H2O(l)
△H=-1135.2kJ/mol
你写对了吗?例3、同素异形体相互转化但反应热相当小而且转化速率慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的观点“不管化学反应是一步完成或分几步完成,这个总过程的热效应是相同的”。已知:P4(s、白磷)+5O2(g)=P4O10(s); = -2983.2 kJ/molP(s、红磷)+5/4O2(g)=1/4P4O10(s); = -738.5 kJ/mol试写出白磷转化为红磷的热化学方程式
。 盖斯定律的应用根据下列反应的焓变,计算C(石墨)与H2(g)反应生成1molC2H2(g)的焓变:
C(石墨)+O2(g)=CO2(g) △H=-393.5KJ/mol
2H2(g)+O2(g)=2H2O(l) △H=-571.6KJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2599.2KJ/mol问题解决二:若某一化学反应可分为多步进行,则其总反应热为各步反应的反应热之和。
即△H= △H1+ △H2+ △H3+……一: 若某化学反应从始态(S)到终态(L)其反应热为△H,而从终态(L)到始态(S)的反应热为△H ’,这两者和为0。
即△H+ △H ’ = 0三:若多步化学反应相加可得到新的化学反应,则新反应的反应热即为上述多步反应的反应热之和。小结:请预习第三部分:能源的充分利用化学选修4 第一单元 化学反应与能量变化能源的充分利用第三课时
复习:若2.6 g 乙炔(C2H2,气态)完全燃烧生成液态水和CO2(g)时放热130 kJ。则乙炔燃烧的热化学方程式为: C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l)ΔH=-1300 kJ/mol或:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)
ΔH=-2600 kJ/mol
看看:你写对了吗?一、标准燃烧热与热值 在101 kPa下,1 mol 物质完全燃烧的反应热,叫做该物质的标准燃烧热。在101KPa下,1g物质完全燃烧的反应热叫做该物质的热值。关于燃烧热的理解:
①研究条件: 25℃ ,101 kPa
②反应程度:完全燃烧
③燃烧物的物质的量:1 mol
④研究内容:放出的热量。(ΔH<0,单位kJ/mol)
⑤在未有特别说明的情况下,外界压强一般指25℃ ,101 kPa.所谓完全燃烧也是完全氧化,它是指物质中的下列元素完全转变成对应的稳定物
如:C→CO2(g);H→H2O(l);S→SO2(g);Cl→HCl(g);N→N2(g)H2(g)+ O2(g)== H2O(l);ΔH= -285.8kJ/mol 由于计算燃烧热时,可燃物质是以1 mol 作为标准来计算的,所以热化学方程式的化学计量系数常出现分数。二、燃烧热的计算及应用
[例题]1.在101 kPa时,1 mol CH4 完全燃烧生成CO2和液态H2O,放出890.3 kJ的热量,试写出CH4燃烧的热化学方程式。1000 L CH4(标准状况)燃烧后所产生的热量为多少? 解析:根据题意,在101 kPa时,1 mol CH4完全燃烧的热化学方程式为:
CH4(g)+2O2(g)==CO2(g)+2H2O(l)ΔH=-890.3 kJ/mol
即CH4的燃烧热为890.3 kJ/mol。
1 000 L CH4(标准状况)的物质的量为:
n(CH4)=1000L÷22.4L·mol-1=44.6 mol
1 mol CH4 完全燃烧放出890.3 kJ的热量,
44.6 mol CH4 完全燃烧放出的热量为:
44.6 mol×890.3 kJ/mol=3.97×104 kJ
答案:CH4的燃烧热为890.3 kJ/mol,1 000 L CH4(标准状况)完全燃烧产生的热量为3.97×104 kJ。将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一。C+H2O=CO+H2
已知:C(s)+O2(g)=CO2(g) △H1=-393.5KJ/mol
H2(g)+1/2O2(g)=H2O(g) △H2=-241.8KJ/mol
CO(g)+1/2O2(g)=CO2(g) △H3=-283.0KJ/mol
甲同学认为:“煤燃烧时加少量的水,可以使煤炭燃烧放出更多的热量。”
乙同学认为:“将煤转化为水煤气再燃烧放出的热量与直接燃烧煤放出的热量一样,而将煤转化为水煤气会增加消耗,因此,将煤转化为水煤气得不偿失。”
你认为他们说得有道理吗?交流与讨论三、能源利用与节能措施 能源就是能提供能量的自然资源,包括化石燃料(煤、石油、天然气)、阳光、风力、流水、潮汐以及柴草等。能源的开发和利用可以用来衡量一个国家或地区的经济发展和科学技术水平。
煤、石油、天然气是当今世界上重要的化石燃料。 但它们的蕴藏有限,且不可再生。解决的办法 :开源节流。即开发新能源,节约现有能源,提高能源的利用率。 节约能源的重要措施:
科学地控制燃烧反应,使燃料充分燃烧,提高能源的利用率。资料卡通过降低反应温度的节能措施——P10阅读材料[问题探讨]1.燃料充分燃烧的条件是什么? 2.燃料燃烧时,若空气过量或不足,会造 成什么后果?3.为什么固体燃料要粉碎后使用?1.使燃料充分燃烧的措施:
(1)通入充足且适量的空气;
(2)固体燃料粉碎、液体燃料喷雾以增大燃料与空气的接触面。四、新能源的开发 1.燃料电池,2.氢能, 3.太阳能, 4.风能,生物能、核能、地热能、潮汐能等 讨论:有一种观点认为:与燃烧化石燃料相比,以乙醇为燃料不会增加大气中二氧化碳的含量。你认为这种观点是否正确?请根据乙醇的来源说明理由。谢谢!
