第十一单元课题1生活中常见的盐综合训练-2021-2022学年九年级化学人教版下册(word版有答案)
文档属性
| 名称 | 第十一单元课题1生活中常见的盐综合训练-2021-2022学年九年级化学人教版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-23 00:00:00 | ||
图片预览


文档简介
初三化学下册第十一单元课题1 生活中常见的盐 综合训练
一、选择题
1.将珍珠放入稀盐酸中,产生能使澄清石灰水变浑浊的气体,则珍珠中可能含有( )
A.氢氧根离子 B.碳酸根离子 C.硝酸根离子 D.硫酸根离子
2. 下列选项中各种溶质的溶液混合,无明显现象的是( )
A.NaOH、KCl、Fe2(SO4)3 B.KNO3、AgNO3、NaCl
C.H2SO4、K2SO4、HNO3 D.KCl、H2SO4、Na2CO3
3.下列各组溶液,不用其他试剂就能鉴别出来的是( )
A.MgSO4、NaOH、NaCl、BaCl2
B.NaNO3、KNO3、FeCl3、NaOH
C.Na2CO3、HCl、CaCl2、KNO3
D.BaCl2、Na2CO3、Na2SO4、KNO3
4. 下列各组离子在水中能大量共存,并形成无色溶液的是( )
A.H+、Na+、CO
B.Ba2+、CO、Cl-
C.Fe2+、H+、SO
D.K+、Ca2+、Cl-
5.食盐NaCl是我们生活中的必需品,下列关于氯化钠的说法中,错误的是( )
6. (2021辽宁鞍山二模)下列各组物质的稀溶液,不需要另加其他试剂就能鉴别出来的是( )
A.Na2SO4、BaCl2、NaCl、Na2CO3
B.CuCl2、Ba(OH)2、HCl、HNO3
C.Ca(OH)2、K2CO3、CaCl2、HCl
D.FeCl3、NaCl、NaOH、HNO3
7. (2021山东临沂一模)下列各组物质能发生反应且溶液质量不变的是( )
A.氢氧化钠溶液和稀硫酸 B.硝酸钾溶液和食盐水
C.小苏打和稀盐酸 D.锌放入硝酸银溶液中
8. (2021·苏州一模)下列反应属于复分解反应的是( )
A.Zn与稀H2SO4反应
B.甲烷燃烧
C.加热碳酸氢铵
D.石灰石与稀盐酸反应
9. (2021·承德一模)下列物质所对应的用途错误的是( )
A.氧化钙:干燥剂
B.氢氧化钠:治疗胃酸过多
C.碳酸氢钠:焙制糕点
D.氯化钠:医疗上配制生理盐水
10.(2021·邵阳中考)含氢氧化铝的药物治疗胃酸过多的反应为Al(OH)3+3HCl===AlCl3+3H2O,该反应属于( )
A.化合反应 B.分解反应
C.复分解反应 D.置换反应
二、填空题
11.某校化学兴趣小组进行粗盐(含有泥沙)提纯实验,并利用所得精盐配制100g 20%的氯化钠溶液。
实验一:如图1是甲同学进行粗盐提纯实验的操作示意图。
(1)写出标号仪器的名称:仪器A________;仪器B________。
(2)操作①中的一处明显错误是________。
(3)操作⑤对应的实验中,停止加热的恰当时机是________。
(4)该同学实验中缺少过滤操作,在此操作中玻璃棒的作用是________。
实验二:乙同学用提纯得到的精盐配制100g 20%的氯化钠溶液。
(5)需称取氯化钠________g;水________g 。
(6)若其他操作均正确,采用如图2所示观察方式量取水,则所配溶液的溶质质量分数________(填“>”“<”或“=”)20%。
12.有A、B、C三瓶失去标签的无色溶液,它们分别是盐酸、澄清石灰水和碳酸钠溶液中的一种。为了鉴别它们,各取少量溶液两两混合,实验结果如下表所示。表中“↓”表示有沉淀产生;“↑”表示有气体产生;“-”表示观察不到明显现象。
A B C
A ↑ —
B ↑ ↓
C — ↓
回答下列问题:
(1)A中溶质的化学式是 ,A与C反应的基本类型是 ;
(2)A与B、B与C反应的化学方程式分别是 、 。
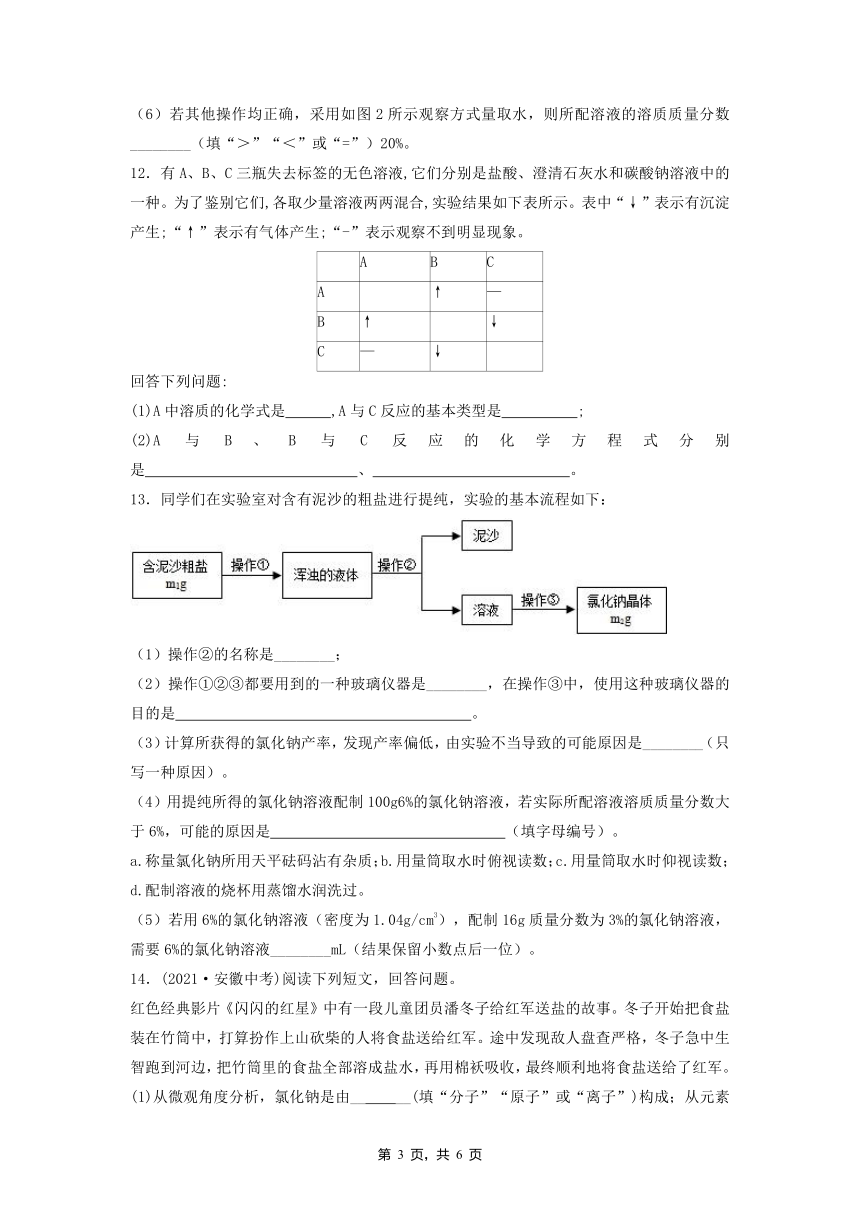
13.同学们在实验室对含有泥沙的粗盐进行提纯,实验的基本流程如下:
(1)操作②的名称是________;
(2)操作①②③都要用到的一种玻璃仪器是________,在操作③中,使用这种玻璃仪器的目的是 。
(3)计算所获得的氯化钠产率,发现产率偏低,由实验不当导致的可能原因是________(只写一种原因)。
(4)用提纯所得的氯化钠溶液配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能的原因是 (填字母编号)。
a.称量氯化钠所用天平砝码沾有杂质;b.用量筒取水时俯视读数;c.用量筒取水时仰视读数;d.配制溶液的烧杯用蒸馏水润洗过。
(5)若用6%的氯化钠溶液(密度为1.04g/cm3),配制16g质量分数为3%的氯化钠溶液,需要6%的氯化钠溶液________mL(结果保留小数点后一位)。
14.(2021·安徽中考)阅读下列短文,回答问题。
红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。
(1)从微观角度分析,氯化钠是由__ __(填“分子”“原子”或“离子”)构成;从元素角度分析,氯化钠溶液中+1价的元素有__ __(填元素符号)。
(2)从盐水中重新得到食盐固体,需进行操作的名称是__ __。
(3)氯化钠的溶解度曲线如图。假设冬子的竹筒中有358 g氯化钠,10 ℃时最少需用__ __ __g水溶解。
(4)氯化钠在生活中的用途有__ __(写出1点即可)。
15.(2021山东泰安期末)现有一瓶NaCl样品(杂质为CaCl2、MgSO4),实验兴趣小组按如图所示流程进行操作,得到精盐(纯氯化钠晶体)。
(1)操作Ⅰ和操作Ⅱ的名称为 。
(2)加入过量Ba(OH)2溶液的目的是 (用化学方程式表示)。
(3)加入过量Na2CO3溶液的目的是 ,得到沉淀Ⅱ的成分为 (填化学式)。
(4)小组成员猜测滤液Ⅱ的成分,认为除了氯化钠外一定还含有两种杂质 (填化学式),请你设计合理的实验方案,通过实验步骤与现象验证他们的猜测是正确的。
实验步骤 实验现象 实验结论
①取少量滤液Ⅱ于试管中,向其中加入过量 溶液 有白色沉淀产生 结论正确
②向步骤①所得上层清液中加
(5)写出加入盐酸发生反应的化学方程式: (写一个即可)。
(6)提纯后得到的精盐质量 (填“>”“<”或“=”)样品中氯化钠的质量。
三、实验探究题
16.(2021广西贺州中考)某化学兴趣小组在实验室探究碳酸钠溶液与稀盐酸的反应原理,请你一起完成实验探究。
实验一:在5 mL稀盐酸中逐滴加入碳酸钠溶液,边滴边振荡,直至滴完5 mL碳酸钠溶液。
现象:开始有气泡产生,一段时间后无气泡产生。写出碳酸钠与稀盐酸反应的化学方程式: 。在反应后的溶液中加入2滴酚酞溶液,溶液变红,则反应后溶液中的溶质是 。
实验二:在5 mL碳酸钠溶液中逐滴加入稀盐酸,边滴边振荡,直至滴完5 mL稀盐酸。
现象:整个实验过程无气泡产生。
【提出问题】用量相同的两种反应物,滴加顺序不同,现象为什么不一样呢
【查阅资料】碳酸钠溶液与盐酸反应:
1.盐酸过量时,反应生成NaCl、CO2和H2O;
2.盐酸不足时,产物是NaCl和NaHCO3。
【假设猜想】实验二结束后,试管中溶液的溶质有哪些
猜想1:NaCl、Na2CO3和NaHCO3
猜想2:
猜想3:NaCl
猜想4:NaCl和HCl
小明认为猜想3和4明显不合理,理由是 。
【实验探究】实验二结束后,将试管中溶液分成三等份,分别做下列三个实验。
序号 实验操作及实验现象 实验结论
实验1 加入硝酸银溶液,产生白色沉淀 再加入稀硝酸,沉淀不消失 溶液中含 (写离子符号)
实验2 加入 溶液,无沉淀产生 猜想1不成立
实验3 加入 ,有 产生 猜想2成立
【交流反思】用量相同的两种反应物,滴加顺序不同,现象和产物可能都不一样。
(参考答案)
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 B C C D C D A D B C
二、填空题
11.(1)酒精灯 烧杯
(2)瓶塞没有倒放
(3)待蒸发皿中出现较多量的固体时
(4)引流
(5)20 80
(6)<
12. (1)HCl 复分解反应 (2)Na2CO3+2HCl2NaCl+H2O+CO2↑ Ca(OH)2+Na2CO3CaCO3↓+2NaOH
13.过滤 玻璃棒 防止液体外溅 蒸发溶液时液体外溅了一部分 ab 7.7
14.离子 Na、H 蒸发 1 000 做调味品
15. (1)过滤 (2)MgSO4+Ba(OH)2BaSO4↓+Mg(OH)2↓ (3)除去CaCl2和过量的Ba(OH)2 CaCO3、BaCO3 (4)Na2CO3、NaOH ①CaCl2(或BaCl2) ②无色酚酞试液 溶液变红 (5)NaOH+HClNaCl+H2O(或Na2CO3+2HCl2NaCl+H2O+CO2↑) (6)>
三、实验探究题
16. 实验一:Na2CO3+2HCl2NaCl+H2O+CO2↑ Na2CO3、NaCl 实验二:【假设猜想】NaCl、NaHCO3 整个实验过程无气泡产生 【实验探究】Cl- 氯化钡(合理即可) 稀盐酸 气泡
第 2 页,共 5 页
一、选择题
1.将珍珠放入稀盐酸中,产生能使澄清石灰水变浑浊的气体,则珍珠中可能含有( )
A.氢氧根离子 B.碳酸根离子 C.硝酸根离子 D.硫酸根离子
2. 下列选项中各种溶质的溶液混合,无明显现象的是( )
A.NaOH、KCl、Fe2(SO4)3 B.KNO3、AgNO3、NaCl
C.H2SO4、K2SO4、HNO3 D.KCl、H2SO4、Na2CO3
3.下列各组溶液,不用其他试剂就能鉴别出来的是( )
A.MgSO4、NaOH、NaCl、BaCl2
B.NaNO3、KNO3、FeCl3、NaOH
C.Na2CO3、HCl、CaCl2、KNO3
D.BaCl2、Na2CO3、Na2SO4、KNO3
4. 下列各组离子在水中能大量共存,并形成无色溶液的是( )
A.H+、Na+、CO
B.Ba2+、CO、Cl-
C.Fe2+、H+、SO
D.K+、Ca2+、Cl-
5.食盐NaCl是我们生活中的必需品,下列关于氯化钠的说法中,错误的是( )
6. (2021辽宁鞍山二模)下列各组物质的稀溶液,不需要另加其他试剂就能鉴别出来的是( )
A.Na2SO4、BaCl2、NaCl、Na2CO3
B.CuCl2、Ba(OH)2、HCl、HNO3
C.Ca(OH)2、K2CO3、CaCl2、HCl
D.FeCl3、NaCl、NaOH、HNO3
7. (2021山东临沂一模)下列各组物质能发生反应且溶液质量不变的是( )
A.氢氧化钠溶液和稀硫酸 B.硝酸钾溶液和食盐水
C.小苏打和稀盐酸 D.锌放入硝酸银溶液中
8. (2021·苏州一模)下列反应属于复分解反应的是( )
A.Zn与稀H2SO4反应
B.甲烷燃烧
C.加热碳酸氢铵
D.石灰石与稀盐酸反应
9. (2021·承德一模)下列物质所对应的用途错误的是( )
A.氧化钙:干燥剂
B.氢氧化钠:治疗胃酸过多
C.碳酸氢钠:焙制糕点
D.氯化钠:医疗上配制生理盐水
10.(2021·邵阳中考)含氢氧化铝的药物治疗胃酸过多的反应为Al(OH)3+3HCl===AlCl3+3H2O,该反应属于( )
A.化合反应 B.分解反应
C.复分解反应 D.置换反应
二、填空题
11.某校化学兴趣小组进行粗盐(含有泥沙)提纯实验,并利用所得精盐配制100g 20%的氯化钠溶液。
实验一:如图1是甲同学进行粗盐提纯实验的操作示意图。
(1)写出标号仪器的名称:仪器A________;仪器B________。
(2)操作①中的一处明显错误是________。
(3)操作⑤对应的实验中,停止加热的恰当时机是________。
(4)该同学实验中缺少过滤操作,在此操作中玻璃棒的作用是________。
实验二:乙同学用提纯得到的精盐配制100g 20%的氯化钠溶液。
(5)需称取氯化钠________g;水________g 。
(6)若其他操作均正确,采用如图2所示观察方式量取水,则所配溶液的溶质质量分数________(填“>”“<”或“=”)20%。
12.有A、B、C三瓶失去标签的无色溶液,它们分别是盐酸、澄清石灰水和碳酸钠溶液中的一种。为了鉴别它们,各取少量溶液两两混合,实验结果如下表所示。表中“↓”表示有沉淀产生;“↑”表示有气体产生;“-”表示观察不到明显现象。
A B C
A ↑ —
B ↑ ↓
C — ↓
回答下列问题:
(1)A中溶质的化学式是 ,A与C反应的基本类型是 ;
(2)A与B、B与C反应的化学方程式分别是 、 。
13.同学们在实验室对含有泥沙的粗盐进行提纯,实验的基本流程如下:
(1)操作②的名称是________;
(2)操作①②③都要用到的一种玻璃仪器是________,在操作③中,使用这种玻璃仪器的目的是 。
(3)计算所获得的氯化钠产率,发现产率偏低,由实验不当导致的可能原因是________(只写一种原因)。
(4)用提纯所得的氯化钠溶液配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能的原因是 (填字母编号)。
a.称量氯化钠所用天平砝码沾有杂质;b.用量筒取水时俯视读数;c.用量筒取水时仰视读数;d.配制溶液的烧杯用蒸馏水润洗过。
(5)若用6%的氯化钠溶液(密度为1.04g/cm3),配制16g质量分数为3%的氯化钠溶液,需要6%的氯化钠溶液________mL(结果保留小数点后一位)。
14.(2021·安徽中考)阅读下列短文,回答问题。
红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。
(1)从微观角度分析,氯化钠是由__ __(填“分子”“原子”或“离子”)构成;从元素角度分析,氯化钠溶液中+1价的元素有__ __(填元素符号)。
(2)从盐水中重新得到食盐固体,需进行操作的名称是__ __。
(3)氯化钠的溶解度曲线如图。假设冬子的竹筒中有358 g氯化钠,10 ℃时最少需用__ __ __g水溶解。
(4)氯化钠在生活中的用途有__ __(写出1点即可)。
15.(2021山东泰安期末)现有一瓶NaCl样品(杂质为CaCl2、MgSO4),实验兴趣小组按如图所示流程进行操作,得到精盐(纯氯化钠晶体)。
(1)操作Ⅰ和操作Ⅱ的名称为 。
(2)加入过量Ba(OH)2溶液的目的是 (用化学方程式表示)。
(3)加入过量Na2CO3溶液的目的是 ,得到沉淀Ⅱ的成分为 (填化学式)。
(4)小组成员猜测滤液Ⅱ的成分,认为除了氯化钠外一定还含有两种杂质 (填化学式),请你设计合理的实验方案,通过实验步骤与现象验证他们的猜测是正确的。
实验步骤 实验现象 实验结论
①取少量滤液Ⅱ于试管中,向其中加入过量 溶液 有白色沉淀产生 结论正确
②向步骤①所得上层清液中加
(5)写出加入盐酸发生反应的化学方程式: (写一个即可)。
(6)提纯后得到的精盐质量 (填“>”“<”或“=”)样品中氯化钠的质量。
三、实验探究题
16.(2021广西贺州中考)某化学兴趣小组在实验室探究碳酸钠溶液与稀盐酸的反应原理,请你一起完成实验探究。
实验一:在5 mL稀盐酸中逐滴加入碳酸钠溶液,边滴边振荡,直至滴完5 mL碳酸钠溶液。
现象:开始有气泡产生,一段时间后无气泡产生。写出碳酸钠与稀盐酸反应的化学方程式: 。在反应后的溶液中加入2滴酚酞溶液,溶液变红,则反应后溶液中的溶质是 。
实验二:在5 mL碳酸钠溶液中逐滴加入稀盐酸,边滴边振荡,直至滴完5 mL稀盐酸。
现象:整个实验过程无气泡产生。
【提出问题】用量相同的两种反应物,滴加顺序不同,现象为什么不一样呢
【查阅资料】碳酸钠溶液与盐酸反应:
1.盐酸过量时,反应生成NaCl、CO2和H2O;
2.盐酸不足时,产物是NaCl和NaHCO3。
【假设猜想】实验二结束后,试管中溶液的溶质有哪些
猜想1:NaCl、Na2CO3和NaHCO3
猜想2:
猜想3:NaCl
猜想4:NaCl和HCl
小明认为猜想3和4明显不合理,理由是 。
【实验探究】实验二结束后,将试管中溶液分成三等份,分别做下列三个实验。
序号 实验操作及实验现象 实验结论
实验1 加入硝酸银溶液,产生白色沉淀 再加入稀硝酸,沉淀不消失 溶液中含 (写离子符号)
实验2 加入 溶液,无沉淀产生 猜想1不成立
实验3 加入 ,有 产生 猜想2成立
【交流反思】用量相同的两种反应物,滴加顺序不同,现象和产物可能都不一样。
(参考答案)
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 B C C D C D A D B C
二、填空题
11.(1)酒精灯 烧杯
(2)瓶塞没有倒放
(3)待蒸发皿中出现较多量的固体时
(4)引流
(5)20 80
(6)<
12. (1)HCl 复分解反应 (2)Na2CO3+2HCl2NaCl+H2O+CO2↑ Ca(OH)2+Na2CO3CaCO3↓+2NaOH
13.过滤 玻璃棒 防止液体外溅 蒸发溶液时液体外溅了一部分 ab 7.7
14.离子 Na、H 蒸发 1 000 做调味品
15. (1)过滤 (2)MgSO4+Ba(OH)2BaSO4↓+Mg(OH)2↓ (3)除去CaCl2和过量的Ba(OH)2 CaCO3、BaCO3 (4)Na2CO3、NaOH ①CaCl2(或BaCl2) ②无色酚酞试液 溶液变红 (5)NaOH+HClNaCl+H2O(或Na2CO3+2HCl2NaCl+H2O+CO2↑) (6)>
三、实验探究题
16. 实验一:Na2CO3+2HCl2NaCl+H2O+CO2↑ Na2CO3、NaCl 实验二:【假设猜想】NaCl、NaHCO3 整个实验过程无气泡产生 【实验探究】Cl- 氯化钡(合理即可) 稀盐酸 气泡
第 2 页,共 5 页
同课章节目录
