第九单元 课题2 溶解度(第1课时)课件—2021-2022学年九年级化学人教版下册(21张PPT)
文档属性
| 名称 | 第九单元 课题2 溶解度(第1课时)课件—2021-2022学年九年级化学人教版下册(21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-23 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
人教版-九年级化学-下册-第九单元
课题2 溶解度
第1课时
教学目标:
1.了解饱和溶液和不饱和溶液的含义。
2.认识饱和溶液与不饱和溶液在一定条件下可以相互转化。
3.能举例说明结晶现象。
1.一种或几种物质分散到另一种物质里,形成 均一、稳定 的 混合物 叫做溶液。
2.溶液的组成:能溶解其他物质的物质是 溶剂 ;被溶解的物质是 溶质 。
复习引入
一、饱和溶液与不饱和溶液
1、概念:在一定温度下、向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做这种溶质的饱和溶液,还能继续溶解的溶液,叫做这种溶质的不饱和溶液。
2、注意:(1)“一定温度”,“一定量溶剂”,因为饱和溶液与不饱和溶液是可以相互转化的。
(2)“某种溶质”的饱和溶液或不饱和溶液,因为有些溶质与溶剂能以任意比例互溶,不能构成饱和溶液,如酒精与水是没有饱和溶液的。
一、饱和溶液与不饱和溶液
3、影响物质溶解限度的因素
(1)溶剂用量的影响
物质在一定量的水中不能无限溶解。
(2)温度的影响
一般情况下,升高温度,物质的溶解能力增大,降低温度,物质的溶解能力减小。
4、饱和溶液与不饱和溶液的相互转化
饱和溶液
不饱和溶液
①增溶剂 ②升高温度
①增溶质 ②蒸发溶剂 ③降低温度
4、饱和溶液与不饱和溶液的相互转化
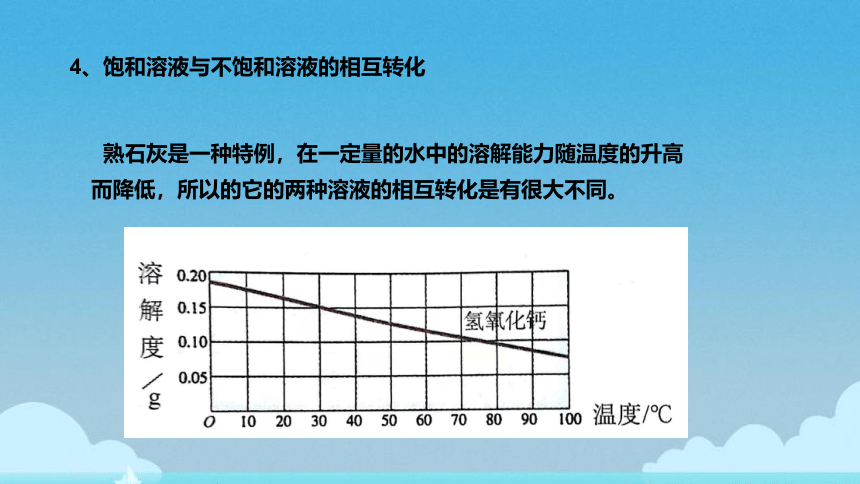
熟石灰是一种特例,在一定量的水中的溶解能力随温度的升高而降低,所以的它的两种溶液的相互转化是有很大不同。
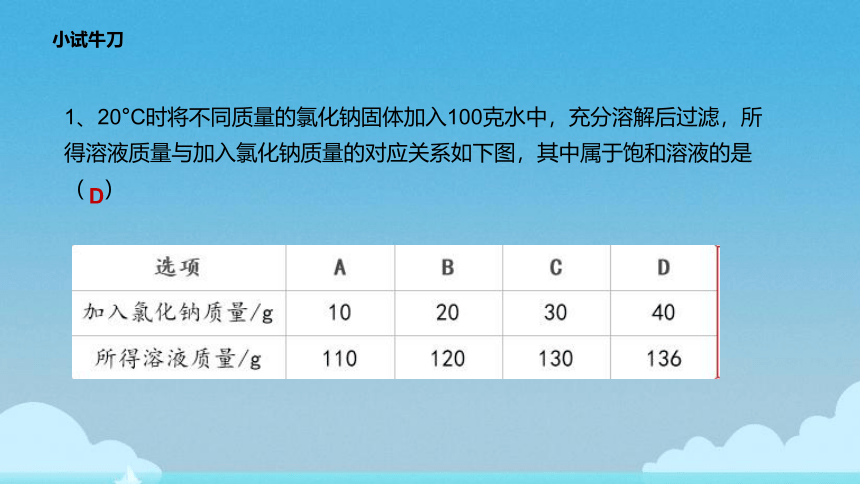
1、20°C时将不同质量的氯化钠固体加入100克水中,充分溶解后过滤,所得溶液质量与加入氯化钠质量的对应关系如下图,其中属于饱和溶液的是( )
小试牛刀
D
小试牛刀
2、要想把一瓶接近饱和的石灰水变成饱和的石灰水,具体操作有:1.加入氢氧化钙;2.升高温度;3.降低温度;4.加入水;5.蒸发水。其中措施正确的是( )
A.1、2、4 B.1、3、4
C.1、3、5 D.1、2、5
D
5、饱和溶液不饱和溶液与浓溶液、稀溶液的关系。
(1)区别:
①溶液是否饱和取决于溶质在一定温度下,一定量的溶剂里溶解量是否达到最大限度。
②溶液的浓与稀取决于溶质在一定量的溶液里含量的多少。
③饱和溶液和不饱溶液受温度影响,必须指明温度,浓溶液与稀溶液不受温度影响。
5、饱和溶液不饱和溶液与浓溶液、稀溶液的关系。
(2)联系:
①溶液的饱和与不饱和溶液的浓与稀没有必然联系。
②饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
③对于同种溶质,在一定温度下,饱和溶液一定比他的不饱和溶液浓。
二、结晶
二、结晶
二、结晶
1、概念:热的饱和溶液冷却后或蒸发溶剂时,溶质以晶体的形式从溶液中析出。
2、结晶的方法:
(1)降温结晶:一般适用于溶解度受温度影响变化较大的物质,如从硝酸钾的饱和溶液中得到硝酸钾。
(2)蒸发溶剂结晶:一般适用于溶解度受温度影响变化不大的物质,如从海水中提取食盐。
二、结晶
3、结晶方法的应用:当两种物质在同一溶剂中的溶解度随温度的改变差别较大时,采用结晶方法分离这两种物质,如图所示,可用结晶方法分离甲、乙。
(1)如果甲物质中会有少量的乙物质,可采用降温结晶法(冷却热饱和溶液法)进行提纯甲,如KNO3中含少量NaCl。
(2)如果乙物质中会有少量的甲物质,可采用蒸发结晶的方法进行提纯乙。如KNO3中含少量NaCl。
小试牛刀
蒸发
A、c
现有一瓶蒸馏水和一瓶稀氯化钾溶液,可用什么简单的办法把它们鉴别开?(注意:在实验室里,任何时候都不能尝液体的味道。)
小试牛刀
三、本节课的收获
1、知道了什么是饱和溶液,什么是不饱和溶液。
2、影响物质溶解限度的因素
(1)溶剂用量的影响
(2)温度的影响
3、饱和溶液与不饱和溶液的相互转化。
4、饱和溶液不饱和溶液与浓溶液、稀溶液的关系。
5、结晶:(1)热的饱和溶液冷却后或蒸发溶剂时,溶质以晶体的形式从溶液中析出。
(2)结晶的方法:降温结晶、蒸发溶剂结晶
1、使接近饱和的硝酸钾溶液变为饱和溶液的三种方法,分别是( )( )( )
2、在60摄氏度时,硝酸钾的溶解度为110克。这句话的含义是什么?
增加溶质
降低温度
四、课堂练习
蒸发溶剂
人教版-九年级化学-下册-第九单元
课题2 溶解度
第1课时
教学目标:
1.了解饱和溶液和不饱和溶液的含义。
2.认识饱和溶液与不饱和溶液在一定条件下可以相互转化。
3.能举例说明结晶现象。
1.一种或几种物质分散到另一种物质里,形成 均一、稳定 的 混合物 叫做溶液。
2.溶液的组成:能溶解其他物质的物质是 溶剂 ;被溶解的物质是 溶质 。
复习引入
一、饱和溶液与不饱和溶液
1、概念:在一定温度下、向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做这种溶质的饱和溶液,还能继续溶解的溶液,叫做这种溶质的不饱和溶液。
2、注意:(1)“一定温度”,“一定量溶剂”,因为饱和溶液与不饱和溶液是可以相互转化的。
(2)“某种溶质”的饱和溶液或不饱和溶液,因为有些溶质与溶剂能以任意比例互溶,不能构成饱和溶液,如酒精与水是没有饱和溶液的。
一、饱和溶液与不饱和溶液
3、影响物质溶解限度的因素
(1)溶剂用量的影响
物质在一定量的水中不能无限溶解。
(2)温度的影响
一般情况下,升高温度,物质的溶解能力增大,降低温度,物质的溶解能力减小。
4、饱和溶液与不饱和溶液的相互转化
饱和溶液
不饱和溶液
①增溶剂 ②升高温度
①增溶质 ②蒸发溶剂 ③降低温度
4、饱和溶液与不饱和溶液的相互转化
熟石灰是一种特例,在一定量的水中的溶解能力随温度的升高而降低,所以的它的两种溶液的相互转化是有很大不同。
1、20°C时将不同质量的氯化钠固体加入100克水中,充分溶解后过滤,所得溶液质量与加入氯化钠质量的对应关系如下图,其中属于饱和溶液的是( )
小试牛刀
D
小试牛刀
2、要想把一瓶接近饱和的石灰水变成饱和的石灰水,具体操作有:1.加入氢氧化钙;2.升高温度;3.降低温度;4.加入水;5.蒸发水。其中措施正确的是( )
A.1、2、4 B.1、3、4
C.1、3、5 D.1、2、5
D
5、饱和溶液不饱和溶液与浓溶液、稀溶液的关系。
(1)区别:
①溶液是否饱和取决于溶质在一定温度下,一定量的溶剂里溶解量是否达到最大限度。
②溶液的浓与稀取决于溶质在一定量的溶液里含量的多少。
③饱和溶液和不饱溶液受温度影响,必须指明温度,浓溶液与稀溶液不受温度影响。
5、饱和溶液不饱和溶液与浓溶液、稀溶液的关系。
(2)联系:
①溶液的饱和与不饱和溶液的浓与稀没有必然联系。
②饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
③对于同种溶质,在一定温度下,饱和溶液一定比他的不饱和溶液浓。
二、结晶
二、结晶
二、结晶
1、概念:热的饱和溶液冷却后或蒸发溶剂时,溶质以晶体的形式从溶液中析出。
2、结晶的方法:
(1)降温结晶:一般适用于溶解度受温度影响变化较大的物质,如从硝酸钾的饱和溶液中得到硝酸钾。
(2)蒸发溶剂结晶:一般适用于溶解度受温度影响变化不大的物质,如从海水中提取食盐。
二、结晶
3、结晶方法的应用:当两种物质在同一溶剂中的溶解度随温度的改变差别较大时,采用结晶方法分离这两种物质,如图所示,可用结晶方法分离甲、乙。
(1)如果甲物质中会有少量的乙物质,可采用降温结晶法(冷却热饱和溶液法)进行提纯甲,如KNO3中含少量NaCl。
(2)如果乙物质中会有少量的甲物质,可采用蒸发结晶的方法进行提纯乙。如KNO3中含少量NaCl。
小试牛刀
蒸发
A、c
现有一瓶蒸馏水和一瓶稀氯化钾溶液,可用什么简单的办法把它们鉴别开?(注意:在实验室里,任何时候都不能尝液体的味道。)
小试牛刀
三、本节课的收获
1、知道了什么是饱和溶液,什么是不饱和溶液。
2、影响物质溶解限度的因素
(1)溶剂用量的影响
(2)温度的影响
3、饱和溶液与不饱和溶液的相互转化。
4、饱和溶液不饱和溶液与浓溶液、稀溶液的关系。
5、结晶:(1)热的饱和溶液冷却后或蒸发溶剂时,溶质以晶体的形式从溶液中析出。
(2)结晶的方法:降温结晶、蒸发溶剂结晶
1、使接近饱和的硝酸钾溶液变为饱和溶液的三种方法,分别是( )( )( )
2、在60摄氏度时,硝酸钾的溶解度为110克。这句话的含义是什么?
增加溶质
降低温度
四、课堂练习
蒸发溶剂
同课章节目录
