安徽省A10联盟2021-2022学年高一下学期开年考化学试题(Word版含答案)
文档属性
| 名称 | 安徽省A10联盟2021-2022学年高一下学期开年考化学试题(Word版含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 721.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-25 17:52:33 | ||
图片预览




文档简介
安徽省A10联盟2021-2022学年高一下学期开年考
化学(人教版)试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100分,考试时间75分钟。请在答题卡上作答。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 A1-27 C1-35.5 Fe-56
第Ⅰ卷(选择题,共45分)
一、选择题(本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.我国古代著作中蕴含丰富的化学知识。下列说法错误的是( )
A.“铜柔锡柔,合两柔则刚”体现了合金硬度方面的特性
B.“司南之构(勺),投之于地,其柢(勺柄)指南”,司南中“构”的材质为
C.“朝坛雾卷,曙岭烟沉”,雾是一种气溶胶,能产生丁达尔现象
D.“以火烧之,紫青烟起,乃真硝石()也”,该方法应用了焰色试验
2.下列说法错误的是( )
A.属于氧化物中的两性氧化物 B.中子数为148的铀原子是
C.HClO的结构式:H-O-Cl D.金刚石和石墨均为碳元素的同素异形体
3.实验室中下列做法正确的是( )
A.金属锂和钠应保存在煤油中,防止与氧气反应
B.不慎将碱沾到皮肤上,应立即用大量水冲洗,然后涂上1%硼酸
C.使用容量瓶配制溶液时,应先检漏,且干燥后才能使用
D.实验后的难溶物或含有重金属的固体废渣,应当做深埋处理
4.可用数字化实验来验证次氯酸光照分解产物,某小组同学在实验室中对氯水的光照实验进行数据采集和分析.得到以下图像,下列说法错误的是( )
A.氯水光照一段时间后其漂白性减弱
B.光照过程中,氯离子浓度增大,说明溶液中有生成
C.综合分析图像可知,次氯酸光照分解的化学方程式为
D.光照过程中,氯水pH降低,说明溶液中的浓度减小
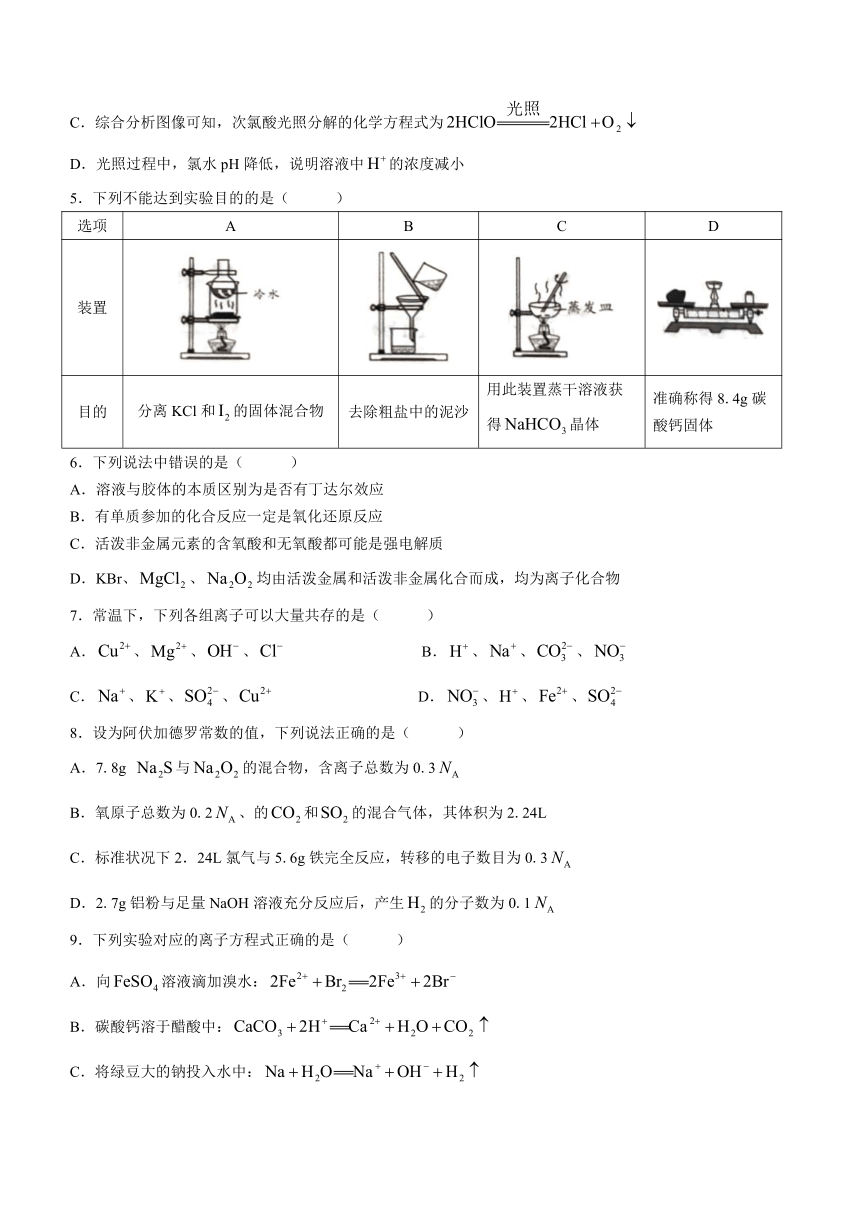
5.下列不能达到实验目的的是( )
选项 A B C D
装置
目的 分离KCl和的固体混合物 去除粗盐中的泥沙 用此装置蒸干溶液获得晶体 准确称得8.4g碳酸钙固体
6.下列说法中错误的是( )
A.溶液与胶体的本质区别为是否有丁达尔效应
B.有单质参加的化合反应一定是氧化还原反应
C.活泼非金属元素的含氧酸和无氧酸都可能是强电解质
D.KBr、、均由活泼金属和活泼非金属化合而成,均为离子化合物
7.常温下,下列各组离子可以大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
8.设为阿伏加德罗常数的值,下列说法正确的是( )
A.7.8g 与的混合物,含离子总数为0.3
B.氧原子总数为0.2、的和的混合气体,其体积为2.24L
C.标准状况下2.24L氯气与5.6g铁完全反应,转移的电子数目为0.3
D.2.7g铝粉与足量NaOH溶液充分反应后,产生的分子数为0.1
9.下列实验对应的离子方程式正确的是( )
A.向溶液滴加溴水:
B.碳酸钙溶于醋酸中:
C.将绿豆大的钠投入水中:
D.向KClO溶液中滴加浓盐酸:
10.下列实验目的、操作或现象均正确的是( )
序号 实验目的 实验操作 实验现象
A 证明某溶液中含有 向该溶液中先滴加氯水,再滴加少量KSCN溶液 溶液变成血红色
B 氧气具有漂白性 干燥的氯气依次通入有色干布条、有色湿布条 干布条无变化,湿布条褪色
C 验证金属铁比铜活泼 将铜粉加入到1.0溶液中 溶液变蓝
D 加碘盐中含有 向加碘盐中加入白醋和KI溶液 溶液呈棕黄色
11.将铜粉加入稀盐酸和氯化铁的混合溶液中,在持续通入空气的条件下生成,其反应原理如图所示:
,下列说法正确的是( )
A.反应Ⅰ过程中,对该反应有催化作用
B.若有6.4g Cu在反应中生成,则消耗11.2L
C.反应过程中,既作氧化剂,又作还原剂
D.反应Ⅱ的离子方程式为:
12.在一定条件下,下列物质间转化不能实现的是( )
A. B.
C. D.
13.R、S、T、X、W、Y、Z七种短周期主族元素,其原子半径及主要化合价如下表所示,其中化合物为淡黄色粉末。下列说法错误的是( )
元素代号 R S T W X Y Z
原子半径/nm 0.0347 0.186 0.074 0.102 0.150 0.160 0.099
主要化合价 、
A.、STR、三种化合物在一定条件下能够相互反应
B.简单氢化物的稳定性:W<T
C.化合物与化合物反应,既是氧化剂又是还原剂
D.Z元素位于第二周期ⅦA
14.汽车安全气囊中填充物的主要成分是、和。汽车发生碰撞后,安全气囊中的物质瞬间反应并释放出气体使安全气囊胀大,从而阻挡人体前冲,发生的反应为、,下列说法正确的是( )
A.是氧化产物,不是还原产物
B.和都是碱性氧化物,万水反应会生成强碱
C.爆炸会产生高温,与反应生成硅酸盐,从而减少对人体皮肤的伤害
D.反应中旬消耗1mol ,时转移2mol电子
15.2021年6月11日国家航天局公布了山“祝融号”火星车拍摄的首批科学影像图。火星气体及岩石中富含X、Y、Z、W四种元素。已知:X、Y、W为原子序数递增的四种短周期元素,其中Z为金属元素,其单质与冷水反应后溶液能使酚酞试液变为红色,X、W为同一主族元素,Y地壳中含量最高的元素,火星岩石含有W的最高价化合物:。下列判断正确的是( )
A.W位于元素周期表第三周期ⅦA族 B.最高价氧化物对应水化物的酸性:X>W
C.X、Y、Z三种元素组成的化合物只含共价键 D.原子半径:Z>W>Y>X
第Ⅱ卷 非选择题(共55分)
二、非选择题(共4小题,共55分)
16.(14分)
下表是元素周期表的一部分,表中每一个序号代表一种元素。
族 周期 ⅠA 0
1 ① ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 ② ③
3 ④ ⑤ ⑥
请回答下列问题:
(1)写出元素①和③形成的化合物的结构式 ,该分子内存在的化学键类型是 。
(2)③在周期表中的位置为 ,与③同族的下一周期元素的原子结构示意图为 ,其最高正化合价为 。
(3)①~⑥中属于非金属元素的有 (填元素符号),试推测⑤⑥的最高价氧化物对应水化物的酸性强弱: > (填化学式)。
(4)元素①和⑥组成的化合物的水溶液与元素④的单质发生反应,其离子方程式为 。
(5)①与氧元素形成的分子可能是_。
A. B. C. D.
17.(14分)
下图是短周期元素的单质及其化合物(或其溶液)的转化关系,已知A、B、C是非金属单质,且常温常压下都是气体,A在B中燃烧发出苍白色火焰,化合物H的焰色试验呈黄色(图中部分产物未标出)。
(Ⅰ)G常温常压下为液体。
①H的电子式为 。
②写出E和G反应生成H和C的化学方程式 。
③短周期金属元素形成的某常见单质可溶于H溶液中,其离子方程式为 。
(Ⅱ)G常温常压下为气体。
①H的俗称为 ;用电子式表示G的形成过程 。
②少量F溶液滴加到H溶液中反应的离子方程式 。
③向H的饱和溶液中通入足量的,产生沉淀的原因是 (写出三点原因)。
18.(14分)
某工业废水(含、、、、),从该废水中回收利用Al和的流程图如下图所示:
(1)在操作a用到的玻璃仪器有烧杯、 、 。操作c为 、 、过滤、洗涤。
(2)固体X、固体Y分别为 、 (填化学式)。
(3)沉淀①在空气中充分灼烧,所得固体为 (填名称)。
(4)向溶液②中加入溶液,可观察到有无色气体和白色沉淀生成,其反应的离子方程式为 。
(5)固体X电解时若转移4电子,可得到 g Al。
(6)溶液③转化成溶液④主要反应的离子方程式是 。
19.(13分)
下图是某实验兴趣小组同学们设计的一套制取纯净干燥氯气装置。(夹持仪器已省略)。
(1)仪器a为恒压滴液漏斗,与普通漏斗相比,其优点是 。
(2)整套实验装置组装好后,首先需进行的必要操作是 。
(3)饱和食盐水的作用是 ,装置C中的试剂是 (填名称)。
(4)二氧化锰与浓盐酸反应的离子方程式为 。
(5)若用湿润的淀粉-KI试纸检验生成的,可观察到的现象是 。
(6)一定温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO、三种含氯产物,其中NaClO与的物质的量之比为3:1,则反应的总离子方程式为 。该温度下,将足量氯气通入400mL 3.0的NaOH溶液中,充分反应后,理论上得到的物质的量浓度为 (溶液体积变化忽略不计)。
安徽省A10联盟2021-2022学年高一下学期开年考
化学(人教版)参考答案
一、选择题(本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)
题号 1 2 3 4 5 6 7 8
答案 B B B D C A C A
题号 9 10 11 12 13 14 15
答案 A D D C D C B
1.B
“金(即铜)柔锡柔,合两柔则刚”体现了合金硬度方面的特性,说明合金硬度大于各成分,A正确;司南中“杓”的材质为有磁性的物质,四氧化三铁具有磁性,所以司南中“杓”的材质为,B错误;雾是一种气溶胶,能产生丁达尔现象,C正确;钾元素焰色试验透过蓝色钴玻璃为紫色,应用的是焰色试验原理,D正确。
2.B
既能与酸反应生成盐和水,又能和碱反应生成盐和水,属于氧化物中的两性氧化物,A正确;铀原子的质子数为92,中子数为148,根据质量数(A)=质子数(Z)+中子数(N)可知,,其正确书写应该为,B错误;HClO的电子式为,故其结构式为H-O-Cl,C正确;金刚石和石墨均为碳元素形成的性质不同的碳单质,是碳元素的同素异形体,D正确。
3.B
金属锂的密度小于煤油,应保存在石蜡油中,A错误;使用容量瓶配制溶液时,应先检漏,以防摇匀过程中溶液流出,容量瓶不需要干燥就能使用,不会带来误差,C错误;实验后的难溶物或含有重金属的固体废渣,应当集中送至环保单位进一步处理,D错误。
4.D
由图可知氯水光照过程中溶液pH减小,氯离子浓度增大,说明次氯酸转化为HCl和,其漂白性减弱,A、B、C均正确;一定条件下,pH越小说明溶液中H的浓度越大,D错误。
5.C
碘易升华,KCl不能升华,选择升华法分离,A正确;粗盐可溶于水,泥沙不可溶于水,B正确;受热易分解,用该装置无法达到实验目的,C错误;托盘天平精确度为0.1g,D正确。
6.A
溶液与胶体的本质区别是分散质直径的大小,A错误;单质参加的化合反应,对应元素一定会发生化合价的变化,因此一定是氧化还原反应,B正确;Cl的含氧酸和无氧酸HCl均是强电解质,C正确;KBr、、均由活泼金属和活泼非金属化合而成,都是由阳离子和阴离子通过离子键构成,都是离子化合物,D正确。
7.C
、与反应均生成沉淀,不能大量共存,A错误;与不能大量共存,其离子方程式为,B错误;、、、之间不反应,可以大量共存,C正确;酸性溶液中,能将氧化,D错误。
8.A
7.8g 物质的量为0.1mol,含离子总数0.3,7.8g 物质的量为0.1mol,含离子总数0.3,因此7.8g 与的混合物,含离子总数为0.3,A正确;缺少标准状况下,因此无法计算气体体积,B错误;5.6g铁(物质的量为0.1mol)与标准状况下2.24L氯气(物质的量为0.1mol)完全反应,由于氯气少量,因此转移的电子数目为0.2,C错误;1mol铝与足量氢氧化钠溶液反应生成1.5mol氢气,则2.7g铝粉与足量氢氧化钠溶液反应生成氢气的分子数为,D错误。
9.A
溶液与溴水,溴水具有氧化性,将二价铁离子氧化为三价铁离子,离子反应式:,A正确;醋酸是弱电解质应写化学式,B错误;钠和水反应生成NaOH和,反应的离子方程式为:,C错误;向KClO溶液中滴加浓盐酸,会生成氯气:,D错误。
10.D
向某溶液中先滴加氯水,再滴加少量KSCN溶液,溶液变成血红色,不能证明原溶液中含有,也可能本来就有,A错误;氯气与水反应生成盐酸和次氯酸,次氯酸具有漂白性,B错误;铁离子与铜反应生成铜离子和亚铁离子,不能证明铁比铜活泼,C错误;酸性条件下碘离子和碘酸钾发生氧化还原反应生成碘,溶液呈棕黄色,D正确。
11.D
在生成的反应过程中,是氧化剂,A错误;没有说明消耗的气体体积是在标准状况下测定的,B错误;是还原产物,同时也作还原剂,C错误;由图可知被氧气氧化为,D正确。
12.C
溶液和不反应,不能生成,故选C。
13.D
化合物为淡黄色粉末,再结合原子半径和主要化合价,R为H、S为Na、T为O、W为S、Z为Al、Y为Mg、Z为Cl。、STR、三种化合物分别为、NaOH、,既能与强酸反应,又能与强碱反应,A正确;非金属性:S<O,故简单氢化物的稳定性:,B正确;中O元素的化合价为-1价,根据氧化还原反应的价态规律,与反应,既是氧化剂又是还原剂,C正确;Cl元素位于第三周期ⅦA,D错误。
14.C
中的N化合价降低被还原,既是氧化产物也是还原产物,A错误;是过氧化物,不是碱性氧化物,B错误;爆炸会产生高温,与反应生成硅酸盐,从而减少对人体皮肤的伤害,C正确;有反应方程式可知反应中每消耗10mol时转移10mol电子,反应中每消耗1mol时转移1mol电子,D错误。
15.B
Z为金属元素,其单质与冷水反应后溶液能使酚酞试液变为红色,Z为Na;Y是地壳中含量最高的元素,Y为O;火星岩石含有:,则W化合价为价,X、W为同一主族元素,且X、Y、Z、W为原子序数递增,则X为C,W为Si;综上所述,X、Y、Z、W分别为C、O、Na、Si。Si位于元素周期表第三周期ⅣA族,A错误;碳酸的酸性大于硅酸的酸性,B正确;中既有离子键又有共价键,C错误;同周期随原子序数增大,原子半径减小,故原子半径:Y<X,D错误。
二、非选择题(共4小题,共55分)
16.(14分)
(1)N-H-N 共价键或极性共价键
(2)第二周期第ⅤA族
(3)H、C、N、S、Cl 、
(4)
(5)D
17.(14分)
(Ⅰ)
①
②
③
(Ⅱ)
①纯碱
②
③同温同压下在水中溶解度小于;生成的质量大于原溶液中质量;溶剂质量减少(各1分,共3分)
18.(14分)
(1)漏斗、玻璃棒 蒸发浓缩、冷却结晶
(2)、Fe(2分,各1分)
(3)氧化铁(或三氧化二铁)
(4)
(5)36
(6)(2分,写了铁与氢离子反应不扣分)
19.(13分)
(1)平衡压强,便于浓盐酸顺利流下
(2)检查装置的气密性
(3)除去氯气中混有的HCl气体 浓硫酸
(4)
(5)湿润的淀粉-KI试纸变蓝
(6) 0.25
化学(人教版)试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100分,考试时间75分钟。请在答题卡上作答。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 A1-27 C1-35.5 Fe-56
第Ⅰ卷(选择题,共45分)
一、选择题(本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.我国古代著作中蕴含丰富的化学知识。下列说法错误的是( )
A.“铜柔锡柔,合两柔则刚”体现了合金硬度方面的特性
B.“司南之构(勺),投之于地,其柢(勺柄)指南”,司南中“构”的材质为
C.“朝坛雾卷,曙岭烟沉”,雾是一种气溶胶,能产生丁达尔现象
D.“以火烧之,紫青烟起,乃真硝石()也”,该方法应用了焰色试验
2.下列说法错误的是( )
A.属于氧化物中的两性氧化物 B.中子数为148的铀原子是
C.HClO的结构式:H-O-Cl D.金刚石和石墨均为碳元素的同素异形体
3.实验室中下列做法正确的是( )
A.金属锂和钠应保存在煤油中,防止与氧气反应
B.不慎将碱沾到皮肤上,应立即用大量水冲洗,然后涂上1%硼酸
C.使用容量瓶配制溶液时,应先检漏,且干燥后才能使用
D.实验后的难溶物或含有重金属的固体废渣,应当做深埋处理
4.可用数字化实验来验证次氯酸光照分解产物,某小组同学在实验室中对氯水的光照实验进行数据采集和分析.得到以下图像,下列说法错误的是( )
A.氯水光照一段时间后其漂白性减弱
B.光照过程中,氯离子浓度增大,说明溶液中有生成
C.综合分析图像可知,次氯酸光照分解的化学方程式为
D.光照过程中,氯水pH降低,说明溶液中的浓度减小
5.下列不能达到实验目的的是( )
选项 A B C D
装置
目的 分离KCl和的固体混合物 去除粗盐中的泥沙 用此装置蒸干溶液获得晶体 准确称得8.4g碳酸钙固体
6.下列说法中错误的是( )
A.溶液与胶体的本质区别为是否有丁达尔效应
B.有单质参加的化合反应一定是氧化还原反应
C.活泼非金属元素的含氧酸和无氧酸都可能是强电解质
D.KBr、、均由活泼金属和活泼非金属化合而成,均为离子化合物
7.常温下,下列各组离子可以大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
8.设为阿伏加德罗常数的值,下列说法正确的是( )
A.7.8g 与的混合物,含离子总数为0.3
B.氧原子总数为0.2、的和的混合气体,其体积为2.24L
C.标准状况下2.24L氯气与5.6g铁完全反应,转移的电子数目为0.3
D.2.7g铝粉与足量NaOH溶液充分反应后,产生的分子数为0.1
9.下列实验对应的离子方程式正确的是( )
A.向溶液滴加溴水:
B.碳酸钙溶于醋酸中:
C.将绿豆大的钠投入水中:
D.向KClO溶液中滴加浓盐酸:
10.下列实验目的、操作或现象均正确的是( )
序号 实验目的 实验操作 实验现象
A 证明某溶液中含有 向该溶液中先滴加氯水,再滴加少量KSCN溶液 溶液变成血红色
B 氧气具有漂白性 干燥的氯气依次通入有色干布条、有色湿布条 干布条无变化,湿布条褪色
C 验证金属铁比铜活泼 将铜粉加入到1.0溶液中 溶液变蓝
D 加碘盐中含有 向加碘盐中加入白醋和KI溶液 溶液呈棕黄色
11.将铜粉加入稀盐酸和氯化铁的混合溶液中,在持续通入空气的条件下生成,其反应原理如图所示:
,下列说法正确的是( )
A.反应Ⅰ过程中,对该反应有催化作用
B.若有6.4g Cu在反应中生成,则消耗11.2L
C.反应过程中,既作氧化剂,又作还原剂
D.反应Ⅱ的离子方程式为:
12.在一定条件下,下列物质间转化不能实现的是( )
A. B.
C. D.
13.R、S、T、X、W、Y、Z七种短周期主族元素,其原子半径及主要化合价如下表所示,其中化合物为淡黄色粉末。下列说法错误的是( )
元素代号 R S T W X Y Z
原子半径/nm 0.0347 0.186 0.074 0.102 0.150 0.160 0.099
主要化合价 、
A.、STR、三种化合物在一定条件下能够相互反应
B.简单氢化物的稳定性:W<T
C.化合物与化合物反应,既是氧化剂又是还原剂
D.Z元素位于第二周期ⅦA
14.汽车安全气囊中填充物的主要成分是、和。汽车发生碰撞后,安全气囊中的物质瞬间反应并释放出气体使安全气囊胀大,从而阻挡人体前冲,发生的反应为、,下列说法正确的是( )
A.是氧化产物,不是还原产物
B.和都是碱性氧化物,万水反应会生成强碱
C.爆炸会产生高温,与反应生成硅酸盐,从而减少对人体皮肤的伤害
D.反应中旬消耗1mol ,时转移2mol电子
15.2021年6月11日国家航天局公布了山“祝融号”火星车拍摄的首批科学影像图。火星气体及岩石中富含X、Y、Z、W四种元素。已知:X、Y、W为原子序数递增的四种短周期元素,其中Z为金属元素,其单质与冷水反应后溶液能使酚酞试液变为红色,X、W为同一主族元素,Y地壳中含量最高的元素,火星岩石含有W的最高价化合物:。下列判断正确的是( )
A.W位于元素周期表第三周期ⅦA族 B.最高价氧化物对应水化物的酸性:X>W
C.X、Y、Z三种元素组成的化合物只含共价键 D.原子半径:Z>W>Y>X
第Ⅱ卷 非选择题(共55分)
二、非选择题(共4小题,共55分)
16.(14分)
下表是元素周期表的一部分,表中每一个序号代表一种元素。
族 周期 ⅠA 0
1 ① ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 ② ③
3 ④ ⑤ ⑥
请回答下列问题:
(1)写出元素①和③形成的化合物的结构式 ,该分子内存在的化学键类型是 。
(2)③在周期表中的位置为 ,与③同族的下一周期元素的原子结构示意图为 ,其最高正化合价为 。
(3)①~⑥中属于非金属元素的有 (填元素符号),试推测⑤⑥的最高价氧化物对应水化物的酸性强弱: > (填化学式)。
(4)元素①和⑥组成的化合物的水溶液与元素④的单质发生反应,其离子方程式为 。
(5)①与氧元素形成的分子可能是_。
A. B. C. D.
17.(14分)
下图是短周期元素的单质及其化合物(或其溶液)的转化关系,已知A、B、C是非金属单质,且常温常压下都是气体,A在B中燃烧发出苍白色火焰,化合物H的焰色试验呈黄色(图中部分产物未标出)。
(Ⅰ)G常温常压下为液体。
①H的电子式为 。
②写出E和G反应生成H和C的化学方程式 。
③短周期金属元素形成的某常见单质可溶于H溶液中,其离子方程式为 。
(Ⅱ)G常温常压下为气体。
①H的俗称为 ;用电子式表示G的形成过程 。
②少量F溶液滴加到H溶液中反应的离子方程式 。
③向H的饱和溶液中通入足量的,产生沉淀的原因是 (写出三点原因)。
18.(14分)
某工业废水(含、、、、),从该废水中回收利用Al和的流程图如下图所示:
(1)在操作a用到的玻璃仪器有烧杯、 、 。操作c为 、 、过滤、洗涤。
(2)固体X、固体Y分别为 、 (填化学式)。
(3)沉淀①在空气中充分灼烧,所得固体为 (填名称)。
(4)向溶液②中加入溶液,可观察到有无色气体和白色沉淀生成,其反应的离子方程式为 。
(5)固体X电解时若转移4电子,可得到 g Al。
(6)溶液③转化成溶液④主要反应的离子方程式是 。
19.(13分)
下图是某实验兴趣小组同学们设计的一套制取纯净干燥氯气装置。(夹持仪器已省略)。
(1)仪器a为恒压滴液漏斗,与普通漏斗相比,其优点是 。
(2)整套实验装置组装好后,首先需进行的必要操作是 。
(3)饱和食盐水的作用是 ,装置C中的试剂是 (填名称)。
(4)二氧化锰与浓盐酸反应的离子方程式为 。
(5)若用湿润的淀粉-KI试纸检验生成的,可观察到的现象是 。
(6)一定温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO、三种含氯产物,其中NaClO与的物质的量之比为3:1,则反应的总离子方程式为 。该温度下,将足量氯气通入400mL 3.0的NaOH溶液中,充分反应后,理论上得到的物质的量浓度为 (溶液体积变化忽略不计)。
安徽省A10联盟2021-2022学年高一下学期开年考
化学(人教版)参考答案
一、选择题(本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)
题号 1 2 3 4 5 6 7 8
答案 B B B D C A C A
题号 9 10 11 12 13 14 15
答案 A D D C D C B
1.B
“金(即铜)柔锡柔,合两柔则刚”体现了合金硬度方面的特性,说明合金硬度大于各成分,A正确;司南中“杓”的材质为有磁性的物质,四氧化三铁具有磁性,所以司南中“杓”的材质为,B错误;雾是一种气溶胶,能产生丁达尔现象,C正确;钾元素焰色试验透过蓝色钴玻璃为紫色,应用的是焰色试验原理,D正确。
2.B
既能与酸反应生成盐和水,又能和碱反应生成盐和水,属于氧化物中的两性氧化物,A正确;铀原子的质子数为92,中子数为148,根据质量数(A)=质子数(Z)+中子数(N)可知,,其正确书写应该为,B错误;HClO的电子式为,故其结构式为H-O-Cl,C正确;金刚石和石墨均为碳元素形成的性质不同的碳单质,是碳元素的同素异形体,D正确。
3.B
金属锂的密度小于煤油,应保存在石蜡油中,A错误;使用容量瓶配制溶液时,应先检漏,以防摇匀过程中溶液流出,容量瓶不需要干燥就能使用,不会带来误差,C错误;实验后的难溶物或含有重金属的固体废渣,应当集中送至环保单位进一步处理,D错误。
4.D
由图可知氯水光照过程中溶液pH减小,氯离子浓度增大,说明次氯酸转化为HCl和,其漂白性减弱,A、B、C均正确;一定条件下,pH越小说明溶液中H的浓度越大,D错误。
5.C
碘易升华,KCl不能升华,选择升华法分离,A正确;粗盐可溶于水,泥沙不可溶于水,B正确;受热易分解,用该装置无法达到实验目的,C错误;托盘天平精确度为0.1g,D正确。
6.A
溶液与胶体的本质区别是分散质直径的大小,A错误;单质参加的化合反应,对应元素一定会发生化合价的变化,因此一定是氧化还原反应,B正确;Cl的含氧酸和无氧酸HCl均是强电解质,C正确;KBr、、均由活泼金属和活泼非金属化合而成,都是由阳离子和阴离子通过离子键构成,都是离子化合物,D正确。
7.C
、与反应均生成沉淀,不能大量共存,A错误;与不能大量共存,其离子方程式为,B错误;、、、之间不反应,可以大量共存,C正确;酸性溶液中,能将氧化,D错误。
8.A
7.8g 物质的量为0.1mol,含离子总数0.3,7.8g 物质的量为0.1mol,含离子总数0.3,因此7.8g 与的混合物,含离子总数为0.3,A正确;缺少标准状况下,因此无法计算气体体积,B错误;5.6g铁(物质的量为0.1mol)与标准状况下2.24L氯气(物质的量为0.1mol)完全反应,由于氯气少量,因此转移的电子数目为0.2,C错误;1mol铝与足量氢氧化钠溶液反应生成1.5mol氢气,则2.7g铝粉与足量氢氧化钠溶液反应生成氢气的分子数为,D错误。
9.A
溶液与溴水,溴水具有氧化性,将二价铁离子氧化为三价铁离子,离子反应式:,A正确;醋酸是弱电解质应写化学式,B错误;钠和水反应生成NaOH和,反应的离子方程式为:,C错误;向KClO溶液中滴加浓盐酸,会生成氯气:,D错误。
10.D
向某溶液中先滴加氯水,再滴加少量KSCN溶液,溶液变成血红色,不能证明原溶液中含有,也可能本来就有,A错误;氯气与水反应生成盐酸和次氯酸,次氯酸具有漂白性,B错误;铁离子与铜反应生成铜离子和亚铁离子,不能证明铁比铜活泼,C错误;酸性条件下碘离子和碘酸钾发生氧化还原反应生成碘,溶液呈棕黄色,D正确。
11.D
在生成的反应过程中,是氧化剂,A错误;没有说明消耗的气体体积是在标准状况下测定的,B错误;是还原产物,同时也作还原剂,C错误;由图可知被氧气氧化为,D正确。
12.C
溶液和不反应,不能生成,故选C。
13.D
化合物为淡黄色粉末,再结合原子半径和主要化合价,R为H、S为Na、T为O、W为S、Z为Al、Y为Mg、Z为Cl。、STR、三种化合物分别为、NaOH、,既能与强酸反应,又能与强碱反应,A正确;非金属性:S<O,故简单氢化物的稳定性:,B正确;中O元素的化合价为-1价,根据氧化还原反应的价态规律,与反应,既是氧化剂又是还原剂,C正确;Cl元素位于第三周期ⅦA,D错误。
14.C
中的N化合价降低被还原,既是氧化产物也是还原产物,A错误;是过氧化物,不是碱性氧化物,B错误;爆炸会产生高温,与反应生成硅酸盐,从而减少对人体皮肤的伤害,C正确;有反应方程式可知反应中每消耗10mol时转移10mol电子,反应中每消耗1mol时转移1mol电子,D错误。
15.B
Z为金属元素,其单质与冷水反应后溶液能使酚酞试液变为红色,Z为Na;Y是地壳中含量最高的元素,Y为O;火星岩石含有:,则W化合价为价,X、W为同一主族元素,且X、Y、Z、W为原子序数递增,则X为C,W为Si;综上所述,X、Y、Z、W分别为C、O、Na、Si。Si位于元素周期表第三周期ⅣA族,A错误;碳酸的酸性大于硅酸的酸性,B正确;中既有离子键又有共价键,C错误;同周期随原子序数增大,原子半径减小,故原子半径:Y<X,D错误。
二、非选择题(共4小题,共55分)
16.(14分)
(1)N-H-N 共价键或极性共价键
(2)第二周期第ⅤA族
(3)H、C、N、S、Cl 、
(4)
(5)D
17.(14分)
(Ⅰ)
①
②
③
(Ⅱ)
①纯碱
②
③同温同压下在水中溶解度小于;生成的质量大于原溶液中质量;溶剂质量减少(各1分,共3分)
18.(14分)
(1)漏斗、玻璃棒 蒸发浓缩、冷却结晶
(2)、Fe(2分,各1分)
(3)氧化铁(或三氧化二铁)
(4)
(5)36
(6)(2分,写了铁与氢离子反应不扣分)
19.(13分)
(1)平衡压强,便于浓盐酸顺利流下
(2)检查装置的气密性
(3)除去氯气中混有的HCl气体 浓硫酸
(4)
(5)湿润的淀粉-KI试纸变蓝
(6) 0.25
同课章节目录
