第七单元常见的酸和碱测试题-2021-2022学年九年级化学鲁教版下册(word版有答案)
文档属性
| 名称 | 第七单元常见的酸和碱测试题-2021-2022学年九年级化学鲁教版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 158.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-25 00:00:00 | ||
图片预览


文档简介
第七单元《常见的酸和碱》测试题
一、单选题
1.下列各组物质中,利用括号内的试剂或物品不能将它们一一鉴别出来的是
A.稀盐酸、氢氧化钠溶液、氯化钠溶液(无色酚酞)
B.空气、氧气、二氧化碳气体(燃着的木条)
C.氧化铁、铜和红磷三种红色固体(稀盐酸)
D.硝酸铵、氢氧化钠和氯化钠三种白色固体(水)
2.下列几组物质按照单质、氧化物、酸、碱顺序排列的是
A.C、H2O、H2SO4、Na2O
B.O3、KClO3、HCl、Ba(OH)2
C.He、HgO、CuSO4、Cu(OH)2
D.O2、Fe2O3、H2SO4、NH3·H2O
3.下列关于实验室洗涤仪器的说法中正确的是
A.用洗涤精清洗带油的试管是利用了溶解原理
B.洗净的试管应当正放在试管架上
C.长期存放石灰水的试剂瓶内壁常有白色固体,可用稀盐酸洗去
D.加热后的试管立即用冷水清洗
4.有甲、乙、丙、丁四种物质,在化学反应中的关系是:甲+乙→丙+丁,则下列说法中正确的是
A.若甲为盐酸,丁为水,则乙一定为碱
B.若甲为含碳、氢的化合物,乙为氧气,则该反应一定为氧化反应
C.若将10g甲和15g乙混合,充分反应后,则生成丙和丁的质量总和一定为25g
D.若甲、乙、丙、丁都是化合物,则该反应一定是复分解反应
5.化学实验中常会呈现颜色之美。下列化学实验中的颜色变化与实验事实不符的是
A.将生锈铁钉投入到稀盐酸中,溶液逐渐变为浅黄色
B.将少量氧化铜粉末加入稀硫酸中,微热,浑浊液体会逐渐变为蓝色溶液
C.向硫酸铜溶液中滴加氢氧化钠溶液会产生蓝色沉淀
D.将通入滴有石蕊的水中,溶液颜色由紫色逐渐变为蓝色
6.从化学视角看“烟、雾、光和焰”是有区别的。下列实验现象正确的是
A.红磷在空气中点燃,产生大量白色烟雾
B.木炭在氧气中燃烧,发出白光,生成使澄清石灰水变浑浊的气体
C.铁丝在氧气中点燃,产生红色火焰,生成黑色固体
D.打开浓盐酸的瓶盖,出现白烟
7.下列洗涤方式应用乳化作用的是
A.用汽油除去衣服上的油污 B.用洗洁精清洗餐具上的油污
C.无水酒精洗手机屏幕 D.用白醋清洗水壶的水垢
8.证据推理是化学学科核心素养的重要内容,下列推理正确的是
A.酸能使紫色石蕊溶液变红色,所以能使紫色石蕊溶液变红色的一定是酸
B.化合物由不同种元素组成,所以由不同种元素组成的纯净物一定是化合物
C.中和反应是有盐和水生成的反应,所以有盐和水生成的反应一定是中和反应
D.单质中只含一种元素,含一种元素的物质一定是单质
9.化学变化常常伴随一些明显的现象,下列实验现象描述错误的是
A.红磷在空气中燃烧,产生白烟 B.打开浓盐酸瓶盖,瓶口产生大量白雾
C.镁带放入食醋,产生氢气 D.“铜绿”加热,固体逐渐变成黑色
10.下列各组固体和液体分别放在如图所示装置,试管中有某种液体,将气球中的某种固体小心地倒入试管中,不能使气球膨胀的是
A.生石灰和水 B.镁和稀盐酸 C.氯化钠和水 D.石灰石和稀盐酸
11.“操作千万条,安全第一条”。化学实验是形成科学探究素养的必要手段。下列实验操作符合安全要求的是
A.点燃酒精灯 B.转移蒸发皿
C.闻气味 D.稀释浓硫酸
二、简答题
12.用学过的化学知识回答下列问题:
(1)洗涤剂能去除餐具上的油污,汽油也可以去除油污,二者原理有什么不同?_______
(2)工业上用稀硫酸来除铁锈,其反应的化学方程式为_______。
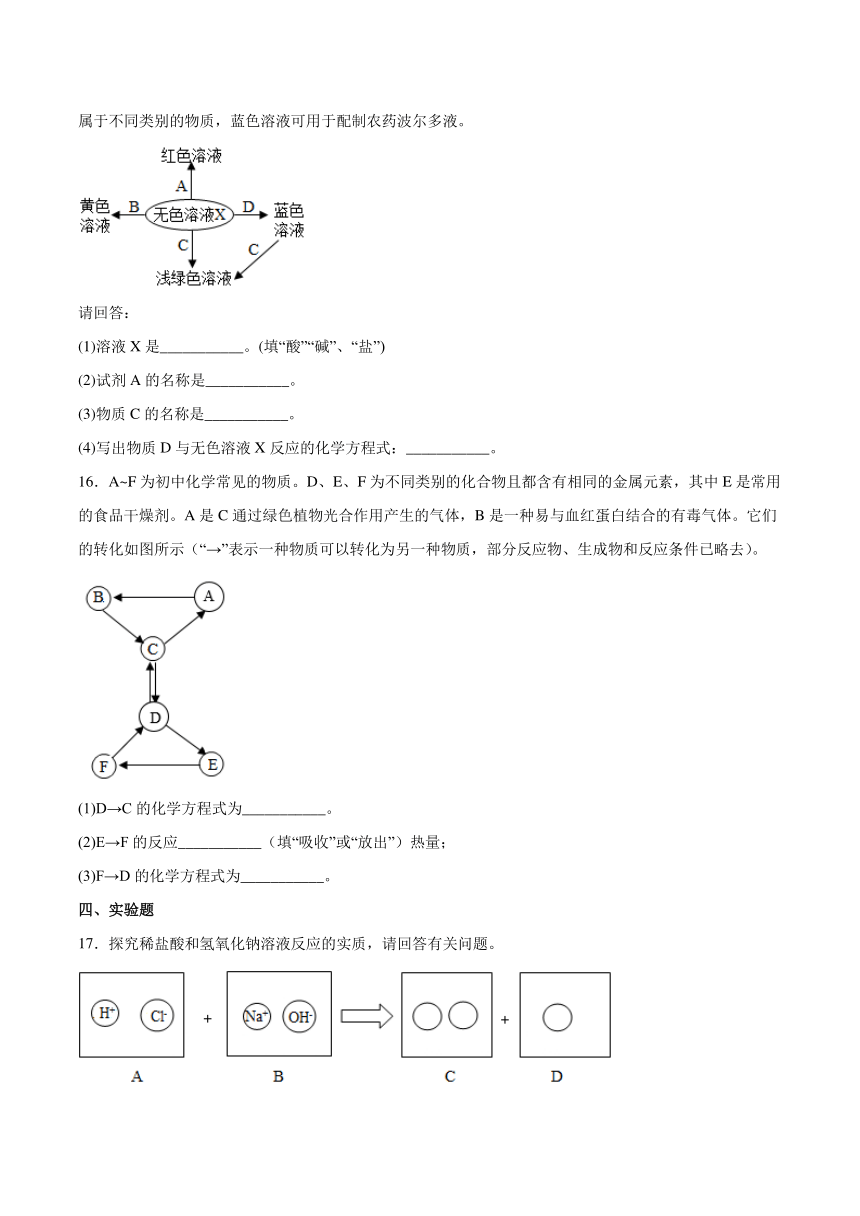
13.根据下图进行实验。
(1)该实验可证明分子具有的性质是______。
(2)此实验能够证明 NaOH 与 HCl 发生了化学反应,理由是______________________
三、推断题
14.A-E是初中化学常见的五种不同类别的物质,其中B由两种元素组成,C常用作食品干燥剂,并且C、D、E含有一种相同的金属元素,它们之间的转化关系如图所示(图中“一”表示两端的物质间能反应,“→”表示物质间存在转化关系,部分反应物、生成物和反应条件已略去)。请回答:
(1)物质C的化学式:___________。
(2)物质D俗称为___________(写一个);
(3)图中涉及的基本反应类型有___________个。
(4)反应“B-E”的化学方程式是___________。
15.如图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”。其中B是铁锈的主要成分,B、C、D分属于不同类别的物质,蓝色溶液可用于配制农药波尔多液。
请回答:
(1)溶液X是___________。(填“酸”“碱”、“盐”)
(2)试剂A的名称是___________。
(3)物质C的名称是___________。
(4)写出物质D与无色溶液X反应的化学方程式:___________。
16.A~F为初中化学常见的物质。D、E、F为不同类别的化合物且都含有相同的金属元素,其中E是常用的食品干燥剂。A是C通过绿色植物光合作用产生的气体,B是一种易与血红蛋白结合的有毒气体。它们的转化如图所示(“→”表示一种物质可以转化为另一种物质,部分反应物、生成物和反应条件已略去)。
(1)D→C的化学方程式为___________。
(2)E→F的反应___________(填“吸收”或“放出”)热量;
(3)F→D的化学方程式为___________。
四、实验题
17.探究稀盐酸和氢氧化钠溶液反应的实质,请回答有关问题。
(1)在上图C、D中的圆圈内应对应的化学式或离子符号填写在下面空白处:C中_________、_________。D中_________。
(2)用化学方程式表示图中所体现的化学反应:_________。此反应的基本类型是_________,此反应的实质是_________。
(3)实验时,甲同学将稀盐酸滴入到装有氢氧化钠固体的试管中,触摸试管有灼热感,他马上得出结论:氢氧化钠与稀盐酸反应会放出大量的热。该同学的观点是否准确?请说明理由:_________。
(4)乙同学进行该实验:在一支试管中加入NaOH溶液,再向其中滴加稀硫酸,振荡,最后滴加2滴酚酞试液,振荡,溶液不变色。乙据此判断酸和碱恰好完全反应。小明得出这样的结论是否正确?理由是_________。
(5)氢氧化钠溶液极易吸收空气中的二氧化碳而变质为_________(写化学式);该反应的化方程式:_________。
(6)证明一瓶氢氧化钠溶液已变质,可用试剂_________,该反应的化方程式为_________:如果已变质,则现象为_________。
18.今有A、B、C、D、E五种装置如下图所示。按下列要求回答问题(所选装置用其代号字母表示)
(1)实验室用高锰酸钾加热分解来制取氧气时,发生装置选用_______,该装置制取氧气的化学方程式为_________。
(2)实验室用大理石和稀盐酸来制取二氧化碳时,发生装置选用_____,收集装置常选用 ________;检验二氧化碳气体是否收集满把燃着的木条伸到_______。
(3)硫化氢(H2S)是一种无色且有臭鸡蛋气味的气体,密度比空气大,能溶于水,可形成一种酸溶液(氢硫酸)。实验室用硫化亚铁跟稀硫酸反应制取硫化氢气体。试回答:
①硫化氢气体具有臭鸡蛋味,这是硫化氢的_____(填“物理”或“化学”)性质。
②硫化氢的水溶液能使紫色石蕊试液变______色。
③实验室制取硫化氢气体时,发生装置应选用_____,收集装置应选用_____。
五、计算题
19.某工厂化验室用15%的氢氧化钠溶液洗涤一定质量石油产品中的残余硫酸,共消耗氢氧化钠溶液80g,洗涤后的溶液呈中性。请计算这一定量石油产品中含H2SO4的质量是______?
20.某同学对上述实验继续展开探究,利用溶质质量分数为3.65%的稀盐酸溶液来测定10gNaOH溶液样品的溶质质量分数,用数字化传感器测得溶液中pH的变化如图所示。
(1)a点时向溶液中滴入无色酚酞试液,溶液显_______色。
(2)c点时溶液中的溶质有________种。
(3)当pH=7时恰好完全反应,求10 g NaOH溶液样品中溶质的质量分数。(反应的化学方程式:)
21.氢氧化钾固体曝露在空气中会吸水潮解,并且与二氧化碳反应生成碳酸钾。实验室有一瓶久置的氢氧化钾固体,称取26.0g固体样品,溶于水,加入足量稀盐酸,生成4.4g二氧化碳。
(1)碳酸钾(K2CO3)与盐酸反应生成二氧化碳,根据化学方程式计算样品中碳酸钾的质量___。
(2)将反应后的溶液蒸干,得到29.8g氯化钾。计算样品中钾元素的质量分数_______。
(3)通过计算确定该氢氧化钾固体样品的组成______。
参考答案:
1.C 2.D 3.C 4.B 5.D 6.B 7.B 8.B 9.C 10.C 11.C
12.(1)前者是乳化作用,后者是溶解
(2)
13. 分子是不断运动的 溶液由红色变为无色
14. CaO 熟石灰(或消石灰) 4 CaCO3+2HCl=CaCl2+H2O+CO2↑
15.(1)酸
(2)石蕊溶液
(3)铁
(4)
16.(1)或者
(2)放出
(3)
17.(1) Na+ Cl- H2O
(2) 复分解反应 氢氧根离子和氢离子反应生成水
(3)不准确,氢氧化钠固体溶于水也会放出大量的热
(4)不正确,若稀硫酸过量,溶液呈酸性时,酚酞试液也为无色
(5) Na2CO3
(6) 氢氧化钙溶液 产生白色沉淀
18.(1) A 2KMnO4K2MnO4+MnO2+O2↑
(2) B C 集气瓶口处
(3) 物理 红 B C
19.解:设含有硫酸的质量为x
x=14.7g
答:这一定量石油产品中含H2SO4的质量是14.7g。
20.(1)红
(2)2
(3)8%
当pH=7时恰好完全反应,设10 g NaOH溶液样品中溶质的质量为x。
x=0.8g
10 g NaOH溶液样品中溶质的质量分数为:=8%。
21.(1)设样品中碳酸钾的质量为x
解得x=13.8g
答:样品中碳酸钾的质量为13.8g。
(2)样品中钾元素的质量:
样品中钾元素的质量分数:
(3)碳酸钾中钾元素的质量:
样品中氢氧化钾的质量︰
水的含量为26.0g-13.8g-11.2g=1g
答:该固体样品由13.8g碳酸钾、11.2g氧氧化钾和1g水组成。
一、单选题
1.下列各组物质中,利用括号内的试剂或物品不能将它们一一鉴别出来的是
A.稀盐酸、氢氧化钠溶液、氯化钠溶液(无色酚酞)
B.空气、氧气、二氧化碳气体(燃着的木条)
C.氧化铁、铜和红磷三种红色固体(稀盐酸)
D.硝酸铵、氢氧化钠和氯化钠三种白色固体(水)
2.下列几组物质按照单质、氧化物、酸、碱顺序排列的是
A.C、H2O、H2SO4、Na2O
B.O3、KClO3、HCl、Ba(OH)2
C.He、HgO、CuSO4、Cu(OH)2
D.O2、Fe2O3、H2SO4、NH3·H2O
3.下列关于实验室洗涤仪器的说法中正确的是
A.用洗涤精清洗带油的试管是利用了溶解原理
B.洗净的试管应当正放在试管架上
C.长期存放石灰水的试剂瓶内壁常有白色固体,可用稀盐酸洗去
D.加热后的试管立即用冷水清洗
4.有甲、乙、丙、丁四种物质,在化学反应中的关系是:甲+乙→丙+丁,则下列说法中正确的是
A.若甲为盐酸,丁为水,则乙一定为碱
B.若甲为含碳、氢的化合物,乙为氧气,则该反应一定为氧化反应
C.若将10g甲和15g乙混合,充分反应后,则生成丙和丁的质量总和一定为25g
D.若甲、乙、丙、丁都是化合物,则该反应一定是复分解反应
5.化学实验中常会呈现颜色之美。下列化学实验中的颜色变化与实验事实不符的是
A.将生锈铁钉投入到稀盐酸中,溶液逐渐变为浅黄色
B.将少量氧化铜粉末加入稀硫酸中,微热,浑浊液体会逐渐变为蓝色溶液
C.向硫酸铜溶液中滴加氢氧化钠溶液会产生蓝色沉淀
D.将通入滴有石蕊的水中,溶液颜色由紫色逐渐变为蓝色
6.从化学视角看“烟、雾、光和焰”是有区别的。下列实验现象正确的是
A.红磷在空气中点燃,产生大量白色烟雾
B.木炭在氧气中燃烧,发出白光,生成使澄清石灰水变浑浊的气体
C.铁丝在氧气中点燃,产生红色火焰,生成黑色固体
D.打开浓盐酸的瓶盖,出现白烟
7.下列洗涤方式应用乳化作用的是
A.用汽油除去衣服上的油污 B.用洗洁精清洗餐具上的油污
C.无水酒精洗手机屏幕 D.用白醋清洗水壶的水垢
8.证据推理是化学学科核心素养的重要内容,下列推理正确的是
A.酸能使紫色石蕊溶液变红色,所以能使紫色石蕊溶液变红色的一定是酸
B.化合物由不同种元素组成,所以由不同种元素组成的纯净物一定是化合物
C.中和反应是有盐和水生成的反应,所以有盐和水生成的反应一定是中和反应
D.单质中只含一种元素,含一种元素的物质一定是单质
9.化学变化常常伴随一些明显的现象,下列实验现象描述错误的是
A.红磷在空气中燃烧,产生白烟 B.打开浓盐酸瓶盖,瓶口产生大量白雾
C.镁带放入食醋,产生氢气 D.“铜绿”加热,固体逐渐变成黑色
10.下列各组固体和液体分别放在如图所示装置,试管中有某种液体,将气球中的某种固体小心地倒入试管中,不能使气球膨胀的是
A.生石灰和水 B.镁和稀盐酸 C.氯化钠和水 D.石灰石和稀盐酸
11.“操作千万条,安全第一条”。化学实验是形成科学探究素养的必要手段。下列实验操作符合安全要求的是
A.点燃酒精灯 B.转移蒸发皿
C.闻气味 D.稀释浓硫酸
二、简答题
12.用学过的化学知识回答下列问题:
(1)洗涤剂能去除餐具上的油污,汽油也可以去除油污,二者原理有什么不同?_______
(2)工业上用稀硫酸来除铁锈,其反应的化学方程式为_______。
13.根据下图进行实验。
(1)该实验可证明分子具有的性质是______。
(2)此实验能够证明 NaOH 与 HCl 发生了化学反应,理由是______________________
三、推断题
14.A-E是初中化学常见的五种不同类别的物质,其中B由两种元素组成,C常用作食品干燥剂,并且C、D、E含有一种相同的金属元素,它们之间的转化关系如图所示(图中“一”表示两端的物质间能反应,“→”表示物质间存在转化关系,部分反应物、生成物和反应条件已略去)。请回答:
(1)物质C的化学式:___________。
(2)物质D俗称为___________(写一个);
(3)图中涉及的基本反应类型有___________个。
(4)反应“B-E”的化学方程式是___________。
15.如图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”。其中B是铁锈的主要成分,B、C、D分属于不同类别的物质,蓝色溶液可用于配制农药波尔多液。
请回答:
(1)溶液X是___________。(填“酸”“碱”、“盐”)
(2)试剂A的名称是___________。
(3)物质C的名称是___________。
(4)写出物质D与无色溶液X反应的化学方程式:___________。
16.A~F为初中化学常见的物质。D、E、F为不同类别的化合物且都含有相同的金属元素,其中E是常用的食品干燥剂。A是C通过绿色植物光合作用产生的气体,B是一种易与血红蛋白结合的有毒气体。它们的转化如图所示(“→”表示一种物质可以转化为另一种物质,部分反应物、生成物和反应条件已略去)。
(1)D→C的化学方程式为___________。
(2)E→F的反应___________(填“吸收”或“放出”)热量;
(3)F→D的化学方程式为___________。
四、实验题
17.探究稀盐酸和氢氧化钠溶液反应的实质,请回答有关问题。
(1)在上图C、D中的圆圈内应对应的化学式或离子符号填写在下面空白处:C中_________、_________。D中_________。
(2)用化学方程式表示图中所体现的化学反应:_________。此反应的基本类型是_________,此反应的实质是_________。
(3)实验时,甲同学将稀盐酸滴入到装有氢氧化钠固体的试管中,触摸试管有灼热感,他马上得出结论:氢氧化钠与稀盐酸反应会放出大量的热。该同学的观点是否准确?请说明理由:_________。
(4)乙同学进行该实验:在一支试管中加入NaOH溶液,再向其中滴加稀硫酸,振荡,最后滴加2滴酚酞试液,振荡,溶液不变色。乙据此判断酸和碱恰好完全反应。小明得出这样的结论是否正确?理由是_________。
(5)氢氧化钠溶液极易吸收空气中的二氧化碳而变质为_________(写化学式);该反应的化方程式:_________。
(6)证明一瓶氢氧化钠溶液已变质,可用试剂_________,该反应的化方程式为_________:如果已变质,则现象为_________。
18.今有A、B、C、D、E五种装置如下图所示。按下列要求回答问题(所选装置用其代号字母表示)
(1)实验室用高锰酸钾加热分解来制取氧气时,发生装置选用_______,该装置制取氧气的化学方程式为_________。
(2)实验室用大理石和稀盐酸来制取二氧化碳时,发生装置选用_____,收集装置常选用 ________;检验二氧化碳气体是否收集满把燃着的木条伸到_______。
(3)硫化氢(H2S)是一种无色且有臭鸡蛋气味的气体,密度比空气大,能溶于水,可形成一种酸溶液(氢硫酸)。实验室用硫化亚铁跟稀硫酸反应制取硫化氢气体。试回答:
①硫化氢气体具有臭鸡蛋味,这是硫化氢的_____(填“物理”或“化学”)性质。
②硫化氢的水溶液能使紫色石蕊试液变______色。
③实验室制取硫化氢气体时,发生装置应选用_____,收集装置应选用_____。
五、计算题
19.某工厂化验室用15%的氢氧化钠溶液洗涤一定质量石油产品中的残余硫酸,共消耗氢氧化钠溶液80g,洗涤后的溶液呈中性。请计算这一定量石油产品中含H2SO4的质量是______?
20.某同学对上述实验继续展开探究,利用溶质质量分数为3.65%的稀盐酸溶液来测定10gNaOH溶液样品的溶质质量分数,用数字化传感器测得溶液中pH的变化如图所示。
(1)a点时向溶液中滴入无色酚酞试液,溶液显_______色。
(2)c点时溶液中的溶质有________种。
(3)当pH=7时恰好完全反应,求10 g NaOH溶液样品中溶质的质量分数。(反应的化学方程式:)
21.氢氧化钾固体曝露在空气中会吸水潮解,并且与二氧化碳反应生成碳酸钾。实验室有一瓶久置的氢氧化钾固体,称取26.0g固体样品,溶于水,加入足量稀盐酸,生成4.4g二氧化碳。
(1)碳酸钾(K2CO3)与盐酸反应生成二氧化碳,根据化学方程式计算样品中碳酸钾的质量___。
(2)将反应后的溶液蒸干,得到29.8g氯化钾。计算样品中钾元素的质量分数_______。
(3)通过计算确定该氢氧化钾固体样品的组成______。
参考答案:
1.C 2.D 3.C 4.B 5.D 6.B 7.B 8.B 9.C 10.C 11.C
12.(1)前者是乳化作用,后者是溶解
(2)
13. 分子是不断运动的 溶液由红色变为无色
14. CaO 熟石灰(或消石灰) 4 CaCO3+2HCl=CaCl2+H2O+CO2↑
15.(1)酸
(2)石蕊溶液
(3)铁
(4)
16.(1)或者
(2)放出
(3)
17.(1) Na+ Cl- H2O
(2) 复分解反应 氢氧根离子和氢离子反应生成水
(3)不准确,氢氧化钠固体溶于水也会放出大量的热
(4)不正确,若稀硫酸过量,溶液呈酸性时,酚酞试液也为无色
(5) Na2CO3
(6) 氢氧化钙溶液 产生白色沉淀
18.(1) A 2KMnO4K2MnO4+MnO2+O2↑
(2) B C 集气瓶口处
(3) 物理 红 B C
19.解:设含有硫酸的质量为x
x=14.7g
答:这一定量石油产品中含H2SO4的质量是14.7g。
20.(1)红
(2)2
(3)8%
当pH=7时恰好完全反应,设10 g NaOH溶液样品中溶质的质量为x。
x=0.8g
10 g NaOH溶液样品中溶质的质量分数为:=8%。
21.(1)设样品中碳酸钾的质量为x
解得x=13.8g
答:样品中碳酸钾的质量为13.8g。
(2)样品中钾元素的质量:
样品中钾元素的质量分数:
(3)碳酸钾中钾元素的质量:
样品中氢氧化钾的质量︰
水的含量为26.0g-13.8g-11.2g=1g
答:该固体样品由13.8g碳酸钾、11.2g氧氧化钾和1g水组成。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
