第5章第2节第2課时《氮及其化合物》课件2021-2022学年下学期高一化学人教版(2019)必修第二册
文档属性
| 名称 | 第5章第2节第2課时《氮及其化合物》课件2021-2022学年下学期高一化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 21.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-27 00:00:00 | ||
图片预览








文档简介
(共24张PPT)
第二节 氮及其化合物
玻尔是丹麦著名的物理学家,曾获得诺贝尔奖。第二次世界大战中,玻尔被迫离开将要被德国占领的祖国。为了表示他一定要返回祖国的决心,他将诺贝尔金质奖章溶解在一种溶液里,装于玻璃瓶中,然后将它放在柜台上。后来,纳粹分子闯进玻尔的住宅,那瓶溶有奖章的溶液就在眼皮底下,他们却一无所知。这是一个多么聪明的办法啊!战争结束后,玻尔又从溶液中还原提取出金,并重新铸成奖章。
新铸成的奖章显得更加灿烂夺目,因为它凝聚着玻尔对祖国无限的热爱和其本人无穷的智慧。那么,玻尔是用什么溶液使金质奖章溶解的呢?原来他用的溶液叫王水。王水是由浓硝酸和浓盐酸按1比3的体积比配制成的混合溶液。你知道其中的硝酸具有怎样的化学性质吗?
硝 酸
⑴纯硝酸是无色、易挥发、有刺激性气味的液体。
⑵能以任意比溶于水;
⑶密度比水大;
⑷沸点低:83℃;
⑸常用浓硝酸的浓度为69%,
98%的浓硝酸叫作“发烟硝酸”。
一、硝酸的物理性质:
常见酸的挥发性
⑴常见的易挥发性酸(或称低沸点酸)
有HNO3、盐酸、H2CO3等;
⑵难挥发性的酸(或称高沸点酸)
有H2SO4、H3PO4等。
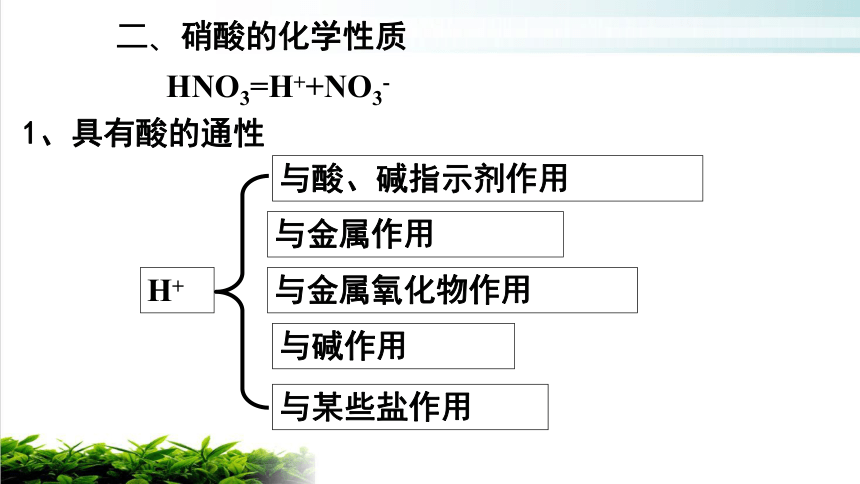
二、硝酸的化学性质
HNO3=H++NO3-
1、具有酸的通性
与酸、碱指示剂作用
与金属作用
与金属氧化物作用
与碱作用
与某些盐作用
H+
2、硝酸的不稳定性:
① 常用浓硝酸为何呈黄色?
② 实验室应怎样贮放浓硝酸?
4HNO3 O2↑ +2H2O + 4NO2↑
△
或光照
久置硝酸分解产生的NO2溶于溶液中,使得溶液变黄!
密封于棕色瓶中,并放在阴暗处!
保存:
3、硝酸具有强氧化性:
Cu+4HNO3(浓)=Cu(NO3)2+ 2NO2↑+2H2O
氧化剂
3Cu +8HNO3(稀)=3Cu(NO3)2 +2NO↑+4H2O
硝酸与氢后不活泼金属反应的规律:
M+ HNO3(稀) → M(NO3)n +H2O +2NO↑
M+ HNO3(浓) → M(NO3)n +H2O +2NO2↑
还原剂
实验
实 验 装 置
稀硝酸 浓硝酸
实 验 现 象 反应缓慢,有少量气泡产生,__________,试管口有红棕色气体产生 反应剧烈,有__________产生,__________,液面上有________气体产生
实 验 结 论 铜与稀硝酸常温下缓慢反应生成___气体 铜与浓硝酸常温下剧烈反应生成___气体
溶液变蓝
大量气泡
溶液变蓝
红棕色
NO
NO2
注意:除Au、Pt 以外的绝大多数金属都能与硝酸反应。常温下Fe 和Al遇到冷的浓硝酸被钝化,被氧化成一层致密的氧化膜,与浓硫酸一样。
氧化性:浓硝酸>稀硝酸
△
C + 4HNO3(浓)===CO2 ↑+ 4NO2↑ + 2H2O
与某些非金属反应
结论:浓硝酸跟非金属反应,生成NO2、 H2O和相应非金属氧化物或其含氧酸
硝酸还能氧化FeO、 Fe(NO3)2(Fe2+)、 HBr(Br-)、 HI(I-) 、H2S (S2-)、 SO2等具有还原性的化合物发生氧化还原反应,因此,不能用硝酸与有关的盐反应制取HI、 SO2、 H2S、 HBr等气体
小结:硝酸与金属反应时,主要是HNO3中+5价的氮得到电子,被还原成较低价氮的物质,稀硝酸的还原产物一般是NO,浓硝酸的还原产物一般是NO2,而不像盐酸与金属反应那样生成H2。
三.硝酸的用途与工业制法
(1)用途:
(2)工业制法:
①工业流程:
②写出有关化学方程式:
N2→NH3: ____________________。
NH3→NO: _______________________。
NO→NO2: ______________。
NO2→HNO3: ____________________。
N2+3H2 2NH3
4NH3+5O2 4NO+6H2O
2NO+O2====2NO2
3NO2+H2O====2HNO3+NO
1. 下列关于硝酸的认识中,正确的是( )
A. 浓硝酸和稀硝酸都具有氧化性
B. 浓硝酸与金属反应不产生氢气,而稀硝酸与金属反应可置换出氢气
C. 因常温下铝和铁不与浓硝酸反应,所以浓硝酸可盛放在铝制或铁制容器中
D. 硝酸与金属反应时,只表现出氧化性
A
【解析】浓、稀硝酸都有氧化性,几乎可与除Au、Pt之外的所有金属反应,且不产生氢气;在与金属反应时,硝酸既表现强氧化性又表现酸性;浓硝酸可盛放在铝制或铁制容器中,因为铝和铁在冷浓硝酸中钝化。
2.单质跟浓HNO3 混合出现的情况依次为:①反应生成相应的硝酸盐②反应生成最高价氧化物③单质呈钝态④不发生反应
符合上述情况的单质是: ( )
A. Cu P Zn Au B. Ag C Al Pt
C. Fe C Zn Hg D. C S Fe Au
B
3. 将铜粉放入稀H2SO4中,加热无明显现象发生,当加入下列一种物质后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出,该物质是( )
A. Fe2(SO4)3 B. Na2SO4 C. KNO3 D. FeSO4
C
1.中国古代海洋小说的产生和发展,从时间的向度来看,有着悠久的历史;从内容和品质的维度来看,却并不是呈现为鲜明的向前发展的进步性,而是出现经常性回复或几种形态并存的倾向。
2.自从古代朝廷采用科举考试选拔人才以来,“金榜题名”与“名落孙山”始终结伴而行。于是,针对考生开发的“补习班”便应运而生。
3.书院除了要求学生熟读“四书五经”,还锻炼学生们写八股文的能力,熟悉八股文的格律、步骤等。唐朝和宋朝的科举考试,策问一科是学生们的重点复习对象。
4.文章通过对比,论证了只有完成由传统经济模式到新动能模式的转型升级,中国经济才有无可限量的未来这一观点。
5.文艺高峰的出现,除客观社会环境外,创作主体至关重要。政治清明、经济繁荣、文化昌盛,为文艺家勇攀文艺高峰创设良好客观条件,但伟大杰出作品的产生依然有赖于文艺家自身努力,换句话说,创作主体高度决定文艺高度。
6.改革开放以来,我国农业从传统走向现代,从单一走向多元,生产技术装备不断升级,农产品产量快速增长都得益于科技对农业的支撑。
7.小说结尾聚焦于父亲与林掌柜的三举杯,这一情景极具仪式感,既是雪夜酒叙情节的收束,也是全文的升华,带给读者无限遐想。
8.作者指出人之所以能适应人生境遇的种种变化,就是因为这些变化是在相当长的时间里达到的。
9.时间之所以让人感到渺茫和不可思议,是因为和空间相比,时间既无法把握,又无法挽留。
10.这篇散文语言优美、细腻,文采飘逸、富有想象力,字里行间流露出浓浓的文学韵味,让人回味无穷。
11.另一种水声,是流水声,细弱又清亮。它来自幽暗的捞纸房某个角落,水从一只装满纸浆的槽缸里溢出来,匍匐进地面。几近难以察觉的流水声,被无边的寂静扩大了。水声泠泠,像由远及近的银铃声从云霄洒落大地。
感谢观看,欢迎指导!
第二节 氮及其化合物
玻尔是丹麦著名的物理学家,曾获得诺贝尔奖。第二次世界大战中,玻尔被迫离开将要被德国占领的祖国。为了表示他一定要返回祖国的决心,他将诺贝尔金质奖章溶解在一种溶液里,装于玻璃瓶中,然后将它放在柜台上。后来,纳粹分子闯进玻尔的住宅,那瓶溶有奖章的溶液就在眼皮底下,他们却一无所知。这是一个多么聪明的办法啊!战争结束后,玻尔又从溶液中还原提取出金,并重新铸成奖章。
新铸成的奖章显得更加灿烂夺目,因为它凝聚着玻尔对祖国无限的热爱和其本人无穷的智慧。那么,玻尔是用什么溶液使金质奖章溶解的呢?原来他用的溶液叫王水。王水是由浓硝酸和浓盐酸按1比3的体积比配制成的混合溶液。你知道其中的硝酸具有怎样的化学性质吗?
硝 酸
⑴纯硝酸是无色、易挥发、有刺激性气味的液体。
⑵能以任意比溶于水;
⑶密度比水大;
⑷沸点低:83℃;
⑸常用浓硝酸的浓度为69%,
98%的浓硝酸叫作“发烟硝酸”。
一、硝酸的物理性质:
常见酸的挥发性
⑴常见的易挥发性酸(或称低沸点酸)
有HNO3、盐酸、H2CO3等;
⑵难挥发性的酸(或称高沸点酸)
有H2SO4、H3PO4等。
二、硝酸的化学性质
HNO3=H++NO3-
1、具有酸的通性
与酸、碱指示剂作用
与金属作用
与金属氧化物作用
与碱作用
与某些盐作用
H+
2、硝酸的不稳定性:
① 常用浓硝酸为何呈黄色?
② 实验室应怎样贮放浓硝酸?
4HNO3 O2↑ +2H2O + 4NO2↑
△
或光照
久置硝酸分解产生的NO2溶于溶液中,使得溶液变黄!
密封于棕色瓶中,并放在阴暗处!
保存:
3、硝酸具有强氧化性:
Cu+4HNO3(浓)=Cu(NO3)2+ 2NO2↑+2H2O
氧化剂
3Cu +8HNO3(稀)=3Cu(NO3)2 +2NO↑+4H2O
硝酸与氢后不活泼金属反应的规律:
M+ HNO3(稀) → M(NO3)n +H2O +2NO↑
M+ HNO3(浓) → M(NO3)n +H2O +2NO2↑
还原剂
实验
实 验 装 置
稀硝酸 浓硝酸
实 验 现 象 反应缓慢,有少量气泡产生,__________,试管口有红棕色气体产生 反应剧烈,有__________产生,__________,液面上有________气体产生
实 验 结 论 铜与稀硝酸常温下缓慢反应生成___气体 铜与浓硝酸常温下剧烈反应生成___气体
溶液变蓝
大量气泡
溶液变蓝
红棕色
NO
NO2
注意:除Au、Pt 以外的绝大多数金属都能与硝酸反应。常温下Fe 和Al遇到冷的浓硝酸被钝化,被氧化成一层致密的氧化膜,与浓硫酸一样。
氧化性:浓硝酸>稀硝酸
△
C + 4HNO3(浓)===CO2 ↑+ 4NO2↑ + 2H2O
与某些非金属反应
结论:浓硝酸跟非金属反应,生成NO2、 H2O和相应非金属氧化物或其含氧酸
硝酸还能氧化FeO、 Fe(NO3)2(Fe2+)、 HBr(Br-)、 HI(I-) 、H2S (S2-)、 SO2等具有还原性的化合物发生氧化还原反应,因此,不能用硝酸与有关的盐反应制取HI、 SO2、 H2S、 HBr等气体
小结:硝酸与金属反应时,主要是HNO3中+5价的氮得到电子,被还原成较低价氮的物质,稀硝酸的还原产物一般是NO,浓硝酸的还原产物一般是NO2,而不像盐酸与金属反应那样生成H2。
三.硝酸的用途与工业制法
(1)用途:
(2)工业制法:
①工业流程:
②写出有关化学方程式:
N2→NH3: ____________________。
NH3→NO: _______________________。
NO→NO2: ______________。
NO2→HNO3: ____________________。
N2+3H2 2NH3
4NH3+5O2 4NO+6H2O
2NO+O2====2NO2
3NO2+H2O====2HNO3+NO
1. 下列关于硝酸的认识中,正确的是( )
A. 浓硝酸和稀硝酸都具有氧化性
B. 浓硝酸与金属反应不产生氢气,而稀硝酸与金属反应可置换出氢气
C. 因常温下铝和铁不与浓硝酸反应,所以浓硝酸可盛放在铝制或铁制容器中
D. 硝酸与金属反应时,只表现出氧化性
A
【解析】浓、稀硝酸都有氧化性,几乎可与除Au、Pt之外的所有金属反应,且不产生氢气;在与金属反应时,硝酸既表现强氧化性又表现酸性;浓硝酸可盛放在铝制或铁制容器中,因为铝和铁在冷浓硝酸中钝化。
2.单质跟浓HNO3 混合出现的情况依次为:①反应生成相应的硝酸盐②反应生成最高价氧化物③单质呈钝态④不发生反应
符合上述情况的单质是: ( )
A. Cu P Zn Au B. Ag C Al Pt
C. Fe C Zn Hg D. C S Fe Au
B
3. 将铜粉放入稀H2SO4中,加热无明显现象发生,当加入下列一种物质后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出,该物质是( )
A. Fe2(SO4)3 B. Na2SO4 C. KNO3 D. FeSO4
C
1.中国古代海洋小说的产生和发展,从时间的向度来看,有着悠久的历史;从内容和品质的维度来看,却并不是呈现为鲜明的向前发展的进步性,而是出现经常性回复或几种形态并存的倾向。
2.自从古代朝廷采用科举考试选拔人才以来,“金榜题名”与“名落孙山”始终结伴而行。于是,针对考生开发的“补习班”便应运而生。
3.书院除了要求学生熟读“四书五经”,还锻炼学生们写八股文的能力,熟悉八股文的格律、步骤等。唐朝和宋朝的科举考试,策问一科是学生们的重点复习对象。
4.文章通过对比,论证了只有完成由传统经济模式到新动能模式的转型升级,中国经济才有无可限量的未来这一观点。
5.文艺高峰的出现,除客观社会环境外,创作主体至关重要。政治清明、经济繁荣、文化昌盛,为文艺家勇攀文艺高峰创设良好客观条件,但伟大杰出作品的产生依然有赖于文艺家自身努力,换句话说,创作主体高度决定文艺高度。
6.改革开放以来,我国农业从传统走向现代,从单一走向多元,生产技术装备不断升级,农产品产量快速增长都得益于科技对农业的支撑。
7.小说结尾聚焦于父亲与林掌柜的三举杯,这一情景极具仪式感,既是雪夜酒叙情节的收束,也是全文的升华,带给读者无限遐想。
8.作者指出人之所以能适应人生境遇的种种变化,就是因为这些变化是在相当长的时间里达到的。
9.时间之所以让人感到渺茫和不可思议,是因为和空间相比,时间既无法把握,又无法挽留。
10.这篇散文语言优美、细腻,文采飘逸、富有想象力,字里行间流露出浓浓的文学韵味,让人回味无穷。
11.另一种水声,是流水声,细弱又清亮。它来自幽暗的捞纸房某个角落,水从一只装满纸浆的槽缸里溢出来,匍匐进地面。几近难以察觉的流水声,被无边的寂静扩大了。水声泠泠,像由远及近的银铃声从云霄洒落大地。
感谢观看,欢迎指导!
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
