5.1硫及其化合物第一课时硫和二氧化硫课件2021-2022学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 5.1硫及其化合物第一课时硫和二氧化硫课件2021-2022学年高一下学期化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 22.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-27 00:00:00 | ||
图片预览








文档简介
(共26张PPT)
2022年1月15日,位于汤加努库阿洛法以北约65公里处的洪阿哈阿帕伊岛海底火山发生第二次剧烈喷发
大家了解火山喷发对人类生产生活会造成什么影响吗?
海啸、空气污染、酸雨
释放出许多含硫物质,火山口有硫单质
火山喷发与含硫物质密切相关,大家对硫元素有多少了解呢?
S的电子式
S的常见价态
S位于周期表中的位置
S的非金属性强弱
常见的含S物质
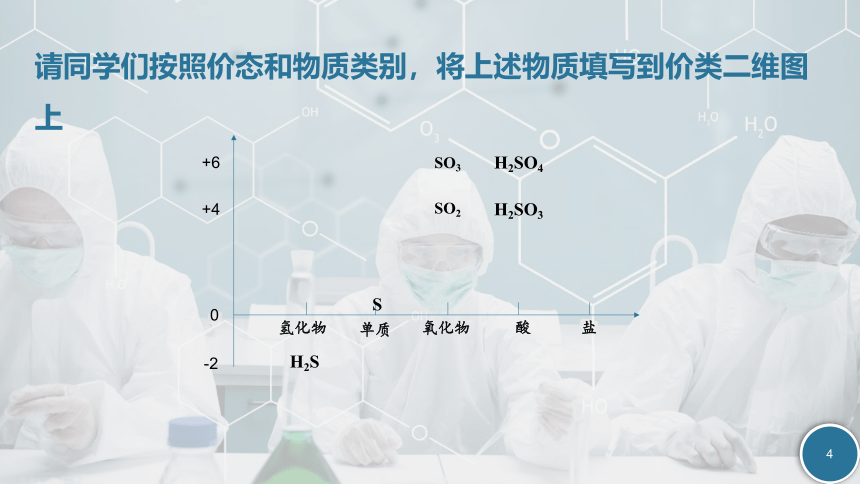
请同学们按照价态和物质类别,将上述物质填写到价类二维图上
+6
+4
-2
0
氢化物
单质
氧化物
酸
盐
H2S
S
H2SO4
H2SO3
SO3
SO2
硫及其化合物
第一节 硫单质
一、硫单质
1.物理性质
俗称硫磺、黄色晶体,质脆、易研成粉末,难溶于水、微溶于酒精、易溶于CS2。
2.化学性质
学生活动:你能推断出硫单质具有怎样的化学性质吗,说出你的理由,设计实验验证。
+6
+4
-2
0
氢化物
单质
氧化物
酸
盐
H2S
S
H2SO4
H2SO3
SO3
SO2
硫单质的化合价为0,可升可降,既有氧化性,又有还原性。
如何体现它的氧化性和还原性呢,设计硫与其它物质的反应,写出方程式
Fe+S=加热=FeS
氧化性:
如何体现它的氧化性和还原性呢,设计硫与其它物质的反应,写出方程式
Fe+S=加热=FeS
氧化性:
2Cu+S=加热=Cu2S
H2+S=加热=H2S
还原性:
O2+S=点燃=SO2
你觉得金属单质硫还有什么化学性质。
3S+6NaOH=加热=2Na2S+Na2SO3+3H2O
火山爆发为什么会形成酸雨呢?什么是酸雨,酸雨的形成主要与什么物质有关呢?
第二节 二氧化硫
二、二氧化硫
1.物理性质
无色,有刺激性气味,有毒气体,密度比空气大,易溶于水,1体积水可溶解40体积的二氧化硫。
大家有没有吸入过这种气体呢?
炮仗的燃烧会放出大量的刺激性气体,里面含有二氧化硫。
二氧化硫与酸雨的形成有什么关系呢,你是怎样考虑的,设计实验证明。
+6
+4
-2
0
氢化物
单质
氧化物
酸
盐
H2S
S
H2SO4
H2SO3
SO3
SO2
2.化学性质
a、SO2+H2O H2SO3
此反应是一个可逆反应,既能正向进行,同时又能逆向进行。
某同学将溶有二氧化硫的水溶液放置一段时间后,再测pH发现此时的pH值比上次小,分析原因为什么。
2.化学性质
a、SO2+H2O H2SO3
b、2SO2+O2 2SO3
SO3+H2O==H2SO4
通过上面的实验,请同学们说明硫酸型酸雨形成的途径,主要途径是什么?
H2SO4
H2SO3
SO3
SO2
O2
使雨水显酸性
如何防止酸雨的形成,从二氧化硫的来源和性质思考,从防的角度,从治的角度。
减少二氧化硫的排放,对工业废气(二氧化硫)进行吸收利用。
通过上面酸雨的形成路径,思考你对工业生产硫酸有什么启示
H2SO4
H2SO3
SO3
SO2
O2
使雨水显酸性
如何以硫磺矿或黄铁矿为原料,如何实现工业生产硫酸。
3.二氧化硫的用途
3.二氧化硫的用途
二氧化硫不仅在工业生产中有重要作用,还可以用于生活方面,如食品添加剂中可以添加适量SO2用于防腐和抗氧化,还可以利用其进行漂白。
2022年1月15日,位于汤加努库阿洛法以北约65公里处的洪阿哈阿帕伊岛海底火山发生第二次剧烈喷发
大家了解火山喷发对人类生产生活会造成什么影响吗?
海啸、空气污染、酸雨
释放出许多含硫物质,火山口有硫单质
火山喷发与含硫物质密切相关,大家对硫元素有多少了解呢?
S的电子式
S的常见价态
S位于周期表中的位置
S的非金属性强弱
常见的含S物质
请同学们按照价态和物质类别,将上述物质填写到价类二维图上
+6
+4
-2
0
氢化物
单质
氧化物
酸
盐
H2S
S
H2SO4
H2SO3
SO3
SO2
硫及其化合物
第一节 硫单质
一、硫单质
1.物理性质
俗称硫磺、黄色晶体,质脆、易研成粉末,难溶于水、微溶于酒精、易溶于CS2。
2.化学性质
学生活动:你能推断出硫单质具有怎样的化学性质吗,说出你的理由,设计实验验证。
+6
+4
-2
0
氢化物
单质
氧化物
酸
盐
H2S
S
H2SO4
H2SO3
SO3
SO2
硫单质的化合价为0,可升可降,既有氧化性,又有还原性。
如何体现它的氧化性和还原性呢,设计硫与其它物质的反应,写出方程式
Fe+S=加热=FeS
氧化性:
如何体现它的氧化性和还原性呢,设计硫与其它物质的反应,写出方程式
Fe+S=加热=FeS
氧化性:
2Cu+S=加热=Cu2S
H2+S=加热=H2S
还原性:
O2+S=点燃=SO2
你觉得金属单质硫还有什么化学性质。
3S+6NaOH=加热=2Na2S+Na2SO3+3H2O
火山爆发为什么会形成酸雨呢?什么是酸雨,酸雨的形成主要与什么物质有关呢?
第二节 二氧化硫
二、二氧化硫
1.物理性质
无色,有刺激性气味,有毒气体,密度比空气大,易溶于水,1体积水可溶解40体积的二氧化硫。
大家有没有吸入过这种气体呢?
炮仗的燃烧会放出大量的刺激性气体,里面含有二氧化硫。
二氧化硫与酸雨的形成有什么关系呢,你是怎样考虑的,设计实验证明。
+6
+4
-2
0
氢化物
单质
氧化物
酸
盐
H2S
S
H2SO4
H2SO3
SO3
SO2
2.化学性质
a、SO2+H2O H2SO3
此反应是一个可逆反应,既能正向进行,同时又能逆向进行。
某同学将溶有二氧化硫的水溶液放置一段时间后,再测pH发现此时的pH值比上次小,分析原因为什么。
2.化学性质
a、SO2+H2O H2SO3
b、2SO2+O2 2SO3
SO3+H2O==H2SO4
通过上面的实验,请同学们说明硫酸型酸雨形成的途径,主要途径是什么?
H2SO4
H2SO3
SO3
SO2
O2
使雨水显酸性
如何防止酸雨的形成,从二氧化硫的来源和性质思考,从防的角度,从治的角度。
减少二氧化硫的排放,对工业废气(二氧化硫)进行吸收利用。
通过上面酸雨的形成路径,思考你对工业生产硫酸有什么启示
H2SO4
H2SO3
SO3
SO2
O2
使雨水显酸性
如何以硫磺矿或黄铁矿为原料,如何实现工业生产硫酸。
3.二氧化硫的用途
3.二氧化硫的用途
二氧化硫不仅在工业生产中有重要作用,还可以用于生活方面,如食品添加剂中可以添加适量SO2用于防腐和抗氧化,还可以利用其进行漂白。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
