人教版九年级化学下册 9.2 溶解度 第一课时(17张PPT)
文档属性
| 名称 | 人教版九年级化学下册 9.2 溶解度 第一课时(17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 18.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-26 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
第九单元
溶液
课题2
溶解度
第1课时
饱和溶液
学习目标:
1、通过实验知道饱和溶液、不饱和溶液的概念。
2、知道饱和溶液和不饱和溶液之间的转化方法。
3、了解结晶的概念,知道结晶有蒸发溶剂和冷却热饱和
溶液两种途径。
活动一
饱和溶液与不饱和溶液的概念
实验探究一
向试管A中加水至第一个红刻度线处,然后按下表步骤进行实验。
步骤
操作
现象
加入1药匙NaCl,震荡
全部溶解
加入2药匙aCl,震荡
不能全部溶解
3
再加水至红刻度线,震荡
全部溶解
结论:在一定条件下,NaC不能无限溶解,当不能溶解时,加水后又
能继续溶解。
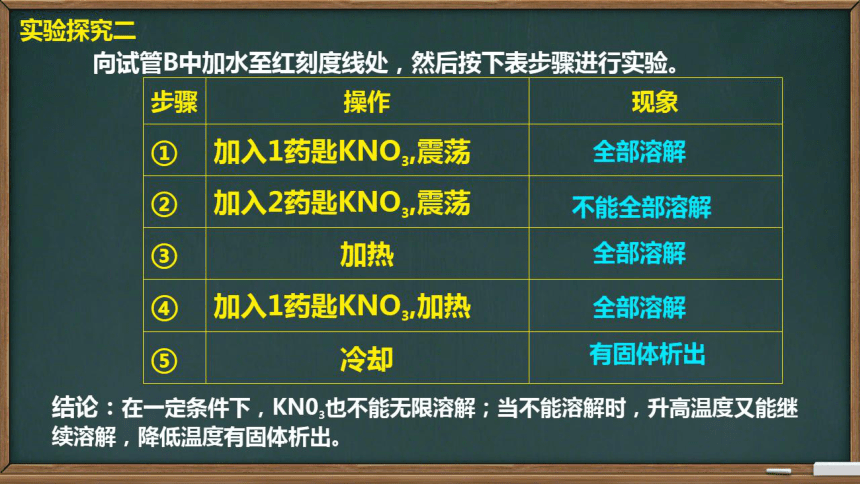
实验探究二
向试管B中加水至红刻度线处,然后按下表步骤进行实验。
步骤
操作
现象
加入1药匙KNO,震荡
全部溶解
2
加入2药匙KNO,震荡
不能全部溶解
3
加热
全部溶解
4
加入1药匙KNO,加热
全部溶解
⑤
冷却
有固体析出
结论:在一定条件下,KN0也不能无限溶解;当不能溶解时,升高温度又能继
续溶解,降低温度有固体析出。
1.上述两个实验活动的”一定条件”是什么?
一定量溶剂
一定温度
2.若改变这两个条件,溶质能否无限制溶解?
若是改变这两个条件,溶质可以无限制溶解。
3.你能根据归纳出饱和溶液和不饱和溶液概念吗?
实验探究三
向KNO,的饱和溶液中加入少量固体硫酸铜,观察实验现象。
现象:试管底部的KNO:固体没有溶解,无色溶液变蓝
结论:某种溶质的饱和溶液还能够溶解其他物质。
饱和溶液与不饱和溶液的概念
在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解
时,所得到的溶液叫做这种溶质的饱和溶液。
在一定温度下,向一定量溶剂里加入某种溶质,还能继续溶解某种溶
质的溶液,叫做这种溶质的不饱和溶液。
活动二
饱和溶液和不饱和溶液的判断方法
根据实验判断下列各溶液,哪些一定是饱和溶液?并说明理由。
5 g NaCl
5g NaCl
-0
加15mL水
-30
A
上B
室温
室温
室温20mL水+
5g KNO3
g KNO3.
5
加热到60℃
-50m
5g KNO3.
50m
-50
冷却。
-50rH
-一30m
一401
-50m
2
3
二4
5
室温
室温
60℃+
至室温。
室温
20mL水w
思考:在一定温度、一定量溶剂的条件下,能否总结出判断饱和溶液的方法?
饱和溶液和不饱和溶液的判断方法:
有未溶或析出固体
这种溶质的饱和溶液
溶液
不溶解
这种溶质的饱和溶液
固体全部溶解
加这种溶质
溶解
这种溶质的不饱和溶液
第九单元
溶液
课题2
溶解度
第1课时
饱和溶液
学习目标:
1、通过实验知道饱和溶液、不饱和溶液的概念。
2、知道饱和溶液和不饱和溶液之间的转化方法。
3、了解结晶的概念,知道结晶有蒸发溶剂和冷却热饱和
溶液两种途径。
活动一
饱和溶液与不饱和溶液的概念
实验探究一
向试管A中加水至第一个红刻度线处,然后按下表步骤进行实验。
步骤
操作
现象
加入1药匙NaCl,震荡
全部溶解
加入2药匙aCl,震荡
不能全部溶解
3
再加水至红刻度线,震荡
全部溶解
结论:在一定条件下,NaC不能无限溶解,当不能溶解时,加水后又
能继续溶解。
实验探究二
向试管B中加水至红刻度线处,然后按下表步骤进行实验。
步骤
操作
现象
加入1药匙KNO,震荡
全部溶解
2
加入2药匙KNO,震荡
不能全部溶解
3
加热
全部溶解
4
加入1药匙KNO,加热
全部溶解
⑤
冷却
有固体析出
结论:在一定条件下,KN0也不能无限溶解;当不能溶解时,升高温度又能继
续溶解,降低温度有固体析出。
1.上述两个实验活动的”一定条件”是什么?
一定量溶剂
一定温度
2.若改变这两个条件,溶质能否无限制溶解?
若是改变这两个条件,溶质可以无限制溶解。
3.你能根据归纳出饱和溶液和不饱和溶液概念吗?
实验探究三
向KNO,的饱和溶液中加入少量固体硫酸铜,观察实验现象。
现象:试管底部的KNO:固体没有溶解,无色溶液变蓝
结论:某种溶质的饱和溶液还能够溶解其他物质。
饱和溶液与不饱和溶液的概念
在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解
时,所得到的溶液叫做这种溶质的饱和溶液。
在一定温度下,向一定量溶剂里加入某种溶质,还能继续溶解某种溶
质的溶液,叫做这种溶质的不饱和溶液。
活动二
饱和溶液和不饱和溶液的判断方法
根据实验判断下列各溶液,哪些一定是饱和溶液?并说明理由。
5 g NaCl
5g NaCl
-0
加15mL水
-30
A
上B
室温
室温
室温20mL水+
5g KNO3
g KNO3.
5
加热到60℃
-50m
5g KNO3.
50m
-50
冷却。
-50rH
-一30m
一401
-50m
2
3
二4
5
室温
室温
60℃+
至室温。
室温
20mL水w
思考:在一定温度、一定量溶剂的条件下,能否总结出判断饱和溶液的方法?
饱和溶液和不饱和溶液的判断方法:
有未溶或析出固体
这种溶质的饱和溶液
溶液
不溶解
这种溶质的饱和溶液
固体全部溶解
加这种溶质
溶解
这种溶质的不饱和溶液
同课章节目录
