第八单元 课题3金属资源的利用和保护课件—2021-2022学年九年级化学人教版下册(共45张PPT内嵌视频)
文档属性
| 名称 | 第八单元 课题3金属资源的利用和保护课件—2021-2022学年九年级化学人教版下册(共45张PPT内嵌视频) |  | |
| 格式 | pptx | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-26 21:05:05 | ||
图片预览










文档简介
(共45张PPT)
课堂导入
自然界中存在各式各样的矿石,但大多都是以化合物形式存在,因此工业上常从含有金属元素并有开采价值的矿石中提炼金属。那究竟如何从矿石中提炼金属呢?
课题3 金属资源的利用和保护
///人教版义务教育教科书化学九年级下册///
一、常见的金属矿石
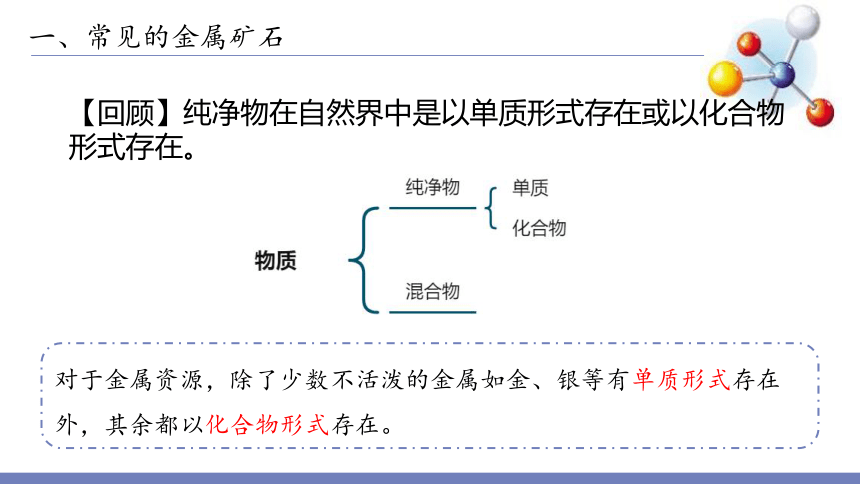
【回顾】纯净物在自然界中是以单质形式存在或以化合物形式存在。
对于金属资源,除了少数不活泼的金属如金、银等有单质形式存在外,其余都以化合物形式存在。
一、常见的金属矿石
1、以单质形式存在
少数化学性质不活泼的金属,以单质形态存在,如金、银、铂。
自然界中以单质形态存在的金
自然界中以单质形态存在的银
游离态
指某元素不与其他元素化合,而能单独存在的状态。
一、常见的金属矿石
2、以化合物形式存在
绝大多数物质都是以化合物的形式存在,如水,二氧化碳等。
化合态
某物质由多种元素组成,那么其状态即被称为化合态。
赤铁矿是红色固体,是自然界分布极广的铁矿物,是重要的炼铁原料,也可用作红色颜料
赤铁矿(主要成分Fe2O3)
一、常见的金属矿石
磁铁矿
(主要成分Fe3O4)
磁铁矿是黑色固体,是矿物中磁性最强的。
【思考1】铁的常见化合价是多少呢?
+2价,+3价
【思考2】铁的常见氧化物有什么呢?
FeO、Fe2O3、Fe3O4
【思考3】自然界中铁矿石成分多为Fe2O3、Fe3O4,基本没有以FeO存在,你可以推断出什么呢?
FeO在自然界中不稳定。
菱铁矿
(主要成分FeCO3)
一、常见的金属矿石
铝土矿
(主要成分Al2O3)
辉铜矿
(主要成分Cu2S)
黄铜矿
(主要成分CuFeS2)
我国是世界上已知矿物种类比较齐全的少数国家之一,矿物储量丰富,其中钨、钼、钛、锡、锑等储量居世界前列,铜、铝、锰等储量在世界上也占有重要地位。
二、铁的冶炼
【回顾】课题1的学习中,我们已知我国早在春秋战国时期便开始生产和使用铁器,那你知道铁是如何冶炼的吗?
二、铁的冶炼
翻译:铁分为生铁和熟铁两种:其中已经出炉但是还没有炒过的是生铁,炒过以后便成了熟铁。……一座炼铁炉可以装铁矿石两千多斤,燃料有的用硬木柴,有的用煤或者用木炭,南方北方可根据方便就地取料。鼓风的风箱要由四个人或者六个人一起推拉。铁矿石化成了铁水之后,就会从炼铁炉腰孔中流出来。
二、铁的冶炼
古代铸铁就是利用鼓风机使燃料充分燃烧,用高温火焰熔化铁矿,并不断加入木炭粉,使其保持液态,令炉渣充分析出,最后用液态的铁碳合金铸造农具和日用品。
炼铁的原理是利用一氧化碳与氧化铁的反应。
古代炼铁时,使燃料(木炭)不断燃烧,并不断加入木炭粉,是为了使木炭充分燃烧生成的二氧化碳与木炭反应生成一氧化碳,一氧化碳将铁矿(氧化铁)反应还原为铁,从而达到炼铁的目的。
1、古代炼铁
二、铁的冶炼
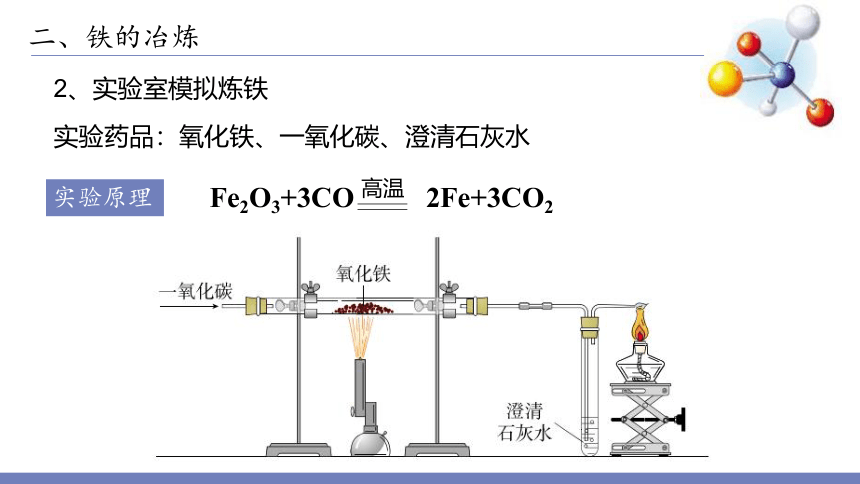
实验药品:氧化铁、一氧化碳、澄清石灰水
实验原理
Fe2O3+3CO 2Fe+3CO2
高温
2、实验室模拟炼铁
二、铁的冶炼
请带着这几个问题观看实验视频。
1.实验开始时为什么要先通入CO后点燃酒精喷灯?
2.实验中,澄清石灰水的作用是?
3.装置中右边的酒精灯起什么作用?
4.实验结束后为什么要先移除热源,待装置冷却才停止通入CO?
二、铁的冶炼
1.实验开始时为什么要先通入CO后点燃酒精喷灯?
2.实验中,澄清石灰水的作用是?
3.装置中右边的酒精灯起什么作用?
4.实验结束后为什么要先移除热源,待装置冷却才停止通入CO?
2CO + O2 2CO2
二、铁的冶炼
实验总结
现象1:红色粉末逐渐变成黑色
Fe2O3+3CO 2Fe+3CO2
高温
现象2:澄清的石灰水变浑浊
CO2+Ca(OH)2==CaCO3↓+ H2O
现象3:尾气燃烧产生蓝色火焰
点燃
二、铁的冶炼
实验总结
1.实验开始时为什么要先通入CO后点燃酒精喷灯?
先通入CO是为了将装置内的空气排除,避免CO与空气混合在加热时可能会发生爆炸。
2.实验中,澄清石灰水的作用是?
检验生成物二氧化碳
注意:澄清石灰水主要成分是Ca(OH)2,遇CO2生成白色沉淀现象明显,可用于CO2的检验。但在澄清石灰水中Ca(OH)2含量较少,若吸收CO2效果较差,常用NaOH吸收CO2。
二、铁的冶炼
实验总结
3.装置中右边的酒精灯起什么作用?
尾气处理,防止污染空气
4.实验结束后为什么要先移除热源,待装置冷却才停止通入CO?
防止产物铁在较高温度下重新被氧化。
若先移除热源,则此时进入装置内部的为空气,高温下铁易与空气中的氧气反应生成氧化铁。
二、铁的冶炼
3、工业炼铁
(1)原料
铁矿石(主要是赤铁矿)、焦炭、石灰石和空气。
(2)原理
在高温下焦炭与氧气反应生成的一氧化碳把铁从铁矿石中还原出来
C+O2===CO2
点燃
CO2+O2===2CO
高温
Fe2O3 +3CO===2Fe +3CO2
高温
二、铁的冶炼
【思考1】为什么铁矿石、焦炭和石灰石是从高炉顶部加入,而热空气是从高炉底部通入?
固体由于受到重力作用,从顶部加入后会往下运动,热空气在底部与焦炭生成CO,CO密度比空气小,会向上运动,从而两反应物可以充分混合。
【思考2】根据【思考1】,开采后的矿石要经过什么处理再加入高炉中呢?
粉碎研磨
二、铁的冶炼
【思考3】已知沙土的主要成分SiO2,那么石灰石的作用是什么?
CaCO3 +SiO2===CaSiO3 +CO2
高温
石灰石(CaCO3)与SiO2的反应方程式为
因此石灰石可以使矿石中二氧化硅转变成硅酸钙炉渣而除去。
二、铁的冶炼
【思考4】高炉产物中的生铁是纯铁吗?
不是,生铁为合金,其含碳量约为2%-4.3%。
【思考5】如何降低生铁中的含碳量?
在高温下将生铁熔化后,鼓入空气,并不断搅拌液态生铁,使其含有的碳可以与氧气充分反应,进而降低含碳量。
二、铁的冶炼
我国宝钢股份宝山基地建成投产30多年来,通过不断消化、吸收、引进技术,加大自主创新力度,逐步走出一条依靠自主集成、引领炼铁前沿技术发展的创新之路。
二、铁的冶炼
4、含杂质物质的化学方程式的计算
在实际生产中,所用的原料或产物一般含有杂质,在计算用料和产量时,应考虑到杂质问题。
例 题
用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少吨?
分 析
1000t并非氧化铁的质量,而是矿石质量,因此氧化铁质量应等于矿石质量乘以80%,求出氧化铁质量后便可列出化学方程式求出产物铁的质量,但铁的质量并非生铁质量,故要再将铁的质量除以96%,即为生铁质量。
二、铁的冶炼
例 题
用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少吨?
解 答
1000t赤铁矿石中含有的氧化铁的质量为:
1000t×80%=800t
设:800t氧化铁理论上可以炼出的铁质量为x。
Fe2O3 +3CO===2Fe +3CO2
高温
160 2×56
800t x
二、铁的冶炼
例 题
用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少吨?
解 答
折合成含铁96%的生铁的质量为:
560t÷96% = 583.3t
答:用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁583.3 t 。
二、铁的冶炼
总 结
纯物质的质量=不纯物质的质量×物质的质量分数
不纯物质的质量=纯物质的质量÷物质的质量分数
参与化学方程式计算的数据应是纯净物的质量,若是混合物,应该先利用下面公式计算出纯净物质量。
二、铁的冶炼
例 题
冶炼2000t含杂质3%的生铁,需要含Fe3O490%的磁铁矿石的质量是多少?
解 答
2000t含杂质3%的生铁中含有的铁的质量为:
2000t×(1-3%)=1940t
设:冶炼1940t铁理论上需要Fe3O4质量为x。
Fe3O4 +4CO===3Fe +4CO2
高温
232 3×56
x 1940t
二、铁的冶炼
例 题
冶炼2000t含杂质3%的生铁,需要含Fe3O490%的磁铁矿石的质量是多少?
解 答
折合成含Fe3O490%的磁铁矿石的质量为:
2679.05t÷90% = 2976.72t
答:冶炼2000t含杂质3%的生铁,需要含Fe3O490%的磁铁矿石的质量是2976.72t。
三、金属的腐蚀与防护
一方面,人类每年要向自然界索取大量的金属矿物资源,以提取数以亿吨计的金属。另一方面,根据有关报导,现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20% ~ 40%。因此,防止金属腐蚀是一大关键问题。
三、金属的腐蚀与防护
【思考】同学们请观察一下下面这两张图,猜想一下金属腐蚀与什么因素有关?
空气
水
三、金属的腐蚀与防护
【猜想1】铁生锈的条件是与氧气接触。
探究实验
【猜想2】铁生锈的条件是与水接触。
【猜想3】铁生锈的条件是同时与氧气、水接触。
①同时与氧气、水接触
②只与水接触
③只与氧气接触
三、金属的腐蚀与防护
实验条件 同时与氧气、水接触 只与水接触 只与氧气接触
实验现象图
实验现象
实验结论
铁钉生锈
铁钉不生锈
铁钉不生锈
铁生锈的条件是同时与氧气、水接触
三、金属的腐蚀与防护
【思考1】试管B中为什么要用煮沸过的蒸馏水,且要加入植物油?
因为氧气微溶于水,为排除氧气对铁钉生锈的影响,需煮沸后使用。且加入植物油后隔离空气。
【思考2】试管C中氯化钙的作用是什么呢?
作为干燥剂,吸收空气中的水蒸气。
讨 论
三、金属的腐蚀与防护
铁制品锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程。铁制品锈蚀需要条件,例如要有能够发生反应的物质,反应物要能相互接触,生成物不会对反应起阻碍作用。
铁生锈的原理
铁在有氧气、水等物质的条件下发生复杂的化学反应生成铁锈(Fe2O3·xH2O),铁锈疏松多孔结构,吸收水分,加速铁制品的生锈(缓慢氧化)。
【思考】在金属活动顺序表中铝比铁活泼,但为什么铝不容易锈蚀呢?
铁锈是多孔疏松结构,能让水分和空气穿过它的空隙,不断向里层渗透,继续跟内层的铁反应,直至铁被完全锈蚀。而铝与氧气生成致密性氧化膜, 阻止铝进一步被氧化。
三、金属的腐蚀与防护
【思考】请根据本节课所学,思考防止钢铁锈蚀的方法有什么?
方法:隔绝空气或水
1、在铁制品表面喷涂油漆、油脂、塑胶或搪瓷等;
三、金属的腐蚀与防护
【思考】请根据本节课所学,思考防止钢铁锈蚀的方法有什么?
方法:隔绝空气或水
2、在铁制品表面镀上其他耐腐蚀的金属, 如镀锡或铬等;
三、金属的腐蚀与防护
【思考】请根据本节课所学,思考防止钢铁锈蚀的方法有什么?
方法:隔绝空气或水
3、使用合金,如加入铬、镍等做成不锈钢。
四、金属资源保护
据估计一些矿物可供开采的年限
矿物的储量有限,而且不能再生。根据已探明的一些矿物的储量,并根据这些金属消耗速度,有人估计一些矿物可供开采的年限如图。
地球上的金属资源是有限的,而且不能再生。为了社会的可持续发展,我们应自觉保护金属资源。
四、金属资源保护
如何保护金属资源呢?
途径1:防止金属锈蚀。
途径2:回收利用废旧金属。
途径3:有计划、合理地开采矿物,严禁不顾国家利益的乱采矿。
途径4:开发研究金属的代用品;
四、金属资源保护
合理地开采矿物
使用塑料代替钢和合金
课堂练习
1、下列做法,能防止菜刀生锈的是( )①在菜刀表面镀锌;②喷刷银粉漆;③切完菜后,尽快将菜刀洗净擦干;④菜刀用完后,至于干燥的环境中;⑤经常用醋浸泡菜刀;⑥在菜刀表面涂上一层油。A.①②③④ B.①②③④⑤⑥ C.③④ D.③④⑤⑥
A
课堂练习
2、有人估计,回收一个废弃的铝质易拉罐要比制造一个新易拉罐节约90%~97%的能源。与用矿石冶炼相比,若回收1吨废钢铁可炼好钢0.9吨(提示:1吨氧化铁中含铁0.7吨),并可以减少空气污染、水污染和固体废弃物。根据信息推测错误的是( )A.制造新易拉罐的铝的冶炼可能需要消耗大量的能量 B.金属冶炼会产生污染空气的气体 C.废钢铁中的铁全部已经被氧化 D.回收废弃金属可以减少空气污染和水污染
C
课堂练习
3、实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质。关于该实验,下列说法错误的是( )
A.实验时,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成 B.实验结束时,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁 C.实验结束时,应先停止通一氧化碳气体,后停止加热D.为了减少空气污染,应增加尾气处理装置
C
课堂练习
4、长期埋在地下的金属管线会被腐蚀。常温下,某金属管线腐蚀速率与土壤含水量的关系如图所示,下列说法正确的是( )A.土壤含水量越高,金属锈蚀速度越快 B.埋在地下的金属管线被腐蚀仅与土壤
中水份有关 C.土壤含水量在20%﹣40%时,金属锈蚀
的速率逐渐加快 D.可以采用刷漆、涂油等方法防止金属
管线锈蚀
D
课堂练习
5、黄铁矿的主要成分为二硫化亚铁(FeS2),可用于工业上冶炼铁和生产浓硫酸,如图所示。下列说法错误的是( )
A.反应前将黄铁矿粉碎,能提高反应速率 B.反应①②③④中都有元素化合价的变化 C.反应②不属于四种基本反应类型之一 D.该过程回收利用了SO2,能减少酸雨的发生
B
课堂练习
6、炼铁的原理是利用一氧化碳与氧化铁反应,某同学设计的实验装置如图:
①实验中玻璃管里的现象是 ,观察到试管里出现的现象是 。②该实验要先通CO后加热,目的是 。
排尽玻璃管中的空气,防止发生爆炸。
红棕色粉末逐渐变黑
澄清石灰水变浑浊
课堂导入
自然界中存在各式各样的矿石,但大多都是以化合物形式存在,因此工业上常从含有金属元素并有开采价值的矿石中提炼金属。那究竟如何从矿石中提炼金属呢?
课题3 金属资源的利用和保护
///人教版义务教育教科书化学九年级下册///
一、常见的金属矿石
【回顾】纯净物在自然界中是以单质形式存在或以化合物形式存在。
对于金属资源,除了少数不活泼的金属如金、银等有单质形式存在外,其余都以化合物形式存在。
一、常见的金属矿石
1、以单质形式存在
少数化学性质不活泼的金属,以单质形态存在,如金、银、铂。
自然界中以单质形态存在的金
自然界中以单质形态存在的银
游离态
指某元素不与其他元素化合,而能单独存在的状态。
一、常见的金属矿石
2、以化合物形式存在
绝大多数物质都是以化合物的形式存在,如水,二氧化碳等。
化合态
某物质由多种元素组成,那么其状态即被称为化合态。
赤铁矿是红色固体,是自然界分布极广的铁矿物,是重要的炼铁原料,也可用作红色颜料
赤铁矿(主要成分Fe2O3)
一、常见的金属矿石
磁铁矿
(主要成分Fe3O4)
磁铁矿是黑色固体,是矿物中磁性最强的。
【思考1】铁的常见化合价是多少呢?
+2价,+3价
【思考2】铁的常见氧化物有什么呢?
FeO、Fe2O3、Fe3O4
【思考3】自然界中铁矿石成分多为Fe2O3、Fe3O4,基本没有以FeO存在,你可以推断出什么呢?
FeO在自然界中不稳定。
菱铁矿
(主要成分FeCO3)
一、常见的金属矿石
铝土矿
(主要成分Al2O3)
辉铜矿
(主要成分Cu2S)
黄铜矿
(主要成分CuFeS2)
我国是世界上已知矿物种类比较齐全的少数国家之一,矿物储量丰富,其中钨、钼、钛、锡、锑等储量居世界前列,铜、铝、锰等储量在世界上也占有重要地位。
二、铁的冶炼
【回顾】课题1的学习中,我们已知我国早在春秋战国时期便开始生产和使用铁器,那你知道铁是如何冶炼的吗?
二、铁的冶炼
翻译:铁分为生铁和熟铁两种:其中已经出炉但是还没有炒过的是生铁,炒过以后便成了熟铁。……一座炼铁炉可以装铁矿石两千多斤,燃料有的用硬木柴,有的用煤或者用木炭,南方北方可根据方便就地取料。鼓风的风箱要由四个人或者六个人一起推拉。铁矿石化成了铁水之后,就会从炼铁炉腰孔中流出来。
二、铁的冶炼
古代铸铁就是利用鼓风机使燃料充分燃烧,用高温火焰熔化铁矿,并不断加入木炭粉,使其保持液态,令炉渣充分析出,最后用液态的铁碳合金铸造农具和日用品。
炼铁的原理是利用一氧化碳与氧化铁的反应。
古代炼铁时,使燃料(木炭)不断燃烧,并不断加入木炭粉,是为了使木炭充分燃烧生成的二氧化碳与木炭反应生成一氧化碳,一氧化碳将铁矿(氧化铁)反应还原为铁,从而达到炼铁的目的。
1、古代炼铁
二、铁的冶炼
实验药品:氧化铁、一氧化碳、澄清石灰水
实验原理
Fe2O3+3CO 2Fe+3CO2
高温
2、实验室模拟炼铁
二、铁的冶炼
请带着这几个问题观看实验视频。
1.实验开始时为什么要先通入CO后点燃酒精喷灯?
2.实验中,澄清石灰水的作用是?
3.装置中右边的酒精灯起什么作用?
4.实验结束后为什么要先移除热源,待装置冷却才停止通入CO?
二、铁的冶炼
1.实验开始时为什么要先通入CO后点燃酒精喷灯?
2.实验中,澄清石灰水的作用是?
3.装置中右边的酒精灯起什么作用?
4.实验结束后为什么要先移除热源,待装置冷却才停止通入CO?
2CO + O2 2CO2
二、铁的冶炼
实验总结
现象1:红色粉末逐渐变成黑色
Fe2O3+3CO 2Fe+3CO2
高温
现象2:澄清的石灰水变浑浊
CO2+Ca(OH)2==CaCO3↓+ H2O
现象3:尾气燃烧产生蓝色火焰
点燃
二、铁的冶炼
实验总结
1.实验开始时为什么要先通入CO后点燃酒精喷灯?
先通入CO是为了将装置内的空气排除,避免CO与空气混合在加热时可能会发生爆炸。
2.实验中,澄清石灰水的作用是?
检验生成物二氧化碳
注意:澄清石灰水主要成分是Ca(OH)2,遇CO2生成白色沉淀现象明显,可用于CO2的检验。但在澄清石灰水中Ca(OH)2含量较少,若吸收CO2效果较差,常用NaOH吸收CO2。
二、铁的冶炼
实验总结
3.装置中右边的酒精灯起什么作用?
尾气处理,防止污染空气
4.实验结束后为什么要先移除热源,待装置冷却才停止通入CO?
防止产物铁在较高温度下重新被氧化。
若先移除热源,则此时进入装置内部的为空气,高温下铁易与空气中的氧气反应生成氧化铁。
二、铁的冶炼
3、工业炼铁
(1)原料
铁矿石(主要是赤铁矿)、焦炭、石灰石和空气。
(2)原理
在高温下焦炭与氧气反应生成的一氧化碳把铁从铁矿石中还原出来
C+O2===CO2
点燃
CO2+O2===2CO
高温
Fe2O3 +3CO===2Fe +3CO2
高温
二、铁的冶炼
【思考1】为什么铁矿石、焦炭和石灰石是从高炉顶部加入,而热空气是从高炉底部通入?
固体由于受到重力作用,从顶部加入后会往下运动,热空气在底部与焦炭生成CO,CO密度比空气小,会向上运动,从而两反应物可以充分混合。
【思考2】根据【思考1】,开采后的矿石要经过什么处理再加入高炉中呢?
粉碎研磨
二、铁的冶炼
【思考3】已知沙土的主要成分SiO2,那么石灰石的作用是什么?
CaCO3 +SiO2===CaSiO3 +CO2
高温
石灰石(CaCO3)与SiO2的反应方程式为
因此石灰石可以使矿石中二氧化硅转变成硅酸钙炉渣而除去。
二、铁的冶炼
【思考4】高炉产物中的生铁是纯铁吗?
不是,生铁为合金,其含碳量约为2%-4.3%。
【思考5】如何降低生铁中的含碳量?
在高温下将生铁熔化后,鼓入空气,并不断搅拌液态生铁,使其含有的碳可以与氧气充分反应,进而降低含碳量。
二、铁的冶炼
我国宝钢股份宝山基地建成投产30多年来,通过不断消化、吸收、引进技术,加大自主创新力度,逐步走出一条依靠自主集成、引领炼铁前沿技术发展的创新之路。
二、铁的冶炼
4、含杂质物质的化学方程式的计算
在实际生产中,所用的原料或产物一般含有杂质,在计算用料和产量时,应考虑到杂质问题。
例 题
用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少吨?
分 析
1000t并非氧化铁的质量,而是矿石质量,因此氧化铁质量应等于矿石质量乘以80%,求出氧化铁质量后便可列出化学方程式求出产物铁的质量,但铁的质量并非生铁质量,故要再将铁的质量除以96%,即为生铁质量。
二、铁的冶炼
例 题
用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少吨?
解 答
1000t赤铁矿石中含有的氧化铁的质量为:
1000t×80%=800t
设:800t氧化铁理论上可以炼出的铁质量为x。
Fe2O3 +3CO===2Fe +3CO2
高温
160 2×56
800t x
二、铁的冶炼
例 题
用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少吨?
解 答
折合成含铁96%的生铁的质量为:
560t÷96% = 583.3t
答:用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁583.3 t 。
二、铁的冶炼
总 结
纯物质的质量=不纯物质的质量×物质的质量分数
不纯物质的质量=纯物质的质量÷物质的质量分数
参与化学方程式计算的数据应是纯净物的质量,若是混合物,应该先利用下面公式计算出纯净物质量。
二、铁的冶炼
例 题
冶炼2000t含杂质3%的生铁,需要含Fe3O490%的磁铁矿石的质量是多少?
解 答
2000t含杂质3%的生铁中含有的铁的质量为:
2000t×(1-3%)=1940t
设:冶炼1940t铁理论上需要Fe3O4质量为x。
Fe3O4 +4CO===3Fe +4CO2
高温
232 3×56
x 1940t
二、铁的冶炼
例 题
冶炼2000t含杂质3%的生铁,需要含Fe3O490%的磁铁矿石的质量是多少?
解 答
折合成含Fe3O490%的磁铁矿石的质量为:
2679.05t÷90% = 2976.72t
答:冶炼2000t含杂质3%的生铁,需要含Fe3O490%的磁铁矿石的质量是2976.72t。
三、金属的腐蚀与防护
一方面,人类每年要向自然界索取大量的金属矿物资源,以提取数以亿吨计的金属。另一方面,根据有关报导,现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20% ~ 40%。因此,防止金属腐蚀是一大关键问题。
三、金属的腐蚀与防护
【思考】同学们请观察一下下面这两张图,猜想一下金属腐蚀与什么因素有关?
空气
水
三、金属的腐蚀与防护
【猜想1】铁生锈的条件是与氧气接触。
探究实验
【猜想2】铁生锈的条件是与水接触。
【猜想3】铁生锈的条件是同时与氧气、水接触。
①同时与氧气、水接触
②只与水接触
③只与氧气接触
三、金属的腐蚀与防护
实验条件 同时与氧气、水接触 只与水接触 只与氧气接触
实验现象图
实验现象
实验结论
铁钉生锈
铁钉不生锈
铁钉不生锈
铁生锈的条件是同时与氧气、水接触
三、金属的腐蚀与防护
【思考1】试管B中为什么要用煮沸过的蒸馏水,且要加入植物油?
因为氧气微溶于水,为排除氧气对铁钉生锈的影响,需煮沸后使用。且加入植物油后隔离空气。
【思考2】试管C中氯化钙的作用是什么呢?
作为干燥剂,吸收空气中的水蒸气。
讨 论
三、金属的腐蚀与防护
铁制品锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程。铁制品锈蚀需要条件,例如要有能够发生反应的物质,反应物要能相互接触,生成物不会对反应起阻碍作用。
铁生锈的原理
铁在有氧气、水等物质的条件下发生复杂的化学反应生成铁锈(Fe2O3·xH2O),铁锈疏松多孔结构,吸收水分,加速铁制品的生锈(缓慢氧化)。
【思考】在金属活动顺序表中铝比铁活泼,但为什么铝不容易锈蚀呢?
铁锈是多孔疏松结构,能让水分和空气穿过它的空隙,不断向里层渗透,继续跟内层的铁反应,直至铁被完全锈蚀。而铝与氧气生成致密性氧化膜, 阻止铝进一步被氧化。
三、金属的腐蚀与防护
【思考】请根据本节课所学,思考防止钢铁锈蚀的方法有什么?
方法:隔绝空气或水
1、在铁制品表面喷涂油漆、油脂、塑胶或搪瓷等;
三、金属的腐蚀与防护
【思考】请根据本节课所学,思考防止钢铁锈蚀的方法有什么?
方法:隔绝空气或水
2、在铁制品表面镀上其他耐腐蚀的金属, 如镀锡或铬等;
三、金属的腐蚀与防护
【思考】请根据本节课所学,思考防止钢铁锈蚀的方法有什么?
方法:隔绝空气或水
3、使用合金,如加入铬、镍等做成不锈钢。
四、金属资源保护
据估计一些矿物可供开采的年限
矿物的储量有限,而且不能再生。根据已探明的一些矿物的储量,并根据这些金属消耗速度,有人估计一些矿物可供开采的年限如图。
地球上的金属资源是有限的,而且不能再生。为了社会的可持续发展,我们应自觉保护金属资源。
四、金属资源保护
如何保护金属资源呢?
途径1:防止金属锈蚀。
途径2:回收利用废旧金属。
途径3:有计划、合理地开采矿物,严禁不顾国家利益的乱采矿。
途径4:开发研究金属的代用品;
四、金属资源保护
合理地开采矿物
使用塑料代替钢和合金
课堂练习
1、下列做法,能防止菜刀生锈的是( )①在菜刀表面镀锌;②喷刷银粉漆;③切完菜后,尽快将菜刀洗净擦干;④菜刀用完后,至于干燥的环境中;⑤经常用醋浸泡菜刀;⑥在菜刀表面涂上一层油。A.①②③④ B.①②③④⑤⑥ C.③④ D.③④⑤⑥
A
课堂练习
2、有人估计,回收一个废弃的铝质易拉罐要比制造一个新易拉罐节约90%~97%的能源。与用矿石冶炼相比,若回收1吨废钢铁可炼好钢0.9吨(提示:1吨氧化铁中含铁0.7吨),并可以减少空气污染、水污染和固体废弃物。根据信息推测错误的是( )A.制造新易拉罐的铝的冶炼可能需要消耗大量的能量 B.金属冶炼会产生污染空气的气体 C.废钢铁中的铁全部已经被氧化 D.回收废弃金属可以减少空气污染和水污染
C
课堂练习
3、实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质。关于该实验,下列说法错误的是( )
A.实验时,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成 B.实验结束时,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁 C.实验结束时,应先停止通一氧化碳气体,后停止加热D.为了减少空气污染,应增加尾气处理装置
C
课堂练习
4、长期埋在地下的金属管线会被腐蚀。常温下,某金属管线腐蚀速率与土壤含水量的关系如图所示,下列说法正确的是( )A.土壤含水量越高,金属锈蚀速度越快 B.埋在地下的金属管线被腐蚀仅与土壤
中水份有关 C.土壤含水量在20%﹣40%时,金属锈蚀
的速率逐渐加快 D.可以采用刷漆、涂油等方法防止金属
管线锈蚀
D
课堂练习
5、黄铁矿的主要成分为二硫化亚铁(FeS2),可用于工业上冶炼铁和生产浓硫酸,如图所示。下列说法错误的是( )
A.反应前将黄铁矿粉碎,能提高反应速率 B.反应①②③④中都有元素化合价的变化 C.反应②不属于四种基本反应类型之一 D.该过程回收利用了SO2,能减少酸雨的发生
B
课堂练习
6、炼铁的原理是利用一氧化碳与氧化铁反应,某同学设计的实验装置如图:
①实验中玻璃管里的现象是 ,观察到试管里出现的现象是 。②该实验要先通CO后加热,目的是 。
排尽玻璃管中的空气,防止发生爆炸。
红棕色粉末逐渐变黑
澄清石灰水变浑浊
同课章节目录
