人教版九年级化学下册 10.2 酸和碱的中和反应第1课时课件(共23张PPT)
文档属性
| 名称 | 人教版九年级化学下册 10.2 酸和碱的中和反应第1课时课件(共23张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-27 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
第十单元
新人教版
自主学习
阅读书本60-61页的有关内容,完成下列问题:
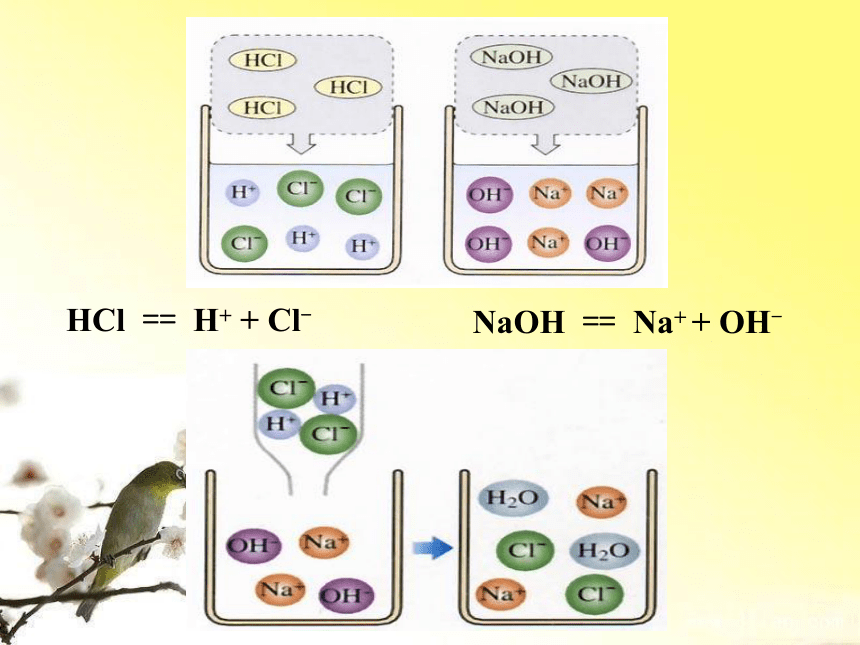
1.认真观察60页图10-14氢氧化钠与盐酸反应的微观粒子示意图,HCl在溶液中离解出 离子和 离子,NaOH在溶液中离解出 和 (用粒子符号表示),而在反应后的溶液中, 离子和 离子消失了,变成了水分子,而 离子和 仍然以离子的形式存在。所以酸碱中和反应的实质H+和OH-反应生成了 。
2.由 和 构成的化合物叫做盐。
3.酸与碱作用生成 和 的反应,叫做中和反应。
H+
Na+
OH-
Na+
Cl-
H2O
金属离子
酸根离子
Cl-
盐
水
H+
OH-
请思考?
1.理解酸碱中和反应的实质;
2.了解中和反应在日常生活和工农业生产中的作用。
学习导航
学习目标
学习重点、难点
1.中和反应的实验验证及应用;
2.从离子的角度理解中和反应的实质。
活动与探究
通过前几堂课的学习,我们已经知道了酸、碱的一些性质,那么酸和碱混合在一起,会怎样呢?会发生化学反应吗?
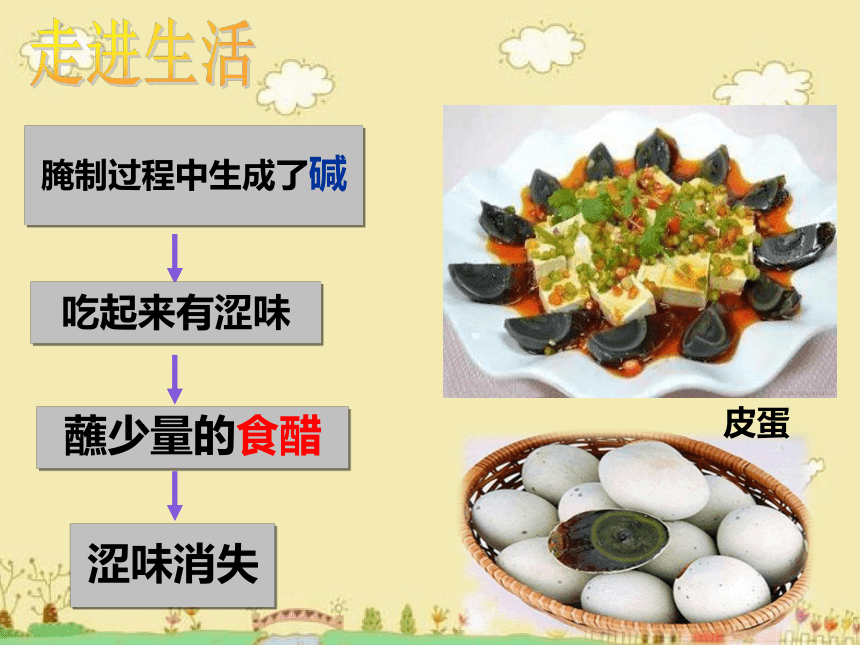
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
皮蛋
问题探究
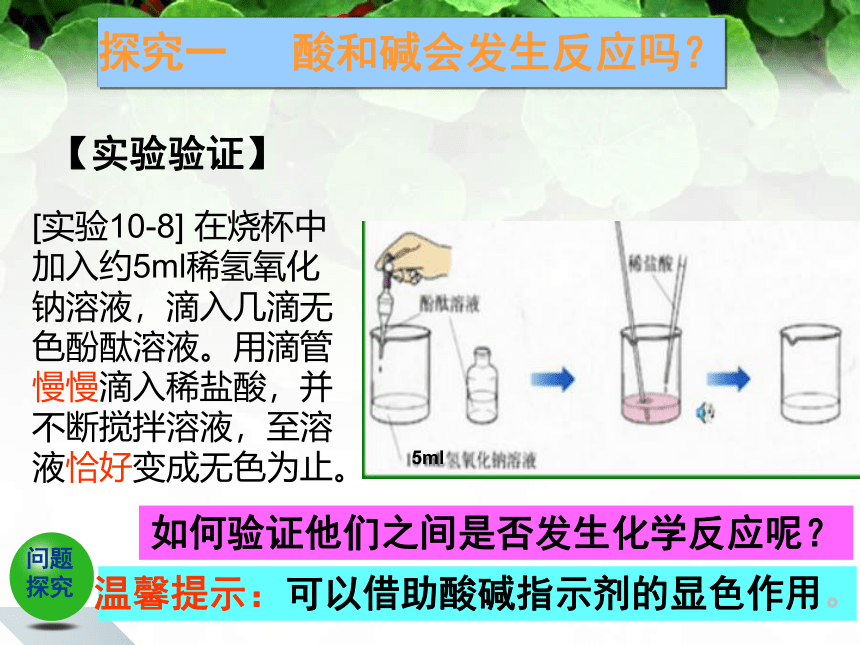
【实验验证】
探究一 酸和碱会发生反应吗?
如何验证他们之间是否发生化学反应呢?
温馨提示:可以借助酸碱指示剂的显色作用。
[实验10-8] 在烧杯中加入约5ml稀氢氧化钠溶液,滴入几滴无色酚酞溶液。用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液恰好变成无色为止。
5ml
思考:为什么酚酞会变成无色呢?说明了什么?
回答:因为氢氧化钠和盐酸反应被消耗,这说明了盐酸和氢氧化钠能发生化学反应。
思考:什么时候盐酸和氢氧化钠恰好完全反应?
当滴加盐酸到溶液由红色刚好变为无色时。
思考:某同学滴加盐酸时速度太快,溶液变无色后,如何判断盐酸是否过量?
(1)滴入氢氧化钠溶液,若没有立即变红,说明过量
(2)滴入石蕊溶液,若变红,说明过量;
(3)加入镁条,若有气泡冒出,说明过量。
HCl == H+ + Cl-
NaOH == Na+ + OH-
氢氧化钠(碱)和稀盐酸(酸)发生的反应
NaOH + HCl === NaCl + H2O
碱
酸
氧化物
?
盐
金属离子
酸根离子
1 、盐:由 金属离子 和 酸根离子 构成的化合物。
HCl + NaOH === NaCl + H2O
酸
+
碱
===
盐
+
水
2HCl + Ca(OH)2 ===
H2SO4 + 2NaOH ===
CaCl2 + 2H2O
Na2SO4 +2H2O
2 、中和反应:酸和碱作用生成盐和水的反应。
反应实质:H+ + OH- == H2O
是不是所有的酸碱中和反应都需要借助酸碱指示剂的颜色变化,才能判断反应是否发生?
请思考?
不一定,有的会有沉淀生成或颜色变化等也可以判断发生化学变化。
展示交流
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
醋酸
发生了什么反应?
发生了中和反应
二、中和反应在实际中的应用
1、改变土壤的酸碱性
VS
酸性土壤
熟石灰
VS
碱性土壤
碳酸
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
能否用NaOH?
碱性太强,价格太贵
2、处理工厂的废水
VS
含酸废水
熟石灰
玉米地的土壤由于工厂排出的废水而变酸性,怎么办?
(碱性废水可用酸中和,酸性废水可用碱中和)
胃乐说明书
[药品名称] 胃乐胶囊
[性状] 本品为胶囊剂,内容物为灰黄棕色,气味香,味微苦
[主要成分] 氢氧化铝[Al(OH)3 ]、甘草提取物、白芨、木香等
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
[用法与用量] 口服,一次2~3粒,一日3次,空腹服用
[规格] 0.4g/粒
[贮藏] 密封,置干燥阴凉处
[包装] 20粒/盒
[有效期] 两年
胃 乐
胶
囊
3.用于医药
胃乐胶囊的主要成分
你知道它的作用吗?
胃酸的主要成分是
盐酸
氢氧化铝
Al(OH)3 + 3HCl === AlCl3 + 3H2O
氢氧化铝能中和胃酸
你能写出化学方程式吗?
4、用于生活
被蚊虫叮咬可涂一些碱性物质如肥皂水、牙膏减轻痛痒
被黄蜂蜇到,毒液呈碱性,可涂食醋
VS
蚁酸
氨水
VS
学完本节课你知道了什么?
2.酸和碱能发生中和反应,生成盐和水。
3.酸碱中和反应在生活和生产中有广泛的应用。
1.盐是由金属离子和酸根离子构成的化合物。
练习:
判断:下列化合物中,哪些是酸,哪些是碱,哪些是盐,哪些是氧化物?
KOH、HCl、CaCl2、HNO3、SO2、BaSO4、CuO、Ca(OH)2、H2SO4、Na2CO3、NH3 · H2O、CaCO3
回答:
酸: HCl、 HNO3、 H2SO4
碱: KOH 、Ca(OH)2、 NH3 · H2O
盐:CaCl2、BaSO4、Na2CO3、CaCO3
氧化物:SO2 、CuO
中考链接一
名称 氢氧化钠 硫酸 氧化铁
化学式 CuSO4
类别
1.下列物质属于盐的是( )
A. CuO B. Cu(OH)2 C. CuSO4 D. HCl
2.填写下表(类别按酸、碱、盐、氧化物填写)
C
NaOH
碱
硫酸铜
盐
H2SO4
酸
Fe2O3
氧化物
中考链接二
下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2↑
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D CO2 + 2NaOH == Na2CO3 + H2O
中考链接三
C
课后作业
完成课本后面的相关习题。
第十单元
新人教版
自主学习
阅读书本60-61页的有关内容,完成下列问题:
1.认真观察60页图10-14氢氧化钠与盐酸反应的微观粒子示意图,HCl在溶液中离解出 离子和 离子,NaOH在溶液中离解出 和 (用粒子符号表示),而在反应后的溶液中, 离子和 离子消失了,变成了水分子,而 离子和 仍然以离子的形式存在。所以酸碱中和反应的实质H+和OH-反应生成了 。
2.由 和 构成的化合物叫做盐。
3.酸与碱作用生成 和 的反应,叫做中和反应。
H+
Na+
OH-
Na+
Cl-
H2O
金属离子
酸根离子
Cl-
盐
水
H+
OH-
请思考?
1.理解酸碱中和反应的实质;
2.了解中和反应在日常生活和工农业生产中的作用。
学习导航
学习目标
学习重点、难点
1.中和反应的实验验证及应用;
2.从离子的角度理解中和反应的实质。
活动与探究
通过前几堂课的学习,我们已经知道了酸、碱的一些性质,那么酸和碱混合在一起,会怎样呢?会发生化学反应吗?
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
皮蛋
问题探究
【实验验证】
探究一 酸和碱会发生反应吗?
如何验证他们之间是否发生化学反应呢?
温馨提示:可以借助酸碱指示剂的显色作用。
[实验10-8] 在烧杯中加入约5ml稀氢氧化钠溶液,滴入几滴无色酚酞溶液。用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液恰好变成无色为止。
5ml
思考:为什么酚酞会变成无色呢?说明了什么?
回答:因为氢氧化钠和盐酸反应被消耗,这说明了盐酸和氢氧化钠能发生化学反应。
思考:什么时候盐酸和氢氧化钠恰好完全反应?
当滴加盐酸到溶液由红色刚好变为无色时。
思考:某同学滴加盐酸时速度太快,溶液变无色后,如何判断盐酸是否过量?
(1)滴入氢氧化钠溶液,若没有立即变红,说明过量
(2)滴入石蕊溶液,若变红,说明过量;
(3)加入镁条,若有气泡冒出,说明过量。
HCl == H+ + Cl-
NaOH == Na+ + OH-
氢氧化钠(碱)和稀盐酸(酸)发生的反应
NaOH + HCl === NaCl + H2O
碱
酸
氧化物
?
盐
金属离子
酸根离子
1 、盐:由 金属离子 和 酸根离子 构成的化合物。
HCl + NaOH === NaCl + H2O
酸
+
碱
===
盐
+
水
2HCl + Ca(OH)2 ===
H2SO4 + 2NaOH ===
CaCl2 + 2H2O
Na2SO4 +2H2O
2 、中和反应:酸和碱作用生成盐和水的反应。
反应实质:H+ + OH- == H2O
是不是所有的酸碱中和反应都需要借助酸碱指示剂的颜色变化,才能判断反应是否发生?
请思考?
不一定,有的会有沉淀生成或颜色变化等也可以判断发生化学变化。
展示交流
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
醋酸
发生了什么反应?
发生了中和反应
二、中和反应在实际中的应用
1、改变土壤的酸碱性
VS
酸性土壤
熟石灰
VS
碱性土壤
碳酸
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
能否用NaOH?
碱性太强,价格太贵
2、处理工厂的废水
VS
含酸废水
熟石灰
玉米地的土壤由于工厂排出的废水而变酸性,怎么办?
(碱性废水可用酸中和,酸性废水可用碱中和)
胃乐说明书
[药品名称] 胃乐胶囊
[性状] 本品为胶囊剂,内容物为灰黄棕色,气味香,味微苦
[主要成分] 氢氧化铝[Al(OH)3 ]、甘草提取物、白芨、木香等
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
[用法与用量] 口服,一次2~3粒,一日3次,空腹服用
[规格] 0.4g/粒
[贮藏] 密封,置干燥阴凉处
[包装] 20粒/盒
[有效期] 两年
胃 乐
胶
囊
3.用于医药
胃乐胶囊的主要成分
你知道它的作用吗?
胃酸的主要成分是
盐酸
氢氧化铝
Al(OH)3 + 3HCl === AlCl3 + 3H2O
氢氧化铝能中和胃酸
你能写出化学方程式吗?
4、用于生活
被蚊虫叮咬可涂一些碱性物质如肥皂水、牙膏减轻痛痒
被黄蜂蜇到,毒液呈碱性,可涂食醋
VS
蚁酸
氨水
VS
学完本节课你知道了什么?
2.酸和碱能发生中和反应,生成盐和水。
3.酸碱中和反应在生活和生产中有广泛的应用。
1.盐是由金属离子和酸根离子构成的化合物。
练习:
判断:下列化合物中,哪些是酸,哪些是碱,哪些是盐,哪些是氧化物?
KOH、HCl、CaCl2、HNO3、SO2、BaSO4、CuO、Ca(OH)2、H2SO4、Na2CO3、NH3 · H2O、CaCO3
回答:
酸: HCl、 HNO3、 H2SO4
碱: KOH 、Ca(OH)2、 NH3 · H2O
盐:CaCl2、BaSO4、Na2CO3、CaCO3
氧化物:SO2 、CuO
中考链接一
名称 氢氧化钠 硫酸 氧化铁
化学式 CuSO4
类别
1.下列物质属于盐的是( )
A. CuO B. Cu(OH)2 C. CuSO4 D. HCl
2.填写下表(类别按酸、碱、盐、氧化物填写)
C
NaOH
碱
硫酸铜
盐
H2SO4
酸
Fe2O3
氧化物
中考链接二
下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2↑
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D CO2 + 2NaOH == Na2CO3 + H2O
中考链接三
C
课后作业
完成课本后面的相关习题。
同课章节目录
