人教版九年级化学第十单元酸和碱 复习导学案
文档属性
| 名称 | 人教版九年级化学第十单元酸和碱 复习导学案 |
|
|
| 格式 | zip | ||
| 文件大小 | 323.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-01 00:00:00 | ||
图片预览


文档简介
第十单元 酸和碱的复习课
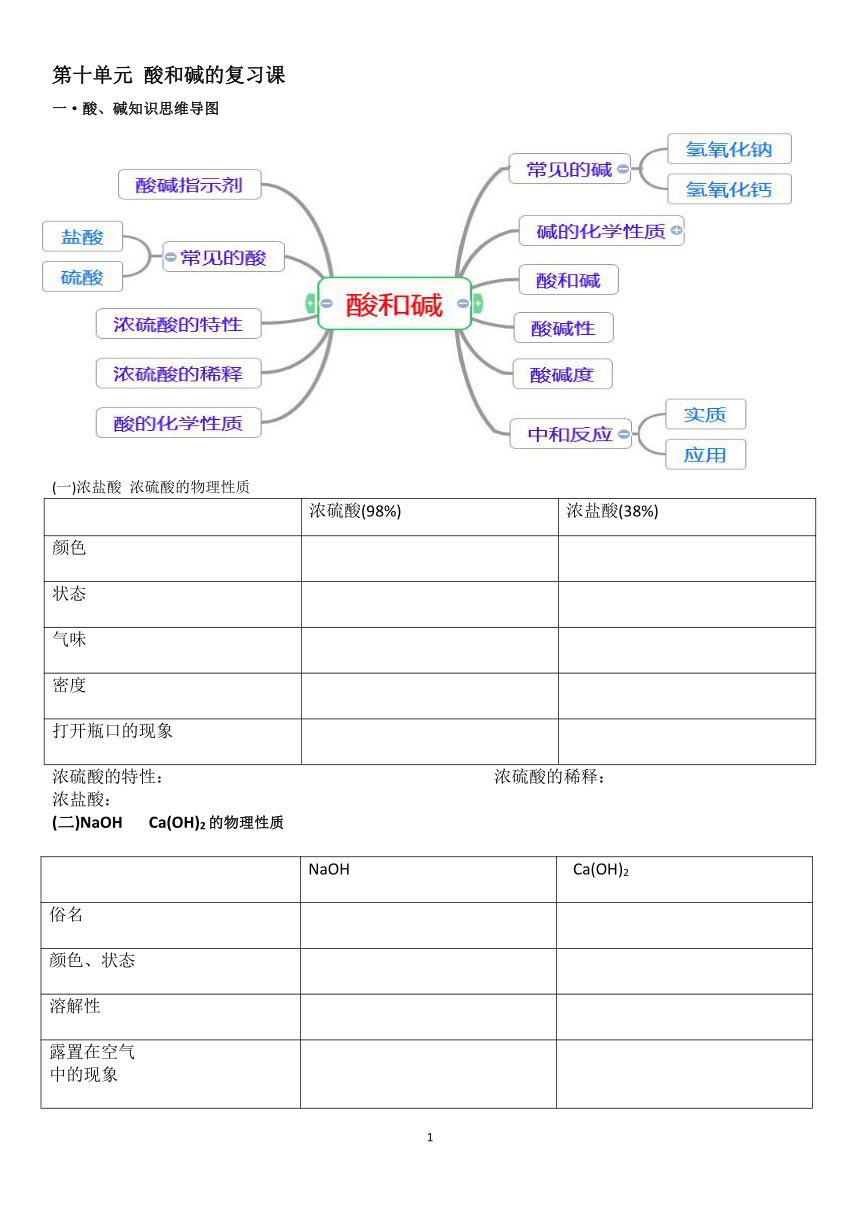
一·酸、碱知识思维导图
(一)浓盐酸 浓硫酸的物理性质
浓硫酸(98%) 浓盐酸(38%)
颜色
状态
气味
密度
打开瓶口的现象
浓硫酸的特性: 浓硫酸的稀释:
浓盐酸:
(二)NaOH Ca(OH)2的物理性质
NaOH Ca(OH)2
俗名
颜色、状态
溶解性
露置在空气 中的现象
氢氧化钠固体可做干燥剂:
化学性质:不同的酸溶液中都含有共同的H+,故酸有相似的化学性质,有以下五条:
不同的碱溶液中都含有共同的OH- ,故碱有相似的化学性质,有以下四条:
【写一写 】现有下列物质:Zn 、 CuO 、 H2SO4 、 HCl 、Ca(OH)2溶液、 NaOH溶液、 Na2CO3溶液、 CO2,请同学们先分类(若是溶液则指溶质)再写出其两两间能反应的化学方程式
【拓展】 NaOH、Ca(OH)2的制取和鉴别
(三) 溶液酸碱性和酸碱度
[请你帮助]小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,
导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【探究1】探究所得溶液的酸碱性
(1)【提出猜想】所得溶液可能呈碱性,也可能呈___ 性,还可能呈 __ 性。
(2)【实验验证】
实验操作 实验现象 结论
用试管取该溶液1~2 mL,滴入1~2滴无色酚酞试液,振荡 溶液不变色
【探究2】探究所得溶液中的溶质成分(不考虑指示剂)
【猜想】猜想一:是NaCl ;猜想二:____________
【实验验证】
实验步骤 实验操作 实验现象 结论
① 取少量烧杯内的溶液于试管中,滴入几紫色石蕊,振荡 _____________ 猜想二成立
② 取少量烧杯内的溶液于另一支试管中,加入一小块石灰石 _____________ 猜想二成立
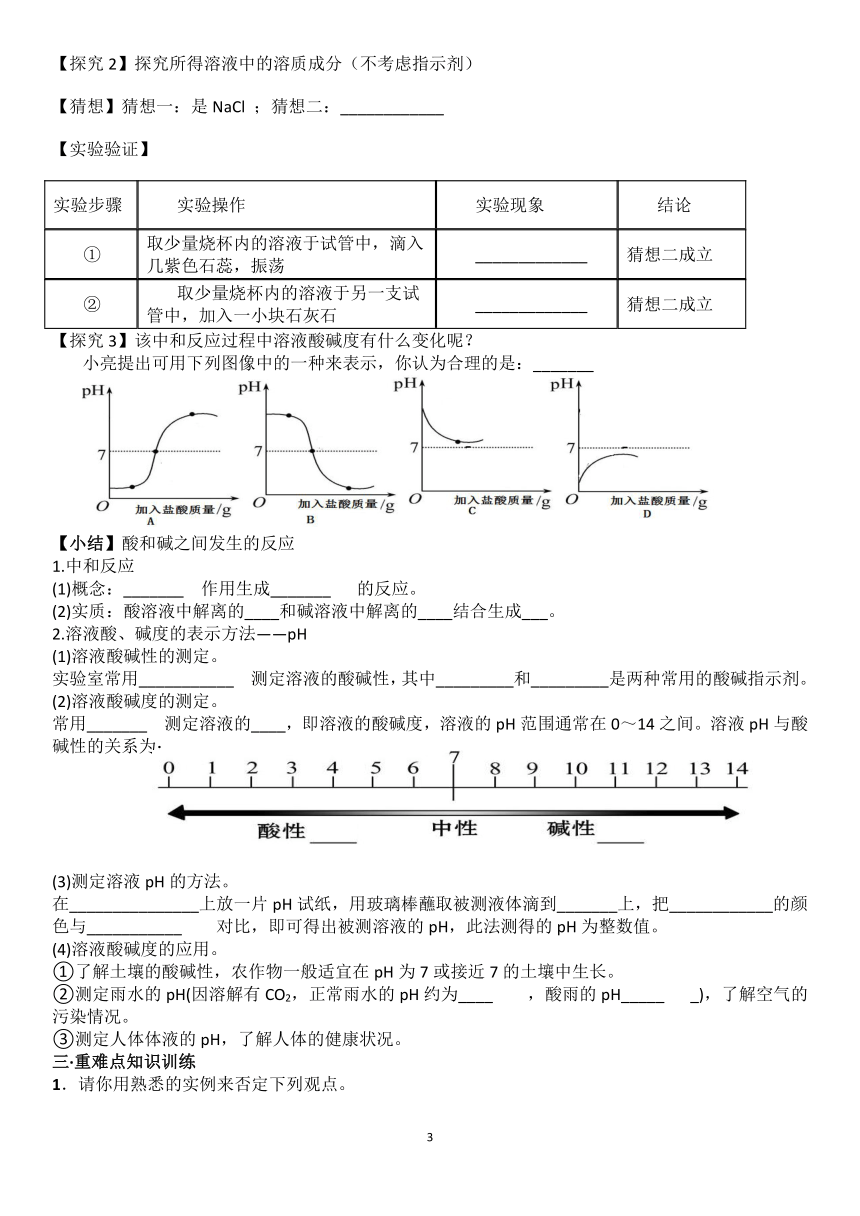
【探究3】该中和反应过程中溶液酸碱度有什么变化呢?
小亮提出可用下列图像中的一种来表示,你认为合理的是:_______
【小结】酸和碱之间发生的反应
1.中和反应
(1)概念:_______ 作用生成_______ 的反应。
(2)实质:酸溶液中解离的____和碱溶液中解离的____结合生成___。
2.溶液酸、碱度的表示方法——pH
(1)溶液酸碱性的测定。
实验室常用___________ 测定溶液的酸碱性,其中_________和_________是两种常用的酸碱指示剂。
(2)溶液酸碱度的测定。
常用_______ 测定溶液的____,即溶液的酸碱度,溶液的pH范围通常在0~14之间。溶液pH与酸碱性的关系为:
(3)测定溶液pH的方法。
在_______________上放一片pH试纸,用玻璃棒蘸取被测液体滴到_______上,把____________的颜色与___________ 对比,即可得出被测溶液的pH,此法测得的pH为整数值。
(4)溶液酸碱度的应用。
①了解土壤的酸碱性,农作物一般适宜在pH为7或接近7的土壤中生长。
②测定雨水的pH(因溶解有CO2,正常雨水的pH约为____ ,酸雨的pH_____ _),了解空气的污染情况。
③测定人体体液的pH,了解人体的健康状况。
三·重难点知识训练
1.请你用熟悉的实例来否定下列观点。
错误观点 否定实例
①所有的酸和碱都能使酸碱指示剂变色
②酸中一定含有氢元素,则含氢元素的物质一定是酸
③碱中一定含有金属元素
④生成盐和水的反应一定是中和反应
2.判断下列说法是否正确(正确的打“√”,错误的打“×”)。
(1)酸碱指示剂能使酸、碱溶液变色。( )
(2)酸溶液能使石蕊溶液变红,那么能使石蕊溶液变红的溶液一定是酸溶液。( )
(3)碱溶液能使无色酚酞变红,所以能使酚酞变红的溶液一定显碱性。( )
(4)使无色酚酞试液不变色的物质不一定是酸性物质。( )
(5)酸能使紫色石蕊试液变红,二氧化碳溶于水也能使紫色石蕊试液变红,
所以二氧化碳属于酸。( )
(6)打开盛有浓盐酸的试剂瓶的瓶塞,瓶口冒白烟。( )
(7)用无色酚酞试液可以鉴别盐酸和氯化钠溶液。( )
(8)镁、锌、铁能与盐酸反应生成氢气,那么它们与稀硫酸反应也能生成氢气。( )
(9)氢氧化钠与氢氧化钙都能用于改良酸性土壤。( )
(10)将pH试纸用水润湿后测定溶液的pH。( )
3.进行如下微型实验,研究物质的性质。
(1)能产生气泡的是__________ (填序号)。
(2)能证明C中发生反应的现象是__________________________ 。
(3)有一只烧杯中的物质不与稀盐酸反应,原因是 ____________________________ 。
(4)E中反应的方程式是________________________________________.
4.请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站。“2~ 5号站”各站的对应物质属于不同类别的物质(若是溶液指溶质)。
(1)若列车上的物质为“氢氧化钙溶液”。
①列车途经“1号站”时,若指示剂为紫色石蕊溶液,溶液变___________ 色。
②列车途经“2号站”时, “2号站”的物质可能为 ______________________________
③ 若“5号站”的物质是金属单质且能与3、4号站的物质发生置换反应,则“4号站”的物质可能是___________ 溶液, 则列车上的物质 “氢氧化钙溶液”________ (填“能”或“不能”)通过“5号站” 。
④列车通过“4号站”时反应的方程式为_______________________
5.甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如图所示的四组实验方案:
(1)其中能达到实验目的的是________。
(2)在C组实验中发生反应的化学方程式为__________________________________。
(3)在D组实验中无现象的化学方程式为________________________________
6.实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变
化。测定结果如下图所示。下列说法不正确的是 ( )
A.反应过程中有热量放出
B.30 s时,溶液中溶质为HCl和NaCl
C.该实验是将稀盐酸滴入稀NaOH溶液
D.从20 s到40 s,溶液的温度升高、pH增大
7.下列实验操作能达到实验目的的是( )
选项 实验目的 实验操作
A 鉴别NaOH和Na2CO3两种无色溶液 分别取少量溶液分别加入无色酚酞溶液
B 除去NaOH溶液中少量Na2CO3 加入稀盐酸至无气泡
C 除去NH3中少量的水蒸气 将混合气体通过装有浓硫酸的洗气瓶
D 鉴别两种黑色粉末 氧化铜粉末和铁粉 分别取少量两种粉末,分别加入稀硫酸
8.A、B、C、D、E、F是初中化学常见的六种物质,已知A是年产量最高的金属 ,
B为红棕色固体,D常用于改良酸性土壤,F与B属于同类物质,其相互反应情况如下图所示
(“—”表示相连的物质间能反应,“→”表示转化关系)。
A的化学式为________;
A与C的反应属于________反应(填基本反应类型)。
(2)写出下列反应或转化的化学方程式:
B与C反应:________________________________; D转化为E:________________________________。
(3)写出F的一种用途:_______________________
9.A、B、C为初中化学常见的三种物质,它们之间有如图所示的转化关系
(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物及
反应条件已略去)。请回答下列问题:
(1)若A、B、C均为碱,且A 可以改良酸性土壤,C为蓝色沉淀,写出A→B反应的化学方程式:
______________________
(2)若A、B、C是三种不同类别的物质,都含有同一种元素,且组成元素分别为三种、
两种和一种,常温下C为最轻的气态,则B的化学式为 ____________。
10.某黑色固体粉末可能是Fe、FeO、CuO和C中的一种或几种。取黑色粉末,加入一定量的稀硫酸,待充分反应后过滤,得到滤液和滤渣,在滤液中插入一根洁净的铁丝。有关说法正确的是( )
A.若滤液呈浅绿色,则原黑色固体粉末中一定有Fe
B.若铁丝表面只有红色固体析出,则滤渣中一定无CuO
C.若铁丝表面无明显现象,则滤渣中最多有四种物质
D.若铁丝表面只有气泡产生,则滤液中溶质一定有H2SO4和FeSO4
一·酸、碱知识思维导图
(一)浓盐酸 浓硫酸的物理性质
浓硫酸(98%) 浓盐酸(38%)
颜色
状态
气味
密度
打开瓶口的现象
浓硫酸的特性: 浓硫酸的稀释:
浓盐酸:
(二)NaOH Ca(OH)2的物理性质
NaOH Ca(OH)2
俗名
颜色、状态
溶解性
露置在空气 中的现象
氢氧化钠固体可做干燥剂:
化学性质:不同的酸溶液中都含有共同的H+,故酸有相似的化学性质,有以下五条:
不同的碱溶液中都含有共同的OH- ,故碱有相似的化学性质,有以下四条:
【写一写 】现有下列物质:Zn 、 CuO 、 H2SO4 、 HCl 、Ca(OH)2溶液、 NaOH溶液、 Na2CO3溶液、 CO2,请同学们先分类(若是溶液则指溶质)再写出其两两间能反应的化学方程式
【拓展】 NaOH、Ca(OH)2的制取和鉴别
(三) 溶液酸碱性和酸碱度
[请你帮助]小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,
导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【探究1】探究所得溶液的酸碱性
(1)【提出猜想】所得溶液可能呈碱性,也可能呈___ 性,还可能呈 __ 性。
(2)【实验验证】
实验操作 实验现象 结论
用试管取该溶液1~2 mL,滴入1~2滴无色酚酞试液,振荡 溶液不变色
【探究2】探究所得溶液中的溶质成分(不考虑指示剂)
【猜想】猜想一:是NaCl ;猜想二:____________
【实验验证】
实验步骤 实验操作 实验现象 结论
① 取少量烧杯内的溶液于试管中,滴入几紫色石蕊,振荡 _____________ 猜想二成立
② 取少量烧杯内的溶液于另一支试管中,加入一小块石灰石 _____________ 猜想二成立
【探究3】该中和反应过程中溶液酸碱度有什么变化呢?
小亮提出可用下列图像中的一种来表示,你认为合理的是:_______
【小结】酸和碱之间发生的反应
1.中和反应
(1)概念:_______ 作用生成_______ 的反应。
(2)实质:酸溶液中解离的____和碱溶液中解离的____结合生成___。
2.溶液酸、碱度的表示方法——pH
(1)溶液酸碱性的测定。
实验室常用___________ 测定溶液的酸碱性,其中_________和_________是两种常用的酸碱指示剂。
(2)溶液酸碱度的测定。
常用_______ 测定溶液的____,即溶液的酸碱度,溶液的pH范围通常在0~14之间。溶液pH与酸碱性的关系为:
(3)测定溶液pH的方法。
在_______________上放一片pH试纸,用玻璃棒蘸取被测液体滴到_______上,把____________的颜色与___________ 对比,即可得出被测溶液的pH,此法测得的pH为整数值。
(4)溶液酸碱度的应用。
①了解土壤的酸碱性,农作物一般适宜在pH为7或接近7的土壤中生长。
②测定雨水的pH(因溶解有CO2,正常雨水的pH约为____ ,酸雨的pH_____ _),了解空气的污染情况。
③测定人体体液的pH,了解人体的健康状况。
三·重难点知识训练
1.请你用熟悉的实例来否定下列观点。
错误观点 否定实例
①所有的酸和碱都能使酸碱指示剂变色
②酸中一定含有氢元素,则含氢元素的物质一定是酸
③碱中一定含有金属元素
④生成盐和水的反应一定是中和反应
2.判断下列说法是否正确(正确的打“√”,错误的打“×”)。
(1)酸碱指示剂能使酸、碱溶液变色。( )
(2)酸溶液能使石蕊溶液变红,那么能使石蕊溶液变红的溶液一定是酸溶液。( )
(3)碱溶液能使无色酚酞变红,所以能使酚酞变红的溶液一定显碱性。( )
(4)使无色酚酞试液不变色的物质不一定是酸性物质。( )
(5)酸能使紫色石蕊试液变红,二氧化碳溶于水也能使紫色石蕊试液变红,
所以二氧化碳属于酸。( )
(6)打开盛有浓盐酸的试剂瓶的瓶塞,瓶口冒白烟。( )
(7)用无色酚酞试液可以鉴别盐酸和氯化钠溶液。( )
(8)镁、锌、铁能与盐酸反应生成氢气,那么它们与稀硫酸反应也能生成氢气。( )
(9)氢氧化钠与氢氧化钙都能用于改良酸性土壤。( )
(10)将pH试纸用水润湿后测定溶液的pH。( )
3.进行如下微型实验,研究物质的性质。
(1)能产生气泡的是__________ (填序号)。
(2)能证明C中发生反应的现象是__________________________ 。
(3)有一只烧杯中的物质不与稀盐酸反应,原因是 ____________________________ 。
(4)E中反应的方程式是________________________________________.
4.请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站。“2~ 5号站”各站的对应物质属于不同类别的物质(若是溶液指溶质)。
(1)若列车上的物质为“氢氧化钙溶液”。
①列车途经“1号站”时,若指示剂为紫色石蕊溶液,溶液变___________ 色。
②列车途经“2号站”时, “2号站”的物质可能为 ______________________________
③ 若“5号站”的物质是金属单质且能与3、4号站的物质发生置换反应,则“4号站”的物质可能是___________ 溶液, 则列车上的物质 “氢氧化钙溶液”________ (填“能”或“不能”)通过“5号站” 。
④列车通过“4号站”时反应的方程式为_______________________
5.甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如图所示的四组实验方案:
(1)其中能达到实验目的的是________。
(2)在C组实验中发生反应的化学方程式为__________________________________。
(3)在D组实验中无现象的化学方程式为________________________________
6.实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变
化。测定结果如下图所示。下列说法不正确的是 ( )
A.反应过程中有热量放出
B.30 s时,溶液中溶质为HCl和NaCl
C.该实验是将稀盐酸滴入稀NaOH溶液
D.从20 s到40 s,溶液的温度升高、pH增大
7.下列实验操作能达到实验目的的是( )
选项 实验目的 实验操作
A 鉴别NaOH和Na2CO3两种无色溶液 分别取少量溶液分别加入无色酚酞溶液
B 除去NaOH溶液中少量Na2CO3 加入稀盐酸至无气泡
C 除去NH3中少量的水蒸气 将混合气体通过装有浓硫酸的洗气瓶
D 鉴别两种黑色粉末 氧化铜粉末和铁粉 分别取少量两种粉末,分别加入稀硫酸
8.A、B、C、D、E、F是初中化学常见的六种物质,已知A是年产量最高的金属 ,
B为红棕色固体,D常用于改良酸性土壤,F与B属于同类物质,其相互反应情况如下图所示
(“—”表示相连的物质间能反应,“→”表示转化关系)。
A的化学式为________;
A与C的反应属于________反应(填基本反应类型)。
(2)写出下列反应或转化的化学方程式:
B与C反应:________________________________; D转化为E:________________________________。
(3)写出F的一种用途:_______________________
9.A、B、C为初中化学常见的三种物质,它们之间有如图所示的转化关系
(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物及
反应条件已略去)。请回答下列问题:
(1)若A、B、C均为碱,且A 可以改良酸性土壤,C为蓝色沉淀,写出A→B反应的化学方程式:
______________________
(2)若A、B、C是三种不同类别的物质,都含有同一种元素,且组成元素分别为三种、
两种和一种,常温下C为最轻的气态,则B的化学式为 ____________。
10.某黑色固体粉末可能是Fe、FeO、CuO和C中的一种或几种。取黑色粉末,加入一定量的稀硫酸,待充分反应后过滤,得到滤液和滤渣,在滤液中插入一根洁净的铁丝。有关说法正确的是( )
A.若滤液呈浅绿色,则原黑色固体粉末中一定有Fe
B.若铁丝表面只有红色固体析出,则滤渣中一定无CuO
C.若铁丝表面无明显现象,则滤渣中最多有四种物质
D.若铁丝表面只有气泡产生,则滤液中溶质一定有H2SO4和FeSO4
同课章节目录
