云南省昭通市民族中学2021-2022学年高二下学期入学考试化学试卷(pdf版无答案)
文档属性
| 名称 | 云南省昭通市民族中学2021-2022学年高二下学期入学考试化学试卷(pdf版无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 328.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-02 00:00:00 | ||
图片预览


文档简介
昭通市民族中学 2023 届高二 2022 年春季学期入学考试
化学学科 试卷
考试时间:90 分钟 满分 100 分。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27
S-32 Cl-35.5 Fe-56 Cu-64 Zn-65
第Ⅰ卷(选择题,共 60 分)
一、单选题(本大题共 20 小题,每题 3 分,共 60 分。在每小题给出的四个选项中,只
有一项是符合题目要求的)
1.芒硝(十水合硫酸钠 Na2SO4·10H2O)具有泻热通便、清火消肿等功效,可用于治疗牙
痛、阑尾炎、便秘等。下列有关芒硝的分类不正确的是
A.钠盐 B.无机化合物 C.硫酸盐 D.金属氧化物
2.AlCl3 溶液、Al(OH)3胶体和 Al(OH)3浊液是重要的分散系。下列叙述中不正确的是
A.三种分散系均是无色透明的液体
B.光线透过三种分散系时,只有胶体可发生丁达尔效应
C.Al(OH)3胶体区别于其他分散系的本质特征是分散质的微粒直径在 10-9~10-7m
D.Al(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
3.下列离子方程式正确的是
A NaOH CO CO +2OH-=CO 2-.向 溶液中通入少量 2: 2 3 + H2O
B.铁与稀盐酸反应:2Fe+6H+=2Fe3+ +3H2↑
C.FeO 溶于足量的稀盐酸:O2- +2H+=H2O
D 2-.向氢氧化钡溶液中加入等量稀硫酸:Ba2+ +OH- +H+ +SO 4 =BaSO4↓+H2O
4.下列物质在给定条件下的转化均能一步实现的是
A.Fe3O4 Fe FeCl3
B.H2O2 H2 H2O
C.CaCl2 溶液 CaCO3 CO2
D.CuSO4溶液 Cu CuO
5.下列价电子表示正确的是
A.29Cu:3d94s2 B.20Ca:3d2 C.39Y :4d15s2 D.26Fe:3d54s2
试卷第 1页,共 8页
6.某物质溶于盐酸,滴加 KSCN 溶液后颜色没有变化,再加入氯水后溶液呈血红色,
这种物质可能是
A.FeCl3 B.FeCl2 C.Fe2O3 D.Fe(OH)3
7.元素 X、Y、Z、Q 的原子序数依次增加,金属元素 X 可用于制备高能电池,Y 的一
种单质是自然界中硬度最大的物质,Z 的最高价氧化物的水化物 M 与其简单氢化物接
触时产生大量白烟,工业上常用 Q 的单质所制的容器储运 M 的浓溶液。下列说法一定
正确的是
A.X 的单质在空气中加热形成的化合物仅含离子键
B.Z 的氢化物沸点高于 Y 的氢化物
C.X、Y、Z 的原子半径依次增大
D.Q 在空气中能形成致密的氧化膜,是一种抗腐蚀的金属
8.LiA1H4是重要的还原剂与储氢材料,其合成方法为:NaA1H4+LiC1=LiA1H4+NaC1。
下列说法正确的是
··
A NaC1 Na :Cl : B 18 18. 的电子式: .中子数为 的氯原子: 17 Cl
··
C.Li+比 H-多一个电子层 D.LiA1H4既含有离子键又含有共价键
9.设 NA为阿伏加德罗常数的数值。下列说法正确的是
A.1mol 甲苯含有 6NA个 C-H 键
B.18gH2O 含有 10NA个质子
C.标准状况下,22.4L 氨水含有 NA个 NH3 分子
D.56g 铁片投入足量浓硫酸中生成 NA个 SO2 分子
10.下列说法正确的是
A. CH3 C CH2 2 的名称为 2-甲基-1-丁烯
B.丙烷的二氯代物有 4 种(不考虑立体异构)
C.苯分子中的碳碳双键可与氢气发生加成反应
D.CH3 CH CH C C CH3 分子中所有碳原子不可能在同一平面上
11.下列有关银镜反应实验的说法不正确的是
A.实验前先用热的烧碱溶液洗涤有油脂的试管,再用蒸馏水洗涤
B.向 2%的硝酸银溶液中滴入 2%的稀氨水,直至产生的沉淀恰好溶解,配得银氨溶液
C.采用水浴加热,不能直接加热
D.可用浓盐酸洗去银镜
试卷第 2页,共 8页
12.下列有关苯酚的叙述正确的是
A.苯酚呈弱酸性,能使紫色石蕊溶液显浅红色
B.苯酚分子中的 13 个原子不可能处于同一平面上
C.苯酚有腐蚀性,不慎沾在皮肤上应立即用酒精冲洗,再用水冲洗
D.苯酚较稳定,在空气中不易被氧化
13.下列属于油脂用途的是
①人类的营养物质②制取肥皂③制取甘油④制备高级脂肪酸⑤制备汽油
A.①②⑤ B.①③⑤ C.②③④⑤ D.①②③④
14. 下列由实验得出的结论正确的是
实验 结论
将乙烯通入溴的四氯化碳溶液,溶液最 生成的 1,2-二溴乙烷无色、可溶于
A.
终变为无色透明 四氯化碳
乙醇和水都可与金属钠反应产生可燃性 乙醇分子中的氢与水分子中的氢具
B.
气体 有相同的活性
C. 用乙酸浸泡水壶中的水垢,可将其清除 乙酸的酸性小于碳酸的酸性
甲烷与氯气在光照下反应后的混合气体
D. 生成的氯甲烷具有酸性
能使湿润的石蕊试纸变红
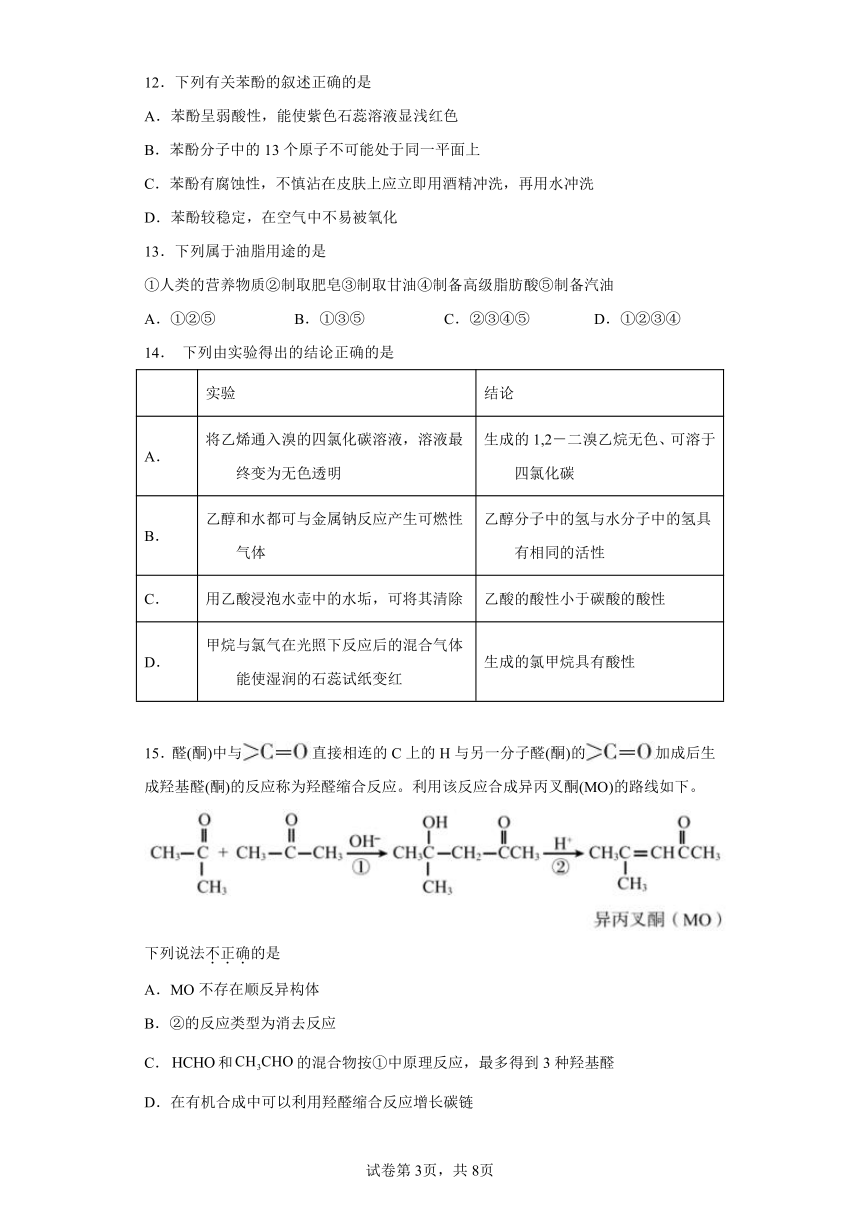
15.醛(酮)中与 直接相连的 C 上的 H 与另一分子醛(酮)的 加成后生
成羟基醛(酮)的反应称为羟醛缩合反应。利用该反应合成异丙叉酮(MO)的路线如下。
下列说法不.正.确.的是
A.MO 不存在顺反异构体
B.②的反应类型为消去反应
C.HCHO和CH3CHO 的混合物按①中原理反应,最多得到 3 种羟基醛
D.在有机合成中可以利用羟醛缩合反应增长碳链
试卷第 3页,共 8页
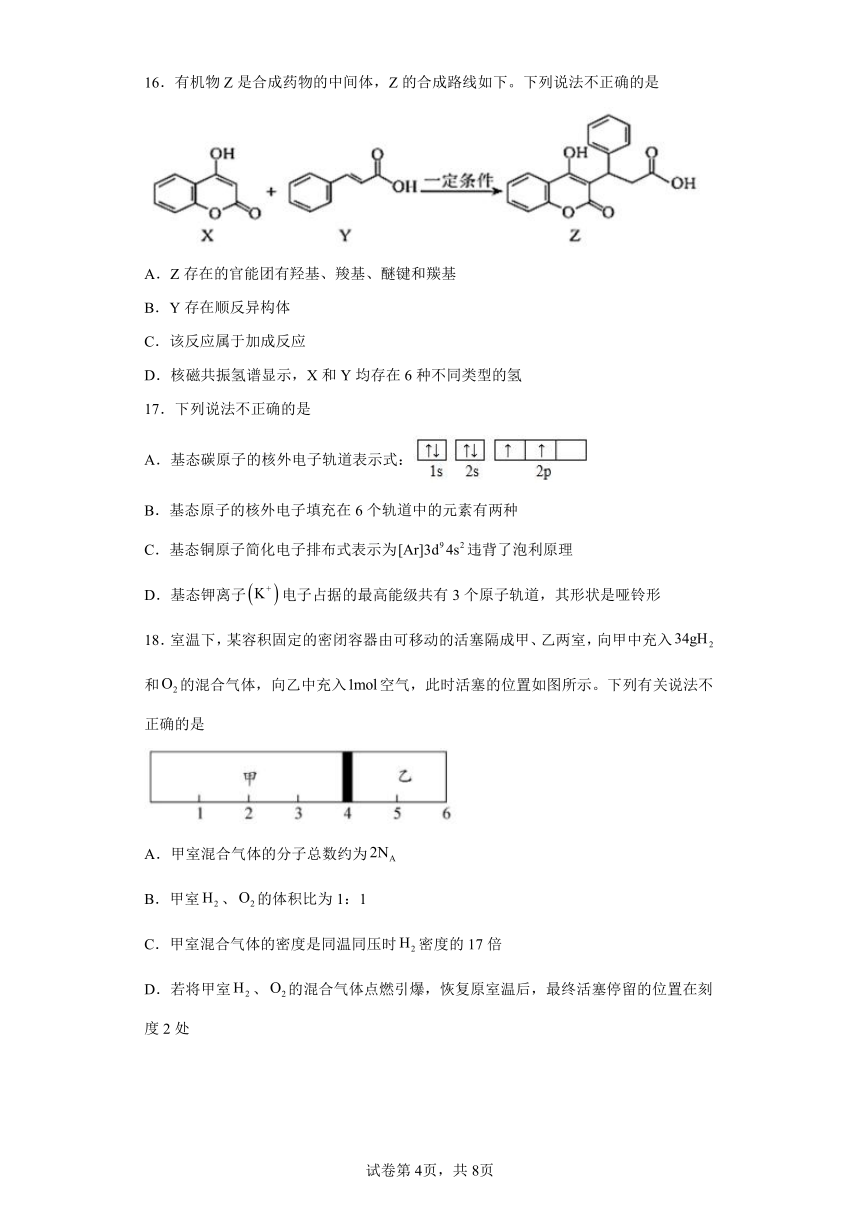
16.有机物 Z 是合成药物的中间体,Z 的合成路线如下。下列说法不正确的是
A.Z 存在的官能团有羟基、羧基、醚键和羰基
B.Y 存在顺反异构体
C.该反应属于加成反应
D.核磁共振氢谱显示,X 和 Y 均存在 6 种不同类型的氢
17.下列说法不正确的是
A.基态碳原子的核外电子轨道表示式:
B.基态原子的核外电子填充在 6 个轨道中的元素有两种
C.基态铜原子简化电子排布式表示为[Ar]3d9 4s2 违背了泡利原理
D +.基态钾离子 K 电子占据的最高能级共有 3 个原子轨道,其形状是哑铃形
18.室温下,某容积固定的密闭容器由可移动的活塞隔成甲、乙两室,向甲中充入34gH 2
和O2的混合气体,向乙中充入1mol空气,此时活塞的位置如图所示。下列有关说法不
正确的是
A.甲室混合气体的分子总数约为 2NA
B.甲室H2 、O2的体积比为 1:1
C.甲室混合气体的密度是同温同压时H2 密度的 17 倍
D.若将甲室H2 、O2的混合气体点燃引爆,恢复原室温后,最终活塞停留的位置在刻
度 2 处
试卷第 4页,共 8页
19.番木鳖酸具有一定的抗炎、抗菌活性,结构简式如图。下列说法不正确的是
A.1mol 该物质与足量饱和 NaHCO3溶液反应,可放出 22.4L(标准状况)CO2
B.一定量的该物质分别与足量 Na、NaOH 反应,消耗二者物质的量之比为 5:1
C.1mol 该物质最多可与 1molH2 发生加成反应
D.该物质可被酸性 KMnO4溶液氧化
20.对于反应A(g)+3B(g)=2C(g)+2D(g) ,下列分别表示不同条件下的反应速率,则反应
速率大小关系正确的是
① v(A)=0.01mol L-1 s-1
② v(B)=1.20mol L-1 min -1
③ v(C)=2.40mol L-1 min-1
④ v(D)=0.02mol L-1 s-1
A.②>③>④>① B.③>①=④>② C.③>④>①=② D.①>④>②>③
第Ⅱ卷(非选择题,共 40 分)
二、非选择题(本大题共 3 小题,共 40 分)
21.(14 分)氟他胺 G 是一种可用于治疗肿瘤的药物。实验室由芳香烃 A 制备 G 的合
成路线如下:
试卷第 5页,共 8页
回答下列问题:
(1)B 的结构简式为____________。A 的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型_____。
(3)反应⑤是取代反应,其反应方程式为_______________。
(4)写出 E 中官能团的名称______________。
(5)4-甲氧基乙酰苯胺( )是重要的精细化工中间体,写出
由苯甲醚( )制备 4-甲氧基乙酰苯胺的合成路线___________(其他试剂
任选)。
22.(14 分)碘( Godine)是人体必需的微量元素,是维持人体甲状腺正常功能所必需的元
素, 人体缺碘时就会患甲状腺肿大,人们主要从饮水、粮食、蔬菜和周围环境中获取碘。
多食海带,海鱼等含碘丰富的食品,对于防治甲状腺肿大很有效。某化学课外活动小组在
实验室以海带为原料获得少量碘水,并以四氯化碳(沸点 76.8℃)为溶剂将碘从碘水中提
取出来,甲同学设计实验流程如图所示。请回答下列问题:
(1)上述流程中灼烧时必.须.用.到.最.主.要.的实验仪器有酒精灯、泥三角和___________(填名
称)。
(2)操作①的名称为___________;
(3)操作②中发生反应的离子方程式为______________________,乙同学对操作②进行了
改进,用绿色氧化剂 H2O2代替氯气并加适量稀盐酸,则所发生的离子反应方程式是
____________________________________。
试卷第 6页,共 8页
(4)操作③的实验名称为___________,最.主.要.的.实验仪器的名称为___________;
(5)丙同学补充增加了一步操作:从碘的 CCl4溶液中经过___________提取了碘单质并回
收 CCl4(填该操作名称)
(6)目前,我国推行全民食用的加碘盐是在食盐中加入___________这一物质(填写化学
式)。
23.(12 分)已知:①甲醛( HCHO )与葡萄糖化学性质相似,都具有还原性;②甲酸钙易
溶于水。为探究过量甲醛和新制Cu OH 2悬浊液反应的产物,进行如下实验。
(1) -1在如图装置中进行实验,向 a中加入0.5mol L CuSO4 溶液50mL和5mol L-1 NaOH溶
液100mL ,振荡,再加入 40% 的甲醛溶液50mL ,缓慢加热20min 后冷却至室温。
①仪器 a 的名称是___________。
②能说明甲醛具有还原性的实验现象是___________。
(2)上述实验有副反应发生,产生的气体为CO、H2 中的一种或两种。为确认气体成分,
将装置 A 和下图所示装置连接后进行实验。
依次连接的合理顺序为
A→B→___________→___________→___________→___________→G,装置 B 的作用
是___________。
(3)反应后 a 中有红色固体产生,为探究其组成,提出如下假设:
假设一:只有Cu2O;
假设二:只有Cu;
试卷第 7页,共 8页
假设三:Cu2O和CuO ;
假设四:___________
假设___________明显不成立,理由是___________。
进行如下实验(以下每步均充分反应):
已知:Cu O 溶 于浓 氨水 Cu(NH) (无色)
在 空气 中 Cu NH2
2+
34 (蓝色)
锥形瓶ⅱ中固体完全溶解得深蓝色溶液的离子方程式为___________。
试卷第 8页,共 8页
化学学科 试卷
考试时间:90 分钟 满分 100 分。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27
S-32 Cl-35.5 Fe-56 Cu-64 Zn-65
第Ⅰ卷(选择题,共 60 分)
一、单选题(本大题共 20 小题,每题 3 分,共 60 分。在每小题给出的四个选项中,只
有一项是符合题目要求的)
1.芒硝(十水合硫酸钠 Na2SO4·10H2O)具有泻热通便、清火消肿等功效,可用于治疗牙
痛、阑尾炎、便秘等。下列有关芒硝的分类不正确的是
A.钠盐 B.无机化合物 C.硫酸盐 D.金属氧化物
2.AlCl3 溶液、Al(OH)3胶体和 Al(OH)3浊液是重要的分散系。下列叙述中不正确的是
A.三种分散系均是无色透明的液体
B.光线透过三种分散系时,只有胶体可发生丁达尔效应
C.Al(OH)3胶体区别于其他分散系的本质特征是分散质的微粒直径在 10-9~10-7m
D.Al(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
3.下列离子方程式正确的是
A NaOH CO CO +2OH-=CO 2-.向 溶液中通入少量 2: 2 3 + H2O
B.铁与稀盐酸反应:2Fe+6H+=2Fe3+ +3H2↑
C.FeO 溶于足量的稀盐酸:O2- +2H+=H2O
D 2-.向氢氧化钡溶液中加入等量稀硫酸:Ba2+ +OH- +H+ +SO 4 =BaSO4↓+H2O
4.下列物质在给定条件下的转化均能一步实现的是
A.Fe3O4 Fe FeCl3
B.H2O2 H2 H2O
C.CaCl2 溶液 CaCO3 CO2
D.CuSO4溶液 Cu CuO
5.下列价电子表示正确的是
A.29Cu:3d94s2 B.20Ca:3d2 C.39Y :4d15s2 D.26Fe:3d54s2
试卷第 1页,共 8页
6.某物质溶于盐酸,滴加 KSCN 溶液后颜色没有变化,再加入氯水后溶液呈血红色,
这种物质可能是
A.FeCl3 B.FeCl2 C.Fe2O3 D.Fe(OH)3
7.元素 X、Y、Z、Q 的原子序数依次增加,金属元素 X 可用于制备高能电池,Y 的一
种单质是自然界中硬度最大的物质,Z 的最高价氧化物的水化物 M 与其简单氢化物接
触时产生大量白烟,工业上常用 Q 的单质所制的容器储运 M 的浓溶液。下列说法一定
正确的是
A.X 的单质在空气中加热形成的化合物仅含离子键
B.Z 的氢化物沸点高于 Y 的氢化物
C.X、Y、Z 的原子半径依次增大
D.Q 在空气中能形成致密的氧化膜,是一种抗腐蚀的金属
8.LiA1H4是重要的还原剂与储氢材料,其合成方法为:NaA1H4+LiC1=LiA1H4+NaC1。
下列说法正确的是
··
A NaC1 Na :Cl : B 18 18. 的电子式: .中子数为 的氯原子: 17 Cl
··
C.Li+比 H-多一个电子层 D.LiA1H4既含有离子键又含有共价键
9.设 NA为阿伏加德罗常数的数值。下列说法正确的是
A.1mol 甲苯含有 6NA个 C-H 键
B.18gH2O 含有 10NA个质子
C.标准状况下,22.4L 氨水含有 NA个 NH3 分子
D.56g 铁片投入足量浓硫酸中生成 NA个 SO2 分子
10.下列说法正确的是
A. CH3 C CH2 2 的名称为 2-甲基-1-丁烯
B.丙烷的二氯代物有 4 种(不考虑立体异构)
C.苯分子中的碳碳双键可与氢气发生加成反应
D.CH3 CH CH C C CH3 分子中所有碳原子不可能在同一平面上
11.下列有关银镜反应实验的说法不正确的是
A.实验前先用热的烧碱溶液洗涤有油脂的试管,再用蒸馏水洗涤
B.向 2%的硝酸银溶液中滴入 2%的稀氨水,直至产生的沉淀恰好溶解,配得银氨溶液
C.采用水浴加热,不能直接加热
D.可用浓盐酸洗去银镜
试卷第 2页,共 8页
12.下列有关苯酚的叙述正确的是
A.苯酚呈弱酸性,能使紫色石蕊溶液显浅红色
B.苯酚分子中的 13 个原子不可能处于同一平面上
C.苯酚有腐蚀性,不慎沾在皮肤上应立即用酒精冲洗,再用水冲洗
D.苯酚较稳定,在空气中不易被氧化
13.下列属于油脂用途的是
①人类的营养物质②制取肥皂③制取甘油④制备高级脂肪酸⑤制备汽油
A.①②⑤ B.①③⑤ C.②③④⑤ D.①②③④
14. 下列由实验得出的结论正确的是
实验 结论
将乙烯通入溴的四氯化碳溶液,溶液最 生成的 1,2-二溴乙烷无色、可溶于
A.
终变为无色透明 四氯化碳
乙醇和水都可与金属钠反应产生可燃性 乙醇分子中的氢与水分子中的氢具
B.
气体 有相同的活性
C. 用乙酸浸泡水壶中的水垢,可将其清除 乙酸的酸性小于碳酸的酸性
甲烷与氯气在光照下反应后的混合气体
D. 生成的氯甲烷具有酸性
能使湿润的石蕊试纸变红
15.醛(酮)中与 直接相连的 C 上的 H 与另一分子醛(酮)的 加成后生
成羟基醛(酮)的反应称为羟醛缩合反应。利用该反应合成异丙叉酮(MO)的路线如下。
下列说法不.正.确.的是
A.MO 不存在顺反异构体
B.②的反应类型为消去反应
C.HCHO和CH3CHO 的混合物按①中原理反应,最多得到 3 种羟基醛
D.在有机合成中可以利用羟醛缩合反应增长碳链
试卷第 3页,共 8页
16.有机物 Z 是合成药物的中间体,Z 的合成路线如下。下列说法不正确的是
A.Z 存在的官能团有羟基、羧基、醚键和羰基
B.Y 存在顺反异构体
C.该反应属于加成反应
D.核磁共振氢谱显示,X 和 Y 均存在 6 种不同类型的氢
17.下列说法不正确的是
A.基态碳原子的核外电子轨道表示式:
B.基态原子的核外电子填充在 6 个轨道中的元素有两种
C.基态铜原子简化电子排布式表示为[Ar]3d9 4s2 违背了泡利原理
D +.基态钾离子 K 电子占据的最高能级共有 3 个原子轨道,其形状是哑铃形
18.室温下,某容积固定的密闭容器由可移动的活塞隔成甲、乙两室,向甲中充入34gH 2
和O2的混合气体,向乙中充入1mol空气,此时活塞的位置如图所示。下列有关说法不
正确的是
A.甲室混合气体的分子总数约为 2NA
B.甲室H2 、O2的体积比为 1:1
C.甲室混合气体的密度是同温同压时H2 密度的 17 倍
D.若将甲室H2 、O2的混合气体点燃引爆,恢复原室温后,最终活塞停留的位置在刻
度 2 处
试卷第 4页,共 8页
19.番木鳖酸具有一定的抗炎、抗菌活性,结构简式如图。下列说法不正确的是
A.1mol 该物质与足量饱和 NaHCO3溶液反应,可放出 22.4L(标准状况)CO2
B.一定量的该物质分别与足量 Na、NaOH 反应,消耗二者物质的量之比为 5:1
C.1mol 该物质最多可与 1molH2 发生加成反应
D.该物质可被酸性 KMnO4溶液氧化
20.对于反应A(g)+3B(g)=2C(g)+2D(g) ,下列分别表示不同条件下的反应速率,则反应
速率大小关系正确的是
① v(A)=0.01mol L-1 s-1
② v(B)=1.20mol L-1 min -1
③ v(C)=2.40mol L-1 min-1
④ v(D)=0.02mol L-1 s-1
A.②>③>④>① B.③>①=④>② C.③>④>①=② D.①>④>②>③
第Ⅱ卷(非选择题,共 40 分)
二、非选择题(本大题共 3 小题,共 40 分)
21.(14 分)氟他胺 G 是一种可用于治疗肿瘤的药物。实验室由芳香烃 A 制备 G 的合
成路线如下:
试卷第 5页,共 8页
回答下列问题:
(1)B 的结构简式为____________。A 的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型_____。
(3)反应⑤是取代反应,其反应方程式为_______________。
(4)写出 E 中官能团的名称______________。
(5)4-甲氧基乙酰苯胺( )是重要的精细化工中间体,写出
由苯甲醚( )制备 4-甲氧基乙酰苯胺的合成路线___________(其他试剂
任选)。
22.(14 分)碘( Godine)是人体必需的微量元素,是维持人体甲状腺正常功能所必需的元
素, 人体缺碘时就会患甲状腺肿大,人们主要从饮水、粮食、蔬菜和周围环境中获取碘。
多食海带,海鱼等含碘丰富的食品,对于防治甲状腺肿大很有效。某化学课外活动小组在
实验室以海带为原料获得少量碘水,并以四氯化碳(沸点 76.8℃)为溶剂将碘从碘水中提
取出来,甲同学设计实验流程如图所示。请回答下列问题:
(1)上述流程中灼烧时必.须.用.到.最.主.要.的实验仪器有酒精灯、泥三角和___________(填名
称)。
(2)操作①的名称为___________;
(3)操作②中发生反应的离子方程式为______________________,乙同学对操作②进行了
改进,用绿色氧化剂 H2O2代替氯气并加适量稀盐酸,则所发生的离子反应方程式是
____________________________________。
试卷第 6页,共 8页
(4)操作③的实验名称为___________,最.主.要.的.实验仪器的名称为___________;
(5)丙同学补充增加了一步操作:从碘的 CCl4溶液中经过___________提取了碘单质并回
收 CCl4(填该操作名称)
(6)目前,我国推行全民食用的加碘盐是在食盐中加入___________这一物质(填写化学
式)。
23.(12 分)已知:①甲醛( HCHO )与葡萄糖化学性质相似,都具有还原性;②甲酸钙易
溶于水。为探究过量甲醛和新制Cu OH 2悬浊液反应的产物,进行如下实验。
(1) -1在如图装置中进行实验,向 a中加入0.5mol L CuSO4 溶液50mL和5mol L-1 NaOH溶
液100mL ,振荡,再加入 40% 的甲醛溶液50mL ,缓慢加热20min 后冷却至室温。
①仪器 a 的名称是___________。
②能说明甲醛具有还原性的实验现象是___________。
(2)上述实验有副反应发生,产生的气体为CO、H2 中的一种或两种。为确认气体成分,
将装置 A 和下图所示装置连接后进行实验。
依次连接的合理顺序为
A→B→___________→___________→___________→___________→G,装置 B 的作用
是___________。
(3)反应后 a 中有红色固体产生,为探究其组成,提出如下假设:
假设一:只有Cu2O;
假设二:只有Cu;
试卷第 7页,共 8页
假设三:Cu2O和CuO ;
假设四:___________
假设___________明显不成立,理由是___________。
进行如下实验(以下每步均充分反应):
已知:Cu O 溶 于浓 氨水 Cu(NH) (无色)
在 空气 中 Cu NH2
2+
34 (蓝色)
锥形瓶ⅱ中固体完全溶解得深蓝色溶液的离子方程式为___________。
试卷第 8页,共 8页
同课章节目录
