1.4 配制溶液 同步练习 (含答案)
文档属性
| 名称 | 1.4 配制溶液 同步练习 (含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 62.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-03-02 00:00:00 | ||
图片预览


文档简介
1.4 配制溶液
一、选择题
1.我国南方的土壤以酸性为主,农民引淡水冲洗以减弱其酸性,在下图中符合冲洗过程酸碱性变化的曲线是( )
A. B. C. D.
2.2012年6月18日,载着景海鹏、刘旺、刘洋三名航天员的神舟九号飞船与天宫一号目标飞行器实现自动交会对接。3名航天员在飞船轨道舱内就餐,在天宫一号内进行科学实验、技术试验、锻炼和休息。在航天飞船的失重环境中下列实验操作最难完成的是( )
A.结晶 B.蒸发 C.溶解 D.过滤
3.在一定温度下,向盛有100g蔗糖溶液的烧杯中再加入10g蔗糖,充分搅拌后,一定不变的是( )
A.溶质的质量 B.溶液的质量 C.溶质的质量分数 D.蔗糖的溶解度
4.茗茗在家用25℃的水溶解一定量的蔗糖,充分搅拌后发现杯底还有部分蔗糖没有溶 解,然后她又用火将其加热至50℃,发现蔗糖全部溶解了,判断在加热前后,以下各量 没有发生改变的是( )
A.蔗糖的溶解度 B.溶液的质量
C.溶剂的质量 D.溶质的质量分数
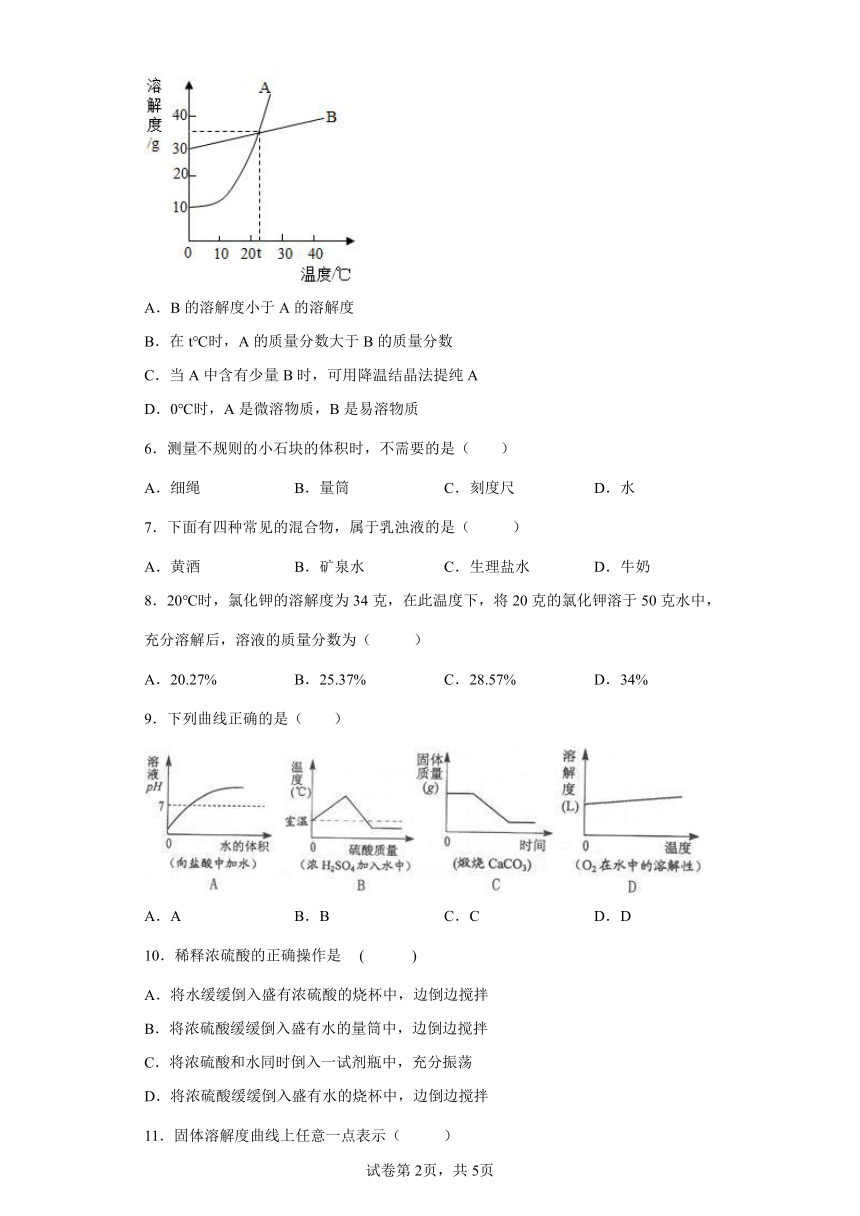
5.图中所示是A、B两种固体物质的溶解度曲线,下列说法正确的是( )
A.B的溶解度小于A的溶解度
B.在t℃时,A的质量分数大于B的质量分数
C.当A中含有少量B时,可用降温结晶法提纯A
D.0℃时,A是微溶物质,B是易溶物质
6.测量不规则的小石块的体积时,不需要的是( )
A.细绳 B.量筒 C.刻度尺 D.水
7.下面有四种常见的混合物,属于乳浊液的是( )
A.黄酒 B.矿泉水 C.生理盐水 D.牛奶
8.20℃时,氯化钾的溶解度为34克,在此温度下,将20克的氯化钾溶于50克水中,充分溶解后,溶液的质量分数为( )
A.20.27% B.25.37% C.28.57% D.34%
9.下列曲线正确的是( )
A.A B.B C.C D.D
10.稀释浓硫酸的正确操作是 ( )
A.将水缓缓倒入盛有浓硫酸的烧杯中,边倒边搅拌
B.将浓硫酸缓缓倒入盛有水的量筒中,边倒边搅拌
C.将浓硫酸和水同时倒入一试剂瓶中,充分振荡
D.将浓硫酸缓缓倒入盛有水的烧杯中,边倒边搅拌
11.固体溶解度曲线上任意一点表示( )
A.溶液达到饱和时溶质的克数
B.该温度下,100克溶剂里最多能溶解溶质的克数
C.该温度下,一定量的溶剂里最多能溶解溶质的克数
D.无任何意义
12.向质量分数为20%的氢氧化钠溶液中加入3 g固体氢氧化钠和12 g水,所得溶液中溶质的质量分数是
A.25% B.23%
C.20.5% D.20%
二、填空题
13.现有三种物质,它们的性质如表
物质 状态 溶于水的情况 溶解度受温度影响
Ⅰ 固态 不溶于水 ──
Ⅱ 固态 溶于水 较大
Ⅲ 固态 溶于水 较小
常用物质分离的方法有A.过滤;B.蒸馏; C.蒸发结晶;D.冷却热饱和溶液;请从上述四种方法中选择适当的方法填空:
(1)若由Ⅰ和Ⅱ两种物质组成的混合物,要把它们分离,应采用 方法。
(2)若由Ⅱ和Ⅲ两种物质组成的混合物,要把它们分离,应采用 方法。
(3)若由Ⅰ、Ⅱ和Ⅲ三种物质组成的混合物,要把它们分离,不需要采用的方法是 。
14.(某化学实验需要用到质量分数为19.6%的稀硫酸,现要将100克98%的浓硫酸硫进行稀释,需加水 克,稀释时需要用到的玻璃仪器为 。
15.实验室欲配制100g15%的食盐水,
(1)计算:计算需食盐______g,水______毫升;
(2)____:用托盘天平称取所需的氯化钠,(应遵循左物______),固体放入烧杯中。选用(“50mL”、“100mL”、“150mL”)____量筒量取所需的水;
(3)溶解:将用量筒量取的水,倒入盛有氯化钠的烧杯中,用玻璃棒搅拌。(搅拌的作用_____)待氯化钠完全溶解时,15%的氯化钠溶液就配置好了。
16.某学生配制50克质量分数为10%的NaCl溶液,其全部过程如下图所示。按要求填空: 指出该实验的其他一个步骤,并指出图中的错误:
(1)第一步:计算,需要NaCl为__________克,水为_______________毫升。
第二步:称量与量取。
第三步:___________________________。
(2)请指出图中的错处:___________________________________。(指出一处即可)
17.pH试纸是常用的酸碱指示剂,pH试纸的一般测试范围是 。
三、简答题
18.传统“陈醋”生产过程中有一步称为“冬捞夏晒”,是指冬天捞出醋中的冰,夏日曝晒蒸发醋中的水分,以提高醋的品质.假设用醋酸的质量分数为3%的半成醋,生产600g克5%的优级醋,过程中醋酸没有损失,(1)需要质量分数为3%的半成醋的质量多少克?(2)捞出的冰和蒸发的水的总质量为多少克?
19.下列为配制l00g质量分数为10.6%的碳酸钠溶液的实验,请分析有关问题:
(1)计算:碳酸钠的质量为_________g。
(2)称量:用托盘天平称量,碳酸钠应放在_______盘。
(3)溶解:用量筒来量取所需的水,量筒的规格是____________ (从下列中选用:10ml、25ml、50ml、l00mL).
(4)反思:配制溶液时,会引起溶液中氯化钠的质量分数偏大的是( )
A 用量筒量取水时俯视读数
B 配制溶液的烧杯用少量蒸馏水润洗
C 氯化钠晶体不纯
D 转移已配好的溶液时,有少量溶液溅出
四、探究题
20.在一烧杯中盛有l00gBaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:
(1)实验过程中,有气体放出,还可以看到的明显的实验现象是 。
(2)在实验过程中放出气体的总质量为多少克?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.D
4.C
5.C
6.C
7.D
8.B
9.C
10.D
11.B
12.D
13.(1)A; (2)D; (3)B
14.400、烧杯和玻璃棒
15. 15 85 称量(称取和量取) 右码 100mL 加速溶解
16. 5 45 溶解 瓶塞正放
17.0<pH<14
18.1000g、400g
19. 10.6 左 100ml A
20.(1)产生白色沉淀(2)4.4克
答案第1页,共2页
答案第1页,共2页
一、选择题
1.我国南方的土壤以酸性为主,农民引淡水冲洗以减弱其酸性,在下图中符合冲洗过程酸碱性变化的曲线是( )
A. B. C. D.
2.2012年6月18日,载着景海鹏、刘旺、刘洋三名航天员的神舟九号飞船与天宫一号目标飞行器实现自动交会对接。3名航天员在飞船轨道舱内就餐,在天宫一号内进行科学实验、技术试验、锻炼和休息。在航天飞船的失重环境中下列实验操作最难完成的是( )
A.结晶 B.蒸发 C.溶解 D.过滤
3.在一定温度下,向盛有100g蔗糖溶液的烧杯中再加入10g蔗糖,充分搅拌后,一定不变的是( )
A.溶质的质量 B.溶液的质量 C.溶质的质量分数 D.蔗糖的溶解度
4.茗茗在家用25℃的水溶解一定量的蔗糖,充分搅拌后发现杯底还有部分蔗糖没有溶 解,然后她又用火将其加热至50℃,发现蔗糖全部溶解了,判断在加热前后,以下各量 没有发生改变的是( )
A.蔗糖的溶解度 B.溶液的质量
C.溶剂的质量 D.溶质的质量分数
5.图中所示是A、B两种固体物质的溶解度曲线,下列说法正确的是( )
A.B的溶解度小于A的溶解度
B.在t℃时,A的质量分数大于B的质量分数
C.当A中含有少量B时,可用降温结晶法提纯A
D.0℃时,A是微溶物质,B是易溶物质
6.测量不规则的小石块的体积时,不需要的是( )
A.细绳 B.量筒 C.刻度尺 D.水
7.下面有四种常见的混合物,属于乳浊液的是( )
A.黄酒 B.矿泉水 C.生理盐水 D.牛奶
8.20℃时,氯化钾的溶解度为34克,在此温度下,将20克的氯化钾溶于50克水中,充分溶解后,溶液的质量分数为( )
A.20.27% B.25.37% C.28.57% D.34%
9.下列曲线正确的是( )
A.A B.B C.C D.D
10.稀释浓硫酸的正确操作是 ( )
A.将水缓缓倒入盛有浓硫酸的烧杯中,边倒边搅拌
B.将浓硫酸缓缓倒入盛有水的量筒中,边倒边搅拌
C.将浓硫酸和水同时倒入一试剂瓶中,充分振荡
D.将浓硫酸缓缓倒入盛有水的烧杯中,边倒边搅拌
11.固体溶解度曲线上任意一点表示( )
A.溶液达到饱和时溶质的克数
B.该温度下,100克溶剂里最多能溶解溶质的克数
C.该温度下,一定量的溶剂里最多能溶解溶质的克数
D.无任何意义
12.向质量分数为20%的氢氧化钠溶液中加入3 g固体氢氧化钠和12 g水,所得溶液中溶质的质量分数是
A.25% B.23%
C.20.5% D.20%
二、填空题
13.现有三种物质,它们的性质如表
物质 状态 溶于水的情况 溶解度受温度影响
Ⅰ 固态 不溶于水 ──
Ⅱ 固态 溶于水 较大
Ⅲ 固态 溶于水 较小
常用物质分离的方法有A.过滤;B.蒸馏; C.蒸发结晶;D.冷却热饱和溶液;请从上述四种方法中选择适当的方法填空:
(1)若由Ⅰ和Ⅱ两种物质组成的混合物,要把它们分离,应采用 方法。
(2)若由Ⅱ和Ⅲ两种物质组成的混合物,要把它们分离,应采用 方法。
(3)若由Ⅰ、Ⅱ和Ⅲ三种物质组成的混合物,要把它们分离,不需要采用的方法是 。
14.(某化学实验需要用到质量分数为19.6%的稀硫酸,现要将100克98%的浓硫酸硫进行稀释,需加水 克,稀释时需要用到的玻璃仪器为 。
15.实验室欲配制100g15%的食盐水,
(1)计算:计算需食盐______g,水______毫升;
(2)____:用托盘天平称取所需的氯化钠,(应遵循左物______),固体放入烧杯中。选用(“50mL”、“100mL”、“150mL”)____量筒量取所需的水;
(3)溶解:将用量筒量取的水,倒入盛有氯化钠的烧杯中,用玻璃棒搅拌。(搅拌的作用_____)待氯化钠完全溶解时,15%的氯化钠溶液就配置好了。
16.某学生配制50克质量分数为10%的NaCl溶液,其全部过程如下图所示。按要求填空: 指出该实验的其他一个步骤,并指出图中的错误:
(1)第一步:计算,需要NaCl为__________克,水为_______________毫升。
第二步:称量与量取。
第三步:___________________________。
(2)请指出图中的错处:___________________________________。(指出一处即可)
17.pH试纸是常用的酸碱指示剂,pH试纸的一般测试范围是 。
三、简答题
18.传统“陈醋”生产过程中有一步称为“冬捞夏晒”,是指冬天捞出醋中的冰,夏日曝晒蒸发醋中的水分,以提高醋的品质.假设用醋酸的质量分数为3%的半成醋,生产600g克5%的优级醋,过程中醋酸没有损失,(1)需要质量分数为3%的半成醋的质量多少克?(2)捞出的冰和蒸发的水的总质量为多少克?
19.下列为配制l00g质量分数为10.6%的碳酸钠溶液的实验,请分析有关问题:
(1)计算:碳酸钠的质量为_________g。
(2)称量:用托盘天平称量,碳酸钠应放在_______盘。
(3)溶解:用量筒来量取所需的水,量筒的规格是____________ (从下列中选用:10ml、25ml、50ml、l00mL).
(4)反思:配制溶液时,会引起溶液中氯化钠的质量分数偏大的是( )
A 用量筒量取水时俯视读数
B 配制溶液的烧杯用少量蒸馏水润洗
C 氯化钠晶体不纯
D 转移已配好的溶液时,有少量溶液溅出
四、探究题
20.在一烧杯中盛有l00gBaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:
(1)实验过程中,有气体放出,还可以看到的明显的实验现象是 。
(2)在实验过程中放出气体的总质量为多少克?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.D
4.C
5.C
6.C
7.D
8.B
9.C
10.D
11.B
12.D
13.(1)A; (2)D; (3)B
14.400、烧杯和玻璃棒
15. 15 85 称量(称取和量取) 右码 100mL 加速溶解
16. 5 45 溶解 瓶塞正放
17.0<pH<14
18.1000g、400g
19. 10.6 左 100ml A
20.(1)产生白色沉淀(2)4.4克
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 水
- 1 地球上的水
- 2 水的三态变化
- 3 水是常用的溶剂
- 4 配制溶液
- 5 水的组成
- 6 水资源的利用和保护
- 第2章 空气
- 1 空气的存在
- 2 空气的成分
- 3 氧气
- 4 二氧化碳
- 5 保护大气圈
- 第3章 阳光
- 1 太阳辐射能
- 2 阳光的传播
- 3 阳光的组成
- 第4章 土壤
- 1 土壤的组成和性状
- 2 土壤与植物
- 3 人类活动与土壤
- 第5章 生态系统
- 1 种群和群落
- 2 生态系统
- 3 生物圈
- 第6章 动物和人的生殖与发育
- 1 动物的生殖与发育
- 2 人的生殖与发育
- 第7章 植物和微生物的生殖与发育
- 1 绿色开花植物的有性生殖和发育
- 2 种子的萌发和幼苗形成
- 3 植物的无性生殖
- 4 细菌和真菌的繁殖
