人教版九年级下册化学达标检测卷—第九单元 溶液(含答案)
文档属性
| 名称 | 人教版九年级下册化学达标检测卷—第九单元 溶液(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-03 10:11:07 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
人教版九年级下册化学第九单元达标检测卷
【检测内容:溶 液 满分:40分】
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Cl—35.5 Zn—65
题 号 一 二 总 分
得 分
一、选择题(本大题包括12小题,每小题1分,共12分;每小题只有一个选项符合题意)
1.溶液在我们生活中有着广泛的用途。下列物质不属于溶液的是( )
A.碘酒 B.食醋 C.生理盐水 D.牛奶
2.下列说法错误的是( )
A.与乳化作用相比,溶解能使物质混合得更均匀
B.20 ℃时,50 g水中溶解15 g硝酸钾,则20 ℃时硝酸钾的溶解度是30 g
C.溶液具有导电性是因为其中含有自由移动的离子
D.硝酸钾的饱和溶液恒温蒸发部分水后,剩余溶液中溶质的质量分数不变
3.下列关于溶液的说法正确的是( )
A.溶液都是无色、无味的液体
B.将植物油加入水中搅拌,可得到溶液
C.氧化钙加入水中搅拌,所得的溶液中溶剂是水,溶质是氧化钙
D.外界条件不改变,溶质不会从溶液中分离出来
4.如图所示,打开止水夹,将液体A滴入试管②中。若试管①中的导管口有较多气泡产生,则液体A和固体B的组合不可能是( )
A.水和生石灰 B.水和氯化钠
C.水和氢氧化钠 D.过氧化氢溶液和二氧化锰
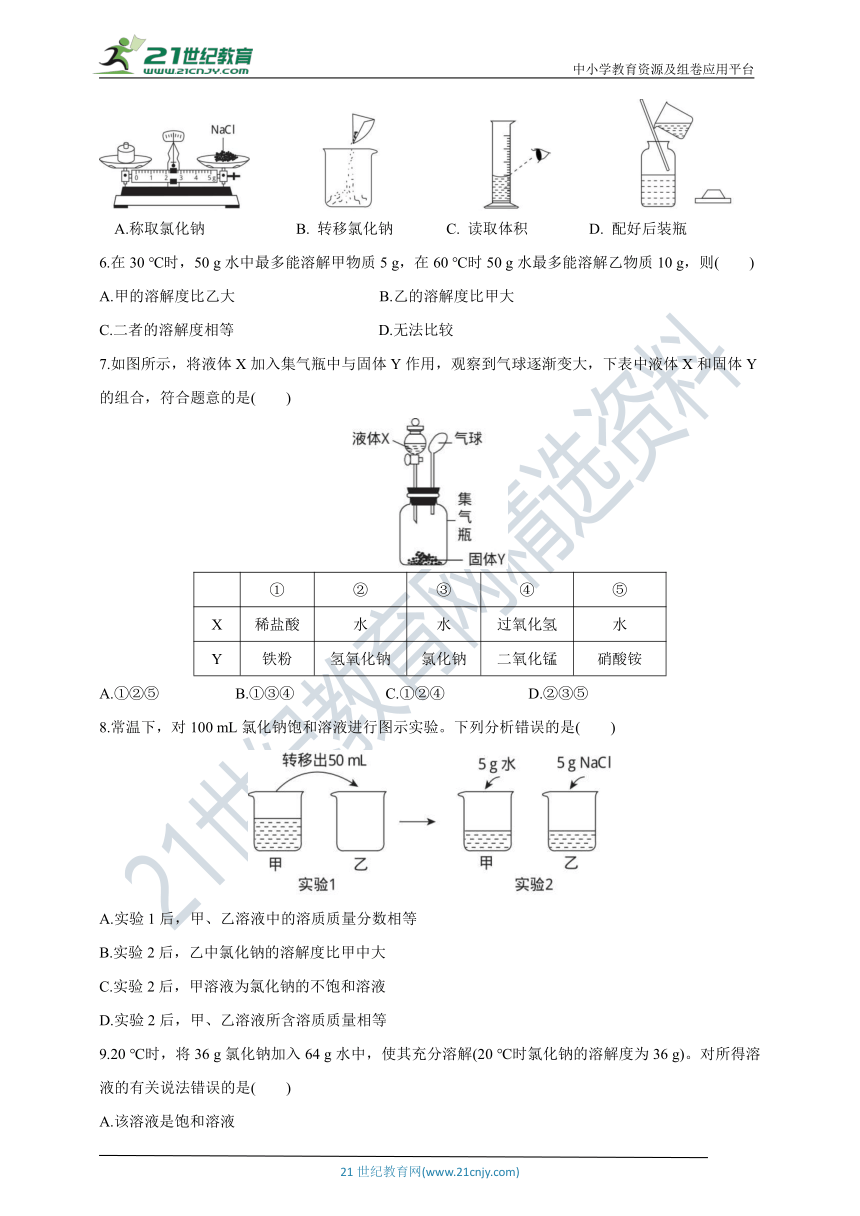
5.配制70 g 16%的NaCl溶液,下列操作会使所配溶液溶质质量分数大于16%的是( )
A.称取氯化钠 B. 转移氯化钠 C. 读取体积 D. 配好后装瓶
6.在30 ℃时,50 g水中最多能溶解甲物质5 g,在60 ℃时50 g水最多能溶解乙物质10 g,则( )
A.甲的溶解度比乙大 B.乙的溶解度比甲大
C.二者的溶解度相等 D.无法比较
7.如图所示,将液体X加入集气瓶中与固体Y作用,观察到气球逐渐变大,下表中液体X和固体Y的组合,符合题意的是( )
① ② ③ ④ ⑤
X 稀盐酸 水 水 过氧化氢 水
Y 铁粉 氢氧化钠 氯化钠 二氧化锰 硝酸铵
A.①②⑤ B.①③④ C.①②④ D.②③⑤
8.常温下,对100 mL氯化钠饱和溶液进行图示实验。下列分析错误的是( )
A.实验1后,甲、乙溶液中的溶质质量分数相等
B.实验2后,乙中氯化钠的溶解度比甲中大
C.实验2后,甲溶液为氯化钠的不饱和溶液
D.实验2后,甲、乙溶液所含溶质质量相等
9.20 ℃时,将36 g氯化钠加入64 g水中,使其充分溶解(20 ℃时氯化钠的溶解度为36 g)。对所得溶液的有关说法错误的是( )
A.该溶液是饱和溶液
B.溶液中Na+和Cl-个数一定相等
C.溶液质量为100 g
D.溶质与溶剂质量比为9∶25
10.某温度时,将20 g KNO3溶解在100 g水中恰好饱和,关于该饱和溶液的叙述正确的是( )
A.m溶质∶m溶剂=1∶6 B.溶质的质量分数为20%
C.升温后,溶质的质量分数增大 D.降温后,有固体析出
11.如图所示,下列判断正确的是( )
A.Y的溶解度比X的溶解度大
B.t1 ℃时,X、Y两种饱和溶液的溶质质量分数都是20%
C.若烧杯内有晶体析出,则烧杯中饱和溶液的溶质为Y
D.t2 ℃时,若X、Y的饱和溶液质量相等,则溶液中溶质的质量:X12.向蒸馏水中加入NaOH颗粒,不断搅拌,用温度传感器记录溶解过程的温度变化如图所示。a、c两点观察到溶液中有固体存在,b点固体完全消失。下列说法不正确的是( )
A.NaOH固体溶于水是放热过程
B.a、c两点时,NaOH的溶解度相同
C.b点时,该溶液一定是饱和溶液
D.c点时的溶剂质量等于a点时的溶剂质量
二、非选择题(本大题包括5小题,共28分)
13.(5分)分析处理图表中的信息是学习化学的一种重要方法。下表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答下列问题。
温度/℃ 10 20 30 40
溶解度/g 氯化钠 35.8 36.0 36.3 36.6
碳酸钠 12.2 21.8 39.7 53.2
(1)40 ℃时,氯化钠的溶解度为 g。
(2)碳酸钠的溶解度随温度的升高而 (填“增大”或“减小”)。20 ℃时,将30 g碳酸钠加入100 g水中,充分搅拌后得到的是碳酸钠的 (填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30 ℃,所得溶液的溶质质量分数为 (结果精确到0.1%)。
(3)10 ℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的是 溶液。
14.(6分)如图是A、B、C三种物质的溶解度曲线,请回答下列问题。
(1)溶解度随温度升高而减小的物质是 ,要使该物质的不饱和溶液变为饱和溶液,可采取的一种方法是 。
(2)t2 ℃时,三种物质的溶解度由大到小的顺序是 。
(3)t3 ℃时,B的饱和溶液中溶质的质量分数 (填“大于”“小于”或“等于”)A的饱和溶液中溶质的质量分数。
(4)t3 ℃时,将50 g A加入50 g水中,充分溶解后所得溶液的质量是 g。
(5)将t2 ℃时的三种物质的饱和溶液降温至t1 ℃时,所得溶液的溶质质量分数的大小关系是 。
15.(6分)我国制碱工业的先驱——侯德榜成功地探索和改进了西方的制碱方法。下表为侯氏制碱法中部分物质的溶解度。
温度/℃ 10 20 30 40
溶解度/g Na2CO3 12.2 21.8 39.7 48.8
NaCl 35.8 36.0 36.3 36.6
NaHCO3 8.2 9.6 11.1 12.7
(1)在30 ℃时,Na2CO3的溶解度 (填“>”“<”或“=”)NaHCO3的溶解度。
(2)由上表可知,在10~40 ℃之间溶解度随温度变化最小的物质是 (填物质名称,下同),三种物质最不易溶于水的是 。
(3)20 ℃时,将15 g氯化钠固体溶解在50 g水中,所得溶液为 (填“饱和溶液”或“不饱和溶液” ),所得溶液中溶质的质量分数为 ( 结果精确到0.1% )。
(4)40 ℃时,将等质量的三种表中物质的饱和溶液降温至20 ℃,所得溶液中溶质的质量分数由大到小的顺序是 ( 用化学式表示 )。
16.(6分)为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验(提示:本实验所用汽油与KMnO4、碘均不发生化学反应)。
【实验1】KMnO4晶体在不同溶剂中的溶解实验,根据实验步骤、实验操作图示填写相关实验现象。
实验步骤 实验操作图示 实验操作及现象
步骤1 向A、B两试管中分别加入5 mL水和5 mL无色汽油,振荡后静置;(1)A试管中晶体全部溶解,溶液呈 色;B试管中晶体不溶解,汽油不变色
步骤2 将步骤1中A试管内溶液倒入B试管中,振荡后静置;(2)B试管中观察到的现象为
【实验2】碘在不同溶剂中的溶解实验,根据实验操作图示回答相关问题。
实验操作图示 实验结论或解释
(3)由图2所示现象可知:碘 (填“不”“微”或“易”)溶于水 (4)图3所示试管中液体分层。上层紫红色溶液的名称是 ;说明碘在汽油中的溶解性比在水中 (填“强”或“弱”)
【实验结论】根据上述实验可得出的结论是 (写出一条即可) 。
[注意:若答对下列小题奖励3分,化学试卷总分不超过40分。]
【反思与应用】(5)①碘易溶于酒精。若【实验2】中用酒精代替汽油,振荡后静置,最终所得液体
(填“分层”或“不分层”)。
②“从稀碘水中提取碘”是“海带提碘”工艺中的一个重要步骤,其原理类似【实验2】中第二步操作。工业上实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是 。
17.(5分)某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表,制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到100 g氯化钾溶液。
加热时间/min 0 t1 t2 t3
固体的质量/g 28.0 23.2 18.4 18.4
(1)共制得氧气 g;
(2)计算所得氯化钾溶液的溶质质量分数。
参 考 答 案
1. D 2. B 3. D 4. A 5. B 6. D 7. C 8. B 9. C 10. D 11. D 12. C
13.(1)36.6 (2)增大 饱和溶液 23.1% (3)碳酸钠
14.(1)C 升高温度(或加入溶质,合理即可) (2)A=B>C (3)小于 (4)90 (5)B>A>C
15.(1)> (2)氯化钠 碳酸氢钠 (3)不饱和溶液 23.1% (4)NaCl>Na2CO3>NaHCO3
16.(1)紫红 (2)试管中晶体溶解,液体分层 (3)微 (4)碘的汽油溶液 强 不同溶质在同种溶剂中的溶解性不同(或同种溶质在不同溶剂中的溶解性不同) (5)①不分层 ②不溶于水,碘在这种液体里的溶解度远大于在水中的溶解度
17.解:(1)9.6
(2)设生成氯化钾的质量为x。
2KC1O32KC1+3O2 ↑
149 96
x 9.6g
= x=14.9 g
×100%= 14.9%
答:所得氯化钾溶液的溶质质量分数为14. 9%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
人教版九年级下册化学第九单元达标检测卷
【检测内容:溶 液 满分:40分】
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Cl—35.5 Zn—65
题 号 一 二 总 分
得 分
一、选择题(本大题包括12小题,每小题1分,共12分;每小题只有一个选项符合题意)
1.溶液在我们生活中有着广泛的用途。下列物质不属于溶液的是( )
A.碘酒 B.食醋 C.生理盐水 D.牛奶
2.下列说法错误的是( )
A.与乳化作用相比,溶解能使物质混合得更均匀
B.20 ℃时,50 g水中溶解15 g硝酸钾,则20 ℃时硝酸钾的溶解度是30 g
C.溶液具有导电性是因为其中含有自由移动的离子
D.硝酸钾的饱和溶液恒温蒸发部分水后,剩余溶液中溶质的质量分数不变
3.下列关于溶液的说法正确的是( )
A.溶液都是无色、无味的液体
B.将植物油加入水中搅拌,可得到溶液
C.氧化钙加入水中搅拌,所得的溶液中溶剂是水,溶质是氧化钙
D.外界条件不改变,溶质不会从溶液中分离出来
4.如图所示,打开止水夹,将液体A滴入试管②中。若试管①中的导管口有较多气泡产生,则液体A和固体B的组合不可能是( )
A.水和生石灰 B.水和氯化钠
C.水和氢氧化钠 D.过氧化氢溶液和二氧化锰
5.配制70 g 16%的NaCl溶液,下列操作会使所配溶液溶质质量分数大于16%的是( )
A.称取氯化钠 B. 转移氯化钠 C. 读取体积 D. 配好后装瓶
6.在30 ℃时,50 g水中最多能溶解甲物质5 g,在60 ℃时50 g水最多能溶解乙物质10 g,则( )
A.甲的溶解度比乙大 B.乙的溶解度比甲大
C.二者的溶解度相等 D.无法比较
7.如图所示,将液体X加入集气瓶中与固体Y作用,观察到气球逐渐变大,下表中液体X和固体Y的组合,符合题意的是( )
① ② ③ ④ ⑤
X 稀盐酸 水 水 过氧化氢 水
Y 铁粉 氢氧化钠 氯化钠 二氧化锰 硝酸铵
A.①②⑤ B.①③④ C.①②④ D.②③⑤
8.常温下,对100 mL氯化钠饱和溶液进行图示实验。下列分析错误的是( )
A.实验1后,甲、乙溶液中的溶质质量分数相等
B.实验2后,乙中氯化钠的溶解度比甲中大
C.实验2后,甲溶液为氯化钠的不饱和溶液
D.实验2后,甲、乙溶液所含溶质质量相等
9.20 ℃时,将36 g氯化钠加入64 g水中,使其充分溶解(20 ℃时氯化钠的溶解度为36 g)。对所得溶液的有关说法错误的是( )
A.该溶液是饱和溶液
B.溶液中Na+和Cl-个数一定相等
C.溶液质量为100 g
D.溶质与溶剂质量比为9∶25
10.某温度时,将20 g KNO3溶解在100 g水中恰好饱和,关于该饱和溶液的叙述正确的是( )
A.m溶质∶m溶剂=1∶6 B.溶质的质量分数为20%
C.升温后,溶质的质量分数增大 D.降温后,有固体析出
11.如图所示,下列判断正确的是( )
A.Y的溶解度比X的溶解度大
B.t1 ℃时,X、Y两种饱和溶液的溶质质量分数都是20%
C.若烧杯内有晶体析出,则烧杯中饱和溶液的溶质为Y
D.t2 ℃时,若X、Y的饱和溶液质量相等,则溶液中溶质的质量:X
A.NaOH固体溶于水是放热过程
B.a、c两点时,NaOH的溶解度相同
C.b点时,该溶液一定是饱和溶液
D.c点时的溶剂质量等于a点时的溶剂质量
二、非选择题(本大题包括5小题,共28分)
13.(5分)分析处理图表中的信息是学习化学的一种重要方法。下表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答下列问题。
温度/℃ 10 20 30 40
溶解度/g 氯化钠 35.8 36.0 36.3 36.6
碳酸钠 12.2 21.8 39.7 53.2
(1)40 ℃时,氯化钠的溶解度为 g。
(2)碳酸钠的溶解度随温度的升高而 (填“增大”或“减小”)。20 ℃时,将30 g碳酸钠加入100 g水中,充分搅拌后得到的是碳酸钠的 (填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30 ℃,所得溶液的溶质质量分数为 (结果精确到0.1%)。
(3)10 ℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的是 溶液。
14.(6分)如图是A、B、C三种物质的溶解度曲线,请回答下列问题。
(1)溶解度随温度升高而减小的物质是 ,要使该物质的不饱和溶液变为饱和溶液,可采取的一种方法是 。
(2)t2 ℃时,三种物质的溶解度由大到小的顺序是 。
(3)t3 ℃时,B的饱和溶液中溶质的质量分数 (填“大于”“小于”或“等于”)A的饱和溶液中溶质的质量分数。
(4)t3 ℃时,将50 g A加入50 g水中,充分溶解后所得溶液的质量是 g。
(5)将t2 ℃时的三种物质的饱和溶液降温至t1 ℃时,所得溶液的溶质质量分数的大小关系是 。
15.(6分)我国制碱工业的先驱——侯德榜成功地探索和改进了西方的制碱方法。下表为侯氏制碱法中部分物质的溶解度。
温度/℃ 10 20 30 40
溶解度/g Na2CO3 12.2 21.8 39.7 48.8
NaCl 35.8 36.0 36.3 36.6
NaHCO3 8.2 9.6 11.1 12.7
(1)在30 ℃时,Na2CO3的溶解度 (填“>”“<”或“=”)NaHCO3的溶解度。
(2)由上表可知,在10~40 ℃之间溶解度随温度变化最小的物质是 (填物质名称,下同),三种物质最不易溶于水的是 。
(3)20 ℃时,将15 g氯化钠固体溶解在50 g水中,所得溶液为 (填“饱和溶液”或“不饱和溶液” ),所得溶液中溶质的质量分数为 ( 结果精确到0.1% )。
(4)40 ℃时,将等质量的三种表中物质的饱和溶液降温至20 ℃,所得溶液中溶质的质量分数由大到小的顺序是 ( 用化学式表示 )。
16.(6分)为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验(提示:本实验所用汽油与KMnO4、碘均不发生化学反应)。
【实验1】KMnO4晶体在不同溶剂中的溶解实验,根据实验步骤、实验操作图示填写相关实验现象。
实验步骤 实验操作图示 实验操作及现象
步骤1 向A、B两试管中分别加入5 mL水和5 mL无色汽油,振荡后静置;(1)A试管中晶体全部溶解,溶液呈 色;B试管中晶体不溶解,汽油不变色
步骤2 将步骤1中A试管内溶液倒入B试管中,振荡后静置;(2)B试管中观察到的现象为
【实验2】碘在不同溶剂中的溶解实验,根据实验操作图示回答相关问题。
实验操作图示 实验结论或解释
(3)由图2所示现象可知:碘 (填“不”“微”或“易”)溶于水 (4)图3所示试管中液体分层。上层紫红色溶液的名称是 ;说明碘在汽油中的溶解性比在水中 (填“强”或“弱”)
【实验结论】根据上述实验可得出的结论是 (写出一条即可) 。
[注意:若答对下列小题奖励3分,化学试卷总分不超过40分。]
【反思与应用】(5)①碘易溶于酒精。若【实验2】中用酒精代替汽油,振荡后静置,最终所得液体
(填“分层”或“不分层”)。
②“从稀碘水中提取碘”是“海带提碘”工艺中的一个重要步骤,其原理类似【实验2】中第二步操作。工业上实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是 。
17.(5分)某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表,制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到100 g氯化钾溶液。
加热时间/min 0 t1 t2 t3
固体的质量/g 28.0 23.2 18.4 18.4
(1)共制得氧气 g;
(2)计算所得氯化钾溶液的溶质质量分数。
参 考 答 案
1. D 2. B 3. D 4. A 5. B 6. D 7. C 8. B 9. C 10. D 11. D 12. C
13.(1)36.6 (2)增大 饱和溶液 23.1% (3)碳酸钠
14.(1)C 升高温度(或加入溶质,合理即可) (2)A=B>C (3)小于 (4)90 (5)B>A>C
15.(1)> (2)氯化钠 碳酸氢钠 (3)不饱和溶液 23.1% (4)NaCl>Na2CO3>NaHCO3
16.(1)紫红 (2)试管中晶体溶解,液体分层 (3)微 (4)碘的汽油溶液 强 不同溶质在同种溶剂中的溶解性不同(或同种溶质在不同溶剂中的溶解性不同) (5)①不分层 ②不溶于水,碘在这种液体里的溶解度远大于在水中的溶解度
17.解:(1)9.6
(2)设生成氯化钾的质量为x。
2KC1O32KC1+3O2 ↑
149 96
x 9.6g
= x=14.9 g
×100%= 14.9%
答:所得氯化钾溶液的溶质质量分数为14. 9%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
