专题八 金属和金属材料检测题-2021-2022学年九年级化学仁爱版下册(word版有答案)
文档属性
| 名称 | 专题八 金属和金属材料检测题-2021-2022学年九年级化学仁爱版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 121.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-02 00:00:00 | ||
图片预览


文档简介
专题8《金属和金属材料》检测题
一、单选题
1.金属材料在生产、生活中使用很广泛。下列用途是利用了金属的导电性的是
A.铁制铁锅 B.金制项链 C.铜制导线 D.铝制易拉罐
2.铁生锈是生活中常见现象如图可探究铁生锈与水有关的是
A.①③ B.①② C.②③ D.②
3.下列各物质的用途,主要与其物理性质相关的是
A.铜丝用做导线 B.液氯用于自来水消毒
C.镁粉用做照明弹 D.二氧化碳用于制作碳酸饮料
4.下列实验方案能达到实验目的的是
选项 实验目的 实验方案
A 鉴别氮气和二氧化碳 分别伸入燃着的木条
B 鉴别木炭粉和铁粉 观察颜色
C 除去铜粉中的氧化铜 在空气中灼烧
D 除去MgSO4溶液中的少量CuSO4 加入足量的镁粉,过滤
A.A B.B C.C D.D
5.向含有AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是
A.滤液中一定含AgNO3、Cu(NO3)2、Zn(NO3)2、Fe(NO3)2
B.滤液中一定含Fe(NO3)2,可能含Zn(NO3)2
C.滤液中一定含Fe(NO3)2、Zn(NO3)2,不含Cu(NO3)2、AgNO3
D.滤液中一定含Fe(NO3)2、Zn(NO3)2,可能含Cu(NO3)2
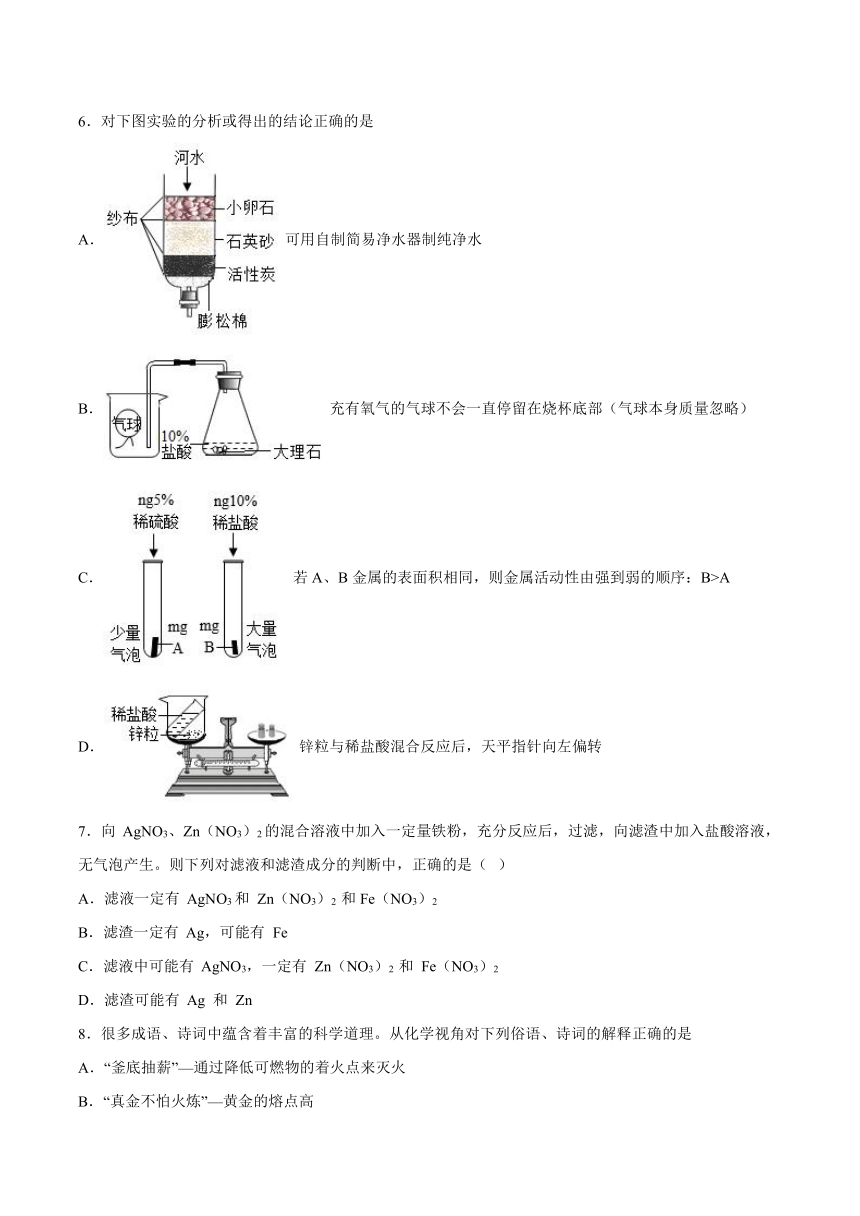
6.对下图实验的分析或得出的结论正确的是
A. 可用自制简易净水器制纯净水
B. 充有氧气的气球不会一直停留在烧杯底部(气球本身质量忽略)
C. 若A、B金属的表面积相同,则金属活动性由强到弱的顺序:B>A
D. 锌粒与稀盐酸混合反应后,天平指针向左偏转
7.向 AgNO3、Zn(NO3)2的混合溶液中加入一定量铁粉,充分反应后,过滤,向滤渣中加入盐酸溶液,无气泡产生。则下列对滤液和滤渣成分的判断中,正确的是( )
A.滤液一定有 AgNO3和 Zn(NO3)2 和Fe(NO3)2
B.滤渣一定有 Ag,可能有 Fe
C.滤液中可能有 AgNO3,一定有 Zn(NO3)2 和 Fe(NO3)2
D.滤渣可能有 Ag 和 Zn
8.很多成语、诗词中蕴含着丰富的科学道理。从化学视角对下列俗语、诗词的解释正确的是
A.“釜底抽薪”—通过降低可燃物的着火点来灭火
B.“真金不怕火炼”—黄金的熔点高
C.点石成金—化学反应改变了元素种类
D.“曾青得铁则化为铜”—用铁置换出铜
9.下列说法正确的是
A.化学变化都遵循质量守恒定律,所以质量不发生改变的变化一定是化学变化
B.铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀
C.相同的木炭在氧气中燃烧比在空气中剧烈,说明反应的剧烈程度与反应物浓度有关
D.化学变化伴随有能量变化,所以有能量变化的一定是化学变化
10.下列对有关实验现象的叙述或实验操作正确的是
A.铁丝在空气燃烧剧烈燃烧,火星四射。
B.镁条在空气中燃烧发出耀眼的白光。
C.将CO还原Fe2O3的尾气直接排入空气。
D.加热高锰酸钾制取氧气,并用排水法收集满氧气后,先撤酒精灯,后移出导管
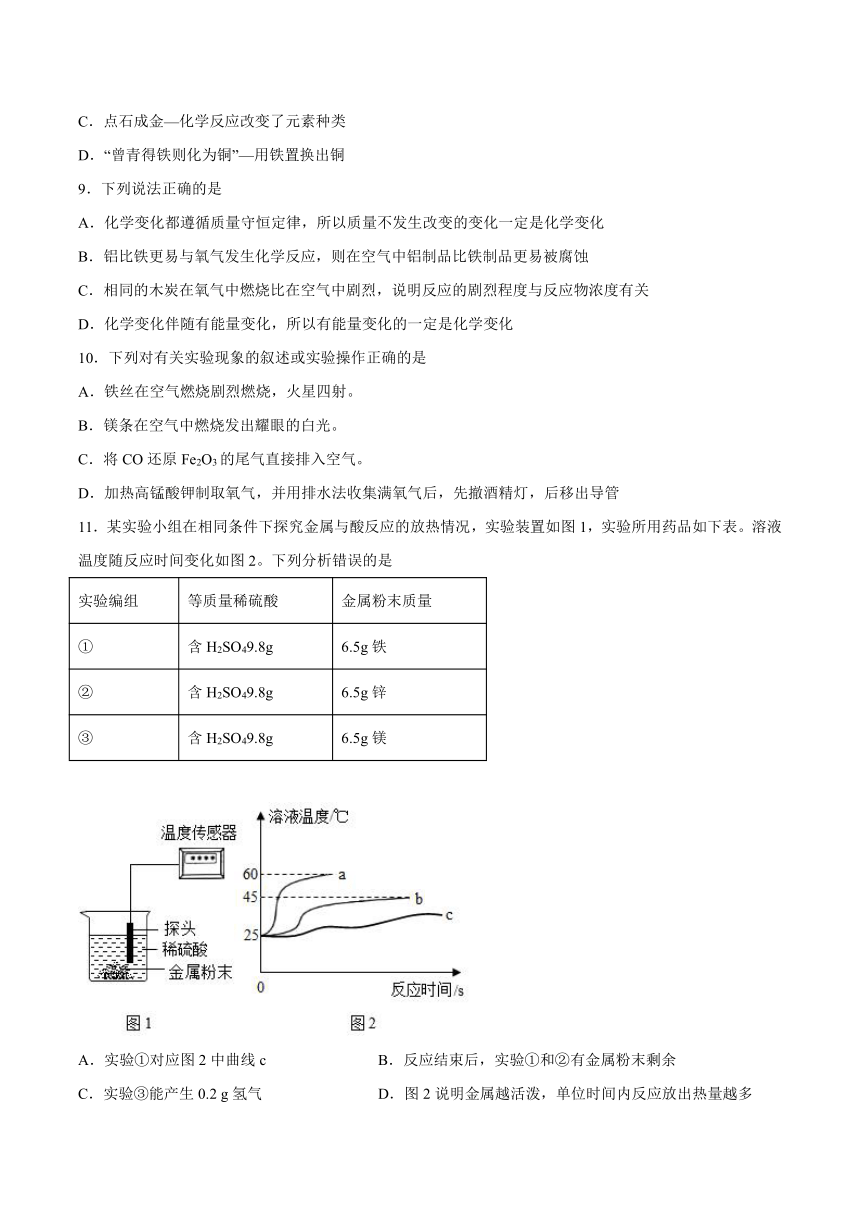
11.某实验小组在相同条件下探究金属与酸反应的放热情况,实验装置如图1,实验所用药品如下表。溶液温度随反应时间变化如图2。下列分析错误的是
实验编组 等质量稀硫酸 金属粉末质量
① 含H2SO49.8g 6.5g铁
② 含H2SO49.8g 6.5g锌
③ 含H2SO49.8g 6.5g镁
A.实验①对应图2中曲线c B.反应结束后,实验①和②有金属粉末剩余
C.实验③能产生0.2 g氢气 D.图2说明金属越活泼,单位时间内反应放出热量越多
12.下列物质的用途,主要利用其化学性质的是
A.金刚石用于裁玻璃 B.石墨用作电极 C.氮气用作保护气 D.铁用于制炊具
二、简答题
13.某硫酸试剂瓶标签上的部分文字说明如图所示。
(1)取10 mL该硫酸可配制成9.8%的硫酸_________g;
(2)取适量该硫酸与锌反应可生成SO4气体:Zn+2H2SO4(浓)=ZnSO4+SO2↑ +2H2O。反应一段时间后,还可能生成另一种气体,请解释原因________。
14.学用结合是我们学习化学知识的重要方法之一。请回答下列问题:
(1)用不同的布怎么擦被雨水淋湿的自行车,才能防止自行车的锈蚀?
(2)做实验时,不慎碰倒了酒精灯,酒精在桌面上燃烧起来。你应该采用什么样的简易灭火方法?
(3)将一杯盛有蔗糖溶液和剩余蔗糖固体的玻璃杯浸入热水盆中,并往盆中慢慢加入开水,边加边用筷子搅拌该蔗糖溶液和蔗糖固体。除了知道蔗糖溶于水之外,你还能得出的一条结论是什么?
三、推断题
15.A、B是初中化学常见的物质,两者间存在如图所示的转化关系:A B(“→”表示一步转化)
(1)A、B为不同类别的物质
若A是相对分子质量最小的单质,则B→A的化学方程式为______。
(2)A、B为同类别的物质,且均为氧化物
若A是有毒气体,A物质是由______(填“原子”、“分子”或“离子”)构成;A→B可用于铁的冶炼,则另一反应物可能是______(填化学式)。
16.已知A、B、C、D、E是初中化学中常见的五种物质其中A、D是黑色固体,B、C、E是无色气体,D中含有使用最广泛的金属元素,它们在一定条件下的转化关系如图所示(其他反应物和生成物已略去)。
请回答下列问题:
(1)C是______(填化学式)。
(2)写出E转化成D的化学方程式______。
(3)写出B在高温条件下还原D的化学方程式______。
(4)B与C组成元素相同,但化学性质不同的原因:______。
17.A~L是初中化学常见的物质,它们之间的转化关系如图所示(反应条件和部分物质已略去)。常温下,A、C是由相同元素组成的无色液体,且A具有杀菌消毒的作用:D、I、J均为无色气体,其中I能使澄清石灰水变浑浊;K为红棕色粉末。
(1)反应①中物质B的作用是___________。
(2)反应⑥的化学方程式为___________。
(3)反应⑦所属的基本反应类型为___________。
四、实验题
18.为探究铁制品锈蚀的条件,寻找防止铁制品锈蚀的方法,现进行如下实验:
步骤1:利用如图所示装置,将干燥的O2从导管a通入U形管(装置气密性良好);待U形管内充满O2后,将导管a、b处的止水夹k1、k2夹紧。
步骤2:一段时间后,观察U形管内三处铁丝表面的变化情况。
回答下列问题:
(1)步骤1中,检验U形管内已充满O2的方法是___________。
(2)步骤2中,观察到①处没有明显变化,说明铁制品锈蚀的条件之一是需要有___________(填化学式),②处可能观察到的现象是___________,③处没有明显变化,说明纯铁的抗腐蚀能力较___________(填“强”或“弱”)。
(3)待U形管内有明显现象后,将b导管插入水中,打开k2,观察到___________现象,说明该条件下铁制品锈蚀过程消耗了O2。
(4)通过上述实验现象,请你提出一种防止铁制品锈蚀的方法___________。
19.铁钉是生活中常见的铁制品。学习小组对不同条件下铁钉的锈蚀进行探究。取四枚铁钉,按图所示进行实验。一天后观察到的现象如下。
试管 a b c d
实验现象 铁钉表面无明显变化 铁钉表面无明显变化 蒸馏水和空气交界处铁钉出现轻微锈蚀 食盐水和空气交界处铁钉出现较多锈蚀
(1)由试管a、b、c中的现象可知铁钉锈蚀的条件是______。
(2)由试管c、d中的现象可以得出的结论是______。
(3)切过成菜的菜刀不及时处理,易生锈。防止切过取菜的菜刀生锈,处理的方法是______。
五、计算题
20.为测定某种钙片中碳酸钙的质量分数(假设钙片中其他物质不溶于水,也不与任何物质发生反应),某化学兴趣小组取20g钙片,研碎后加入到100g稀盐酸中恰好完全反应,反应后所得固液混合物共115.6g,请你帮忙计算:
(1)恰好完全反应时产生二氧化碳的质量为______g。
(2)计算该品牌钙片中碳酸钙的质量分数(写出计算过程)。
21.赤铁矿为工业炼铁的常用原料,其原理是将其中的Fe2O3转化为Fe。
(1)Fe2O3中铁元素和氧元素的质量比为___________。
(2)治炼1120t含杂质3%的生铁,需要含Fe2O380%的赤铁矿的质量是多少?(写出完整的计算步骤)
参考答案:
1.C 2.A 3.A 4.D 5.C 6.B 7.C 8.D 9.C 10.B 11.B 12.C
13.(1)184 g
(2)随着硫酸的消耗和水的生成,硫酸变稀,锌与稀硫酸反应能生成氢气
14.(1)先用干抹布擦干净水后用带油的抹布擦
(2)用湿抹布盖灭
(3)温度升高,蔗糖的溶解度会增大
15.(1)
(2) 分子 Fe2O3(合理答案均可)
16.(1)CO2
(2)
(3)
(4)分子构成不同
17.(1)催化作用
(2)
(3)置换反应
18.(1)将带火星的木条放在b导管的末端,若木条复燃,证明U形管内已充满O2
(2) H2O 铁丝生锈 强
(3)水进入导管
(4)保持铁制品干燥(合理即可)
19.(1)铁钉生锈需要与水和空气接触
(2)食盐可以加快铁钉锈蚀
(3)洗涤干净后擦干,放置在干燥处
20.(1)4.4
(2)解:设该品牌钙片中碳酸钙的质量分数为x
x=50%
答:该品牌钙片中碳酸钙的质量分数为50%
21.(1)7:3
(2)解:设需要含Fe2O380%的赤铁矿质量为x
x=1940t
答:需要含Fe2O380%的赤铁矿质量为1940t
一、单选题
1.金属材料在生产、生活中使用很广泛。下列用途是利用了金属的导电性的是
A.铁制铁锅 B.金制项链 C.铜制导线 D.铝制易拉罐
2.铁生锈是生活中常见现象如图可探究铁生锈与水有关的是
A.①③ B.①② C.②③ D.②
3.下列各物质的用途,主要与其物理性质相关的是
A.铜丝用做导线 B.液氯用于自来水消毒
C.镁粉用做照明弹 D.二氧化碳用于制作碳酸饮料
4.下列实验方案能达到实验目的的是
选项 实验目的 实验方案
A 鉴别氮气和二氧化碳 分别伸入燃着的木条
B 鉴别木炭粉和铁粉 观察颜色
C 除去铜粉中的氧化铜 在空气中灼烧
D 除去MgSO4溶液中的少量CuSO4 加入足量的镁粉,过滤
A.A B.B C.C D.D
5.向含有AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是
A.滤液中一定含AgNO3、Cu(NO3)2、Zn(NO3)2、Fe(NO3)2
B.滤液中一定含Fe(NO3)2,可能含Zn(NO3)2
C.滤液中一定含Fe(NO3)2、Zn(NO3)2,不含Cu(NO3)2、AgNO3
D.滤液中一定含Fe(NO3)2、Zn(NO3)2,可能含Cu(NO3)2
6.对下图实验的分析或得出的结论正确的是
A. 可用自制简易净水器制纯净水
B. 充有氧气的气球不会一直停留在烧杯底部(气球本身质量忽略)
C. 若A、B金属的表面积相同,则金属活动性由强到弱的顺序:B>A
D. 锌粒与稀盐酸混合反应后,天平指针向左偏转
7.向 AgNO3、Zn(NO3)2的混合溶液中加入一定量铁粉,充分反应后,过滤,向滤渣中加入盐酸溶液,无气泡产生。则下列对滤液和滤渣成分的判断中,正确的是( )
A.滤液一定有 AgNO3和 Zn(NO3)2 和Fe(NO3)2
B.滤渣一定有 Ag,可能有 Fe
C.滤液中可能有 AgNO3,一定有 Zn(NO3)2 和 Fe(NO3)2
D.滤渣可能有 Ag 和 Zn
8.很多成语、诗词中蕴含着丰富的科学道理。从化学视角对下列俗语、诗词的解释正确的是
A.“釜底抽薪”—通过降低可燃物的着火点来灭火
B.“真金不怕火炼”—黄金的熔点高
C.点石成金—化学反应改变了元素种类
D.“曾青得铁则化为铜”—用铁置换出铜
9.下列说法正确的是
A.化学变化都遵循质量守恒定律,所以质量不发生改变的变化一定是化学变化
B.铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀
C.相同的木炭在氧气中燃烧比在空气中剧烈,说明反应的剧烈程度与反应物浓度有关
D.化学变化伴随有能量变化,所以有能量变化的一定是化学变化
10.下列对有关实验现象的叙述或实验操作正确的是
A.铁丝在空气燃烧剧烈燃烧,火星四射。
B.镁条在空气中燃烧发出耀眼的白光。
C.将CO还原Fe2O3的尾气直接排入空气。
D.加热高锰酸钾制取氧气,并用排水法收集满氧气后,先撤酒精灯,后移出导管
11.某实验小组在相同条件下探究金属与酸反应的放热情况,实验装置如图1,实验所用药品如下表。溶液温度随反应时间变化如图2。下列分析错误的是
实验编组 等质量稀硫酸 金属粉末质量
① 含H2SO49.8g 6.5g铁
② 含H2SO49.8g 6.5g锌
③ 含H2SO49.8g 6.5g镁
A.实验①对应图2中曲线c B.反应结束后,实验①和②有金属粉末剩余
C.实验③能产生0.2 g氢气 D.图2说明金属越活泼,单位时间内反应放出热量越多
12.下列物质的用途,主要利用其化学性质的是
A.金刚石用于裁玻璃 B.石墨用作电极 C.氮气用作保护气 D.铁用于制炊具
二、简答题
13.某硫酸试剂瓶标签上的部分文字说明如图所示。
(1)取10 mL该硫酸可配制成9.8%的硫酸_________g;
(2)取适量该硫酸与锌反应可生成SO4气体:Zn+2H2SO4(浓)=ZnSO4+SO2↑ +2H2O。反应一段时间后,还可能生成另一种气体,请解释原因________。
14.学用结合是我们学习化学知识的重要方法之一。请回答下列问题:
(1)用不同的布怎么擦被雨水淋湿的自行车,才能防止自行车的锈蚀?
(2)做实验时,不慎碰倒了酒精灯,酒精在桌面上燃烧起来。你应该采用什么样的简易灭火方法?
(3)将一杯盛有蔗糖溶液和剩余蔗糖固体的玻璃杯浸入热水盆中,并往盆中慢慢加入开水,边加边用筷子搅拌该蔗糖溶液和蔗糖固体。除了知道蔗糖溶于水之外,你还能得出的一条结论是什么?
三、推断题
15.A、B是初中化学常见的物质,两者间存在如图所示的转化关系:A B(“→”表示一步转化)
(1)A、B为不同类别的物质
若A是相对分子质量最小的单质,则B→A的化学方程式为______。
(2)A、B为同类别的物质,且均为氧化物
若A是有毒气体,A物质是由______(填“原子”、“分子”或“离子”)构成;A→B可用于铁的冶炼,则另一反应物可能是______(填化学式)。
16.已知A、B、C、D、E是初中化学中常见的五种物质其中A、D是黑色固体,B、C、E是无色气体,D中含有使用最广泛的金属元素,它们在一定条件下的转化关系如图所示(其他反应物和生成物已略去)。
请回答下列问题:
(1)C是______(填化学式)。
(2)写出E转化成D的化学方程式______。
(3)写出B在高温条件下还原D的化学方程式______。
(4)B与C组成元素相同,但化学性质不同的原因:______。
17.A~L是初中化学常见的物质,它们之间的转化关系如图所示(反应条件和部分物质已略去)。常温下,A、C是由相同元素组成的无色液体,且A具有杀菌消毒的作用:D、I、J均为无色气体,其中I能使澄清石灰水变浑浊;K为红棕色粉末。
(1)反应①中物质B的作用是___________。
(2)反应⑥的化学方程式为___________。
(3)反应⑦所属的基本反应类型为___________。
四、实验题
18.为探究铁制品锈蚀的条件,寻找防止铁制品锈蚀的方法,现进行如下实验:
步骤1:利用如图所示装置,将干燥的O2从导管a通入U形管(装置气密性良好);待U形管内充满O2后,将导管a、b处的止水夹k1、k2夹紧。
步骤2:一段时间后,观察U形管内三处铁丝表面的变化情况。
回答下列问题:
(1)步骤1中,检验U形管内已充满O2的方法是___________。
(2)步骤2中,观察到①处没有明显变化,说明铁制品锈蚀的条件之一是需要有___________(填化学式),②处可能观察到的现象是___________,③处没有明显变化,说明纯铁的抗腐蚀能力较___________(填“强”或“弱”)。
(3)待U形管内有明显现象后,将b导管插入水中,打开k2,观察到___________现象,说明该条件下铁制品锈蚀过程消耗了O2。
(4)通过上述实验现象,请你提出一种防止铁制品锈蚀的方法___________。
19.铁钉是生活中常见的铁制品。学习小组对不同条件下铁钉的锈蚀进行探究。取四枚铁钉,按图所示进行实验。一天后观察到的现象如下。
试管 a b c d
实验现象 铁钉表面无明显变化 铁钉表面无明显变化 蒸馏水和空气交界处铁钉出现轻微锈蚀 食盐水和空气交界处铁钉出现较多锈蚀
(1)由试管a、b、c中的现象可知铁钉锈蚀的条件是______。
(2)由试管c、d中的现象可以得出的结论是______。
(3)切过成菜的菜刀不及时处理,易生锈。防止切过取菜的菜刀生锈,处理的方法是______。
五、计算题
20.为测定某种钙片中碳酸钙的质量分数(假设钙片中其他物质不溶于水,也不与任何物质发生反应),某化学兴趣小组取20g钙片,研碎后加入到100g稀盐酸中恰好完全反应,反应后所得固液混合物共115.6g,请你帮忙计算:
(1)恰好完全反应时产生二氧化碳的质量为______g。
(2)计算该品牌钙片中碳酸钙的质量分数(写出计算过程)。
21.赤铁矿为工业炼铁的常用原料,其原理是将其中的Fe2O3转化为Fe。
(1)Fe2O3中铁元素和氧元素的质量比为___________。
(2)治炼1120t含杂质3%的生铁,需要含Fe2O380%的赤铁矿的质量是多少?(写出完整的计算步骤)
参考答案:
1.C 2.A 3.A 4.D 5.C 6.B 7.C 8.D 9.C 10.B 11.B 12.C
13.(1)184 g
(2)随着硫酸的消耗和水的生成,硫酸变稀,锌与稀硫酸反应能生成氢气
14.(1)先用干抹布擦干净水后用带油的抹布擦
(2)用湿抹布盖灭
(3)温度升高,蔗糖的溶解度会增大
15.(1)
(2) 分子 Fe2O3(合理答案均可)
16.(1)CO2
(2)
(3)
(4)分子构成不同
17.(1)催化作用
(2)
(3)置换反应
18.(1)将带火星的木条放在b导管的末端,若木条复燃,证明U形管内已充满O2
(2) H2O 铁丝生锈 强
(3)水进入导管
(4)保持铁制品干燥(合理即可)
19.(1)铁钉生锈需要与水和空气接触
(2)食盐可以加快铁钉锈蚀
(3)洗涤干净后擦干,放置在干燥处
20.(1)4.4
(2)解:设该品牌钙片中碳酸钙的质量分数为x
x=50%
答:该品牌钙片中碳酸钙的质量分数为50%
21.(1)7:3
(2)解:设需要含Fe2O380%的赤铁矿质量为x
x=1940t
答:需要含Fe2O380%的赤铁矿质量为1940t
