第10章金属检测题-2021-2022学年九年级化学京改版下册(word版 含答案)
文档属性
| 名称 | 第10章金属检测题-2021-2022学年九年级化学京改版下册(word版 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 247.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-03 00:00:00 | ||
图片预览




文档简介
第10章《金属》检测题
一、单选题
1.以下分类正确的是
A.合金:青铜 B.溶液;蒸馏水 C.氧化物:酒精 D.混合物:铁水
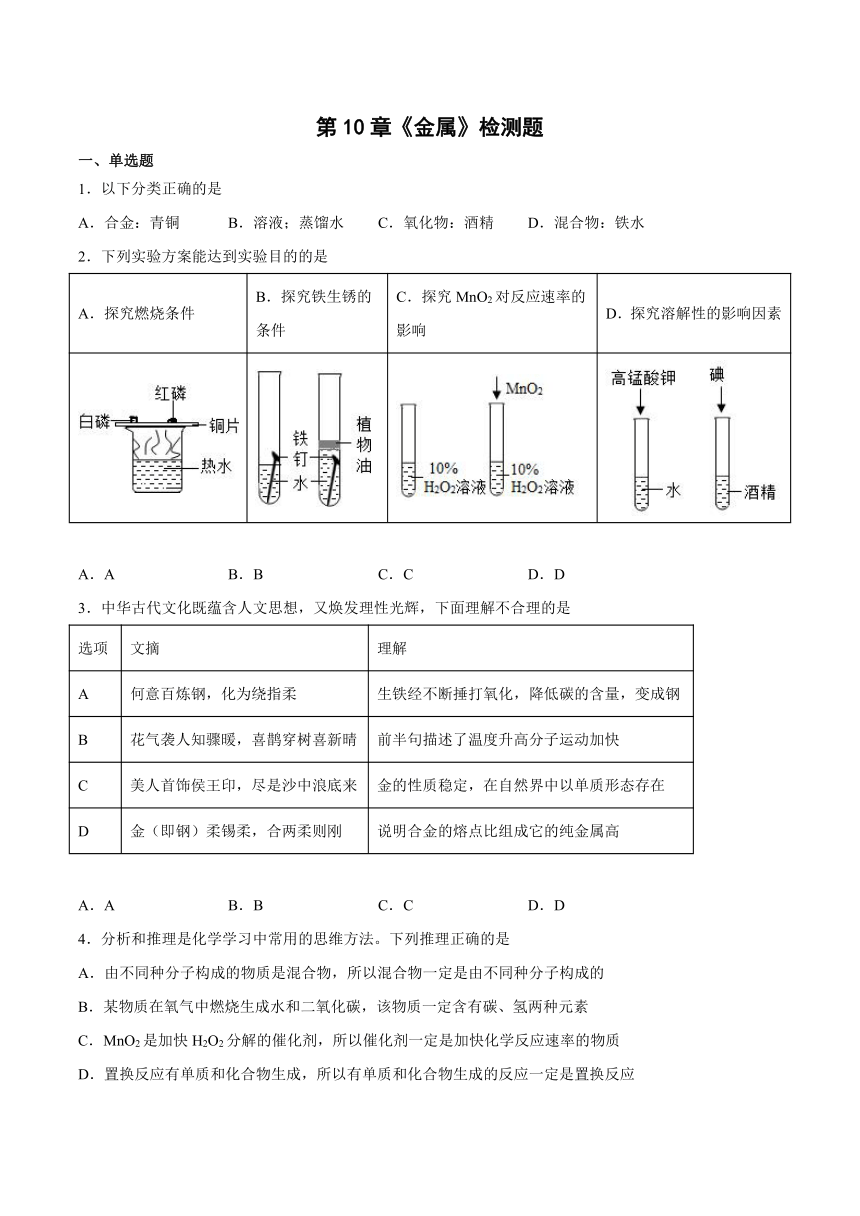
2.下列实验方案能达到实验目的的是
A.探究燃烧条件 B.探究铁生锈的条件 C.探究MnO2对反应速率的影响 D.探究溶解性的影响因素
A.A B.B C.C D.D
3.中华古代文化既蕴含人文思想,又焕发理性光辉,下面理解不合理的是
选项 文摘 理解
A 何意百炼钢,化为绕指柔 生铁经不断捶打氧化,降低碳的含量,变成钢
B 花气袭人知骤暖,喜鹊穿树喜新晴 前半句描述了温度升高分子运动加快
C 美人首饰侯王印,尽是沙中浪底来 金的性质稳定,在自然界中以单质形态存在
D 金(即钢)柔锡柔,合两柔则刚 说明合金的熔点比组成它的纯金属高
A.A B.B C.C D.D
4.分析和推理是化学学习中常用的思维方法。下列推理正确的是
A.由不同种分子构成的物质是混合物,所以混合物一定是由不同种分子构成的
B.某物质在氧气中燃烧生成水和二氧化碳,该物质一定含有碳、氢两种元素
C.MnO2是加快H2O2分解的催化剂,所以催化剂一定是加快化学反应速率的物质
D.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
5.下列图像能正确反映对应变化关系的是
A. ①用碳还原一定质量的氧化铜粉末
B. ②用两份等质量、等浓度的过氧化氢溶液分别制取氧气
C. ③表示向足量的稀硫酸中,分别加入等质量的镁粉和铝粉
D. ④将水通电一段时间,生成气体的体积随时间的变化
6.下列各组物质的分类正确的是
A.混合物:可燃冰、稀有气体 B.氧化物:冰水、氯酸钾
C.化合物:生石灰、C60 D.金属单质:钢、水银
7.碳和碳的化合物是一个庞大的家族,下列关于碳及其化合物的说法正确的是
A.金刚石、石墨、C60都是由碳原子构成的单质
B.CO2可以使含有紫色石蕊的干燥纸花变红
C.工业炼铁中焦炭只起提供热量的作用,炼得的生铁与钢的含碳量不同
D.CO有毒而CO2无毒,是因为它们的分子构成不同
8.下列实验方案能达到实验目的的是
实验目的 实验方案
A 证明二氧化碳能与水反应 将二氧化碳通入装有水的烧杯中
B 验证质量守恒定律 50g水和50g酒精混合后为100g
C 鉴别黄金和黄铜(铜锌合金) 取样,分别于空气中灼烧
D 持续增加大棚内二氧化碳的量 将块状大理石与稀硫酸反应
A.A B.B C.C D.D
9.下列物质的用途中,主要利用了其物理性质的是
A.石墨用于制铅笔芯 B.氮气用作食品保护气
C.氧气用于急救病人 D.焦炭用于冶炼金属
10.北斗系统的全面建成彰显了中国航天的力量。在航天科技中运用了大量金属材料,下列有关金属材料的说法正确的是
A.纯金属的熔点一般比它们组成合金的熔点更低 B.金属单质在常温下都是固体
C.金属变成合金后,内部的组成和结构发生变化 D.合金中一定只含金属元素
11.金属材料在生产、生活中使用很广泛。下列用途是利用了金属的导电性的是
A.铁制铁锅 B.金制项链 C.铜制导线 D.铝制易拉罐
12.现对Ag、Fe、Cu三种金属的活动性顺序进行探究,下列所选试剂可行的是
A.Cu、Ag、FeSO4溶液 B.Fe、Ag、CuSO4溶液
C.Fe、Cu、AgNO3溶液 D.Fe、AgNO3溶液、Cu(NO3)2溶液
13.在工业制硝酸时,可发生反应:。下列对该反应的理解正确的是
A.该反应属于置换反应 B.氮元素的化合价由+3价降低为+2价
C.反应物和生成物都是由分子构成的 D.参加反应的NH3与O2的质量比为17:32
二、简答题
14.实验过程中预期现象明显即是实验获得了成功。请你说出“铁钉锈蚀条件的探究”这个实验预期现象是什么?为了保证实验成功,在此实验中应注意哪些(答出两点)?
三、推断题
15.A~I是初中化学常见的物质,其中A是天然气的主要成分,在空气中不完全燃烧生成B、C、D三种物质,G是红色固体单质,H为红棕色粉末,它们之间存在如图所示的关系。
请回答下列问题:
(1)A物质的一种用途是_________,E的化学式为___________。
(2)在化学变化中,有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂。D和H发生的反应中,___________是氧化剂。
(3)I生成G的反应化学方程式____________。
16.A~H是初中化学常见的物质,其中A、C、E为无色气体,D的固体可用于人工降雨,F为红色金属,G、H为黑色固体。它们的转化关系如图所示(部分反应物、生成物和反应条件已略去),请回答。
(1)B的化学式是____________。
(2)D→E的转化是__________(填“吸热”或“放热”)反应。
(3)C→B的转化,一定是化合反应,该说法____________(填“正确”或“错误”)。
(4)E→F的化学方程式为____________,该反应在工业上的应用为____________。
17.物质间的转化关系图所示(注:图中各路线均为一步完成的化学反应)。
回答下列问题:
(1)A B C三种物质同属于氧化物,B是二氧化碳。若变化Ⅰ属于化合反应,变化Ⅱ的化学方程式为:______。
(2)A B C三种物质同属于单质,B是氢气写出变化Ⅱ的化学方程式:______,其基本反应类型属于______。
四、实验题
18.纳米铁(单质铁)在环保领域应用广泛。以菱铁矿(主要成分为FeCO3,不考虑杂质)为原料可以制备纳米铁。学习小组对制备得到的某固体成分进行探究。
【提出问题】固体成分是什么?
【做出猜想】
(1)固体成分:猜想一:Fe;猜想二:FeCO3;猜想三:_________。
【查阅资料】①FeCO3+ H2SO4=FeSO4 + H2O + CO2 ↑
②氢气具有还原性,可以用来冶炼金属 ③白色的无水硫酸铜固体遇到水蒸气变为蓝色
【实验探究】该学习小组利用下图装置,对固体成分进行探究。
(2)菱铁矿主要成分为碳酸亚铁,化学式为FeCO3,标出碳酸亚铁中碳元素的化合价_________。
(3)向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,小芳同学判断猜想一正确,小刚同学认为小芳的判断不合理,理由是:_________。
(4)装置B中溶液变浑浊,发生反应的方程式为_________。
(5)观察到装置D中固体由黑色变为红色,E中固体变蓝,D中反应的化学方程式为_________,据此判定固体中一定含_________。
【实验结论】
(6)猜想_________正确。
19.下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。
(1)先通CO后加热的原因是________;
(2)C装置中可观察到的现象是_________;
(3)B中反应的化学方程式________;
(4)从环保角度考虑,请写出一种尾气处理方法_______。
五、计算题
20.工业上,把铁矿石和石灰石等物质一起加入高炉,通入热空气,经过一系列反应最终可得到生铁。
(1)炼铁的原料除了铁矿石和石灰石外,还需要的一种物质是___________。
(2)工业上计划生产含杂质4%的生铁350t,则需含氧化铁80%的赤铁矿原料的质量是多少?
21.小阳同学想测定粗锌中锌的含量。她在实验室里用10g粗锌与足量稀硫酸反应,制得氢气0.2g(粗锌所含的杂质不与稀硫酸反应)。
(1)该反应属于_____________(填基本反应类型)。
(2)计算粗锌中锌的质量分数。
参考答案:
1.A 2.C 3.D 4.B 5.C 6.A 7.D 8.C 9.A 10.C 11.C 12.B 13.C
14.实验预期现象为:试管A中铁钉生锈,试管B、C中铁钉不生锈;
实验应该注意的问题有:①要用煮沸并迅速冷却的蒸馏水;②实验前一定要把铁钉表面的铁锈除去;③C装置一定要密封等。
15.(1) 作燃料 H2
(2)氧化铁
(3)
16.(1)H2O
(2)吸热
(3)错误
(4) 冶炼金属(或炼铜)
17.(1)
(2)
置换反应
18.(1)Fe、FeCO3
(2)
(3)碳酸亚铁和稀硫酸反应A中也能产生气泡且溶液变为浅绿色
(4)
(5) 铁##Fe
(6)三
19.(1)排尽装置内的空气
(2)澄清石灰水变浑浊
(3)
(4)在装置末尾放一燃着的酒精灯点燃尾气一氧化碳。
20.(1)焦炭
(2)设至少需含氧化铁80%的赤铁矿的质量为x
解得:x=600t
答:需储备含氧化铁80%的赤铁矿原料至少不低于600t。
21.(1)置换反应
(2)解:设粗锌中锌的质量为.
粗锌中锌的质量分数为:.
答:粗锌中锌的质量分数为65%。
一、单选题
1.以下分类正确的是
A.合金:青铜 B.溶液;蒸馏水 C.氧化物:酒精 D.混合物:铁水
2.下列实验方案能达到实验目的的是
A.探究燃烧条件 B.探究铁生锈的条件 C.探究MnO2对反应速率的影响 D.探究溶解性的影响因素
A.A B.B C.C D.D
3.中华古代文化既蕴含人文思想,又焕发理性光辉,下面理解不合理的是
选项 文摘 理解
A 何意百炼钢,化为绕指柔 生铁经不断捶打氧化,降低碳的含量,变成钢
B 花气袭人知骤暖,喜鹊穿树喜新晴 前半句描述了温度升高分子运动加快
C 美人首饰侯王印,尽是沙中浪底来 金的性质稳定,在自然界中以单质形态存在
D 金(即钢)柔锡柔,合两柔则刚 说明合金的熔点比组成它的纯金属高
A.A B.B C.C D.D
4.分析和推理是化学学习中常用的思维方法。下列推理正确的是
A.由不同种分子构成的物质是混合物,所以混合物一定是由不同种分子构成的
B.某物质在氧气中燃烧生成水和二氧化碳,该物质一定含有碳、氢两种元素
C.MnO2是加快H2O2分解的催化剂,所以催化剂一定是加快化学反应速率的物质
D.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
5.下列图像能正确反映对应变化关系的是
A. ①用碳还原一定质量的氧化铜粉末
B. ②用两份等质量、等浓度的过氧化氢溶液分别制取氧气
C. ③表示向足量的稀硫酸中,分别加入等质量的镁粉和铝粉
D. ④将水通电一段时间,生成气体的体积随时间的变化
6.下列各组物质的分类正确的是
A.混合物:可燃冰、稀有气体 B.氧化物:冰水、氯酸钾
C.化合物:生石灰、C60 D.金属单质:钢、水银
7.碳和碳的化合物是一个庞大的家族,下列关于碳及其化合物的说法正确的是
A.金刚石、石墨、C60都是由碳原子构成的单质
B.CO2可以使含有紫色石蕊的干燥纸花变红
C.工业炼铁中焦炭只起提供热量的作用,炼得的生铁与钢的含碳量不同
D.CO有毒而CO2无毒,是因为它们的分子构成不同
8.下列实验方案能达到实验目的的是
实验目的 实验方案
A 证明二氧化碳能与水反应 将二氧化碳通入装有水的烧杯中
B 验证质量守恒定律 50g水和50g酒精混合后为100g
C 鉴别黄金和黄铜(铜锌合金) 取样,分别于空气中灼烧
D 持续增加大棚内二氧化碳的量 将块状大理石与稀硫酸反应
A.A B.B C.C D.D
9.下列物质的用途中,主要利用了其物理性质的是
A.石墨用于制铅笔芯 B.氮气用作食品保护气
C.氧气用于急救病人 D.焦炭用于冶炼金属
10.北斗系统的全面建成彰显了中国航天的力量。在航天科技中运用了大量金属材料,下列有关金属材料的说法正确的是
A.纯金属的熔点一般比它们组成合金的熔点更低 B.金属单质在常温下都是固体
C.金属变成合金后,内部的组成和结构发生变化 D.合金中一定只含金属元素
11.金属材料在生产、生活中使用很广泛。下列用途是利用了金属的导电性的是
A.铁制铁锅 B.金制项链 C.铜制导线 D.铝制易拉罐
12.现对Ag、Fe、Cu三种金属的活动性顺序进行探究,下列所选试剂可行的是
A.Cu、Ag、FeSO4溶液 B.Fe、Ag、CuSO4溶液
C.Fe、Cu、AgNO3溶液 D.Fe、AgNO3溶液、Cu(NO3)2溶液
13.在工业制硝酸时,可发生反应:。下列对该反应的理解正确的是
A.该反应属于置换反应 B.氮元素的化合价由+3价降低为+2价
C.反应物和生成物都是由分子构成的 D.参加反应的NH3与O2的质量比为17:32
二、简答题
14.实验过程中预期现象明显即是实验获得了成功。请你说出“铁钉锈蚀条件的探究”这个实验预期现象是什么?为了保证实验成功,在此实验中应注意哪些(答出两点)?
三、推断题
15.A~I是初中化学常见的物质,其中A是天然气的主要成分,在空气中不完全燃烧生成B、C、D三种物质,G是红色固体单质,H为红棕色粉末,它们之间存在如图所示的关系。
请回答下列问题:
(1)A物质的一种用途是_________,E的化学式为___________。
(2)在化学变化中,有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂。D和H发生的反应中,___________是氧化剂。
(3)I生成G的反应化学方程式____________。
16.A~H是初中化学常见的物质,其中A、C、E为无色气体,D的固体可用于人工降雨,F为红色金属,G、H为黑色固体。它们的转化关系如图所示(部分反应物、生成物和反应条件已略去),请回答。
(1)B的化学式是____________。
(2)D→E的转化是__________(填“吸热”或“放热”)反应。
(3)C→B的转化,一定是化合反应,该说法____________(填“正确”或“错误”)。
(4)E→F的化学方程式为____________,该反应在工业上的应用为____________。
17.物质间的转化关系图所示(注:图中各路线均为一步完成的化学反应)。
回答下列问题:
(1)A B C三种物质同属于氧化物,B是二氧化碳。若变化Ⅰ属于化合反应,变化Ⅱ的化学方程式为:______。
(2)A B C三种物质同属于单质,B是氢气写出变化Ⅱ的化学方程式:______,其基本反应类型属于______。
四、实验题
18.纳米铁(单质铁)在环保领域应用广泛。以菱铁矿(主要成分为FeCO3,不考虑杂质)为原料可以制备纳米铁。学习小组对制备得到的某固体成分进行探究。
【提出问题】固体成分是什么?
【做出猜想】
(1)固体成分:猜想一:Fe;猜想二:FeCO3;猜想三:_________。
【查阅资料】①FeCO3+ H2SO4=FeSO4 + H2O + CO2 ↑
②氢气具有还原性,可以用来冶炼金属 ③白色的无水硫酸铜固体遇到水蒸气变为蓝色
【实验探究】该学习小组利用下图装置,对固体成分进行探究。
(2)菱铁矿主要成分为碳酸亚铁,化学式为FeCO3,标出碳酸亚铁中碳元素的化合价_________。
(3)向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,小芳同学判断猜想一正确,小刚同学认为小芳的判断不合理,理由是:_________。
(4)装置B中溶液变浑浊,发生反应的方程式为_________。
(5)观察到装置D中固体由黑色变为红色,E中固体变蓝,D中反应的化学方程式为_________,据此判定固体中一定含_________。
【实验结论】
(6)猜想_________正确。
19.下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。
(1)先通CO后加热的原因是________;
(2)C装置中可观察到的现象是_________;
(3)B中反应的化学方程式________;
(4)从环保角度考虑,请写出一种尾气处理方法_______。
五、计算题
20.工业上,把铁矿石和石灰石等物质一起加入高炉,通入热空气,经过一系列反应最终可得到生铁。
(1)炼铁的原料除了铁矿石和石灰石外,还需要的一种物质是___________。
(2)工业上计划生产含杂质4%的生铁350t,则需含氧化铁80%的赤铁矿原料的质量是多少?
21.小阳同学想测定粗锌中锌的含量。她在实验室里用10g粗锌与足量稀硫酸反应,制得氢气0.2g(粗锌所含的杂质不与稀硫酸反应)。
(1)该反应属于_____________(填基本反应类型)。
(2)计算粗锌中锌的质量分数。
参考答案:
1.A 2.C 3.D 4.B 5.C 6.A 7.D 8.C 9.A 10.C 11.C 12.B 13.C
14.实验预期现象为:试管A中铁钉生锈,试管B、C中铁钉不生锈;
实验应该注意的问题有:①要用煮沸并迅速冷却的蒸馏水;②实验前一定要把铁钉表面的铁锈除去;③C装置一定要密封等。
15.(1) 作燃料 H2
(2)氧化铁
(3)
16.(1)H2O
(2)吸热
(3)错误
(4) 冶炼金属(或炼铜)
17.(1)
(2)
置换反应
18.(1)Fe、FeCO3
(2)
(3)碳酸亚铁和稀硫酸反应A中也能产生气泡且溶液变为浅绿色
(4)
(5) 铁##Fe
(6)三
19.(1)排尽装置内的空气
(2)澄清石灰水变浑浊
(3)
(4)在装置末尾放一燃着的酒精灯点燃尾气一氧化碳。
20.(1)焦炭
(2)设至少需含氧化铁80%的赤铁矿的质量为x
解得:x=600t
答:需储备含氧化铁80%的赤铁矿原料至少不低于600t。
21.(1)置换反应
(2)解:设粗锌中锌的质量为.
粗锌中锌的质量分数为:.
答:粗锌中锌的质量分数为65%。
