专题7初识酸、碱和盐检测题-2021-2022学年九年级化学仁爱版下册(word版 含答案)
文档属性
| 名称 | 专题7初识酸、碱和盐检测题-2021-2022学年九年级化学仁爱版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 120.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-03 00:00:00 | ||
图片预览



文档简介
专题7《初识酸、碱和盐》检测题
一、单选题
1.学习化学知识可以用来辨别“真”“伪”。下列叙述属于“真”的是
A.焙制面包时,加入适量小苏打使面包松软
B.氧气具有助燃性,常作火箭推进燃料
C.氢氧化钠具有碱性,可用于治疗胃酸过多
D.活性炭具有吸附性,可使硬水软化
2.类比推理是化学学习中常用的思维方法,下列推理正确的是
A.中和反应生成盐和水,生成盐和水的反应一定是中和反应
B.氧化物中含有氧元素,含氧元素的化合物一定是氧化物
C.酸溶液中都含有H+,则酸具有相似的化学性质
D.酸能使紫色石蕊试液变红色,CO2也能使石蕊试液变红色,所以CO2是酸
3.下列对实验现象和结论描述都正确的是
A.打开浓盐酸瓶口产生白烟,说明盐酸具有挥发性
B.二氧化碳通入紫色石蕊试液中,溶液变红,说明二氧化碳具有酸性
C.向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱性溶液
D.浓硫酸放入水中稀释放热,说明浓硫酸与水发生化学反应是放热反应
4.下列能在pH为1的溶液中大量共存,且溶液为无色透明的一组是
A.FeCl3、Na2SO4、NaCl
B.BaCl2、Na2CO3、NaOH
C.NaNO3、Na2CO3、KCl
D.K2SO4、NaNO3、NH4Cl
5.物质的性质决定其用途。下列有关物质用途的说法正确的是
A.液态氮气可用于冷藏血液
B.氧气可作为推进火箭上天的高能燃料
C.烧碱用于治疗胃酸过多
D.石灰石用于改良酸性土壤
6.下列有关物质的化学式、名称、俗名完全对应的是
A.NaOH、氢氧化钠、烧碱 B.NaCl、氯化钠、食盐
C.H2O2、过氧化氢、双氧水 D.CaO、氧化钙、熟石灰
7.化学反应涉及到的物质中,属于氧化物的是
A.Cu(OH)2 B.H2SO4 C.CuSO4 D.H2O
8.下列事实中,利用物质化学性质的是
A.稀有气体制成霓虹灯 B.盐酸除锈
C.铜作导线 D.铁铸成锅
9.化学就在我们身边,下列说法正确的是
A.空气是一种混合物,空气的成分按体积计算,氮气约占78%
B.二氧化碳极易与血红蛋白结合,造成生物体内缺氧
C.pH值小于7的降雨称为酸雨
D.溶液在生活中应用广泛,均一、稳定的液体都是溶液
10.物质存放在烧杯中一段时间后,质量变大且变质的是
①浓盐酸②浓硫酸③烧碱④生石灰⑤熟石灰
A.③④⑤ B.②③④⑤ C.①②③④⑤ D.④⑤
11.下列有关物质的性质和用途对应关系正确的是
A.氖气通电时能发出带颜色的光,可用于霓虹灯
B.液氮化学性质不活泼,可用作冷冻麻醉剂
C.石墨硬度很大,可用作石墨电极
D.CO2具有酸性,能使紫色石蕊溶液变红色
12.下列有关物质的检验、鉴别、分离、提纯所用的试剂或方法正确的是
选项 实验目的 所用试剂或方法
区别二氧化锰和氯化钾 是否溶于水
区别木炭和铁粉 观察颜色
区别二氧化碳和氮气 用燃着的木条
除去 溶于水
A.A B.B C.C D.D
二、简答题
13.用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示。
(1)熟石灰与盐酸反应的化学方程式为?
(2)当加入熟石灰mg时,溶液中的溶质为?
(3)若改用ng氢氧化钠与相同量盐酸反应,所得溶液的pH大小?
14.我们的家乡是座美丽的滨海小城,海洋蕴含着丰富的资源,以下是人们从海洋中获取某些物质的方法:
①膜法淡化海水获得淡水
②蒸馏法从海水中提取淡水
③向海水中添加石灰乳,再向得到的沉淀中加稀盐酸,然后电解获得的氯化镁制得镁
④开采出原油并进行分馏获得汽油、煤油等产品
⑤用贝壳(主要成分碳酸钙)制石灰乳
(1)请从物质变化的角度对上述方法进行分类:一类是___________(填写序号),另一类是___________(填写序号),你的分类依据是___________。
(2)和①膜法淡化海水原理相同的一个实验操作是________,原理都是依据__________不同将混合物中的各成分分离。
(3)在②蒸馏法淡化海水时水的三态变化过程与自然界中___________循环的原理类似。检验蒸馏法得到水是淡水的化学方法是___________。(用方程式表示)
(4)写出③中电解氯化镁的反应化学方程式___________。
(5)贝壳制得的生石灰可用来做干燥剂,日常生活中常见的干燥剂除了生石灰干燥剂外。还有一种硅胶干燥剂,硅胶吸附性能高、化学性质稳定,其内部为毛孔网状结构,能够吸收水分,并将水分保留住。根据提供的信息分析他们的干燥原理是否相同?___________,理由是____________________。
三、推断题
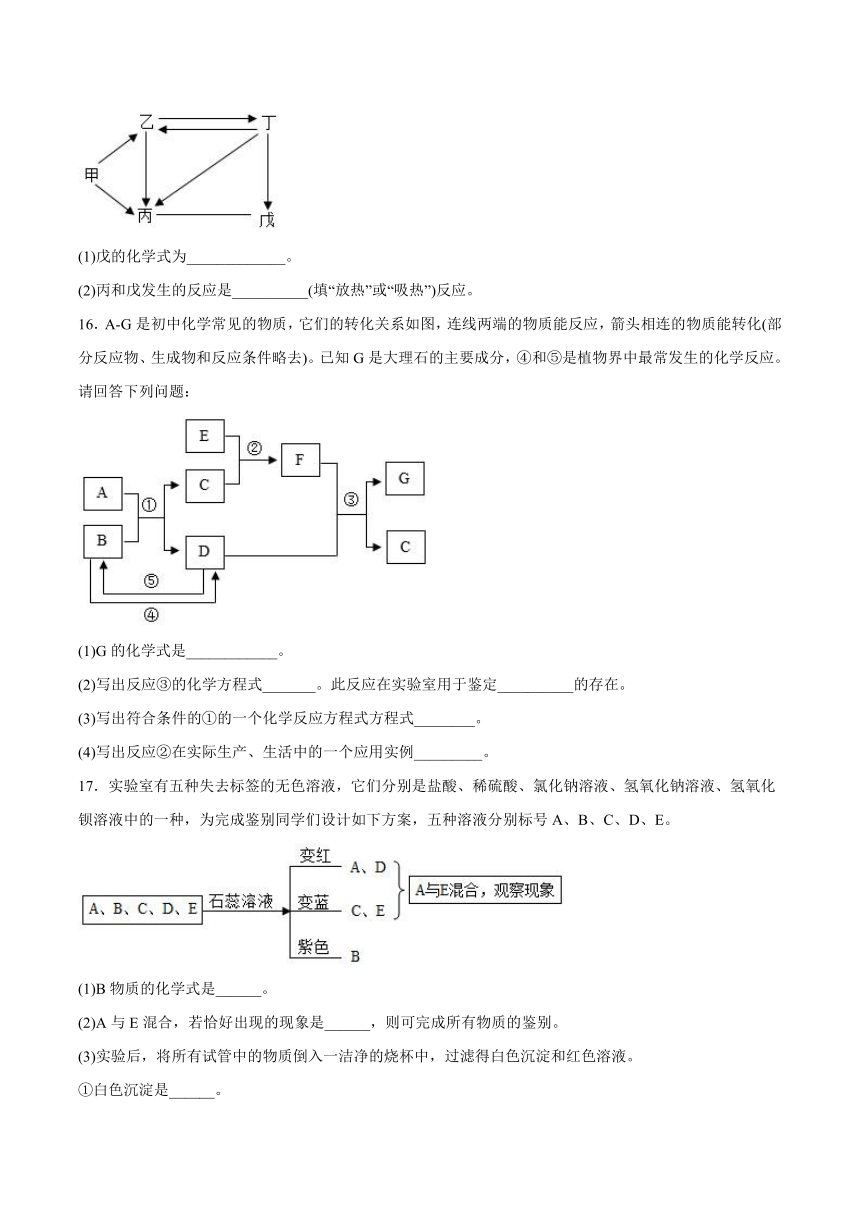
15.甲、乙、丙、丁、戊是初中化学常见的物质,其中甲是一种常见气体,丁是大理石的主要成分,乙的固体俗称干冰,它们之间部分转化关系如图所示。(“→“表示某种物质经一步反应可转化成另一种物质,“一”表示两种物质能发生化学反应)
(1)戊的化学式为_____________。
(2)丙和戊发生的反应是__________(填“放热”或“吸热”)反应。
16.A-G是初中化学常见的物质,它们的转化关系如图,连线两端的物质能反应,箭头相连的物质能转化(部分反应物、生成物和反应条件略去)。已知G是大理石的主要成分,④和⑤是植物界中最常发生的化学反应。请回答下列问题:
(1)G的化学式是____________。
(2)写出反应③的化学方程式_______。此反应在实验室用于鉴定__________的存在。
(3)写出符合条件的①的一个化学反应方程式方程式________。
(4)写出反应②在实际生产、生活中的一个应用实例_________。
17.实验室有五种失去标签的无色溶液,它们分别是盐酸、稀硫酸、氯化钠溶液、氢氧化钠溶液、氢氧化钡溶液中的一种,为完成鉴别同学们设计如下方案,五种溶液分别标号A、B、C、D、E。
(1)B物质的化学式是______。
(2)A与E混合,若恰好出现的现象是______,则可完成所有物质的鉴别。
(3)实验后,将所有试管中的物质倒入一洁净的烧杯中,过滤得白色沉淀和红色溶液。
①白色沉淀是______。
②向所得红色溶液中加入下列物质,可能会有实验现象的是______。
A.AgNO3溶液B.Na2SO4溶液C.Na2CO3溶液D.BaCl2溶液
四、实验题
18.探究学习小组在制作“叶脉书签”时,需要将树叶放在质量分数为10%的氢氧化钠溶液中煮沸。下图所示为该小组配制10%的氢氧化钠溶液的操作过程:
(1)图中仪器a的名称是___________,写出该仪器的另一种用途___________。
(2)操作B中,必须将氢氧化钠固体放在___________里。
(3)操作D中,用量筒量取所需体积的蒸馏水时还用到___________(填写仪器名称)。某同学在读取量筒读数时仰视,若其他操作正确,则所配制氢氧化钠溶液的质量分数___________(填“偏大”、“偏小”或“无影响”)。
(4)制作“叶脉书签“结束后,刘强同学想继续测定废液的酸碱度,下列用品不需要的是___________(填写字母标号)。
a、玻璃棒b、pH试纸c、酚酞试液d、白瓷板或玻璃片
19.请结合如图回答问题。
(1)仪器名称:①______,②______。
(2)实验室制取CO2的化学方程式为______。
(3)已知CaCl2的水溶液呈中性。用图1装置探究制取CO2的实验。实验开始时,向锥形瓶中加入一定量的盐酸图2表示实验过程中装置G和Ⅰ中的溶液pH变化曲线。
①装置H的作用为______。
②请判断t2时,锥形瓶中______(填“有”或“无”)盐酸剩余。
③t1后,显示器B中曲线几乎无变化,其原因是______。
五、计算题
20.某碳酸钠样品中含有少量氯化钠。为测定样品中碳酸钠的质量分数,现称取该样品6g,加入到盛有50g稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为53.8g。计算:
(1)反应后生成的二氧化碳的质量为______g。
(2)求此碳酸钠样品中碳酸钠的质量分数;
21.某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50.00g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如图所示。(结果保留两位小数)。
(1)当滴加Ba(OH)2溶液50g时烧杯内溶液的pH__________7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数_____。(结果保留0.01%)。
参考答案:
1.A 2.C 3.C 4.D 5.A 6.A 7.D 8.B 9.A 10.A 11.A 12.A
13.(1)Ca(OH)2+2HCl═CaCl2+2H2O
(2)CaCl2和HCl
(3)pH<7
14.(1) ①、②、④ ③和⑤ 是否发生化学变化
(2) 过滤 颗粒大小
(3) 水
(4)
(5) 不相同 生石灰干燥是化学变化,硅胶干燥剂干燥过程为物理变化
15.(1)CaO
(2)放热
16.(1)CaCO3
(2) CO2##二氧化碳
(3)或
(4)食品袋中的干燥剂(或自热饭的热源)
17.(1)NaCl
(2)生成白色沉淀
(3) BaSO4 BD
18.(1) 烧杯 作反应容器
(2)玻璃器皿
(3) 胶头滴管 偏小
(4)c
19.(1) 酒精灯 长颈漏斗
(2)
(3) 吸收氯化氢 有 溶液中二氧化碳已经达到饱和
20.(1)2.2
(2)设碳酸钠样品中碳酸钠的质量为x
此碳酸钠样品中碳酸钠的质量分数为。
答:此碳酸钠样品中碳酸钠的质量分数为88.3%。
21.(1)<
(2)3.92%
解:由图可知,加入100g氢氧化钡溶液两者恰好完全反应,设50g稀硫酸中含H2SO4的质量为x,
硫酸溶液的溶质质量分数为×100%=3.92%;
答:硫酸溶液的溶质质量分数3.92%。
一、单选题
1.学习化学知识可以用来辨别“真”“伪”。下列叙述属于“真”的是
A.焙制面包时,加入适量小苏打使面包松软
B.氧气具有助燃性,常作火箭推进燃料
C.氢氧化钠具有碱性,可用于治疗胃酸过多
D.活性炭具有吸附性,可使硬水软化
2.类比推理是化学学习中常用的思维方法,下列推理正确的是
A.中和反应生成盐和水,生成盐和水的反应一定是中和反应
B.氧化物中含有氧元素,含氧元素的化合物一定是氧化物
C.酸溶液中都含有H+,则酸具有相似的化学性质
D.酸能使紫色石蕊试液变红色,CO2也能使石蕊试液变红色,所以CO2是酸
3.下列对实验现象和结论描述都正确的是
A.打开浓盐酸瓶口产生白烟,说明盐酸具有挥发性
B.二氧化碳通入紫色石蕊试液中,溶液变红,说明二氧化碳具有酸性
C.向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱性溶液
D.浓硫酸放入水中稀释放热,说明浓硫酸与水发生化学反应是放热反应
4.下列能在pH为1的溶液中大量共存,且溶液为无色透明的一组是
A.FeCl3、Na2SO4、NaCl
B.BaCl2、Na2CO3、NaOH
C.NaNO3、Na2CO3、KCl
D.K2SO4、NaNO3、NH4Cl
5.物质的性质决定其用途。下列有关物质用途的说法正确的是
A.液态氮气可用于冷藏血液
B.氧气可作为推进火箭上天的高能燃料
C.烧碱用于治疗胃酸过多
D.石灰石用于改良酸性土壤
6.下列有关物质的化学式、名称、俗名完全对应的是
A.NaOH、氢氧化钠、烧碱 B.NaCl、氯化钠、食盐
C.H2O2、过氧化氢、双氧水 D.CaO、氧化钙、熟石灰
7.化学反应涉及到的物质中,属于氧化物的是
A.Cu(OH)2 B.H2SO4 C.CuSO4 D.H2O
8.下列事实中,利用物质化学性质的是
A.稀有气体制成霓虹灯 B.盐酸除锈
C.铜作导线 D.铁铸成锅
9.化学就在我们身边,下列说法正确的是
A.空气是一种混合物,空气的成分按体积计算,氮气约占78%
B.二氧化碳极易与血红蛋白结合,造成生物体内缺氧
C.pH值小于7的降雨称为酸雨
D.溶液在生活中应用广泛,均一、稳定的液体都是溶液
10.物质存放在烧杯中一段时间后,质量变大且变质的是
①浓盐酸②浓硫酸③烧碱④生石灰⑤熟石灰
A.③④⑤ B.②③④⑤ C.①②③④⑤ D.④⑤
11.下列有关物质的性质和用途对应关系正确的是
A.氖气通电时能发出带颜色的光,可用于霓虹灯
B.液氮化学性质不活泼,可用作冷冻麻醉剂
C.石墨硬度很大,可用作石墨电极
D.CO2具有酸性,能使紫色石蕊溶液变红色
12.下列有关物质的检验、鉴别、分离、提纯所用的试剂或方法正确的是
选项 实验目的 所用试剂或方法
区别二氧化锰和氯化钾 是否溶于水
区别木炭和铁粉 观察颜色
区别二氧化碳和氮气 用燃着的木条
除去 溶于水
A.A B.B C.C D.D
二、简答题
13.用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示。
(1)熟石灰与盐酸反应的化学方程式为?
(2)当加入熟石灰mg时,溶液中的溶质为?
(3)若改用ng氢氧化钠与相同量盐酸反应,所得溶液的pH大小?
14.我们的家乡是座美丽的滨海小城,海洋蕴含着丰富的资源,以下是人们从海洋中获取某些物质的方法:
①膜法淡化海水获得淡水
②蒸馏法从海水中提取淡水
③向海水中添加石灰乳,再向得到的沉淀中加稀盐酸,然后电解获得的氯化镁制得镁
④开采出原油并进行分馏获得汽油、煤油等产品
⑤用贝壳(主要成分碳酸钙)制石灰乳
(1)请从物质变化的角度对上述方法进行分类:一类是___________(填写序号),另一类是___________(填写序号),你的分类依据是___________。
(2)和①膜法淡化海水原理相同的一个实验操作是________,原理都是依据__________不同将混合物中的各成分分离。
(3)在②蒸馏法淡化海水时水的三态变化过程与自然界中___________循环的原理类似。检验蒸馏法得到水是淡水的化学方法是___________。(用方程式表示)
(4)写出③中电解氯化镁的反应化学方程式___________。
(5)贝壳制得的生石灰可用来做干燥剂,日常生活中常见的干燥剂除了生石灰干燥剂外。还有一种硅胶干燥剂,硅胶吸附性能高、化学性质稳定,其内部为毛孔网状结构,能够吸收水分,并将水分保留住。根据提供的信息分析他们的干燥原理是否相同?___________,理由是____________________。
三、推断题
15.甲、乙、丙、丁、戊是初中化学常见的物质,其中甲是一种常见气体,丁是大理石的主要成分,乙的固体俗称干冰,它们之间部分转化关系如图所示。(“→“表示某种物质经一步反应可转化成另一种物质,“一”表示两种物质能发生化学反应)
(1)戊的化学式为_____________。
(2)丙和戊发生的反应是__________(填“放热”或“吸热”)反应。
16.A-G是初中化学常见的物质,它们的转化关系如图,连线两端的物质能反应,箭头相连的物质能转化(部分反应物、生成物和反应条件略去)。已知G是大理石的主要成分,④和⑤是植物界中最常发生的化学反应。请回答下列问题:
(1)G的化学式是____________。
(2)写出反应③的化学方程式_______。此反应在实验室用于鉴定__________的存在。
(3)写出符合条件的①的一个化学反应方程式方程式________。
(4)写出反应②在实际生产、生活中的一个应用实例_________。
17.实验室有五种失去标签的无色溶液,它们分别是盐酸、稀硫酸、氯化钠溶液、氢氧化钠溶液、氢氧化钡溶液中的一种,为完成鉴别同学们设计如下方案,五种溶液分别标号A、B、C、D、E。
(1)B物质的化学式是______。
(2)A与E混合,若恰好出现的现象是______,则可完成所有物质的鉴别。
(3)实验后,将所有试管中的物质倒入一洁净的烧杯中,过滤得白色沉淀和红色溶液。
①白色沉淀是______。
②向所得红色溶液中加入下列物质,可能会有实验现象的是______。
A.AgNO3溶液B.Na2SO4溶液C.Na2CO3溶液D.BaCl2溶液
四、实验题
18.探究学习小组在制作“叶脉书签”时,需要将树叶放在质量分数为10%的氢氧化钠溶液中煮沸。下图所示为该小组配制10%的氢氧化钠溶液的操作过程:
(1)图中仪器a的名称是___________,写出该仪器的另一种用途___________。
(2)操作B中,必须将氢氧化钠固体放在___________里。
(3)操作D中,用量筒量取所需体积的蒸馏水时还用到___________(填写仪器名称)。某同学在读取量筒读数时仰视,若其他操作正确,则所配制氢氧化钠溶液的质量分数___________(填“偏大”、“偏小”或“无影响”)。
(4)制作“叶脉书签“结束后,刘强同学想继续测定废液的酸碱度,下列用品不需要的是___________(填写字母标号)。
a、玻璃棒b、pH试纸c、酚酞试液d、白瓷板或玻璃片
19.请结合如图回答问题。
(1)仪器名称:①______,②______。
(2)实验室制取CO2的化学方程式为______。
(3)已知CaCl2的水溶液呈中性。用图1装置探究制取CO2的实验。实验开始时,向锥形瓶中加入一定量的盐酸图2表示实验过程中装置G和Ⅰ中的溶液pH变化曲线。
①装置H的作用为______。
②请判断t2时,锥形瓶中______(填“有”或“无”)盐酸剩余。
③t1后,显示器B中曲线几乎无变化,其原因是______。
五、计算题
20.某碳酸钠样品中含有少量氯化钠。为测定样品中碳酸钠的质量分数,现称取该样品6g,加入到盛有50g稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为53.8g。计算:
(1)反应后生成的二氧化碳的质量为______g。
(2)求此碳酸钠样品中碳酸钠的质量分数;
21.某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50.00g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如图所示。(结果保留两位小数)。
(1)当滴加Ba(OH)2溶液50g时烧杯内溶液的pH__________7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数_____。(结果保留0.01%)。
参考答案:
1.A 2.C 3.C 4.D 5.A 6.A 7.D 8.B 9.A 10.A 11.A 12.A
13.(1)Ca(OH)2+2HCl═CaCl2+2H2O
(2)CaCl2和HCl
(3)pH<7
14.(1) ①、②、④ ③和⑤ 是否发生化学变化
(2) 过滤 颗粒大小
(3) 水
(4)
(5) 不相同 生石灰干燥是化学变化,硅胶干燥剂干燥过程为物理变化
15.(1)CaO
(2)放热
16.(1)CaCO3
(2) CO2##二氧化碳
(3)或
(4)食品袋中的干燥剂(或自热饭的热源)
17.(1)NaCl
(2)生成白色沉淀
(3) BaSO4 BD
18.(1) 烧杯 作反应容器
(2)玻璃器皿
(3) 胶头滴管 偏小
(4)c
19.(1) 酒精灯 长颈漏斗
(2)
(3) 吸收氯化氢 有 溶液中二氧化碳已经达到饱和
20.(1)2.2
(2)设碳酸钠样品中碳酸钠的质量为x
此碳酸钠样品中碳酸钠的质量分数为。
答:此碳酸钠样品中碳酸钠的质量分数为88.3%。
21.(1)<
(2)3.92%
解:由图可知,加入100g氢氧化钡溶液两者恰好完全反应,设50g稀硫酸中含H2SO4的质量为x,
硫酸溶液的溶质质量分数为×100%=3.92%;
答:硫酸溶液的溶质质量分数3.92%。
