第5章初识酸和碱检测题-2021-2022学年九年级化学沪教版(上海)第二学期(word版 含答案)
文档属性
| 名称 | 第5章初识酸和碱检测题-2021-2022学年九年级化学沪教版(上海)第二学期(word版 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 182.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-04 00:00:00 | ||
图片预览




文档简介
第5章《初识酸和碱》检测题
一、单选题
1.下列有关实验现象的描述正确的是
A.镁条放入食醋时没有明显现象 B.铁丝生锈后产生一种红棕色固体
C.磷在氧气中燃烧产生大量烟雾 D.木炭在氧气中燃烧发出白光,生成二氧化碳
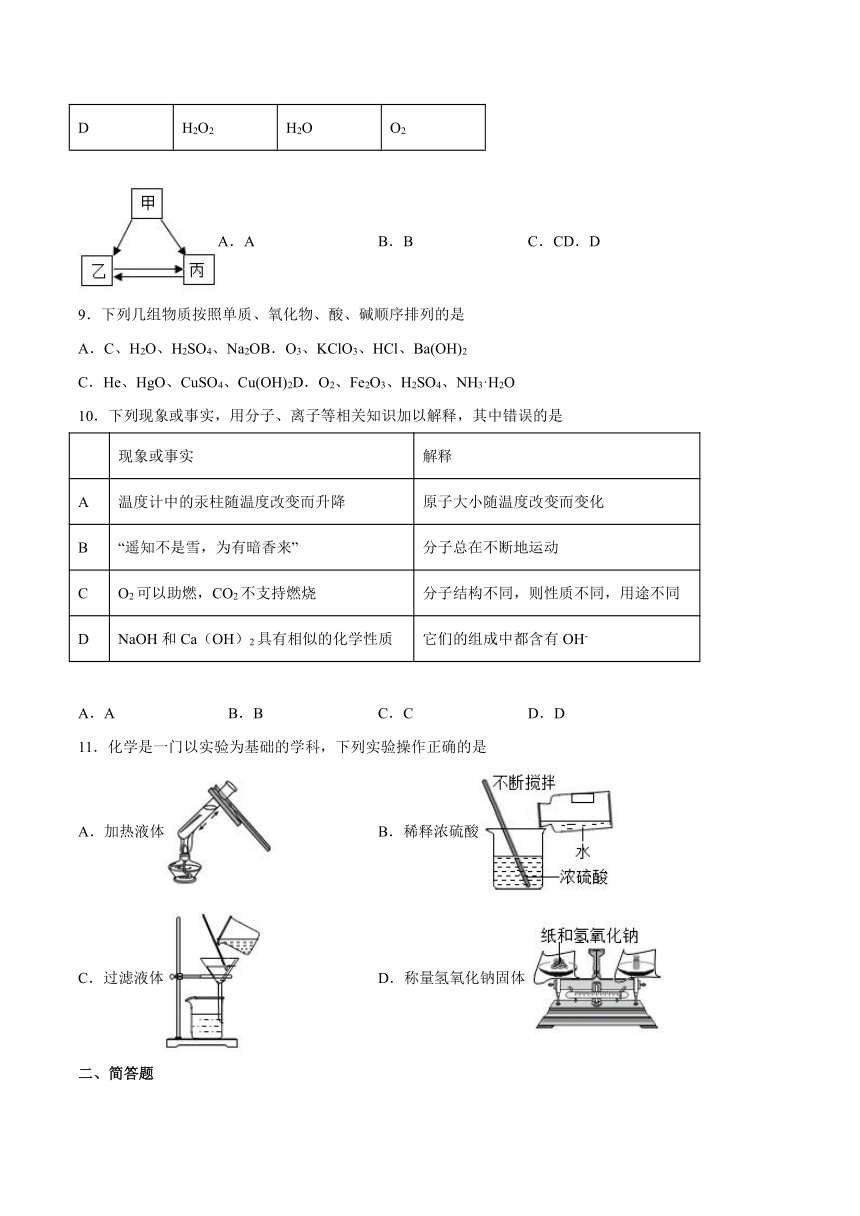
2.正确规范的操作是实验成功和人身安全的重要保证。下列实验操作正确的是
A.测定溶液pH B.配制溶液
C.称量固体质量 D.稀释浓硫酸
3.下列对于宏观现象的微观解释中,错误的是
A.水通电发生分解是因为水分子被破坏形成了新的分子
B.气体受压体积缩小是因为气体中每个分子受压变小了
C.氧气和液氧都能支持燃烧是因为构成它们的分子相同
D.酸具有相似的化学性质是因为酸溶液中都含有氢离子
4.下列实验操作符合规范的是
A.过滤 B.滴加液体
C.测定溶液pH值 D.稀释浓硫酸
5.下列变化过程中,一定发生物理变化的是
A.澄清石灰水敞口放置在空气中变浑浊B.河水结冰C.煤气中毒D.煤气泄漏遇明火爆炸
6.我国研制的航天服为航天员的舱外行走提供了安全保障。航天服内含有与氢氧化钠性质相似的氢氧化锂(LiOH),它不可能有的化学性质是
A.能与二氧化碳反应 B.能与氧化铁反应
C.能与氯化铁溶液反应 D.能与稀硫酸反应
7.学习化学的过程中,常常对所学知识进行归纳总结,下列归纳总结完全正确的是
A.化学中的“三” B.化学与安全
①三种可燃性气体:H2、CO2、O2 ②构成物质的三种微粒:分子、原子、离子 ①夜晚厨房燃气泄漏——立即开灯检查 ②做铁丝在氧气中燃烧的实验时,瓶底预先加少量水——防止集气瓶炸裂
C.化学中的“不一定” D.化学与类比推理
①由同种元素组成的物质不一定是单质 ②能与稀盐酸反应放出气体的不一定是金属 ①CO2能与NaOH溶液发生反应,则CO也能 ②浓硫酸具有吸水性,则浓盐酸也具有吸水性
A.A B.B C.C D.D
8.部分物质间的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。如图,不能通过一步反应实现转化的是
甲 乙 丙
A H2SO4 H2 H2O
B C CO CO2
C H2O2 H2O H2
D H2O2 H2O O2
A.A B.B C.C D.D
9.下列几组物质按照单质、氧化物、酸、碱顺序排列的是
A.C、H2O、H2SO4、Na2OB.O3、KClO3、HCl、Ba(OH)2
C.He、HgO、CuSO4、Cu(OH)2D.O2、Fe2O3、H2SO4、NH3·H2O
10.下列现象或事实,用分子、离子等相关知识加以解释,其中错误的是
现象或事实 解释
A 温度计中的汞柱随温度改变而升降 原子大小随温度改变而变化
B “遥知不是雪,为有暗香来” 分子总在不断地运动
C O2可以助燃,CO2不支持燃烧 分子结构不同,则性质不同,用途不同
D NaOH和Ca(OH)2具有相似的化学性质 它们的组成中都含有OH-
A.A B.B C.C D.D
11.化学是一门以实验为基础的学科,下列实验操作正确的是
A.加热液体 B.稀释浓硫酸
C.过滤液体 D.称量氢氧化钠固体
二、简答题
12.设计如图所示装置进行实验验证质量守恒定律。反应前托盘天平的指针指向刻度盘中间,充分反应后发现指针向右偏, 写出其中发生反应的化学方程式____________________________。
13.化学与生活息息相关,请用化学知识解释下列问题:
(1)在书写具有保存价值的档案时,规定应使用碳素墨水,为什么?______
(2)室内起火时,如果打开门窗,火反而会烧得更旺,为什么?______
(3)头发的主要成分是蛋白质,容易受碱性溶液的浸蚀,所以我们洗头发时先用洗发剂后用护发剂,为什么? ______
14.学用结合是我们学习化学知识的重要方法之一。请回答下列问题:
(1)在约500mL的饮料瓶中加入2勺白糖和适量果汁,加入约1.5g小苏打(碳酸氢钠),注入凉开水,再加入约1.5g柠檬酸,立即旋紧瓶盖,摇匀,放入冰箱。半小时后,你就可以喝到清凉甘甜的汽水。在上述过程中加入柠檬酸的作用是什么?____________
(2)生理盐水是医疗上常用的一种溶液,合格的生理盐水是无色透明的。一瓶合格的生理盐水密封放置一段时间后,为什么不会出现浑浊现象?_____________
(3)吸烟对人体有害。燃着的香烟产生的烟气中含有一种能与血液中血红蛋白结合的有毒气体,它是什么气体?______________
三、推断题
15.A~K均为初中化学常见物质,其中只有A、C属于单质,并且C是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)B的化学式可能是______。
(2)G的一种用途是______。
(3)写出一个反应④的化学方程式______。
(4)如图转化关系中一定未涉及到的基本反应类型______。
16.A、B、C、D、E是九年级化学中常见的五种物质。已知C是人体胃液中可以帮助消化的物质,D是大理石的主要成分,其相互反应及转化关系如下图所示,“一”表示相连的两物质之间能发生反应,“→”表示一种物质能转化为另一种物质,部分反应条件、反应物、生成物已略去。
(1)B化学式______;B与E的反应是______(填“吸热”或“放热”)反应。
(2)C转化为A的基本反应类型属于______。
(3)写出E物质的一种用途______。
(4)C与D的反应化学方程式:______。
17.A~I是初中化学常见的物质,它们之间有如图所示的转化关系,“→”表示物质间存在着相应的转化关系,“一”表示物质间能发生反应(部分反应物、生成物和反应条件未标出)。A、B、G、H、I中均含有同一种元素,且A为单质,D是大理石的主要成分,G的水溶液呈蓝色。请回答:
(1)C的化学式为______;
(2)写出H→G的化学方程式______。
四、实验题
18.请根据如图回答问题:
(1)写出标有序号仪器的名称:①______;②______。
(2)实验室用高锰酸钾固体制取氧气的化学方程式为______;若要收集干燥的氧气,应选用装置______(填“A”、“B”或“C”)。
(3)装置D可以用来测量生成CO2的体积,其中在水面上放一层植物油的目的是______。
(4)收集CO2时,用燃着的木条来验满,是利用CO2______的化学性质。
(5)NH3是一种碱性气体,干燥时不能选用______作干燥剂(填“浓硫酸”或“生石灰”)。
19.请结合下图回答问题:
(1)仪器名称:①_________;②_________。
(2)用高锰酸钾制取氧气,可选用的发生装置是_________(填序号),该反应的化学方程式为___________,该反应的基本反应类型是_________。
(3)实验室制取CO2,反应的化学方程式为__________,为方便控制反应的发生和停止,应选择的发生装置是__________(填序号)。
(4)下列气体可用G所示装置干燥、收集的是_________(填序号)。
①H2 ②O2 ③CO2 ④SO2 ⑤CH4 ⑥NH3
五、计算题
20.实验室预测定一瓶标签破损的稀硫酸的质量分数。现取10克稀硫酸样品,将5%的氢氧化钠溶液逐滴加入,边加边搅拌,同时测定pH值,其记录结果如图:
回答下列问题:
(1)a点溶液中含有的阳离子有________。
(2)求该稀硫酸总溶质的质量分数。
21.为测定某盐酸中溶质的质量分数,小明同学取该盐酸50g,向其中加入足量的碳酸钠粉末,完全反应后收集到6.6g气体。
500mL 品名:盐酸 化学式:HCl 相对分子质量:36.5 溶质质量分数:25%
(1)计算该盐酸中溶质的质量分数。
(2)小明将测定结果与标签上所示信息(标签如图)进行对比,发现测定结果与标签有偏差。若实验操作过程均无误,则引起结果偏差的原因可能是______。
22.为测定某镁矿石中镁元素的质量分数,兴趣小组的同学取了5g该镁矿石粉末,加入过量的稀硫酸,充分反应后过滤、除杂,得到只含有MgSO4和H2SO4两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取40g氢氧化钠溶液,分4次加入到盛有100g混合溶液的烧杯中充分反应,测得的实验数据如下表所示:
实验编号 第一次 第二次 第三次 第四次
加入氢氧化钠溶液质量/g 10 10 10 10
烧杯中生成沉淀的总质量/g 0.464 1.044 1.160 1.160
请计算:
(1)100g混合溶液中硫酸镁的质量。
(2)该镁矿石中镁元素的质量分数。(假设5g镁矿石中的镁元素全部转化为100g混合溶液中MgSO4中的镁元素)。
(3)加入的氢氧化钠溶液的溶质质量分数。
参考答案:
1.B 2.A 3.B 4.A 5.B 6.B 7.C 8.C 9.D 10.A 11.C
12.Fe2O3+6HCl=2FeCl3+3H2O、Fe+2HCl=FeCl2+H2↑
13. 碳素墨水中所含的碳单质在常温下化学性质稳定 打开门窗会起到补充氧气的作用,使火越烧越旺 洗发剂一般显碱性,容易浸蚀头发,而护发素显中性或弱酸性能保护头发,故洗头发时先用洗发剂后用护发剂。
14. )柠檬酸能与小苏打反应生成二氧化碳气体 因为生理盐水这种溶液具有稳定性 一氧化碳或 CO
15.(1)CH4
(2)冶炼金属
(3)
(4)化合反应、分解反应、置换反应
16. H2O 放热 置换 作食品干燥剂 CaCO3+2HCl=CaCl2+H2O+CO2↑
17. CO2 CuSO4+BaCl2=BaSO4↓+CuCl2
18.(1) 集气瓶 量筒
(2) A
(3)防止二氧化碳溶于水,且与水反应
(4)不燃烧,也不支持燃烧
(5)浓硫酸
19.(1) 铁架台 分液漏斗
(2) A 分解反应
(3) C
(4)①⑤⑥
20.(1)Na+ 、H+
(2)设该稀硫酸溶质的质量分数为x。
x=9.8%
答:该稀硫酸溶质的质量分数为9.8%。
21.(1)解:设该盐酸中氯化氢的质量为x
,x=10.95g
该盐酸的溶质质量分数为:
答:该盐酸的溶质质量分数为21.9%;
(2)浓盐酸具有挥发性,溶质挥发后导致溶质质量分数变小。
22.解:(1)设100g混合溶液中硫酸镁的质量为x
=
解得x=2.400g
故100g混合溶液中硫酸镁的质量为2.400g。
(2)2.40g硫酸镁中镁元素的质量为2.40g××100%=0.480g
则该镁矿石中镁元素的质量分数为 ×100%=9.6%
(3)加入的氢氧化钠溶液的溶质质量分数为y
=
解得y =8.0%
故加入的氢氧化钠溶液的溶质质量分数8.0%
答:(1)100g混合溶液中硫酸镁的质量为2.400g。
(2)该镁矿石中镁元素的质量分数为9.6%。
(3)加入的氢氧化钠溶液的溶质质量分数为8.0%。
一、单选题
1.下列有关实验现象的描述正确的是
A.镁条放入食醋时没有明显现象 B.铁丝生锈后产生一种红棕色固体
C.磷在氧气中燃烧产生大量烟雾 D.木炭在氧气中燃烧发出白光,生成二氧化碳
2.正确规范的操作是实验成功和人身安全的重要保证。下列实验操作正确的是
A.测定溶液pH B.配制溶液
C.称量固体质量 D.稀释浓硫酸
3.下列对于宏观现象的微观解释中,错误的是
A.水通电发生分解是因为水分子被破坏形成了新的分子
B.气体受压体积缩小是因为气体中每个分子受压变小了
C.氧气和液氧都能支持燃烧是因为构成它们的分子相同
D.酸具有相似的化学性质是因为酸溶液中都含有氢离子
4.下列实验操作符合规范的是
A.过滤 B.滴加液体
C.测定溶液pH值 D.稀释浓硫酸
5.下列变化过程中,一定发生物理变化的是
A.澄清石灰水敞口放置在空气中变浑浊B.河水结冰C.煤气中毒D.煤气泄漏遇明火爆炸
6.我国研制的航天服为航天员的舱外行走提供了安全保障。航天服内含有与氢氧化钠性质相似的氢氧化锂(LiOH),它不可能有的化学性质是
A.能与二氧化碳反应 B.能与氧化铁反应
C.能与氯化铁溶液反应 D.能与稀硫酸反应
7.学习化学的过程中,常常对所学知识进行归纳总结,下列归纳总结完全正确的是
A.化学中的“三” B.化学与安全
①三种可燃性气体:H2、CO2、O2 ②构成物质的三种微粒:分子、原子、离子 ①夜晚厨房燃气泄漏——立即开灯检查 ②做铁丝在氧气中燃烧的实验时,瓶底预先加少量水——防止集气瓶炸裂
C.化学中的“不一定” D.化学与类比推理
①由同种元素组成的物质不一定是单质 ②能与稀盐酸反应放出气体的不一定是金属 ①CO2能与NaOH溶液发生反应,则CO也能 ②浓硫酸具有吸水性,则浓盐酸也具有吸水性
A.A B.B C.C D.D
8.部分物质间的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。如图,不能通过一步反应实现转化的是
甲 乙 丙
A H2SO4 H2 H2O
B C CO CO2
C H2O2 H2O H2
D H2O2 H2O O2
A.A B.B C.C D.D
9.下列几组物质按照单质、氧化物、酸、碱顺序排列的是
A.C、H2O、H2SO4、Na2OB.O3、KClO3、HCl、Ba(OH)2
C.He、HgO、CuSO4、Cu(OH)2D.O2、Fe2O3、H2SO4、NH3·H2O
10.下列现象或事实,用分子、离子等相关知识加以解释,其中错误的是
现象或事实 解释
A 温度计中的汞柱随温度改变而升降 原子大小随温度改变而变化
B “遥知不是雪,为有暗香来” 分子总在不断地运动
C O2可以助燃,CO2不支持燃烧 分子结构不同,则性质不同,用途不同
D NaOH和Ca(OH)2具有相似的化学性质 它们的组成中都含有OH-
A.A B.B C.C D.D
11.化学是一门以实验为基础的学科,下列实验操作正确的是
A.加热液体 B.稀释浓硫酸
C.过滤液体 D.称量氢氧化钠固体
二、简答题
12.设计如图所示装置进行实验验证质量守恒定律。反应前托盘天平的指针指向刻度盘中间,充分反应后发现指针向右偏, 写出其中发生反应的化学方程式____________________________。
13.化学与生活息息相关,请用化学知识解释下列问题:
(1)在书写具有保存价值的档案时,规定应使用碳素墨水,为什么?______
(2)室内起火时,如果打开门窗,火反而会烧得更旺,为什么?______
(3)头发的主要成分是蛋白质,容易受碱性溶液的浸蚀,所以我们洗头发时先用洗发剂后用护发剂,为什么? ______
14.学用结合是我们学习化学知识的重要方法之一。请回答下列问题:
(1)在约500mL的饮料瓶中加入2勺白糖和适量果汁,加入约1.5g小苏打(碳酸氢钠),注入凉开水,再加入约1.5g柠檬酸,立即旋紧瓶盖,摇匀,放入冰箱。半小时后,你就可以喝到清凉甘甜的汽水。在上述过程中加入柠檬酸的作用是什么?____________
(2)生理盐水是医疗上常用的一种溶液,合格的生理盐水是无色透明的。一瓶合格的生理盐水密封放置一段时间后,为什么不会出现浑浊现象?_____________
(3)吸烟对人体有害。燃着的香烟产生的烟气中含有一种能与血液中血红蛋白结合的有毒气体,它是什么气体?______________
三、推断题
15.A~K均为初中化学常见物质,其中只有A、C属于单质,并且C是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)B的化学式可能是______。
(2)G的一种用途是______。
(3)写出一个反应④的化学方程式______。
(4)如图转化关系中一定未涉及到的基本反应类型______。
16.A、B、C、D、E是九年级化学中常见的五种物质。已知C是人体胃液中可以帮助消化的物质,D是大理石的主要成分,其相互反应及转化关系如下图所示,“一”表示相连的两物质之间能发生反应,“→”表示一种物质能转化为另一种物质,部分反应条件、反应物、生成物已略去。
(1)B化学式______;B与E的反应是______(填“吸热”或“放热”)反应。
(2)C转化为A的基本反应类型属于______。
(3)写出E物质的一种用途______。
(4)C与D的反应化学方程式:______。
17.A~I是初中化学常见的物质,它们之间有如图所示的转化关系,“→”表示物质间存在着相应的转化关系,“一”表示物质间能发生反应(部分反应物、生成物和反应条件未标出)。A、B、G、H、I中均含有同一种元素,且A为单质,D是大理石的主要成分,G的水溶液呈蓝色。请回答:
(1)C的化学式为______;
(2)写出H→G的化学方程式______。
四、实验题
18.请根据如图回答问题:
(1)写出标有序号仪器的名称:①______;②______。
(2)实验室用高锰酸钾固体制取氧气的化学方程式为______;若要收集干燥的氧气,应选用装置______(填“A”、“B”或“C”)。
(3)装置D可以用来测量生成CO2的体积,其中在水面上放一层植物油的目的是______。
(4)收集CO2时,用燃着的木条来验满,是利用CO2______的化学性质。
(5)NH3是一种碱性气体,干燥时不能选用______作干燥剂(填“浓硫酸”或“生石灰”)。
19.请结合下图回答问题:
(1)仪器名称:①_________;②_________。
(2)用高锰酸钾制取氧气,可选用的发生装置是_________(填序号),该反应的化学方程式为___________,该反应的基本反应类型是_________。
(3)实验室制取CO2,反应的化学方程式为__________,为方便控制反应的发生和停止,应选择的发生装置是__________(填序号)。
(4)下列气体可用G所示装置干燥、收集的是_________(填序号)。
①H2 ②O2 ③CO2 ④SO2 ⑤CH4 ⑥NH3
五、计算题
20.实验室预测定一瓶标签破损的稀硫酸的质量分数。现取10克稀硫酸样品,将5%的氢氧化钠溶液逐滴加入,边加边搅拌,同时测定pH值,其记录结果如图:
回答下列问题:
(1)a点溶液中含有的阳离子有________。
(2)求该稀硫酸总溶质的质量分数。
21.为测定某盐酸中溶质的质量分数,小明同学取该盐酸50g,向其中加入足量的碳酸钠粉末,完全反应后收集到6.6g气体。
500mL 品名:盐酸 化学式:HCl 相对分子质量:36.5 溶质质量分数:25%
(1)计算该盐酸中溶质的质量分数。
(2)小明将测定结果与标签上所示信息(标签如图)进行对比,发现测定结果与标签有偏差。若实验操作过程均无误,则引起结果偏差的原因可能是______。
22.为测定某镁矿石中镁元素的质量分数,兴趣小组的同学取了5g该镁矿石粉末,加入过量的稀硫酸,充分反应后过滤、除杂,得到只含有MgSO4和H2SO4两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取40g氢氧化钠溶液,分4次加入到盛有100g混合溶液的烧杯中充分反应,测得的实验数据如下表所示:
实验编号 第一次 第二次 第三次 第四次
加入氢氧化钠溶液质量/g 10 10 10 10
烧杯中生成沉淀的总质量/g 0.464 1.044 1.160 1.160
请计算:
(1)100g混合溶液中硫酸镁的质量。
(2)该镁矿石中镁元素的质量分数。(假设5g镁矿石中的镁元素全部转化为100g混合溶液中MgSO4中的镁元素)。
(3)加入的氢氧化钠溶液的溶质质量分数。
参考答案:
1.B 2.A 3.B 4.A 5.B 6.B 7.C 8.C 9.D 10.A 11.C
12.Fe2O3+6HCl=2FeCl3+3H2O、Fe+2HCl=FeCl2+H2↑
13. 碳素墨水中所含的碳单质在常温下化学性质稳定 打开门窗会起到补充氧气的作用,使火越烧越旺 洗发剂一般显碱性,容易浸蚀头发,而护发素显中性或弱酸性能保护头发,故洗头发时先用洗发剂后用护发剂。
14. )柠檬酸能与小苏打反应生成二氧化碳气体 因为生理盐水这种溶液具有稳定性 一氧化碳或 CO
15.(1)CH4
(2)冶炼金属
(3)
(4)化合反应、分解反应、置换反应
16. H2O 放热 置换 作食品干燥剂 CaCO3+2HCl=CaCl2+H2O+CO2↑
17. CO2 CuSO4+BaCl2=BaSO4↓+CuCl2
18.(1) 集气瓶 量筒
(2) A
(3)防止二氧化碳溶于水,且与水反应
(4)不燃烧,也不支持燃烧
(5)浓硫酸
19.(1) 铁架台 分液漏斗
(2) A 分解反应
(3) C
(4)①⑤⑥
20.(1)Na+ 、H+
(2)设该稀硫酸溶质的质量分数为x。
x=9.8%
答:该稀硫酸溶质的质量分数为9.8%。
21.(1)解:设该盐酸中氯化氢的质量为x
,x=10.95g
该盐酸的溶质质量分数为:
答:该盐酸的溶质质量分数为21.9%;
(2)浓盐酸具有挥发性,溶质挥发后导致溶质质量分数变小。
22.解:(1)设100g混合溶液中硫酸镁的质量为x
=
解得x=2.400g
故100g混合溶液中硫酸镁的质量为2.400g。
(2)2.40g硫酸镁中镁元素的质量为2.40g××100%=0.480g
则该镁矿石中镁元素的质量分数为 ×100%=9.6%
(3)加入的氢氧化钠溶液的溶质质量分数为y
=
解得y =8.0%
故加入的氢氧化钠溶液的溶质质量分数8.0%
答:(1)100g混合溶液中硫酸镁的质量为2.400g。
(2)该镁矿石中镁元素的质量分数为9.6%。
(3)加入的氢氧化钠溶液的溶质质量分数为8.0%。
