第5章初识酸和碱检测题—2021-2022学年九年级化学沪教版(上海)下册 (word版 含答案)
文档属性
| 名称 | 第5章初识酸和碱检测题—2021-2022学年九年级化学沪教版(上海)下册 (word版 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 179.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-06 00:00:00 | ||
图片预览

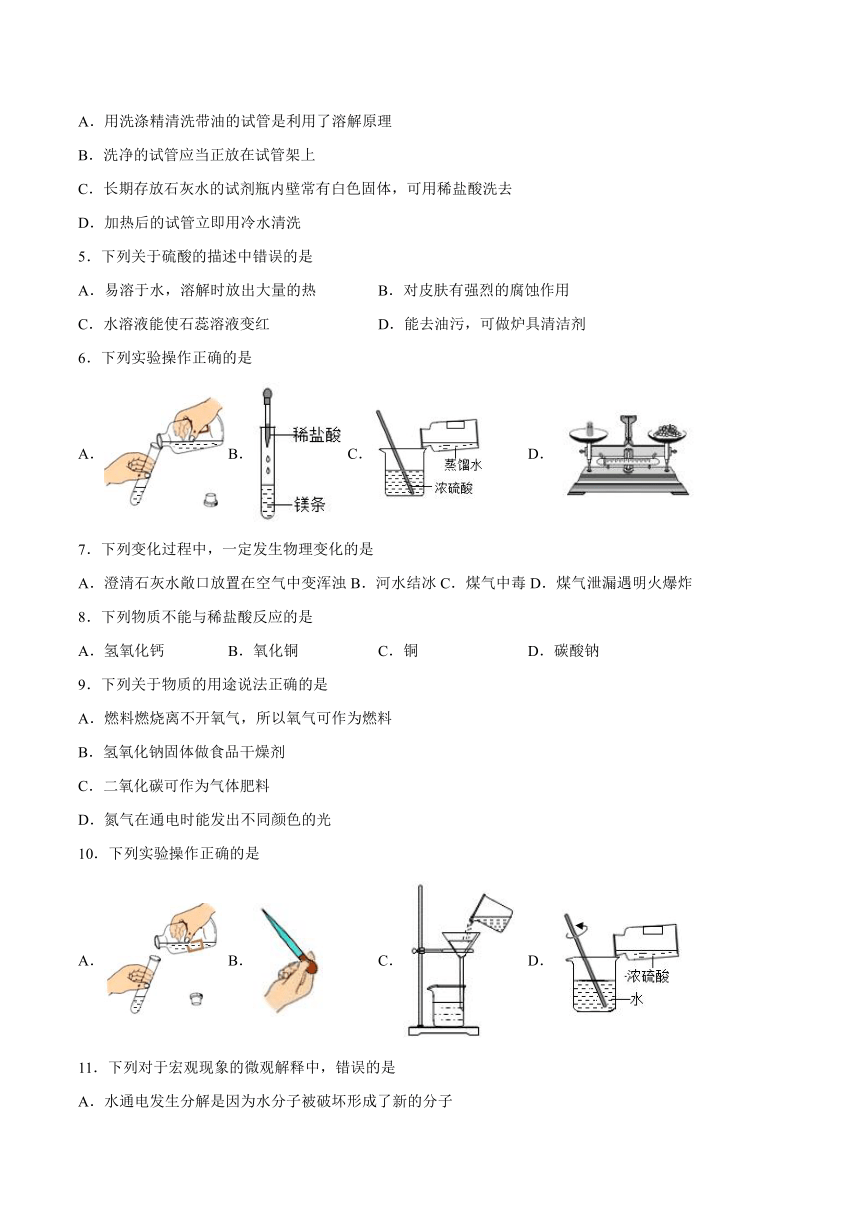


文档简介
第5章《初识酸和碱》检测题
一、单选题
1.下列实验操作正确的是( )
A. B. C. D.
2.实验室可用 制取H2,下列实验操作或实验装置正确的是
A.配制稀硫酸 B.制备H2
C.干燥H2 D.收集H2
3.“宏观辨识与微观探析”是化学学科核心素养之一。下列微观解释不正确的是
选项 客观事实 微观解释
A 利用水银温度计测量体温 温度升高,原子的体积变大
B HCl、H2SO4化学性质相似 溶液中都含有H+
C CO和CO2的性质不同 分子的结构不同
D 水加热沸腾变为水蒸气 分子的间隔发生变化
A.A B.B C.C D.D
4.下列关于实验室洗涤仪器的说法中正确的是
A.用洗涤精清洗带油的试管是利用了溶解原理
B.洗净的试管应当正放在试管架上
C.长期存放石灰水的试剂瓶内壁常有白色固体,可用稀盐酸洗去
D.加热后的试管立即用冷水清洗
5.下列关于硫酸的描述中错误的是
A.易溶于水,溶解时放出大量的热 B.对皮肤有强烈的腐蚀作用
C.水溶液能使石蕊溶液变红 D.能去油污,可做炉具清洁剂
6.下列实验操作正确的是
A. B.C. D.
7.下列变化过程中,一定发生物理变化的是
A.澄清石灰水敞口放置在空气中变浑浊B.河水结冰C.煤气中毒D.煤气泄漏遇明火爆炸
8.下列物质不能与稀盐酸反应的是
A.氢氧化钙 B.氧化铜 C.铜 D.碳酸钠
9.下列关于物质的用途说法正确的是
A.燃料燃烧离不开氧气,所以氧气可作为燃料
B.氢氧化钠固体做食品干燥剂
C.二氧化碳可作为气体肥料
D.氮气在通电时能发出不同颜色的光
10.下列实验操作正确的是
A. B. C. D.
11.下列对于宏观现象的微观解释中,错误的是
A.水通电发生分解是因为水分子被破坏形成了新的分子
B.气体受压体积缩小是因为气体中每个分子受压变小了
C.氧气和液氧都能支持燃烧是因为构成它们的分子相同
D.酸具有相似的化学性质是因为酸溶液中都含有氢离子
12.A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况。B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入一种物质后,甲试管中固体减少,乙试管中的固体增加,则加入的物质不可能是
A.浓硫酸 B.氢氧化钠 C.氧化钙 D.氯化钠
二、简答题
13.运用所学的化学知识解释下列问题。
(1)为什么燃气燃烧出现黄色或橙色火焰,锅底出现黑色时,需要调节炉具的进风口?
(2)为什么氮气可以用作焊接保护气?
(3)园林工人常在树木上涂刷含有硫磺粉等的石灰浆。这样做的目的是什么?
14.小刚同学向氯化铜和盐酸的混合溶液中逐滴加入氢氧化钠溶液直至过量(假设每次滴加氢氧化钠溶液后都充分反应),他根据实验绘制下图,请根据图回答下列问题:
(1) 若横坐标表示加入氢氧化钠的质量,则纵坐标表示的含义____;
(2) BC段反应的化学方程式____;
(3) A点对应的溶液中溶质有____。
三、推断题
15.A、B、C、D、E是初中化学常见的五种物质,A是石灰石的主要成分,E是能与血红蛋白结合的有毒气体,→表示转化关系,部分反应条件未注明。回答下列问题。
(1)物质E的化学式____________。
(2)写出物质E转化为物质C的化学反应方程式____________。
(3)物质B转化为物质D的过程会____________(填“吸收”或“放出”)热量。
16.A~K均为初中化学常见物质,其中只有A、C属于单质,并且C是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)B的化学式可能是______。
(2)G的一种用途是______。
(3)写出一个反应④的化学方程式______。
(4)如图转化关系中一定未涉及到的基本反应类型______。
17.有核电荷数小于18的A、B、C、D四种元素,A元素组成的单质是清洁的能源;B单质的体积在空气中占21%;C原子有3个电子层,最内层电子数是最外层的2倍;D元素是农作物生长所需要的营养元素,其组成的单质可以被豆科植物的根瘤菌吸收、利用。
(1)写出B、D元素的名称:B_________、D___________。
(2)写出A、B可能形成化合物的化学式__________、_________。
(3)写出由A、B、D三种元素组成的两种化合物之间发生中和反应的化学方程式:___。
(4)活泼性强的金属氢化物的化学式可表示为MHn,它与水剧烈反应生成碱和A的单质请写出C的氢化物与水发生反应的化学方程式_____________。
四、实验题
18.国家发改委、生态环境部等九部门联合印发《关于扎实推进塑料污染治理工作的通知》,提出自2021年1月1日起,禁止使用不可降解塑料袋。某化学研究小组的同学欲对某种塑料袋的组成进行分析探究,并测定元素的质量分数。
【查阅资料】①浓硫酸具有吸水性,且不与CO2反应。
②碱石灰可以吸收空气中的二氧化碳和水蒸气。
③该种塑料只含有碳、氢两种元素,燃烧产物为CO2和H2O。
【实验探究】按照下图所示的装置进行探究实验。
(1)A装置中CuSO4溶液起_________作用。
(2)E中的澄清石灰水__________,可以判断出塑料中含有碳元素,E中发生反应的化学方程式为________。
(3)若没有连接B装置,则测定出氢元素的质量分数会________(填“不变”“偏大”或“偏小”)。
【反思与评价】
(4)某同学认为F装置在该实验中没有作用,可以撤掉。请你对该同学的观点进行评价_________。
19.实验室用98%的浓硫酸(密度为1.84克/mL)配制100克溶质质量分数为20%的稀硫酸。
(1)配制该溶液的步骤、___________、量取、混匀、装瓶贴标签。
(2)溶解过程如图所示,b中盛放的物质是___________;a的作用是___________。
(3)配制后溶液中溶质的质量分数小于20%,分析引起这一结果的原因可能是___________。(写出一种即可)
五、计算题
20.为测定某氧化铜和铜的固体混合物中氧化铜的质量分数。小丁同学取20g固体混合物置于烧杯中,将100g稀硫酸分为四等份依次加入其中进行实验。测得数据如下:
第一次 第二次 第三次 第四次
加入稀硫酸的质量(g) 25 25 25 25
剩余固体的质量(g) 16 a 10 10
(反应的化学方程式为:CuO+H2SO4=CuSO4+H2O)
回答下列问题:
(1)上表中,a的值为_______。
(2)原固体混合物中,氧化铜的质量分数为_______。
(3)计算该实验所用稀硫酸的溶质质量分数。(写出计算过程,结果精确到0.1%)
21.为测定某样品中碳酸钙的含量,课外活动小组的同学称取24g样品(杂质不溶于水也不与稀盐酸反应)。向其中逐渐加入100g稀盐酸,所用稀盐酸的质量与剩余固体的质量关系如图所示,请根据图中的数据进行计算:
(1)24g样品中碳酸钙的质量为______g。
(2)所用稀盐酸中溶质的质量分数(写计算过程,结果精确到0.01%)。
参考答案:
1.B 2.B 3.A 4.C 5.D 6.A 7.B 8.C 9.C 10.D 11.B 12.D
13.(1)调大炉具的进风口,使燃料充分燃烧
(2)氮气的化学性质不活泼
(3)防止冻伤树木,防止害虫生卵
14. 生成沉淀的质量 2NaOH+CuCl2═2NaCl+Cu(OH)2↓ 氯化铜、氯化氢、氯化钠
15.(1)CO
(2)
(3)放热
16.(1)CH4
(2)冶炼金属
(3)
(4)化合反应、分解反应、置换反应
17.(1) 氧 氮
(2) H2O H2O2
(3)HNO3+NH3·H2O=NH4NO3+H2O
(4)NaH+H2O=NaOH+H2↑
18.(1)催化
(2) 变浑浊
(3)偏大
(4)该同学的观点不正确,F装置可以防止空气中二氧化碳的干扰,故不能撤掉(合理即可)
19.(1)计算
(2) 浓H2SO4 搅拌、使热量尽快散发出去
(3)量取浓硫酸时,俯视读数
20.(1)12
(2)50%
(3)解:设该实验所用稀硫酸的溶质质量分数为x
x=19.6%
答:该实验所用稀硫酸的溶质质量分数为19.6%
21.(1)20
(2)解:设80g稀盐酸中的溶质的质量为x,则有
稀盐酸中溶质的质量分数=;
答:所用稀盐酸中溶质的质量分数为18.25%。
一、单选题
1.下列实验操作正确的是( )
A. B. C. D.
2.实验室可用 制取H2,下列实验操作或实验装置正确的是
A.配制稀硫酸 B.制备H2
C.干燥H2 D.收集H2
3.“宏观辨识与微观探析”是化学学科核心素养之一。下列微观解释不正确的是
选项 客观事实 微观解释
A 利用水银温度计测量体温 温度升高,原子的体积变大
B HCl、H2SO4化学性质相似 溶液中都含有H+
C CO和CO2的性质不同 分子的结构不同
D 水加热沸腾变为水蒸气 分子的间隔发生变化
A.A B.B C.C D.D
4.下列关于实验室洗涤仪器的说法中正确的是
A.用洗涤精清洗带油的试管是利用了溶解原理
B.洗净的试管应当正放在试管架上
C.长期存放石灰水的试剂瓶内壁常有白色固体,可用稀盐酸洗去
D.加热后的试管立即用冷水清洗
5.下列关于硫酸的描述中错误的是
A.易溶于水,溶解时放出大量的热 B.对皮肤有强烈的腐蚀作用
C.水溶液能使石蕊溶液变红 D.能去油污,可做炉具清洁剂
6.下列实验操作正确的是
A. B.C. D.
7.下列变化过程中,一定发生物理变化的是
A.澄清石灰水敞口放置在空气中变浑浊B.河水结冰C.煤气中毒D.煤气泄漏遇明火爆炸
8.下列物质不能与稀盐酸反应的是
A.氢氧化钙 B.氧化铜 C.铜 D.碳酸钠
9.下列关于物质的用途说法正确的是
A.燃料燃烧离不开氧气,所以氧气可作为燃料
B.氢氧化钠固体做食品干燥剂
C.二氧化碳可作为气体肥料
D.氮气在通电时能发出不同颜色的光
10.下列实验操作正确的是
A. B. C. D.
11.下列对于宏观现象的微观解释中,错误的是
A.水通电发生分解是因为水分子被破坏形成了新的分子
B.气体受压体积缩小是因为气体中每个分子受压变小了
C.氧气和液氧都能支持燃烧是因为构成它们的分子相同
D.酸具有相似的化学性质是因为酸溶液中都含有氢离子
12.A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况。B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入一种物质后,甲试管中固体减少,乙试管中的固体增加,则加入的物质不可能是
A.浓硫酸 B.氢氧化钠 C.氧化钙 D.氯化钠
二、简答题
13.运用所学的化学知识解释下列问题。
(1)为什么燃气燃烧出现黄色或橙色火焰,锅底出现黑色时,需要调节炉具的进风口?
(2)为什么氮气可以用作焊接保护气?
(3)园林工人常在树木上涂刷含有硫磺粉等的石灰浆。这样做的目的是什么?
14.小刚同学向氯化铜和盐酸的混合溶液中逐滴加入氢氧化钠溶液直至过量(假设每次滴加氢氧化钠溶液后都充分反应),他根据实验绘制下图,请根据图回答下列问题:
(1) 若横坐标表示加入氢氧化钠的质量,则纵坐标表示的含义____;
(2) BC段反应的化学方程式____;
(3) A点对应的溶液中溶质有____。
三、推断题
15.A、B、C、D、E是初中化学常见的五种物质,A是石灰石的主要成分,E是能与血红蛋白结合的有毒气体,→表示转化关系,部分反应条件未注明。回答下列问题。
(1)物质E的化学式____________。
(2)写出物质E转化为物质C的化学反应方程式____________。
(3)物质B转化为物质D的过程会____________(填“吸收”或“放出”)热量。
16.A~K均为初中化学常见物质,其中只有A、C属于单质,并且C是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)B的化学式可能是______。
(2)G的一种用途是______。
(3)写出一个反应④的化学方程式______。
(4)如图转化关系中一定未涉及到的基本反应类型______。
17.有核电荷数小于18的A、B、C、D四种元素,A元素组成的单质是清洁的能源;B单质的体积在空气中占21%;C原子有3个电子层,最内层电子数是最外层的2倍;D元素是农作物生长所需要的营养元素,其组成的单质可以被豆科植物的根瘤菌吸收、利用。
(1)写出B、D元素的名称:B_________、D___________。
(2)写出A、B可能形成化合物的化学式__________、_________。
(3)写出由A、B、D三种元素组成的两种化合物之间发生中和反应的化学方程式:___。
(4)活泼性强的金属氢化物的化学式可表示为MHn,它与水剧烈反应生成碱和A的单质请写出C的氢化物与水发生反应的化学方程式_____________。
四、实验题
18.国家发改委、生态环境部等九部门联合印发《关于扎实推进塑料污染治理工作的通知》,提出自2021年1月1日起,禁止使用不可降解塑料袋。某化学研究小组的同学欲对某种塑料袋的组成进行分析探究,并测定元素的质量分数。
【查阅资料】①浓硫酸具有吸水性,且不与CO2反应。
②碱石灰可以吸收空气中的二氧化碳和水蒸气。
③该种塑料只含有碳、氢两种元素,燃烧产物为CO2和H2O。
【实验探究】按照下图所示的装置进行探究实验。
(1)A装置中CuSO4溶液起_________作用。
(2)E中的澄清石灰水__________,可以判断出塑料中含有碳元素,E中发生反应的化学方程式为________。
(3)若没有连接B装置,则测定出氢元素的质量分数会________(填“不变”“偏大”或“偏小”)。
【反思与评价】
(4)某同学认为F装置在该实验中没有作用,可以撤掉。请你对该同学的观点进行评价_________。
19.实验室用98%的浓硫酸(密度为1.84克/mL)配制100克溶质质量分数为20%的稀硫酸。
(1)配制该溶液的步骤、___________、量取、混匀、装瓶贴标签。
(2)溶解过程如图所示,b中盛放的物质是___________;a的作用是___________。
(3)配制后溶液中溶质的质量分数小于20%,分析引起这一结果的原因可能是___________。(写出一种即可)
五、计算题
20.为测定某氧化铜和铜的固体混合物中氧化铜的质量分数。小丁同学取20g固体混合物置于烧杯中,将100g稀硫酸分为四等份依次加入其中进行实验。测得数据如下:
第一次 第二次 第三次 第四次
加入稀硫酸的质量(g) 25 25 25 25
剩余固体的质量(g) 16 a 10 10
(反应的化学方程式为:CuO+H2SO4=CuSO4+H2O)
回答下列问题:
(1)上表中,a的值为_______。
(2)原固体混合物中,氧化铜的质量分数为_______。
(3)计算该实验所用稀硫酸的溶质质量分数。(写出计算过程,结果精确到0.1%)
21.为测定某样品中碳酸钙的含量,课外活动小组的同学称取24g样品(杂质不溶于水也不与稀盐酸反应)。向其中逐渐加入100g稀盐酸,所用稀盐酸的质量与剩余固体的质量关系如图所示,请根据图中的数据进行计算:
(1)24g样品中碳酸钙的质量为______g。
(2)所用稀盐酸中溶质的质量分数(写计算过程,结果精确到0.01%)。
参考答案:
1.B 2.B 3.A 4.C 5.D 6.A 7.B 8.C 9.C 10.D 11.B 12.D
13.(1)调大炉具的进风口,使燃料充分燃烧
(2)氮气的化学性质不活泼
(3)防止冻伤树木,防止害虫生卵
14. 生成沉淀的质量 2NaOH+CuCl2═2NaCl+Cu(OH)2↓ 氯化铜、氯化氢、氯化钠
15.(1)CO
(2)
(3)放热
16.(1)CH4
(2)冶炼金属
(3)
(4)化合反应、分解反应、置换反应
17.(1) 氧 氮
(2) H2O H2O2
(3)HNO3+NH3·H2O=NH4NO3+H2O
(4)NaH+H2O=NaOH+H2↑
18.(1)催化
(2) 变浑浊
(3)偏大
(4)该同学的观点不正确,F装置可以防止空气中二氧化碳的干扰,故不能撤掉(合理即可)
19.(1)计算
(2) 浓H2SO4 搅拌、使热量尽快散发出去
(3)量取浓硫酸时,俯视读数
20.(1)12
(2)50%
(3)解:设该实验所用稀硫酸的溶质质量分数为x
x=19.6%
答:该实验所用稀硫酸的溶质质量分数为19.6%
21.(1)20
(2)解:设80g稀盐酸中的溶质的质量为x,则有
稀盐酸中溶质的质量分数=;
答:所用稀盐酸中溶质的质量分数为18.25%。
