第10章金属检测题-2021-2022学年九年级化学京改版(2013)下册(word版有答案)
文档属性
| 名称 | 第10章金属检测题-2021-2022学年九年级化学京改版(2013)下册(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 145.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-06 00:00:00 | ||
图片预览





文档简介
第10章《金属》检测题
一、单选题
1.下列有关物质的说法正确的是
A.硬水通过活性炭吸附可变成软水
B.铁片放入硫酸铜溶液中,过一段时间溶液质量变大
C.氧气可以转化为二氧化碳,二氧化碳不能转化为氧气
D.合金与组成合金的纯金属相比,合金的硬度大,熔点低
2.下列实验方案能达到实验目的的是
选项 实验目的 实验方案
A 鉴别氮气和二氧化碳 分别伸入燃着的木条
B 鉴别木炭粉和铁粉 观察颜色
C 除去铜粉中的氧化铜 在空气中灼烧
D 除去MgSO4溶液中的少量CuSO4 加入足量的镁粉,过滤
A.A B.B C.C D.D
3.下列关于物质的用途说法错误的是
A.镁条燃烧时产生耀眼白光,可用于制造烟花
B.加热氯酸钾和二氧化锰制氧气,二氧化锰起催化作用
C.铅是制作铅笔芯的主要材料
D.钛合金可用于制造人造骨
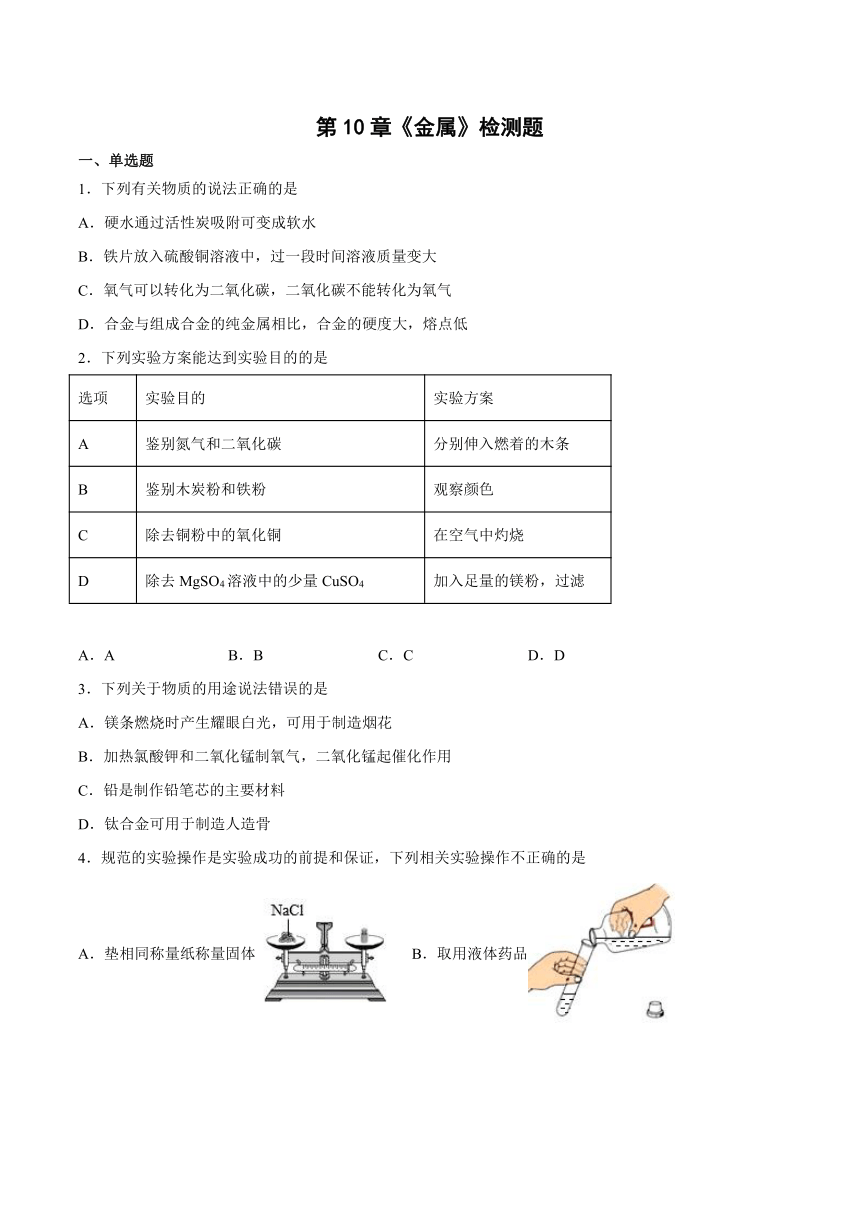
4.规范的实验操作是实验成功的前提和保证,下列相关实验操作不正确的是
A.垫相同称量纸称量固体 B.取用液体药品
C.添加固体药品 D.比较金属硬度
5.可持续发展战略的重要内容之一是保护资源。下列关于金属资源的锈蚀与保护的说法中不正确的是
A.金属易被腐蚀,从结构看是因为金属原子的最外层电子数一般少于4个,易失电子
B.铁制品表面涂油漆能防锈蚀的原因是隔绝了氧气和水
C.铜锈的主要成分是Cu2(OH)2CO3,铜制品的锈蚀是铜与氧气、水蒸气共同作用的结果
D.回收废旧金属也是保护金属资源的一项重要措施
6.逻辑推理是化学学习中常用的一种思维方法。下列推理正确的是( )
A.化学变化中分子种类发生改变,则分子种类发生改变的变化一定是化学变化
B.氧化物是含氧元素的化合物,则含氧元素的化合物一定是氧化物
C.一氧化碳和二氧化碳的组成元素相同,所以它们的化学性质相同
D.置换反应生成物是单质和化合物,则有单质和化合物生成的反应一定是置换反应
7.A、B、C、D、E是初中化学常见的物质,常温下A、B、C都为无色气体,且A为单质,B有毒性,D、E都为黑色粉末,且D为化合物。物质间的转化关系如图所示(“一”表示相邻的两种物质间能发生反应,“→”表示两种物质间的转化关系,部分反应物、生成物及反应条件已略去)。下列说法正确的是
A.B与D的反应是置换反应
B.D一定是CuO
C.A与C不能相互转化
D.B→C的反应过程中可能放出热量也可能吸收热量
8.下列实验目的通过对应实验操作能达到目的是
序号 实验目的 实验操作
A 配制10%的NaOH溶液 将10gNaOH放入100mL水中溶解
B 比较铜片和黄铜片的硬度 互相刻划
C 除去KNO3溶液中混有的少量NaCl 蒸发结晶
D 除去碳酸钙中的氧化钙 高温煅烧
A.A B.B C.C D.D
9.下列属于金属材料的是
A.磁铁矿 B.武德合金 C.铜绿 D.铁锈
10.一定质量的铜和镁组成的混合物与足量稀盐酸反应,过滤后,将滤渣在空气中充分加热所得产物的质量恰好等于原混合物的质量。那么原混合物中铜的质量分数是( )
A.30% B.50% C.60% D.80%
11.下列各组物质能验证、、三种金属活动性强弱的是
A.、、、稀盐酸 B.、溶液、溶液
C.、、溶液 D.、溶液、溶液
12.某同学整理的部分化学知识如下,你认为正确的选项是
A.水烧开后,壶盖被顶开,因为分子体积变大
B.釜底抽薪和熄灭酒精灯的灭火原理相同
C.金刚石和石墨的物理性质差别较大,这是因为碳原子的排列方式不同
D.真金不怕火炼,说明金的熔点高
二、简答题
13.某化学小组向Cu(NO3)2和Zn(NO3)2的混合溶液中加入一定量的Mg粉,充分反应后过滤。
(1)若向滤渣中加入稀盐酸,有气泡冒出。请分析滤渣的成分。
(2)若滤液呈蓝色,则滤液中的溶质有哪些?(写化学式)
三、推断题
14.甲、乙是初中化学常见的物质,它们与氧气之间存在如下图所示的反应关系(“一”表示物质间相互反应,“→”表示物质间转化,部分反应物、生成物及反应条件略去)
(1)若甲是一种黑色的固态非金屈单质,乙是一种氧化物。
①乙的化学式为______。
②甲与氧气反应的基本反应类型是______。
(2)若甲、乙均为金属单质,且乙呈紫红色。
①乙在生活中的一种用途是______。
②“甲→乙”的化学反应方程式为______。
③用稀硫酸代替氧气,图中所示反应关系不能成立,原因是______。
15.已知A、B、C、D、E、F是初中化学中常见的六种物质,均含有同一种元素。其中A是一种红棕色固体,B、E的组成元素相同,C→F常用于实验室检验某种气体。它们在一定条件下的一些转化关系如如图所示(→表示转化)。
请按要求回答:
(1)写出A物质的化学式___
(2)日常生活中为避免D→A,可采用的措施是___;
(3)写出C→F的化学方程式___。
(4)写出B→E的化学方程式___。
16.A—G是初中化学常见物质,它们的转化关系如图所示(部分反应物、生成物、反应条件已略去),已知A、D都是黑色固体,E为红色固体,C是石灰石的主要成分,F是无色溶液。请回答下列题:
(1)物质A的化学式为_____。
(2)反应①的基本反应类型是_____。
(3)物质B的一种用途是_____。
(4)反应②和③的化学方程式分别为_____、_____。
(5)实验室中,反应③的用途是_____。
四、实验题
17.金属及其化合物是中学化学学习的重要内容。
(1)《梦溪笔谈》中记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折。……”,剂钢、柔铁均为铁的合金,说明合金比纯金属__________________(填字母)。
a.硬度大、耐腐蚀 b.硬度小、熔点高 c.熔点高、耐腐蚀
(2)某兴趣小组为探究Zn、Fe、Cu、Ag四种金属的活动性,进行如图甲、乙、丙三个实验。
①请写出丙实验中的现象________________,甲中发生反应的化学方程式为_____________________。
②小组同学随后发现该实验无法得出四种金属的活动性顺序,于是补充图丁实验,最终得出四种金属活动性顺序。若图丁中的溶液B为稀盐酸,则A是______________________。
(3)某校化学实验室废液桶中收集了溶有大量FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如图实验方案。结合实验方案回答下列问题:
①金属X为_______________,加入适量溶液Y的目的是_______________________。
②理论上所得硫酸亚铁晶体的质量_______________(填“>”、“<”或“=”)原废液中硫酸亚铁的质量。
18.中国制造业正在持续发展,汽车制造是制造业的一个代表。请根据所学知识按要求填空。
(1)钢铁车壳表面喷漆不仅美观,而且可有效防止与空气中的______(填两种物质名称)接触而生锈。
(2)汽车制造需要钢铁,工业上高炉炼铁常用赤铁矿(主要成分为氧化铁)与一氧化碳来炼铁,其化学方程式为______。
(3)如右上图为模拟工业炼铁:若B处盛放氧化铁粉末。在A处通入一氧化碳一段时间后,B处下方用酒精喷灯加热,B处可观察到的现象为______,该装置的不足______。《自然》杂志刊载“绿色炼铁”技术:电解熔融的氧化铁得到铁和氧气,该反应的化学方程式:______。
(4)保护金属资源的有效途径,除了防止金属锈蚀外,还有______(写出一条即可)。
19.小高同学拿来一块黄色的金属向同学们说他捡到了黄金,小新同学说他曾在网上看到过有一种铜锌合金外观和黄金相似,常被误认为黄金,于是他和小高开始探究。
【提出问题】这块黄色的金属是黄金黄色铜锌合金?
【猜想】(1)小高认为是黄金;
(2)小新认为是铜锌合金
【查阅资料】合金中的金属保持各自的化学性质,金在高温下不与氧气反应,锌在高温下与氧气反应生成白色固体。
【设计实验】(1)小高设计的实验是:截取一小片黄色金属放在石棉网上用酒精灯加热。
(2)小新设计的实验是:截取一小片黄色金属放入硝酸银溶液中。
【现象与结论】
(1)小高在实验中观察到黄色的金属变黑,则他的猜想__________(填正确或错误),黑色的物质是_________。
(2)小新在实验中能观察到的现象是_________,写出反应的化学方程式_________。
【反思与应用】
(3)假如你的观点和小新的观点相同,你还可以设计一个实验,具体做法是截取一小片黄色金属放入某种液体物质中观察现象,这种物质是_________,你在实验中观察到的现象是________,也可以证明你们的观点正确。
五、计算题
20.小鸿设计如下实验,探究粗锌粒中锌的质量分数(粗锌所含的杂质不跟稀硫酸反应)。
计算:(写出计算过程)
(1)粗锌中锌的质量分数。(精确到0.1%)
(2)100g稀硫酸中硫酸的质量。
21.铜锌合金的组成对其性能影响较大,用于冷热加压加工的铜锌合金,要求锌量小于35%。化学社团同学对某铜锌合金进行探究:取合金样品加工成粉末,取20g合金粉末置于烧杯中,取120g稀盐酸,分6次加入,充分反应后测定剩余固体的质量,实验数据如下:
实验次序 1 2 3 4 5 6
加入稀盐酸的质量/g 20 20 20 20 20 20
剩余固体的质量/g 18.7 17.4 16.1 14.8 13.5 13.5
请回答:
(1)实验时先将合金粉碎,其目的是_____,每次加入稀盐酸充分反应后,将剩余固体分离出来时,需用到的玻璃仪器是_____(填一种即可)。
(2)该铜锌合金_____(填“可用于”或“不适于”)冷热加压加工。
(3)整个实验过程中产生氢气的质量是多少?(写出计算过程)
(4)第6次加入稀盐酸后溶液中的溶质有_____。
参考答案:
1.D 2.D 3.C 4.C 5.C 6.A 7.D 8.B 9.B 10.D 11.D 12.C
13.(1)一定含有Cu、Zn,可能含有Mg
(2)Cu(NO3)2、Zn(NO3)2、Mg(NO3)2
14.(1) CO 化合反应
(2) 用于制导线 在金属活动性顺序中,铜排在氢的后,铜不与稀酸发生反应
15.(1)Fe2O3
(2)涂油或刷油漆等
(3)CO2+Ca(OH)2=CaCO3↓+H2O
(4)2H2O22H2O+O2↑
16.(1)C
(2)置换反应
(3)用于灭火
(4)
(5)检验二氧化碳
17.(1)a
(2) 铜片上有银白色固体析出,溶液由无色变成蓝色 铜片
(3) 铁(或Fe) 除去混在铜粉里的铁粉 >
18.(1)水和氧气
(2)Fe2O3+3CO 2Fe+3CO2
(3) 红色固体变为黑色 没有尾气处理装置 2Fe2O34Fe+3O2↑
(4)回收利用废旧金属
19.(1) 错误 氧化铜##CuO
(2) 黄色的金属表面有银白色固体生成 (或)
(3) 稀盐酸(或稀硫酸) 有气泡生成
20.(1)解:设粗锌中锌的质量为x,100g稀硫酸中硫酸的质量为y
解得x=6.5g,y=9.8g
所以粗锌中锌的质量分数
答:粗锌中锌的质量分数为65%。
(2)答:100g稀硫酸中硫酸的质量为9.8g。
21.(1) 增大反应物之间的接触面积,使反应更充分 烧杯或漏斗或玻璃棒
(2)可用于
(3)解:设整个实验过程中产生氢气的质量是x
x=0.2g
答:整个实验过程中产生氢气的质量是0.2g
(4)ZnCl2、HCl
一、单选题
1.下列有关物质的说法正确的是
A.硬水通过活性炭吸附可变成软水
B.铁片放入硫酸铜溶液中,过一段时间溶液质量变大
C.氧气可以转化为二氧化碳,二氧化碳不能转化为氧气
D.合金与组成合金的纯金属相比,合金的硬度大,熔点低
2.下列实验方案能达到实验目的的是
选项 实验目的 实验方案
A 鉴别氮气和二氧化碳 分别伸入燃着的木条
B 鉴别木炭粉和铁粉 观察颜色
C 除去铜粉中的氧化铜 在空气中灼烧
D 除去MgSO4溶液中的少量CuSO4 加入足量的镁粉,过滤
A.A B.B C.C D.D
3.下列关于物质的用途说法错误的是
A.镁条燃烧时产生耀眼白光,可用于制造烟花
B.加热氯酸钾和二氧化锰制氧气,二氧化锰起催化作用
C.铅是制作铅笔芯的主要材料
D.钛合金可用于制造人造骨
4.规范的实验操作是实验成功的前提和保证,下列相关实验操作不正确的是
A.垫相同称量纸称量固体 B.取用液体药品
C.添加固体药品 D.比较金属硬度
5.可持续发展战略的重要内容之一是保护资源。下列关于金属资源的锈蚀与保护的说法中不正确的是
A.金属易被腐蚀,从结构看是因为金属原子的最外层电子数一般少于4个,易失电子
B.铁制品表面涂油漆能防锈蚀的原因是隔绝了氧气和水
C.铜锈的主要成分是Cu2(OH)2CO3,铜制品的锈蚀是铜与氧气、水蒸气共同作用的结果
D.回收废旧金属也是保护金属资源的一项重要措施
6.逻辑推理是化学学习中常用的一种思维方法。下列推理正确的是( )
A.化学变化中分子种类发生改变,则分子种类发生改变的变化一定是化学变化
B.氧化物是含氧元素的化合物,则含氧元素的化合物一定是氧化物
C.一氧化碳和二氧化碳的组成元素相同,所以它们的化学性质相同
D.置换反应生成物是单质和化合物,则有单质和化合物生成的反应一定是置换反应
7.A、B、C、D、E是初中化学常见的物质,常温下A、B、C都为无色气体,且A为单质,B有毒性,D、E都为黑色粉末,且D为化合物。物质间的转化关系如图所示(“一”表示相邻的两种物质间能发生反应,“→”表示两种物质间的转化关系,部分反应物、生成物及反应条件已略去)。下列说法正确的是
A.B与D的反应是置换反应
B.D一定是CuO
C.A与C不能相互转化
D.B→C的反应过程中可能放出热量也可能吸收热量
8.下列实验目的通过对应实验操作能达到目的是
序号 实验目的 实验操作
A 配制10%的NaOH溶液 将10gNaOH放入100mL水中溶解
B 比较铜片和黄铜片的硬度 互相刻划
C 除去KNO3溶液中混有的少量NaCl 蒸发结晶
D 除去碳酸钙中的氧化钙 高温煅烧
A.A B.B C.C D.D
9.下列属于金属材料的是
A.磁铁矿 B.武德合金 C.铜绿 D.铁锈
10.一定质量的铜和镁组成的混合物与足量稀盐酸反应,过滤后,将滤渣在空气中充分加热所得产物的质量恰好等于原混合物的质量。那么原混合物中铜的质量分数是( )
A.30% B.50% C.60% D.80%
11.下列各组物质能验证、、三种金属活动性强弱的是
A.、、、稀盐酸 B.、溶液、溶液
C.、、溶液 D.、溶液、溶液
12.某同学整理的部分化学知识如下,你认为正确的选项是
A.水烧开后,壶盖被顶开,因为分子体积变大
B.釜底抽薪和熄灭酒精灯的灭火原理相同
C.金刚石和石墨的物理性质差别较大,这是因为碳原子的排列方式不同
D.真金不怕火炼,说明金的熔点高
二、简答题
13.某化学小组向Cu(NO3)2和Zn(NO3)2的混合溶液中加入一定量的Mg粉,充分反应后过滤。
(1)若向滤渣中加入稀盐酸,有气泡冒出。请分析滤渣的成分。
(2)若滤液呈蓝色,则滤液中的溶质有哪些?(写化学式)
三、推断题
14.甲、乙是初中化学常见的物质,它们与氧气之间存在如下图所示的反应关系(“一”表示物质间相互反应,“→”表示物质间转化,部分反应物、生成物及反应条件略去)
(1)若甲是一种黑色的固态非金屈单质,乙是一种氧化物。
①乙的化学式为______。
②甲与氧气反应的基本反应类型是______。
(2)若甲、乙均为金属单质,且乙呈紫红色。
①乙在生活中的一种用途是______。
②“甲→乙”的化学反应方程式为______。
③用稀硫酸代替氧气,图中所示反应关系不能成立,原因是______。
15.已知A、B、C、D、E、F是初中化学中常见的六种物质,均含有同一种元素。其中A是一种红棕色固体,B、E的组成元素相同,C→F常用于实验室检验某种气体。它们在一定条件下的一些转化关系如如图所示(→表示转化)。
请按要求回答:
(1)写出A物质的化学式___
(2)日常生活中为避免D→A,可采用的措施是___;
(3)写出C→F的化学方程式___。
(4)写出B→E的化学方程式___。
16.A—G是初中化学常见物质,它们的转化关系如图所示(部分反应物、生成物、反应条件已略去),已知A、D都是黑色固体,E为红色固体,C是石灰石的主要成分,F是无色溶液。请回答下列题:
(1)物质A的化学式为_____。
(2)反应①的基本反应类型是_____。
(3)物质B的一种用途是_____。
(4)反应②和③的化学方程式分别为_____、_____。
(5)实验室中,反应③的用途是_____。
四、实验题
17.金属及其化合物是中学化学学习的重要内容。
(1)《梦溪笔谈》中记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折。……”,剂钢、柔铁均为铁的合金,说明合金比纯金属__________________(填字母)。
a.硬度大、耐腐蚀 b.硬度小、熔点高 c.熔点高、耐腐蚀
(2)某兴趣小组为探究Zn、Fe、Cu、Ag四种金属的活动性,进行如图甲、乙、丙三个实验。
①请写出丙实验中的现象________________,甲中发生反应的化学方程式为_____________________。
②小组同学随后发现该实验无法得出四种金属的活动性顺序,于是补充图丁实验,最终得出四种金属活动性顺序。若图丁中的溶液B为稀盐酸,则A是______________________。
(3)某校化学实验室废液桶中收集了溶有大量FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如图实验方案。结合实验方案回答下列问题:
①金属X为_______________,加入适量溶液Y的目的是_______________________。
②理论上所得硫酸亚铁晶体的质量_______________(填“>”、“<”或“=”)原废液中硫酸亚铁的质量。
18.中国制造业正在持续发展,汽车制造是制造业的一个代表。请根据所学知识按要求填空。
(1)钢铁车壳表面喷漆不仅美观,而且可有效防止与空气中的______(填两种物质名称)接触而生锈。
(2)汽车制造需要钢铁,工业上高炉炼铁常用赤铁矿(主要成分为氧化铁)与一氧化碳来炼铁,其化学方程式为______。
(3)如右上图为模拟工业炼铁:若B处盛放氧化铁粉末。在A处通入一氧化碳一段时间后,B处下方用酒精喷灯加热,B处可观察到的现象为______,该装置的不足______。《自然》杂志刊载“绿色炼铁”技术:电解熔融的氧化铁得到铁和氧气,该反应的化学方程式:______。
(4)保护金属资源的有效途径,除了防止金属锈蚀外,还有______(写出一条即可)。
19.小高同学拿来一块黄色的金属向同学们说他捡到了黄金,小新同学说他曾在网上看到过有一种铜锌合金外观和黄金相似,常被误认为黄金,于是他和小高开始探究。
【提出问题】这块黄色的金属是黄金黄色铜锌合金?
【猜想】(1)小高认为是黄金;
(2)小新认为是铜锌合金
【查阅资料】合金中的金属保持各自的化学性质,金在高温下不与氧气反应,锌在高温下与氧气反应生成白色固体。
【设计实验】(1)小高设计的实验是:截取一小片黄色金属放在石棉网上用酒精灯加热。
(2)小新设计的实验是:截取一小片黄色金属放入硝酸银溶液中。
【现象与结论】
(1)小高在实验中观察到黄色的金属变黑,则他的猜想__________(填正确或错误),黑色的物质是_________。
(2)小新在实验中能观察到的现象是_________,写出反应的化学方程式_________。
【反思与应用】
(3)假如你的观点和小新的观点相同,你还可以设计一个实验,具体做法是截取一小片黄色金属放入某种液体物质中观察现象,这种物质是_________,你在实验中观察到的现象是________,也可以证明你们的观点正确。
五、计算题
20.小鸿设计如下实验,探究粗锌粒中锌的质量分数(粗锌所含的杂质不跟稀硫酸反应)。
计算:(写出计算过程)
(1)粗锌中锌的质量分数。(精确到0.1%)
(2)100g稀硫酸中硫酸的质量。
21.铜锌合金的组成对其性能影响较大,用于冷热加压加工的铜锌合金,要求锌量小于35%。化学社团同学对某铜锌合金进行探究:取合金样品加工成粉末,取20g合金粉末置于烧杯中,取120g稀盐酸,分6次加入,充分反应后测定剩余固体的质量,实验数据如下:
实验次序 1 2 3 4 5 6
加入稀盐酸的质量/g 20 20 20 20 20 20
剩余固体的质量/g 18.7 17.4 16.1 14.8 13.5 13.5
请回答:
(1)实验时先将合金粉碎,其目的是_____,每次加入稀盐酸充分反应后,将剩余固体分离出来时,需用到的玻璃仪器是_____(填一种即可)。
(2)该铜锌合金_____(填“可用于”或“不适于”)冷热加压加工。
(3)整个实验过程中产生氢气的质量是多少?(写出计算过程)
(4)第6次加入稀盐酸后溶液中的溶质有_____。
参考答案:
1.D 2.D 3.C 4.C 5.C 6.A 7.D 8.B 9.B 10.D 11.D 12.C
13.(1)一定含有Cu、Zn,可能含有Mg
(2)Cu(NO3)2、Zn(NO3)2、Mg(NO3)2
14.(1) CO 化合反应
(2) 用于制导线 在金属活动性顺序中,铜排在氢的后,铜不与稀酸发生反应
15.(1)Fe2O3
(2)涂油或刷油漆等
(3)CO2+Ca(OH)2=CaCO3↓+H2O
(4)2H2O22H2O+O2↑
16.(1)C
(2)置换反应
(3)用于灭火
(4)
(5)检验二氧化碳
17.(1)a
(2) 铜片上有银白色固体析出,溶液由无色变成蓝色 铜片
(3) 铁(或Fe) 除去混在铜粉里的铁粉 >
18.(1)水和氧气
(2)Fe2O3+3CO 2Fe+3CO2
(3) 红色固体变为黑色 没有尾气处理装置 2Fe2O34Fe+3O2↑
(4)回收利用废旧金属
19.(1) 错误 氧化铜##CuO
(2) 黄色的金属表面有银白色固体生成 (或)
(3) 稀盐酸(或稀硫酸) 有气泡生成
20.(1)解:设粗锌中锌的质量为x,100g稀硫酸中硫酸的质量为y
解得x=6.5g,y=9.8g
所以粗锌中锌的质量分数
答:粗锌中锌的质量分数为65%。
(2)答:100g稀硫酸中硫酸的质量为9.8g。
21.(1) 增大反应物之间的接触面积,使反应更充分 烧杯或漏斗或玻璃棒
(2)可用于
(3)解:设整个实验过程中产生氢气的质量是x
x=0.2g
答:整个实验过程中产生氢气的质量是0.2g
(4)ZnCl2、HCl
