第六单元课题3二氧化碳和一氧化碳课件—2021-2022学年九年级化学人教版上册(共51张PPT)
文档属性
| 名称 | 第六单元课题3二氧化碳和一氧化碳课件—2021-2022学年九年级化学人教版上册(共51张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-06 00:00:00 | ||
图片预览



文档简介
(共51张PPT)
课题3 二氧化碳和一氧化碳
人教版·九年级·上册
(第一课时)二氧化碳
【学习目标】
1、了解二氧化碳和一氧化碳的性质。
2、了解二氧化碳的用途。
3、了解并关注温室效应。
4、会对实验现象进行观察分析、归纳。
5、会运用已学知识解决实际问题。
6、强化保护环境、解决环境问题的意识。
化学用语天天练
一、用化学方程式表示碳和碳的化合物之间的转化关系:
1、木炭燃烧:
2C + O2 2CO
点燃
C + O2 CO2
点燃
2、碳与二氧化碳在高温下反应:
C + CO2 2CO
高温
3、碳与氧化铜在高温下反应:
C+2CuO 2Cu+ CO2↑
高温
4、实验室制取二氧化碳:
CaCO3+2HCl CaCl2+H2O+ CO2↑
5、工业制取二氧化碳:
CaCO3 CaO+ CO2↑
高温
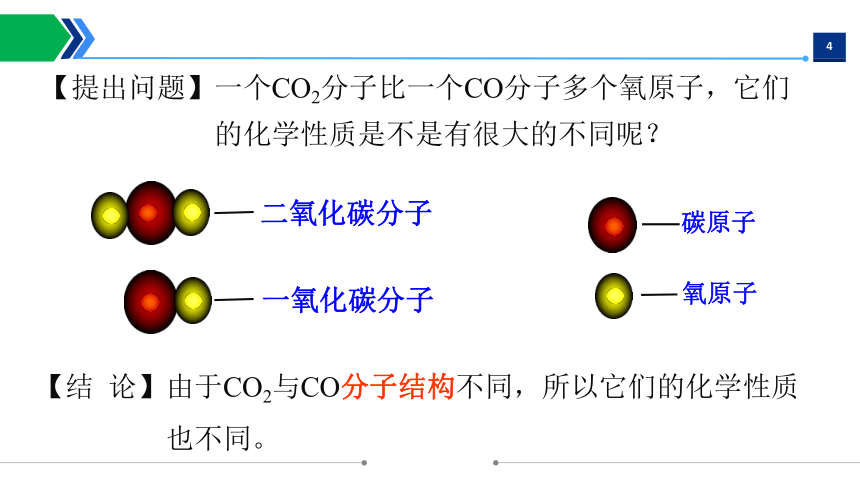
二氧化碳分子
一氧化碳分子
【结 论】由于CO2与CO分子结构不同,所以它们的化学性质
也不同。
【提出问题】一个CO2分子比一个CO分子多个氧原子,它们
的化学性质是不是有很大的不同呢?
碳原子
氧原子
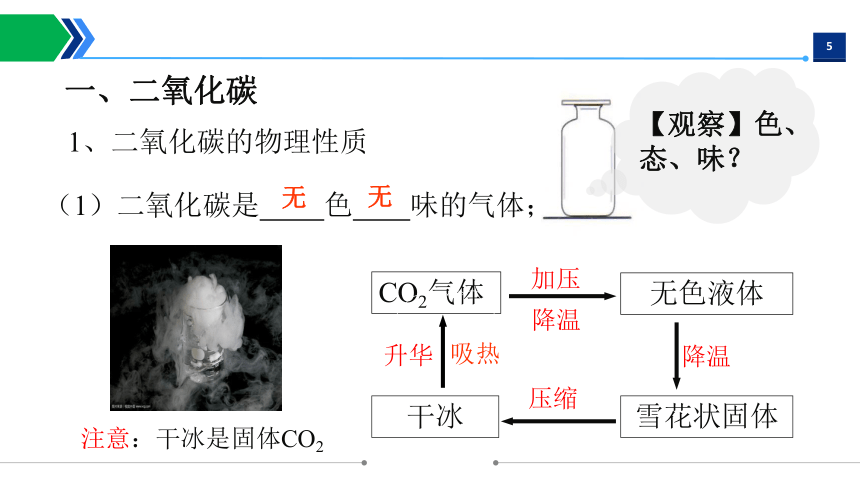
一、二氧化碳
1、二氧化碳的物理性质
(1)二氧化碳是 色 味的气体;
【观察】色、态、味?
无
无
吸热
CO2气体
无色液体
雪花状固体
干冰
加压
降温
压缩
升华
降温
注意:干冰是固体CO2
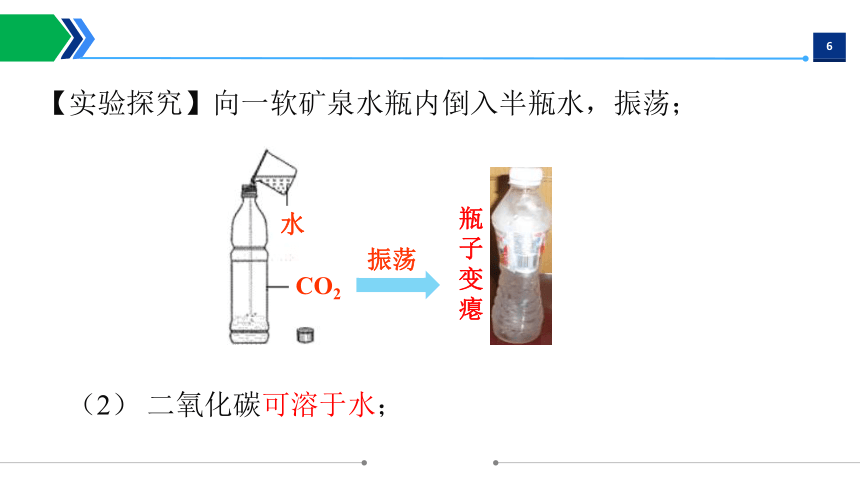
瓶子变瘪
水
CO2
振荡
(2) 二氧化碳可溶于水;
【实验探究】向一软矿泉水瓶内倒入半瓶水,振荡;
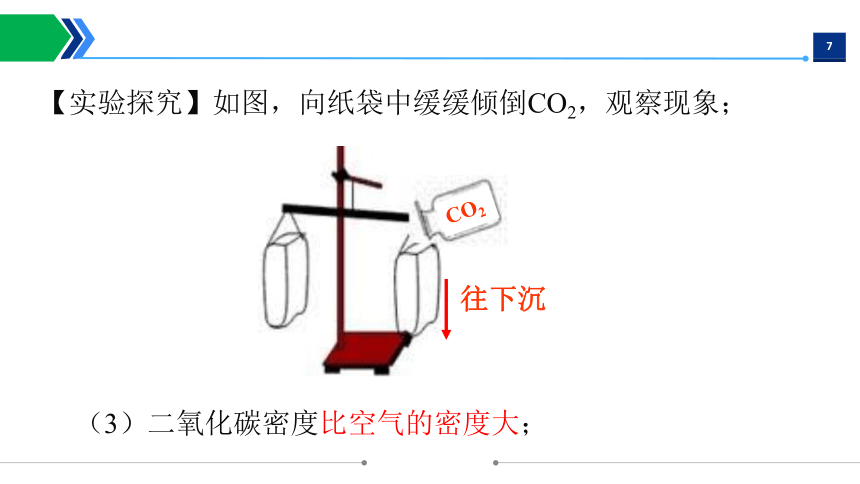
(3)二氧化碳密度比空气的密度大;
CO2
往下沉
【实验探究】如图,向纸袋中缓缓倾倒CO2,观察现象;
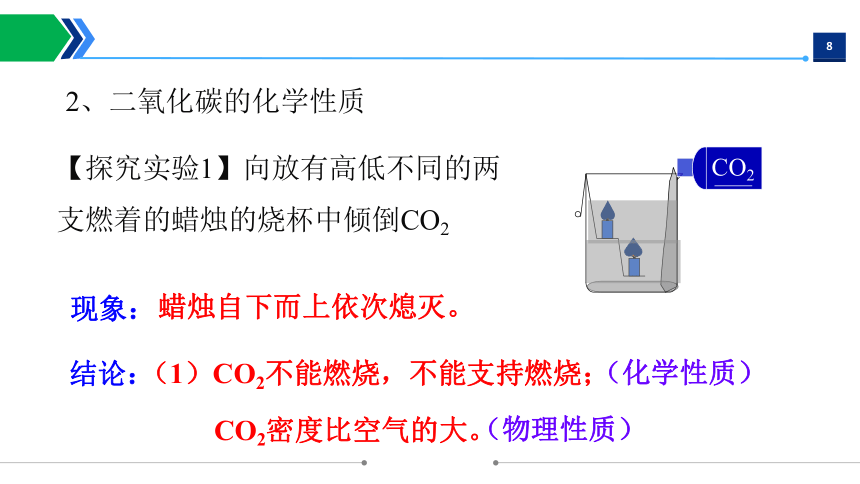
2、二氧化碳的化学性质
CO2
CO2
现象:
蜡烛自下而上依次熄灭。
结论:
CO2密度比空气的大。
【探究实验1】向放有高低不同的两支燃着的蜡烛的烧杯中倾倒CO2
(1)CO2不能燃烧,不能支持燃烧;
(化学性质)
(物理性质)
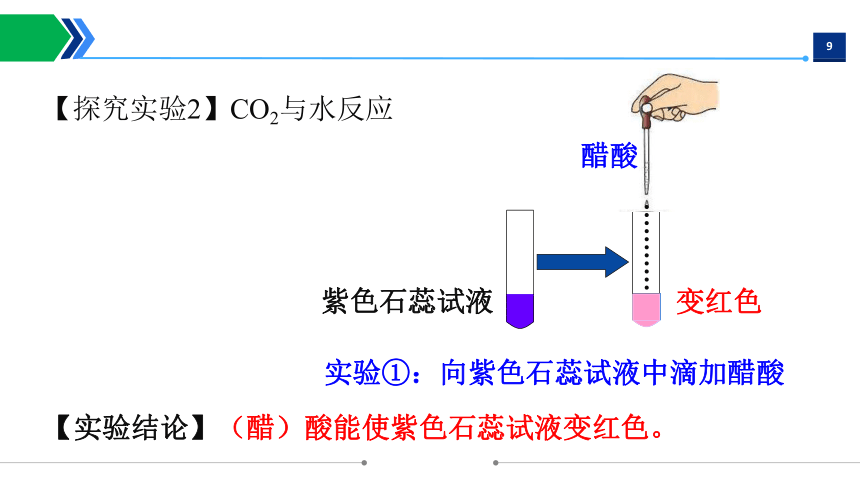
醋酸
【实验结论】(醋)酸能使紫色石蕊试液变红色。
紫色石蕊试液
变红色
实验①:向紫色石蕊试液中滴加醋酸
醋酸
【探究实验2】CO2与水反应
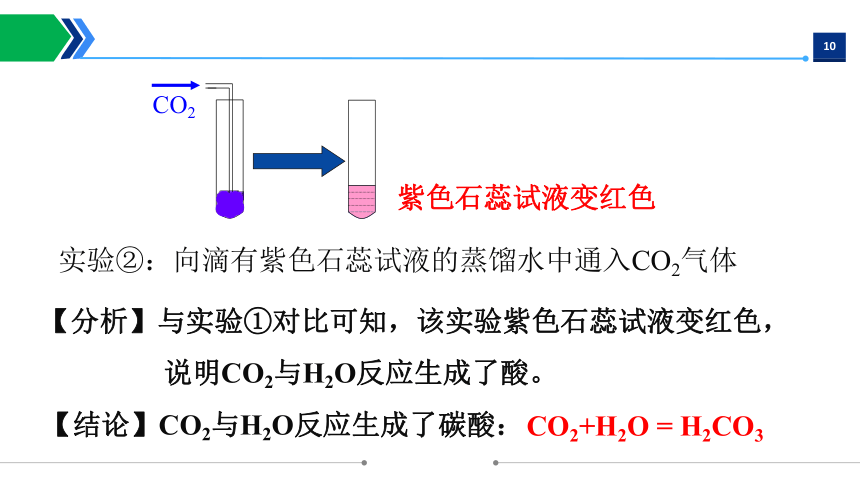
CO2
实验②:向滴有紫色石蕊试液的蒸馏水中通入CO2气体
紫色石蕊试液变红色
【分析】与实验①对比可知,该实验紫色石蕊试液变红色,
说明CO2与H2O反应生成了酸。
【结论】CO2与H2O反应生成了碳酸:
CO2+H2O = H2CO3
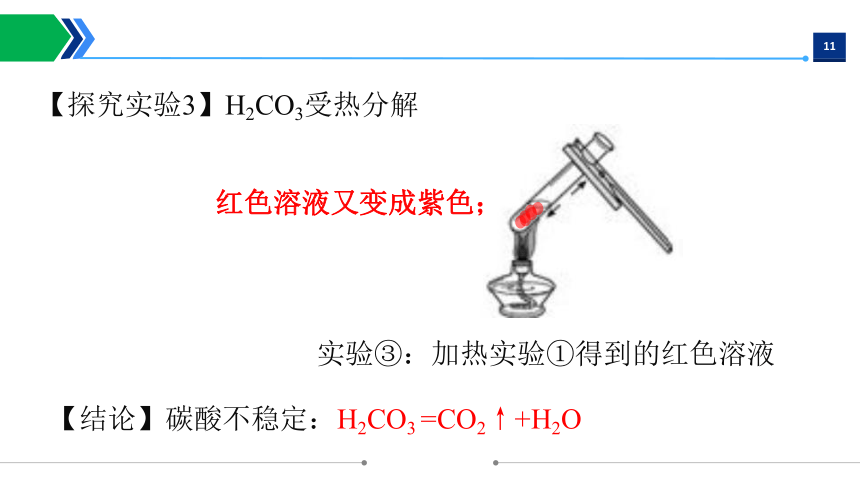
【结论】碳酸不稳定:H2CO3 =CO2↑+H2O
【探究实验3】H2CO3受热分解
实验③:加热实验①得到的红色溶液
红色溶液又变成紫色;
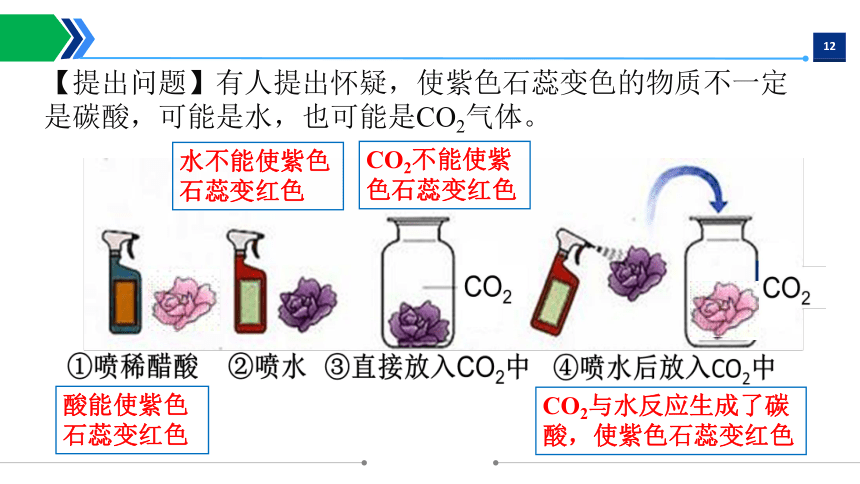
【提出问题】有人提出怀疑,使紫色石蕊变色的物质不一定是碳酸,可能是水,也可能是CO2气体。
酸能使紫色石蕊变红色
水不能使紫色石蕊变红色
CO2不能使紫色石蕊变红色
CO2与水反应生成了碳酸,使紫色石蕊变红色
【探究实验4】向澄清石灰水[Ca(OH)2]中通入CO2
澄清石灰水
变浑浊
CO2+ Ca(OH)2 = H2O +CaCO3 ↓
【分析】CO2与Ca(OH)2反应生成了
不溶于水的白色固体碳酸钙。
【结论】CO2能与澄清石灰水反应:
【归纳小结】CO2的性质
2、CO2可以与水反应;
3、CO2与澄清石灰水反应;
CO2+H2O = H2CO3
碳酸不稳定:H2CO3=CO2↑+H2O
CO2+ Ca(OH)2 = H2O +CaCO3 ↓
1、CO2是无色无味的气体;
2、CO2可溶于水;
3、CO2的密度比空气大;
物理性质
化学性质
1、CO2不能燃烧、不能 助燃,
也不能供呼吸;
灭火剂
作制冷剂
导致温室效应!
CO2
3、CO2的 利 与 弊
制汽水
作气体肥料
涨知识
CaCO3
CaO
Ca(OH)2
①
②
③
①
② CaO + H2O = Ca(OH)2
③ Ca(OH)2 + CO2 =CaCO3 ↓+H2O
烈火焚烧若等闲
粉身碎骨浑不怕
要留清白在人间
巩固练习
( )1.下列关于CO2性质的信息,正确的是:
① 可以助燃 ② 能使澄清石灰水变浑浊
③ 可溶于水,但不能与水反应
④ 可供绿色植物进行光合作用
A.②④ B.①③ C.①② D.②③
A
( )2.如图所示实验能够说明二氧化碳具有的性质有:
①不能燃烧 ②不能支持燃烧 ③还原性
④密度比空气大 ⑤密度比空气小
A.①②③ B.②③④
C.①②④ D.①②⑤
C
( )3.常温下能与二氧化碳发生化合反应的物质是:
A.水 B.澄清石灰水 C.氧气 D.木炭
A
( )4.向石蕊溶液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是:
A.红色→紫色→红色 B.紫色→红色→紫色
C.红色→紫色→蓝色 D.红色→无色→红色
B
巩固练习
巩固练习
( )5.鉴别二氧化碳和氧气,下列试剂或方法不可行的是:
A.澄清石灰水 B.燃着的木条
C.紫色石蕊试液 D.闻气味
D
( )6.下列有关CO2的实验中,只能证明CO2物理性质的实验是:
A
( )7.全球气候变暖正成为人类关注的环境问题,引起温室效应的主要气体是:
A.N2 B.O2 C.H2 D.CO2
D
( )8.下列说法不正确的是:
A.温室里施用CO2可提高农作物产量
B.干冰用于人工降雨和制冷剂,是物理变化
C.CO2属于氧化物,也属于化合物和纯净物
D.CO2的大量排放导致了酸雨的形成
D
巩固练习
( )9.下列有关“物质——性质——用途”的叙述中,用途与性质不相关的是:
序号 物质 性质 用途
A 干冰 升华时吸收热量 制冷剂
B 活性炭 吸附性 防毒面具
C 氧气 助燃性 医疗急救
D 木炭 可燃性 作燃料
C
巩固练习
巩固练习
A.④比①先红,②、③不变红
B.①比④先红,②、③不变红
C.④变红,①②③不变红
D.①变红,②③④不变红
( )10、如图所示的实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球。下列能准确描述实验现象的是:
A
11.某同学用微型实验装置(如图)制取二氧化碳并检验其性质,回答问题。
(1)试管中发生反应的化学方程式是: ______________ _。
CaCO3+2HCl CaCl2+H2O+ CO2↑
巩固练习
(2)b处出现的现象是 。
(3)根据烧杯中的变化现象,得出二氧化碳的化学性质是
。
(4)另一同学操作时,误将浓盐酸当稀盐酸使用,结果 处没有明显现象。
(5)你认为微型实验的优点是 (写一条即可)。
澄清的石灰水变浑浊
不能燃烧且不能支持燃烧
b
节约药品
巩固练习
(1)写出A、甲、乙的化学式:
A ;
甲 ;
乙 。
C
CO2
CO
12、A、B是两种常见的单质,甲、乙是两种常见的气体化合物,且组成元素相同。常温下A为黑色固体,其余均为气体。在一定条件下它们之间相互转化的关系如下图所示:
巩固练习
(2)按要求完成下列化学反应方程式:
① 甲+A反应的化学方程式:
;
② 乙+B反应的化学方程式:
。
12、A、B是两种常见的单质,甲、乙是两种常见的气体化合物,且组成元素相同。常温下A为黑色固体,其余均为气体。在一定条件下它们之间相互转化的关系如下图所示:
巩固练习
13、甲、乙、丙是初中化学中常见的物质,其中一种物质为单质,另外两种物质均为氧化物,且组成元素相同。其转化关系如右图所示:
(1)若甲为固体单质,写出相应的反应方程式。
① ;
该反应基本反应类型为______;
③ 。
化合
巩固练习
点燃
(2)若丙为气体单质,
①反应的化学方程式为:
;
该基本该反应类型为 。
分解反应
2H2O2 2H2O+O2↑
MnO2
13、甲、乙、丙是初中化学中常见的物质,其中一种物质为单质,另外两种物质均为氧化物,且组成元素相同。其转化关系如右图所示:
巩固练习
课题3 二氧化碳和一氧化碳
人教版·九年级·上册
(第二课时)一氧化碳
化学用语天天练
一、用化学方程式表示碳和碳的化合物之间的转化关系:
1、木炭燃烧:
2C + O2 2CO
点燃
C + O2 CO2
点燃
2、碳与二氧化碳在高温下反应:
C + CO2 2CO
高温
3、碳与氧化铜在高温下反应:
C+2CuO 2Cu+ CO2↑
高温
4、实验室制取二氧化碳:
CaCO3+2HCl CaCl2+H2O+ CO2↑
5、工业制取二氧化碳:
CaCO3 CaO+ CO2↑
高温
化学用语天天练
6、二氧化碳和水反应:
CO2+H2O H2CO3
7、碳酸分解:
H2CO3 H2O+ CO2↑
8、二氧化碳与澄清石灰水反应:
Ca(OH)2+CO2 CaCO3↓+H2O
【问题】CO是怎么产生的?
【解析】O2不充足时,碳不完全燃烧生成:
(剧毒气体)
2C+O2 2CO
点燃
二、一氧化碳
1、CO的物理性质
(1)通常情况下,CO是 的气体;
(3)CO 于水;
(2)CO的密度比空气的密度 ;
CO俗称煤气,有剧毒,是“隐形”杀手;
实验室收集CO能否用向下排空气法?
有人说,在燃着的煤炉上放一壶水,就可防止煤气中毒,你觉得呢?
无色、无味
略小
难溶
2、CO的化学性质
(1)CO具有 ;
① 现象:
2CO+O2 2CO2
点燃
③ 注意:与H2一样,点燃CO前,要检验纯度;
② 反应原理:
可燃性
CO燃烧时放出热量,
发出蓝色的火焰。
否则会发生爆炸!!!
(2)CO具有 ;
还原性
澄清石灰水
CuO
CO
处理尾气
黑色粉末变红色
澄清石灰水变白色浑浊
【探究实验】:CO与CuO在加热条件下反应
(Ⅰ)实验现象:
①黑色粉末变成 ;
②澄清的石灰水 。
(Ⅱ)反应原理:
CO+CuO Cu+CO2
△
(Ⅲ)尾气处理:将尾气(含CO) :
2CO+O2 2CO2
点燃
红色光亮固体
变白色浑浊
点燃
CO与CuO在加热条件下反应
(Ⅳ)CO还原CuO实验的正确步骤:
① 先通入CO气体;
③ 熄灭酒精灯;
② 加热;
④ 停止通入CO;
气
灯
灯
气
①②颠倒会爆炸!
③④颠倒会氧化!
(3)CO有 ;
CO有剧毒。这是因为CO容易与血液里的血红蛋白结合,形成碳氧血红蛋白,使血红蛋白丧失携氧的能力和作用,造成组织窒息,导致人体窒息而死亡。
毒性
【归纳小结】CO的化学性质
(1)CO具有可燃性:
(2)CO具有还原性:
(3)CO有剧毒:
易与血红蛋白结合,丧失携氧能力
3、CO的用途
(1)CO具有可燃性,常用作 ;
(2)CO具有还原性,工业上常用来 ;
燃料
冶炼金属
CO+CuO Cu+CO2
△
2CO+O2 2CO2
点燃
巩固练习
( )1.下列关于一氧化碳的说法错误的是:
A.一氧化碳能使紫色石蕊溶液变红
B.一氧化碳难溶于水
C.一氧化碳有毒,会污染空气
D.一氧化碳可用作燃料
A
( )2.下列属于有毒气体的是:
A.CO B.CO2 C.O2 D.N2
A
巩固练习
( )3.三氧化二碳(化学式C2O3)通常情况下是一种无色无味的气体,可溶于水,与水反应生成草酸,且常温下不稳定,其他的化学性质与一氧化碳相似。下列有关三氧化二碳说法错误的是:
A.C2O3中碳元素的化合价为+4价
B.三氧化二碳具有还原性
C.在空气中燃烧的产物为二氧化碳
D.C2O3有毒
A
( )4.一氧化碳有毒是因为:
A.它具有可燃性
B.它具有还原性
C.它能与血液里的氧气结合生成二氧化碳
D.它能与血液里的血红蛋白结合,使血红蛋白不能
很好地与氧气结合
D
巩固练习
( )5.下列有关碳及碳的氧化物的描述不正确的是:
A.一氧化碳可用来冶炼金属
B.一氧化碳有毒,二氧化碳无毒
C.碳在氧气中燃烧一定生成二氧化碳
D.二氧化碳是导致温室效应的主要气体之一
C
巩固练习
6.根据下列装置图回答问题:
(1)写出图中仪器a和b的名称:
a: ,b: 。
长颈漏斗
酒精灯
巩固练习
(2)装置C中产生的现象是 。
(3)装置D中产生的现象是 。
(4)装置E处气体燃烧时产生 色火焰。
(5)装置A中反应的化学方程式是:
。
黑色粉末变成光亮的红色粉末
澄清的石灰水变浑浊
蓝
CaCO3+2HCl CaCl2+H2O+ CO2↑
巩固练习
7.碳和部分碳的化合物间转化关系如图所示,请回答下列问题:
(1)物质X的化学式为 。
(2)从图中任选一种物质,说说它的一种用途: 。
CO2
CO可作燃料
巩固练习
(3)写出在此题中涉及的五个化合反应的化学方程式:
① ;
② ;
③ ;
④ ;
⑤ 。
2C + O2 2CO
点燃
C + O2 CO2
点燃
C + CO2 2CO
高温
CO2+H2O H2CO3
巩固练习
2CO+O2 2CO2
8、右图是木炭还原氧化铜的探究实验装置。
【提出问题】木炭还原氧化铜产生什么气体?
【提出猜想】产生的气体有三种情况:
① 只有CO
② 只有CO2
③_______________。
CO与CO2
巩固练习
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,数据设计如下:
称量对象 反应前质量 反应后质量 质量差
试管+固体混合物 M1 M2 △m1即( M1-M2)
烧杯+澄清石灰水 M3 M4 △m2即( M4-M3)
(1)若△m2=0,则猜想 成立。
(2)若猜想②正确,理论上△m1与△m2 的关系是:
△m1 △m2(填“>”、“<”或“=”)。
①
=
巩固练习
【实验并记录】实验得到的数据如下表:
称量对象 反应前质量 反应后质量 质量差
试管+固体混合物 69.8g 65.4g △m1
烧杯+澄清石灰水 118.8g 122.6g △m2
【得出结论】通过对表中实验数据分析,最终确定是猜想_______成立。
③
巩固练习
本课题已学完,请及时巩固复习!
课题3 二氧化碳和一氧化碳
人教版·九年级·上册
(第一课时)二氧化碳
【学习目标】
1、了解二氧化碳和一氧化碳的性质。
2、了解二氧化碳的用途。
3、了解并关注温室效应。
4、会对实验现象进行观察分析、归纳。
5、会运用已学知识解决实际问题。
6、强化保护环境、解决环境问题的意识。
化学用语天天练
一、用化学方程式表示碳和碳的化合物之间的转化关系:
1、木炭燃烧:
2C + O2 2CO
点燃
C + O2 CO2
点燃
2、碳与二氧化碳在高温下反应:
C + CO2 2CO
高温
3、碳与氧化铜在高温下反应:
C+2CuO 2Cu+ CO2↑
高温
4、实验室制取二氧化碳:
CaCO3+2HCl CaCl2+H2O+ CO2↑
5、工业制取二氧化碳:
CaCO3 CaO+ CO2↑
高温
二氧化碳分子
一氧化碳分子
【结 论】由于CO2与CO分子结构不同,所以它们的化学性质
也不同。
【提出问题】一个CO2分子比一个CO分子多个氧原子,它们
的化学性质是不是有很大的不同呢?
碳原子
氧原子
一、二氧化碳
1、二氧化碳的物理性质
(1)二氧化碳是 色 味的气体;
【观察】色、态、味?
无
无
吸热
CO2气体
无色液体
雪花状固体
干冰
加压
降温
压缩
升华
降温
注意:干冰是固体CO2
瓶子变瘪
水
CO2
振荡
(2) 二氧化碳可溶于水;
【实验探究】向一软矿泉水瓶内倒入半瓶水,振荡;
(3)二氧化碳密度比空气的密度大;
CO2
往下沉
【实验探究】如图,向纸袋中缓缓倾倒CO2,观察现象;
2、二氧化碳的化学性质
CO2
CO2
现象:
蜡烛自下而上依次熄灭。
结论:
CO2密度比空气的大。
【探究实验1】向放有高低不同的两支燃着的蜡烛的烧杯中倾倒CO2
(1)CO2不能燃烧,不能支持燃烧;
(化学性质)
(物理性质)
醋酸
【实验结论】(醋)酸能使紫色石蕊试液变红色。
紫色石蕊试液
变红色
实验①:向紫色石蕊试液中滴加醋酸
醋酸
【探究实验2】CO2与水反应
CO2
实验②:向滴有紫色石蕊试液的蒸馏水中通入CO2气体
紫色石蕊试液变红色
【分析】与实验①对比可知,该实验紫色石蕊试液变红色,
说明CO2与H2O反应生成了酸。
【结论】CO2与H2O反应生成了碳酸:
CO2+H2O = H2CO3
【结论】碳酸不稳定:H2CO3 =CO2↑+H2O
【探究实验3】H2CO3受热分解
实验③:加热实验①得到的红色溶液
红色溶液又变成紫色;
【提出问题】有人提出怀疑,使紫色石蕊变色的物质不一定是碳酸,可能是水,也可能是CO2气体。
酸能使紫色石蕊变红色
水不能使紫色石蕊变红色
CO2不能使紫色石蕊变红色
CO2与水反应生成了碳酸,使紫色石蕊变红色
【探究实验4】向澄清石灰水[Ca(OH)2]中通入CO2
澄清石灰水
变浑浊
CO2+ Ca(OH)2 = H2O +CaCO3 ↓
【分析】CO2与Ca(OH)2反应生成了
不溶于水的白色固体碳酸钙。
【结论】CO2能与澄清石灰水反应:
【归纳小结】CO2的性质
2、CO2可以与水反应;
3、CO2与澄清石灰水反应;
CO2+H2O = H2CO3
碳酸不稳定:H2CO3=CO2↑+H2O
CO2+ Ca(OH)2 = H2O +CaCO3 ↓
1、CO2是无色无味的气体;
2、CO2可溶于水;
3、CO2的密度比空气大;
物理性质
化学性质
1、CO2不能燃烧、不能 助燃,
也不能供呼吸;
灭火剂
作制冷剂
导致温室效应!
CO2
3、CO2的 利 与 弊
制汽水
作气体肥料
涨知识
CaCO3
CaO
Ca(OH)2
①
②
③
①
② CaO + H2O = Ca(OH)2
③ Ca(OH)2 + CO2 =CaCO3 ↓+H2O
烈火焚烧若等闲
粉身碎骨浑不怕
要留清白在人间
巩固练习
( )1.下列关于CO2性质的信息,正确的是:
① 可以助燃 ② 能使澄清石灰水变浑浊
③ 可溶于水,但不能与水反应
④ 可供绿色植物进行光合作用
A.②④ B.①③ C.①② D.②③
A
( )2.如图所示实验能够说明二氧化碳具有的性质有:
①不能燃烧 ②不能支持燃烧 ③还原性
④密度比空气大 ⑤密度比空气小
A.①②③ B.②③④
C.①②④ D.①②⑤
C
( )3.常温下能与二氧化碳发生化合反应的物质是:
A.水 B.澄清石灰水 C.氧气 D.木炭
A
( )4.向石蕊溶液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是:
A.红色→紫色→红色 B.紫色→红色→紫色
C.红色→紫色→蓝色 D.红色→无色→红色
B
巩固练习
巩固练习
( )5.鉴别二氧化碳和氧气,下列试剂或方法不可行的是:
A.澄清石灰水 B.燃着的木条
C.紫色石蕊试液 D.闻气味
D
( )6.下列有关CO2的实验中,只能证明CO2物理性质的实验是:
A
( )7.全球气候变暖正成为人类关注的环境问题,引起温室效应的主要气体是:
A.N2 B.O2 C.H2 D.CO2
D
( )8.下列说法不正确的是:
A.温室里施用CO2可提高农作物产量
B.干冰用于人工降雨和制冷剂,是物理变化
C.CO2属于氧化物,也属于化合物和纯净物
D.CO2的大量排放导致了酸雨的形成
D
巩固练习
( )9.下列有关“物质——性质——用途”的叙述中,用途与性质不相关的是:
序号 物质 性质 用途
A 干冰 升华时吸收热量 制冷剂
B 活性炭 吸附性 防毒面具
C 氧气 助燃性 医疗急救
D 木炭 可燃性 作燃料
C
巩固练习
巩固练习
A.④比①先红,②、③不变红
B.①比④先红,②、③不变红
C.④变红,①②③不变红
D.①变红,②③④不变红
( )10、如图所示的实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球。下列能准确描述实验现象的是:
A
11.某同学用微型实验装置(如图)制取二氧化碳并检验其性质,回答问题。
(1)试管中发生反应的化学方程式是: ______________ _。
CaCO3+2HCl CaCl2+H2O+ CO2↑
巩固练习
(2)b处出现的现象是 。
(3)根据烧杯中的变化现象,得出二氧化碳的化学性质是
。
(4)另一同学操作时,误将浓盐酸当稀盐酸使用,结果 处没有明显现象。
(5)你认为微型实验的优点是 (写一条即可)。
澄清的石灰水变浑浊
不能燃烧且不能支持燃烧
b
节约药品
巩固练习
(1)写出A、甲、乙的化学式:
A ;
甲 ;
乙 。
C
CO2
CO
12、A、B是两种常见的单质,甲、乙是两种常见的气体化合物,且组成元素相同。常温下A为黑色固体,其余均为气体。在一定条件下它们之间相互转化的关系如下图所示:
巩固练习
(2)按要求完成下列化学反应方程式:
① 甲+A反应的化学方程式:
;
② 乙+B反应的化学方程式:
。
12、A、B是两种常见的单质,甲、乙是两种常见的气体化合物,且组成元素相同。常温下A为黑色固体,其余均为气体。在一定条件下它们之间相互转化的关系如下图所示:
巩固练习
13、甲、乙、丙是初中化学中常见的物质,其中一种物质为单质,另外两种物质均为氧化物,且组成元素相同。其转化关系如右图所示:
(1)若甲为固体单质,写出相应的反应方程式。
① ;
该反应基本反应类型为______;
③ 。
化合
巩固练习
点燃
(2)若丙为气体单质,
①反应的化学方程式为:
;
该基本该反应类型为 。
分解反应
2H2O2 2H2O+O2↑
MnO2
13、甲、乙、丙是初中化学中常见的物质,其中一种物质为单质,另外两种物质均为氧化物,且组成元素相同。其转化关系如右图所示:
巩固练习
课题3 二氧化碳和一氧化碳
人教版·九年级·上册
(第二课时)一氧化碳
化学用语天天练
一、用化学方程式表示碳和碳的化合物之间的转化关系:
1、木炭燃烧:
2C + O2 2CO
点燃
C + O2 CO2
点燃
2、碳与二氧化碳在高温下反应:
C + CO2 2CO
高温
3、碳与氧化铜在高温下反应:
C+2CuO 2Cu+ CO2↑
高温
4、实验室制取二氧化碳:
CaCO3+2HCl CaCl2+H2O+ CO2↑
5、工业制取二氧化碳:
CaCO3 CaO+ CO2↑
高温
化学用语天天练
6、二氧化碳和水反应:
CO2+H2O H2CO3
7、碳酸分解:
H2CO3 H2O+ CO2↑
8、二氧化碳与澄清石灰水反应:
Ca(OH)2+CO2 CaCO3↓+H2O
【问题】CO是怎么产生的?
【解析】O2不充足时,碳不完全燃烧生成:
(剧毒气体)
2C+O2 2CO
点燃
二、一氧化碳
1、CO的物理性质
(1)通常情况下,CO是 的气体;
(3)CO 于水;
(2)CO的密度比空气的密度 ;
CO俗称煤气,有剧毒,是“隐形”杀手;
实验室收集CO能否用向下排空气法?
有人说,在燃着的煤炉上放一壶水,就可防止煤气中毒,你觉得呢?
无色、无味
略小
难溶
2、CO的化学性质
(1)CO具有 ;
① 现象:
2CO+O2 2CO2
点燃
③ 注意:与H2一样,点燃CO前,要检验纯度;
② 反应原理:
可燃性
CO燃烧时放出热量,
发出蓝色的火焰。
否则会发生爆炸!!!
(2)CO具有 ;
还原性
澄清石灰水
CuO
CO
处理尾气
黑色粉末变红色
澄清石灰水变白色浑浊
【探究实验】:CO与CuO在加热条件下反应
(Ⅰ)实验现象:
①黑色粉末变成 ;
②澄清的石灰水 。
(Ⅱ)反应原理:
CO+CuO Cu+CO2
△
(Ⅲ)尾气处理:将尾气(含CO) :
2CO+O2 2CO2
点燃
红色光亮固体
变白色浑浊
点燃
CO与CuO在加热条件下反应
(Ⅳ)CO还原CuO实验的正确步骤:
① 先通入CO气体;
③ 熄灭酒精灯;
② 加热;
④ 停止通入CO;
气
灯
灯
气
①②颠倒会爆炸!
③④颠倒会氧化!
(3)CO有 ;
CO有剧毒。这是因为CO容易与血液里的血红蛋白结合,形成碳氧血红蛋白,使血红蛋白丧失携氧的能力和作用,造成组织窒息,导致人体窒息而死亡。
毒性
【归纳小结】CO的化学性质
(1)CO具有可燃性:
(2)CO具有还原性:
(3)CO有剧毒:
易与血红蛋白结合,丧失携氧能力
3、CO的用途
(1)CO具有可燃性,常用作 ;
(2)CO具有还原性,工业上常用来 ;
燃料
冶炼金属
CO+CuO Cu+CO2
△
2CO+O2 2CO2
点燃
巩固练习
( )1.下列关于一氧化碳的说法错误的是:
A.一氧化碳能使紫色石蕊溶液变红
B.一氧化碳难溶于水
C.一氧化碳有毒,会污染空气
D.一氧化碳可用作燃料
A
( )2.下列属于有毒气体的是:
A.CO B.CO2 C.O2 D.N2
A
巩固练习
( )3.三氧化二碳(化学式C2O3)通常情况下是一种无色无味的气体,可溶于水,与水反应生成草酸,且常温下不稳定,其他的化学性质与一氧化碳相似。下列有关三氧化二碳说法错误的是:
A.C2O3中碳元素的化合价为+4价
B.三氧化二碳具有还原性
C.在空气中燃烧的产物为二氧化碳
D.C2O3有毒
A
( )4.一氧化碳有毒是因为:
A.它具有可燃性
B.它具有还原性
C.它能与血液里的氧气结合生成二氧化碳
D.它能与血液里的血红蛋白结合,使血红蛋白不能
很好地与氧气结合
D
巩固练习
( )5.下列有关碳及碳的氧化物的描述不正确的是:
A.一氧化碳可用来冶炼金属
B.一氧化碳有毒,二氧化碳无毒
C.碳在氧气中燃烧一定生成二氧化碳
D.二氧化碳是导致温室效应的主要气体之一
C
巩固练习
6.根据下列装置图回答问题:
(1)写出图中仪器a和b的名称:
a: ,b: 。
长颈漏斗
酒精灯
巩固练习
(2)装置C中产生的现象是 。
(3)装置D中产生的现象是 。
(4)装置E处气体燃烧时产生 色火焰。
(5)装置A中反应的化学方程式是:
。
黑色粉末变成光亮的红色粉末
澄清的石灰水变浑浊
蓝
CaCO3+2HCl CaCl2+H2O+ CO2↑
巩固练习
7.碳和部分碳的化合物间转化关系如图所示,请回答下列问题:
(1)物质X的化学式为 。
(2)从图中任选一种物质,说说它的一种用途: 。
CO2
CO可作燃料
巩固练习
(3)写出在此题中涉及的五个化合反应的化学方程式:
① ;
② ;
③ ;
④ ;
⑤ 。
2C + O2 2CO
点燃
C + O2 CO2
点燃
C + CO2 2CO
高温
CO2+H2O H2CO3
巩固练习
2CO+O2 2CO2
8、右图是木炭还原氧化铜的探究实验装置。
【提出问题】木炭还原氧化铜产生什么气体?
【提出猜想】产生的气体有三种情况:
① 只有CO
② 只有CO2
③_______________。
CO与CO2
巩固练习
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,数据设计如下:
称量对象 反应前质量 反应后质量 质量差
试管+固体混合物 M1 M2 △m1即( M1-M2)
烧杯+澄清石灰水 M3 M4 △m2即( M4-M3)
(1)若△m2=0,则猜想 成立。
(2)若猜想②正确,理论上△m1与△m2 的关系是:
△m1 △m2(填“>”、“<”或“=”)。
①
=
巩固练习
【实验并记录】实验得到的数据如下表:
称量对象 反应前质量 反应后质量 质量差
试管+固体混合物 69.8g 65.4g △m1
烧杯+澄清石灰水 118.8g 122.6g △m2
【得出结论】通过对表中实验数据分析,最终确定是猜想_______成立。
③
巩固练习
本课题已学完,请及时巩固复习!
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
