8.2金属的化学性质同步练习—2021-2022学年九年级化学人教版下册(word版 含解析)
文档属性
| 名称 | 8.2金属的化学性质同步练习—2021-2022学年九年级化学人教版下册(word版 含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 127.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-07 00:00:00 | ||
图片预览


文档简介
金属的化学性质
一、单选题
下列化学反应中不属于置换反应的是
A. B.
C. D.
下列金属中,不能从溶液中置换出的是
A. B. C. D.
利用盐酸和硝酸银探究铁、铜、银的金属活动顺序,下列实验可以不需要进行的是
A. 铁稀盐酸 B. 铜稀盐酸
C. 银稀盐酸 D. 铜硝酸银溶液
某化学兴趣小组为验证、、三种金属的活动性顺序,设计了如图所示的实验操作。其中可以达到实验目的的组合是
A. 或或 B. 或或
C. 或或 D. 或或
镍和锰都是重要的金属,将丝插入溶液中,无明显现象;插入溶液中,丝表面有红色固体析出,则这三种金属的活动性由强到弱的顺序是
A. 、、 B. 、、
C. 、、 D. 、、
探究锌、铜、镁的金属活动性时,下列现象、分析或结论正确的是
A. 盐酸的浓度可以不同
B. 铜片表面有气泡
C. 镁片的试管表面发烫
D. 活动性
下列物质可通过金属与稀盐酸反应直接得到的是
A. B. C. D.
下列物质可以由相应的金属和酸发生置换反应而制得的是
A. B. C. D.
下列物质不能用来鉴别铁和银的是
A. 磁铁 B. 硝酸银溶液 C. 稀硫酸 D. 硫酸锌溶液
下列不能与稀盐酸反应的金属是
A. B. C. D.
在金属化学性质的实验中,下列操作不能达成实验目的是
选项 实验目的 实验操作
研究金属是否都能与盐酸反应 将镁、锌、铜片分别放入稀盐酸中
证明不同金属与酸反应的剧烈程度不同 将铜和银分别放入稀盐酸中
证明铁的活动性比铜强 将铁放入硫酸铜溶液中
比较锌和铜的金属活动性 将锌和铜分别放入稀硫酸中
A. B. C. D.
往硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后有金属析出,过滤后往滤渣中加入稀盐酸,有无色气体放出,则滤渣中一定存在的金属是
A. 、 B. 、
C. 、 D. 、、
二、实验题
某同学为了探究相关金属的化学性质,做了下列实验:
试管中的实验现象是____________________。
只通过和实验尚不能证明铜、银两种金属的活动性强弱,需补充一个实验来证明,补充实验所用试剂合理的是________________。
A.、、稀盐酸 、溶液
实验中物质充分反应后,某同学对试管中固体的成分提出以下四种猜想:
A.、、 、 、
这四种猜想中明显不合理的是________填编号。
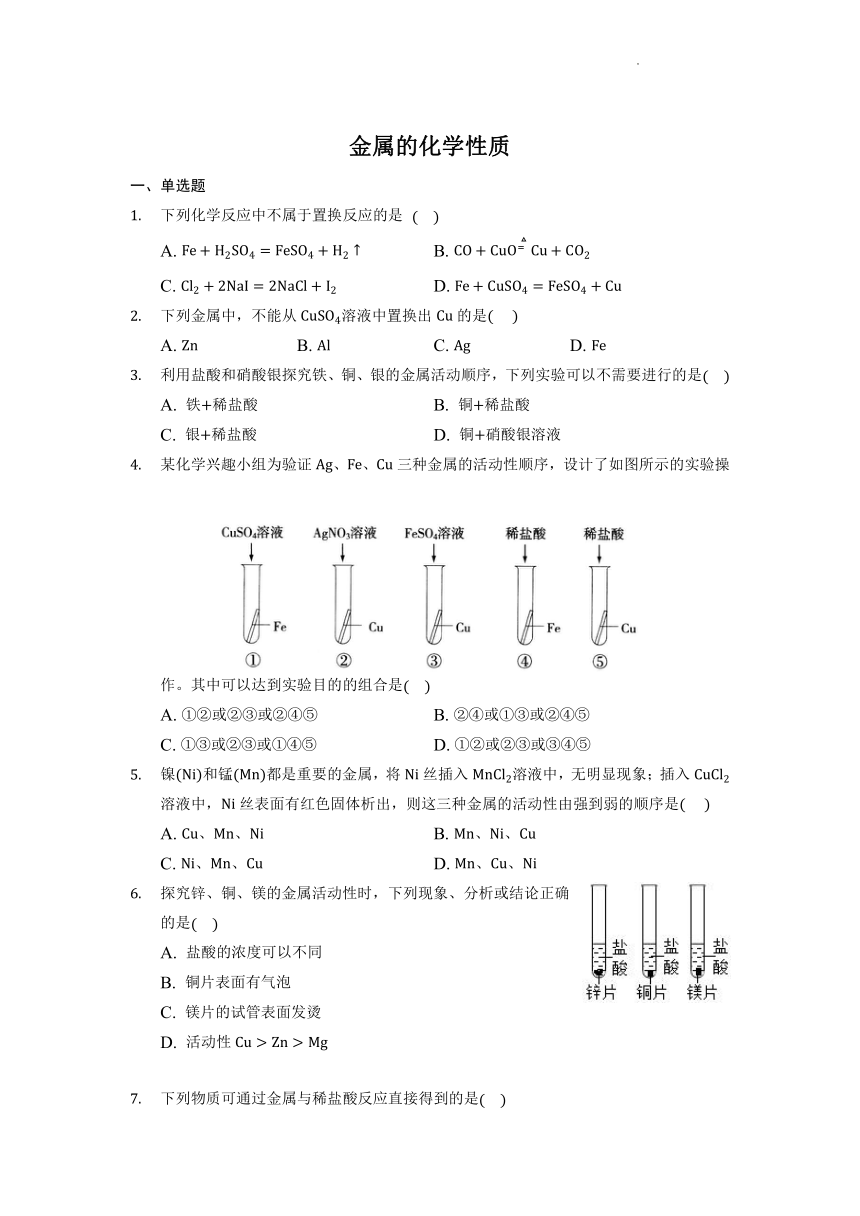
为探究铁、铜、银三种金属的活动性顺序,设计了、两个方案
能验证三种金属活动性顺序的方案是______。
方案中,发生反应的化学方程式是______。
方案中,证明铁的活动性比铜强的现象是______。
方案 方案
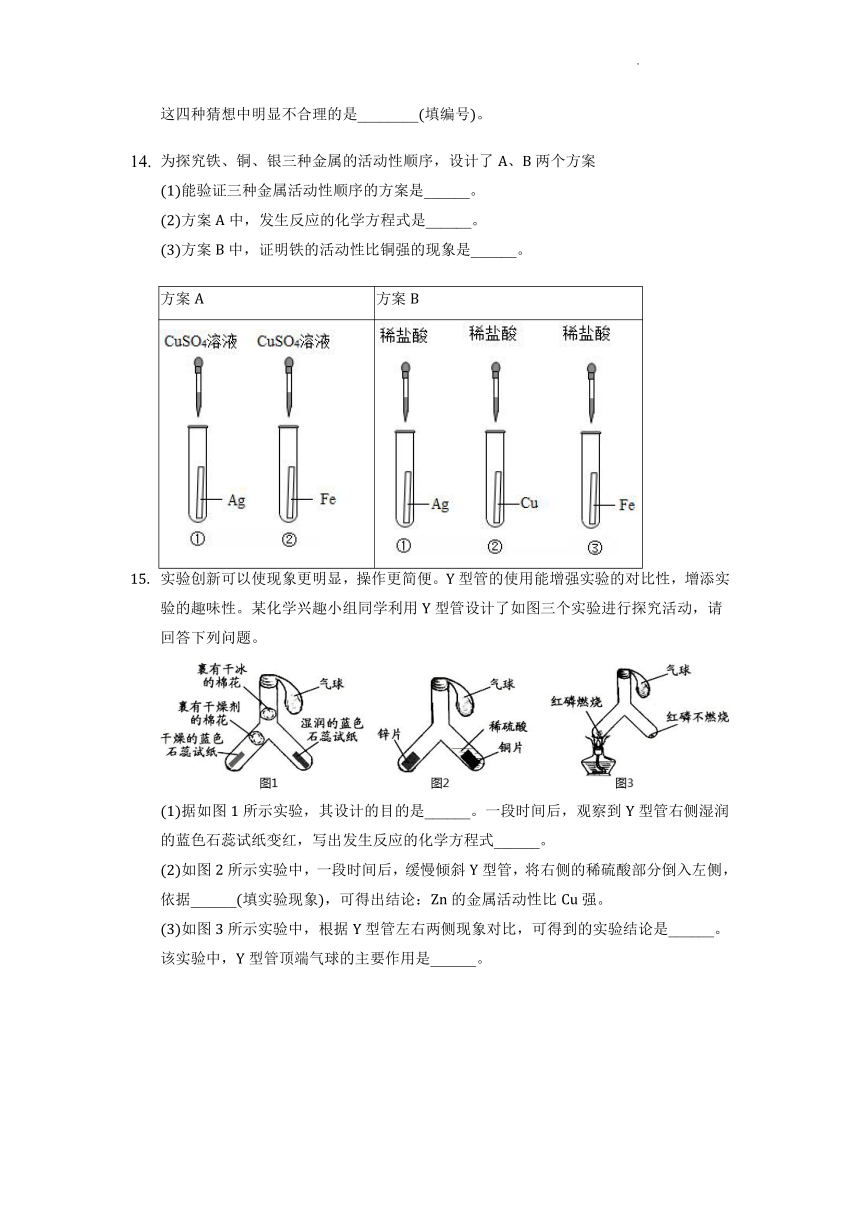
实验创新可以使现象更明显,操作更简便。型管的使用能增强实验的对比性,增添实验的趣味性。某化学兴趣小组同学利用型管设计了如图三个实验进行探究活动,请回答下列问题。
据如图所示实验,其设计的目的是______。一段时间后,观察到型管右侧湿润的蓝色石蕊试纸变红,写出发生反应的化学方程式______。
如图所示实验中,一段时间后,缓慢倾斜型管,将右侧的稀硫酸部分倒入左侧,依据______填实验现象,可得出结论:的金属活动性比强。
如图所示实验中,根据型管左右两侧现象对比,可得到的实验结论是______。该实验中,型管顶端气球的主要作用是______。
答案和解析
1.【答案】
【解答】
A、,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误。
B、,该反应的反应物均为化合物,不属于置换反应,故选项正确。
C、,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误。
D、,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误。
故选:。
2.【答案】
3.【答案】
【解答】
A.通过铁稀盐酸反应,可以判断铁在氢的前边;
B.通过铜稀盐酸不反应,可以判断铜在氢的后面;
C.通过银稀盐酸不反应,可以判断银在氢的后面;
D.通过铜硝酸银溶液反应,可以判断铜在银的前边。
综合以上分析可知,通过、、就可以比较出铁、铜、银的金属活动性顺序,可以不必进行的是。
故选C。
4.【答案】
【解析】中铁与溶液反应置换出铜,说明金属活动性:铁铜,中铜与硝酸银溶液反应生成银,说明金属活动性:铜银,组合可得出三种金属活动性:铁铜银;中铜与硫酸亚铁溶液不反应,说明铜的金属活动性比铁弱,即活动性:铁铜,组合可得出三种金属活动性:铁铜银;中铁与稀盐酸反应置换出氢气,说明活动性:铁氢,中铜与稀盐酸不反应,说明活动性:氢铜,可说明金属活动性:铁铜,组合可得出三种金属活动性:铁铜银,选项正确。
5.【答案】
【解析】由题意可知,将镍丝插入溶液中,无明显现象,说明锰比镍活泼;将镍丝插入溶液中,镍丝表面有红色固体析出,说明镍比铜活泼,则、、的活动性由强到弱的顺序是。
6.【答案】
【解答】
A、探究锌、铜、镁的金属活动性时,要注意变量的控制,即除探究要素不同之外,其它条件应该保持相同,则盐酸的浓度必须相同,故选项说法错误;
B、铜的金属活动性比氢弱,与稀盐酸不反应,铜片表面无明显变化,故选项说法错误;
C、金属与酸的反应属于放热反应,镁片的试管表面会发烫,故选项说法正确;
D、根据金属活动性顺序,活动性,故选项说法错误。
故选C。
7.【答案】
【解析】解:、在金属活动性顺序中,铜排在氢后面,铜和盐酸不能发生反应,不能生成氯化铜,故选项错误。
B、在金属活动性顺序中,银排在氢后面,银和盐酸不能发生反应,不能生成氯化银,故选项错误。
C、在金属活动性顺序中,锌排在氢前面,锌和盐酸反应生成氯化锌和氢气,故选项正确。
D、在金属活动性顺序中,铁排在氢前面,能和盐酸反应生成氯化亚铁和氢气,不能生成氯化铁,故选项错误。
8.【答案】
【解答】
A.铁的金属活动性在氢前,能与稀硫酸发生置换反应,但生成的是硫酸亚铁,而非硫酸铁,故A不符合题意;
B.铜的金属活动性在氢后,所以不能与稀盐酸发生置换反应生成氯化铜,故B不符合题意;
C.银的金属活动性在氢后,所以不能与稀盐酸发生置换反应生成氯化银,故C不符合题意;
D.铝的金属活动性在氢前,所以能与稀硫酸发生置换反应生成氢气和硫酸铝,故D符合题意。
故选D。
9.【答案】
【解析】解:、磁铁能吸附铁不能吸附银,现象不同,可以鉴别;
B、硝酸银溶液能与铁反应不能与银反应,现象不同,可以鉴别;
C、稀硫酸能与铁反应不能与硝酸银,现象不同,可以鉴别;
D、硫酸锌溶液与铁和银都不反应,没有现象,现象相同,无法鉴别。
10.【答案】
【解析】金属活动性顺序中,后面的金属不能和稀酸发生置换反应。
11.【答案】
【解析】解:、将镁、锌、铜片分别放入稀盐酸中,能研究金属是否都能与盐酸反应,故A不符合题意;
B、将铜和银分别放入稀盐酸中,都不反应,无法比较不同金属与酸反应的剧烈程度不同,故B符合题意;
C、将铁放入硫酸铜溶液中,铁能将铜置换出来,证明铁的活动性比铜强,故C不符合题意;
D、将锌和铜分别放入稀硫酸中,锌能反应,铜不反应,能比较锌和铜的金属活动性,故D不符合题意。
12.【答案】
【解答】
根据题意“滤渣中加入稀盐酸,有无色气体放出”说明铁粉剩余,根据在金属活动顺序表中排在前面的金属就能把排在后面的金属从其盐溶液中置换出来,可知铁粉可以和反应,分别置换出银和铜。
所以滤渣中一定存在铁、银和铜。
故选D。
13.【答案】锌片表面覆盖一层红色固体物质,溶液由蓝色逐渐变为无色
14.【答案】;
;
铁能与稀盐酸反应生成气体,铜与稀盐酸不反应。
【解析】解:银与溶液不反应,说明了金属活动性铜银;铁与溶液反应置换出铜,说明了金属活动性铁铜;由此可得出三种金属活动性铁铜银。
铁能与稀盐酸反应生成氢气,铜、银均不能与稀盐酸反应,无法确定银和铜的活动性强弱。
方案中,铁与溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式为。
方案中,证明铁的活动性比铜强的现象是铁能与稀盐酸反应生成气体,铜与稀盐酸不反应。
15.【答案】验证二氧化碳能与水反应;;
产生大量气泡;
燃烧的条件之一是温度需要达到着火点;防止红磷燃烧产生的五氧化二磷污染空气
【解析】解:根据图中实验,干燥的蓝色石蕊试纸不变色,湿润的蓝色石蕊试纸变红色,是因为二氧化碳与水反应生成碳酸,设计的目的是验证二氧化碳能与水反应,反应的化学方程式为。
图中实验,铜与稀硫酸不反应,一段时间后,缓慢倾斜型管,将右侧的稀硫酸部分倒入左侧,产生大量气泡,说明锌能与稀硫酸反应,说明的金属活动性比强。
根据型管左右两侧现象对比,左侧的红磷能燃烧,右侧的红磷不能燃烧,是因为左侧的红磷温度达到了着火点,说明燃烧的条件之一是温度需要达到着火点。
红磷燃烧放出大量的热,产生有毒物质五氧化二磷,型管顶端气球的主要作用是防止红磷燃烧产生的五氧化二磷污染空气。
第2页,共2页
一、单选题
下列化学反应中不属于置换反应的是
A. B.
C. D.
下列金属中,不能从溶液中置换出的是
A. B. C. D.
利用盐酸和硝酸银探究铁、铜、银的金属活动顺序,下列实验可以不需要进行的是
A. 铁稀盐酸 B. 铜稀盐酸
C. 银稀盐酸 D. 铜硝酸银溶液
某化学兴趣小组为验证、、三种金属的活动性顺序,设计了如图所示的实验操作。其中可以达到实验目的的组合是
A. 或或 B. 或或
C. 或或 D. 或或
镍和锰都是重要的金属,将丝插入溶液中,无明显现象;插入溶液中,丝表面有红色固体析出,则这三种金属的活动性由强到弱的顺序是
A. 、、 B. 、、
C. 、、 D. 、、
探究锌、铜、镁的金属活动性时,下列现象、分析或结论正确的是
A. 盐酸的浓度可以不同
B. 铜片表面有气泡
C. 镁片的试管表面发烫
D. 活动性
下列物质可通过金属与稀盐酸反应直接得到的是
A. B. C. D.
下列物质可以由相应的金属和酸发生置换反应而制得的是
A. B. C. D.
下列物质不能用来鉴别铁和银的是
A. 磁铁 B. 硝酸银溶液 C. 稀硫酸 D. 硫酸锌溶液
下列不能与稀盐酸反应的金属是
A. B. C. D.
在金属化学性质的实验中,下列操作不能达成实验目的是
选项 实验目的 实验操作
研究金属是否都能与盐酸反应 将镁、锌、铜片分别放入稀盐酸中
证明不同金属与酸反应的剧烈程度不同 将铜和银分别放入稀盐酸中
证明铁的活动性比铜强 将铁放入硫酸铜溶液中
比较锌和铜的金属活动性 将锌和铜分别放入稀硫酸中
A. B. C. D.
往硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后有金属析出,过滤后往滤渣中加入稀盐酸,有无色气体放出,则滤渣中一定存在的金属是
A. 、 B. 、
C. 、 D. 、、
二、实验题
某同学为了探究相关金属的化学性质,做了下列实验:
试管中的实验现象是____________________。
只通过和实验尚不能证明铜、银两种金属的活动性强弱,需补充一个实验来证明,补充实验所用试剂合理的是________________。
A.、、稀盐酸 、溶液
实验中物质充分反应后,某同学对试管中固体的成分提出以下四种猜想:
A.、、 、 、
这四种猜想中明显不合理的是________填编号。
为探究铁、铜、银三种金属的活动性顺序,设计了、两个方案
能验证三种金属活动性顺序的方案是______。
方案中,发生反应的化学方程式是______。
方案中,证明铁的活动性比铜强的现象是______。
方案 方案
实验创新可以使现象更明显,操作更简便。型管的使用能增强实验的对比性,增添实验的趣味性。某化学兴趣小组同学利用型管设计了如图三个实验进行探究活动,请回答下列问题。
据如图所示实验,其设计的目的是______。一段时间后,观察到型管右侧湿润的蓝色石蕊试纸变红,写出发生反应的化学方程式______。
如图所示实验中,一段时间后,缓慢倾斜型管,将右侧的稀硫酸部分倒入左侧,依据______填实验现象,可得出结论:的金属活动性比强。
如图所示实验中,根据型管左右两侧现象对比,可得到的实验结论是______。该实验中,型管顶端气球的主要作用是______。
答案和解析
1.【答案】
【解答】
A、,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误。
B、,该反应的反应物均为化合物,不属于置换反应,故选项正确。
C、,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误。
D、,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误。
故选:。
2.【答案】
3.【答案】
【解答】
A.通过铁稀盐酸反应,可以判断铁在氢的前边;
B.通过铜稀盐酸不反应,可以判断铜在氢的后面;
C.通过银稀盐酸不反应,可以判断银在氢的后面;
D.通过铜硝酸银溶液反应,可以判断铜在银的前边。
综合以上分析可知,通过、、就可以比较出铁、铜、银的金属活动性顺序,可以不必进行的是。
故选C。
4.【答案】
【解析】中铁与溶液反应置换出铜,说明金属活动性:铁铜,中铜与硝酸银溶液反应生成银,说明金属活动性:铜银,组合可得出三种金属活动性:铁铜银;中铜与硫酸亚铁溶液不反应,说明铜的金属活动性比铁弱,即活动性:铁铜,组合可得出三种金属活动性:铁铜银;中铁与稀盐酸反应置换出氢气,说明活动性:铁氢,中铜与稀盐酸不反应,说明活动性:氢铜,可说明金属活动性:铁铜,组合可得出三种金属活动性:铁铜银,选项正确。
5.【答案】
【解析】由题意可知,将镍丝插入溶液中,无明显现象,说明锰比镍活泼;将镍丝插入溶液中,镍丝表面有红色固体析出,说明镍比铜活泼,则、、的活动性由强到弱的顺序是。
6.【答案】
【解答】
A、探究锌、铜、镁的金属活动性时,要注意变量的控制,即除探究要素不同之外,其它条件应该保持相同,则盐酸的浓度必须相同,故选项说法错误;
B、铜的金属活动性比氢弱,与稀盐酸不反应,铜片表面无明显变化,故选项说法错误;
C、金属与酸的反应属于放热反应,镁片的试管表面会发烫,故选项说法正确;
D、根据金属活动性顺序,活动性,故选项说法错误。
故选C。
7.【答案】
【解析】解:、在金属活动性顺序中,铜排在氢后面,铜和盐酸不能发生反应,不能生成氯化铜,故选项错误。
B、在金属活动性顺序中,银排在氢后面,银和盐酸不能发生反应,不能生成氯化银,故选项错误。
C、在金属活动性顺序中,锌排在氢前面,锌和盐酸反应生成氯化锌和氢气,故选项正确。
D、在金属活动性顺序中,铁排在氢前面,能和盐酸反应生成氯化亚铁和氢气,不能生成氯化铁,故选项错误。
8.【答案】
【解答】
A.铁的金属活动性在氢前,能与稀硫酸发生置换反应,但生成的是硫酸亚铁,而非硫酸铁,故A不符合题意;
B.铜的金属活动性在氢后,所以不能与稀盐酸发生置换反应生成氯化铜,故B不符合题意;
C.银的金属活动性在氢后,所以不能与稀盐酸发生置换反应生成氯化银,故C不符合题意;
D.铝的金属活动性在氢前,所以能与稀硫酸发生置换反应生成氢气和硫酸铝,故D符合题意。
故选D。
9.【答案】
【解析】解:、磁铁能吸附铁不能吸附银,现象不同,可以鉴别;
B、硝酸银溶液能与铁反应不能与银反应,现象不同,可以鉴别;
C、稀硫酸能与铁反应不能与硝酸银,现象不同,可以鉴别;
D、硫酸锌溶液与铁和银都不反应,没有现象,现象相同,无法鉴别。
10.【答案】
【解析】金属活动性顺序中,后面的金属不能和稀酸发生置换反应。
11.【答案】
【解析】解:、将镁、锌、铜片分别放入稀盐酸中,能研究金属是否都能与盐酸反应,故A不符合题意;
B、将铜和银分别放入稀盐酸中,都不反应,无法比较不同金属与酸反应的剧烈程度不同,故B符合题意;
C、将铁放入硫酸铜溶液中,铁能将铜置换出来,证明铁的活动性比铜强,故C不符合题意;
D、将锌和铜分别放入稀硫酸中,锌能反应,铜不反应,能比较锌和铜的金属活动性,故D不符合题意。
12.【答案】
【解答】
根据题意“滤渣中加入稀盐酸,有无色气体放出”说明铁粉剩余,根据在金属活动顺序表中排在前面的金属就能把排在后面的金属从其盐溶液中置换出来,可知铁粉可以和反应,分别置换出银和铜。
所以滤渣中一定存在铁、银和铜。
故选D。
13.【答案】锌片表面覆盖一层红色固体物质,溶液由蓝色逐渐变为无色
14.【答案】;
;
铁能与稀盐酸反应生成气体,铜与稀盐酸不反应。
【解析】解:银与溶液不反应,说明了金属活动性铜银;铁与溶液反应置换出铜,说明了金属活动性铁铜;由此可得出三种金属活动性铁铜银。
铁能与稀盐酸反应生成氢气,铜、银均不能与稀盐酸反应,无法确定银和铜的活动性强弱。
方案中,铁与溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式为。
方案中,证明铁的活动性比铜强的现象是铁能与稀盐酸反应生成气体,铜与稀盐酸不反应。
15.【答案】验证二氧化碳能与水反应;;
产生大量气泡;
燃烧的条件之一是温度需要达到着火点;防止红磷燃烧产生的五氧化二磷污染空气
【解析】解:根据图中实验,干燥的蓝色石蕊试纸不变色,湿润的蓝色石蕊试纸变红色,是因为二氧化碳与水反应生成碳酸,设计的目的是验证二氧化碳能与水反应,反应的化学方程式为。
图中实验,铜与稀硫酸不反应,一段时间后,缓慢倾斜型管,将右侧的稀硫酸部分倒入左侧,产生大量气泡,说明锌能与稀硫酸反应,说明的金属活动性比强。
根据型管左右两侧现象对比,左侧的红磷能燃烧,右侧的红磷不能燃烧,是因为左侧的红磷温度达到了着火点,说明燃烧的条件之一是温度需要达到着火点。
红磷燃烧放出大量的热,产生有毒物质五氧化二磷,型管顶端气球的主要作用是防止红磷燃烧产生的五氧化二磷污染空气。
第2页,共2页
同课章节目录
