专题8金属和金属材料检测题-2021-2022学年九年级化学仁爱版下册(word版有答案)
文档属性
| 名称 | 专题8金属和金属材料检测题-2021-2022学年九年级化学仁爱版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 147.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-07 00:00:00 | ||
图片预览


文档简介
专题8 金属和金属材料 检测题
一、单选题
1.下列反应中,吸收热量的是
A.生石灰与水反应 B.硫燃烧
C.镁与稀盐酸反应 D.碳与二氧化碳反应
2.下列有关物质的性质与用途具有对应关系的是
A.铝导热性好,可用于制作炊具
B.氮气难溶于水,可用作保护气
C.一氧化碳有毒性,可用于炼铁
D.活性炭具有吸附性,可用作干燥剂
3.如图所示:将铁钉置于水中,则铁钉三个不同部位,最先生锈的是
A.a处 B.b处 C.c处 D.以上都有可能
4.化学就在我们身边,下列说法或做法中正确的是
A.用洗洁精清洗油污是因为洗洁精能溶解油污
B.用伍德合金做保险丝利用了它熔点低的物理性质
C.用活性炭净水是因为活性炭有吸附性,这属于它的化学性质
D.测定空气中氧气含量的实验中,未等装置冷却就读数会使测量结果偏大
5.化学知识常应用在生活中,下列做法正确的是
A.铁锅炖鱼后,应将铁锅洗净后擦干并放于干燥处
B.学校计算机房里放置了很多精密仪器建议配用干粉灭火器
C.发生一氧化碳中毒时,要立即送到医院救治
D.用炉具清洁剂清洗沾有油污的羊毛外套
6.现有一块合金,其质量为35g,使它与足量的稀硫酸完全反应后生成氢气2g,则此合金的组成可能为
A.和 B.和 C.和 D.和
7.下列图像与对应的叙述相符合的是
A.电解一定质量的水
B.高温煅烧一定质量的石灰石
C.氢气和氧气在密闭容器中燃烧
D.向等质量的铁和锌粉中分别逐滴加入相同的稀硫酸至过量
8.下列各组中,除去杂质所选用的试剂或方法正确的是
组别 物质 杂质(少量) 除杂试剂或操作方法
A CO CO2 通过灼热的氧化铜
B CuO C 隔绝空气加强热
C FeSO4 溶液 CuSO4 加入过量的锌粉,过滤
D 铜粉 镁粉 加入足量稀硫酸溶液,过滤、洗涤、烘干
A.A B.B C.C D.D
9.下列图象中正确的是
A. 甲:向相同质量的铁粉和锌粉中分别加入足量稀盐酸
B. 乙:向三份等质量、等浓度的稀盐酸中分别加入足量的镁、铝、铁
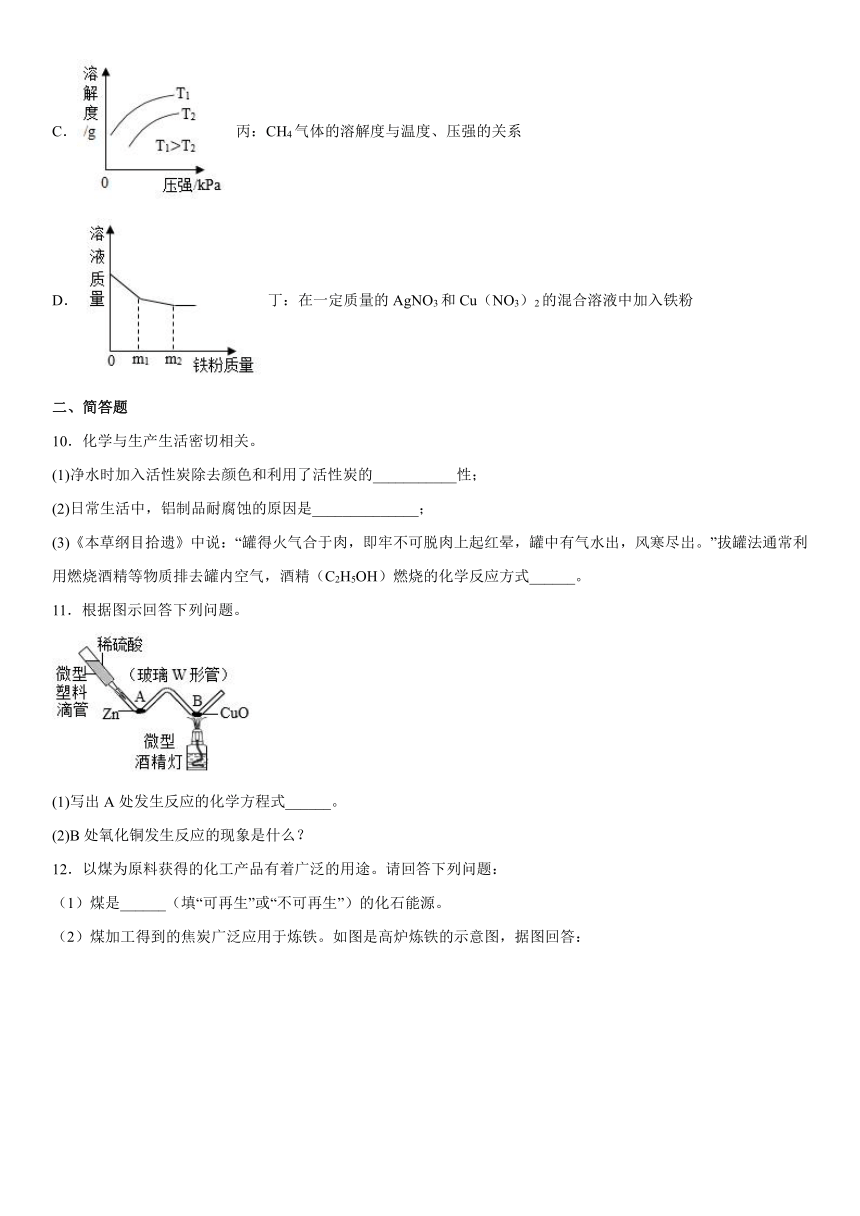
C. 丙:CH4气体的溶解度与温度、压强的关系
D. 丁:在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉
二、简答题
10.化学与生产生活密切相关。
(1)净水时加入活性炭除去颜色和利用了活性炭的___________性;
(2)日常生活中,铝制品耐腐蚀的原因是______________;
(3)《本草纲目拾遗》中说:“罐得火气合于肉,即牢不可脱肉上起红晕,罐中有气水出,风寒尽岀。”拔罐法通常利用燃烧酒精等物质排去罐内空气,酒精(C2H5OH)燃烧的化学反应方式______。
11.根据图示回答下列问题。
(1)写出A处发生反应的化学方程式______。
(2)B处氧化铜发生反应的现象是什么?
12.以煤为原料获得的化工产品有着广泛的用途。请回答下列问题:
(1)煤是______(填“可再生”或“不可再生”)的化石能源。
(2)煤加工得到的焦炭广泛应用于炼铁。如图是高炉炼铁的示意图,据图回答:
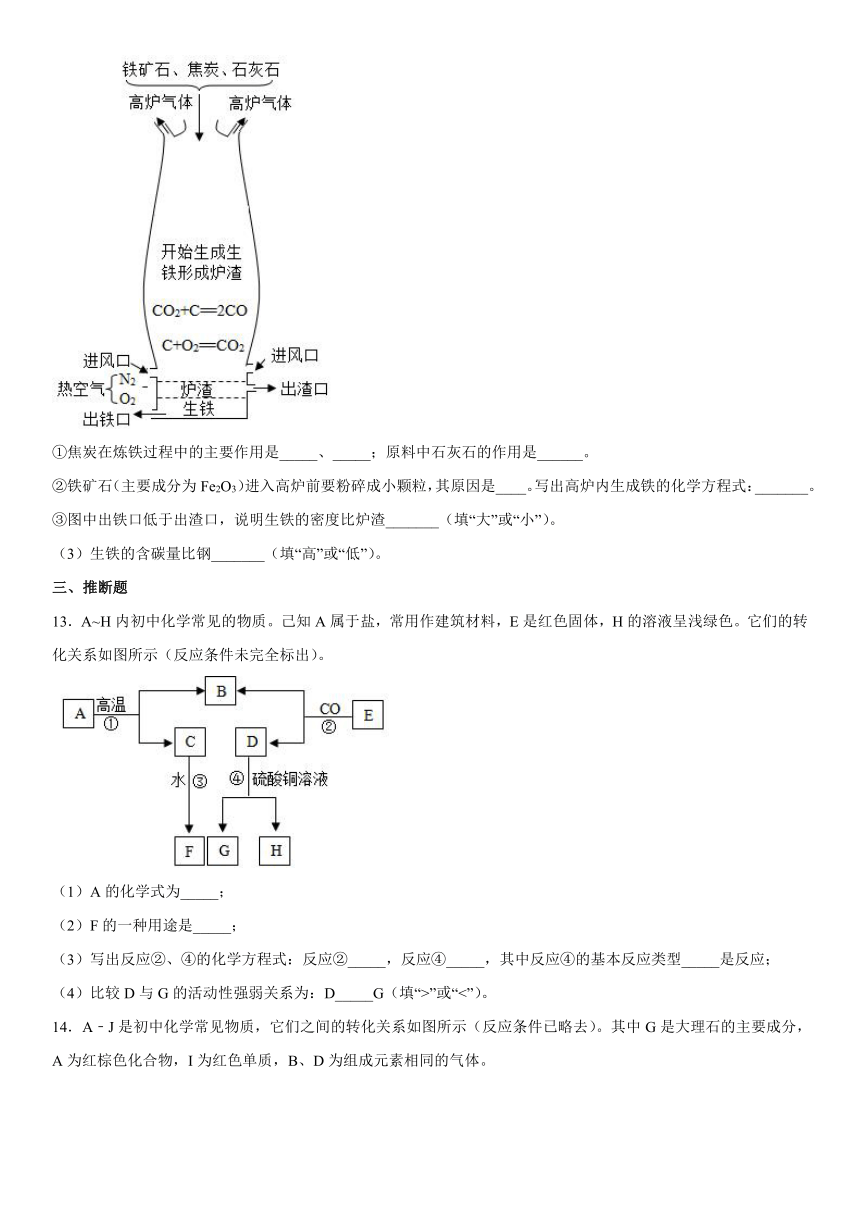
①焦炭在炼铁过程中的主要作用是_____、_____;原料中石灰石的作用是______。
②铁矿石(主要成分为Fe2O3)进入高炉前要粉碎成小颗粒,其原因是____。写出高炉内生成铁的化学方程式:_______。
③图中出铁口低于出渣口,说明生铁的密度比炉渣_______(填“大”或“小”)。
(3)生铁的含碳量比钢_______(填“高”或“低”)。
三、推断题
13.A~H内初中化学常见的物质。己知A属于盐,常用作建筑材料,E是红色固体,H的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全标出)。
(1)A的化学式为_____;
(2)F的一种用途是_____;
(3)写出反应②、④的化学方程式:反应②_____,反应④_____,其中反应④的基本反应类型_____是反应;
(4)比较D与G的活动性强弱关系为:D_____G(填“>”或“<”)。
14.A﹣J是初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去)。其中G是大理石的主要成分,A为红棕色化合物,I为红色单质,B、D为组成元素相同的气体。
请回答下列问题:
(1)I的化学式为_____。
(2)反应①的反应化学方程式为_____。
(3)反应②的反应化学方程式为_____。
(4)反应③的基本反应类型为_____。
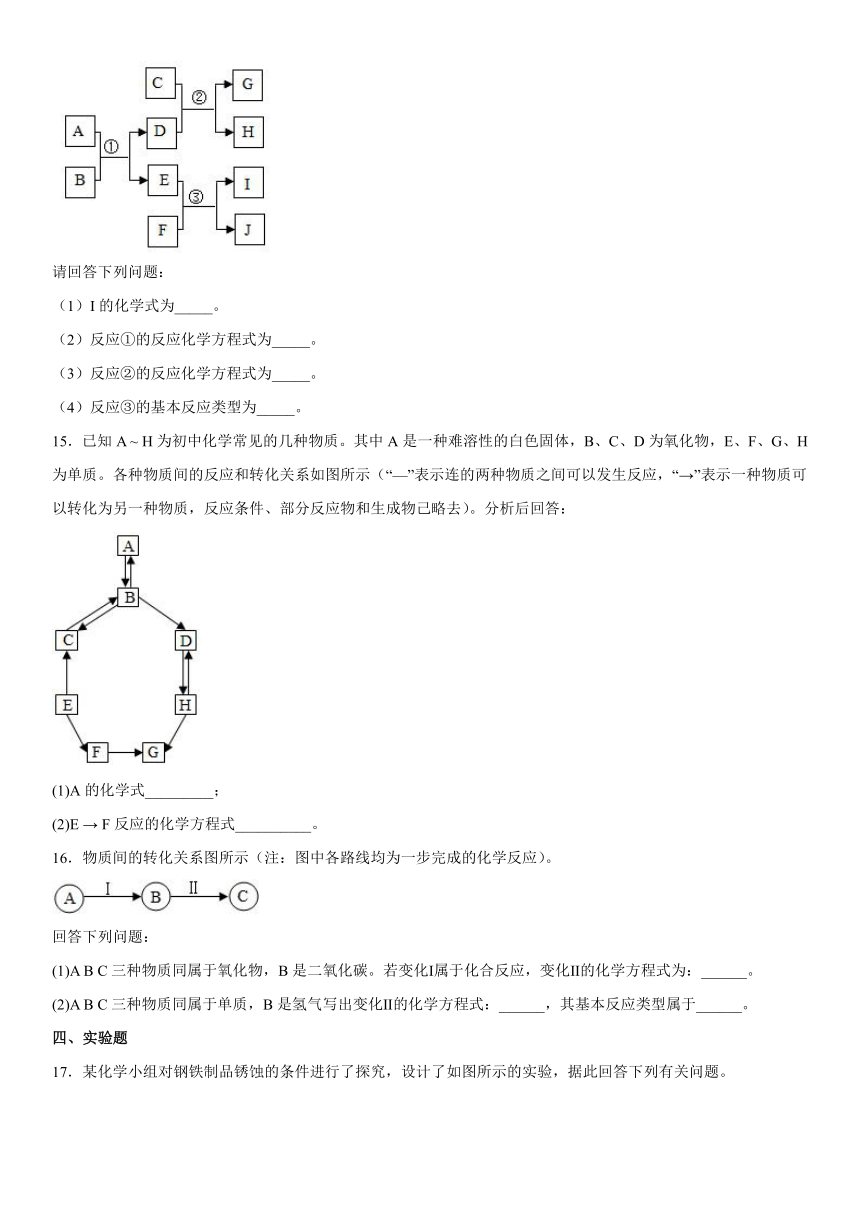
15.已知A ~ H为初中化学常见的几种物质。其中A是一种难溶性的白色固体,B、C、D为氧化物,E、F、G、H为单质。各种物质间的反应和转化关系如图所示(“—”表示连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物己略去)。分析后回答:
(1)A的化学式_________;
(2)E → F反应的化学方程式__________。
16.物质间的转化关系图所示(注:图中各路线均为一步完成的化学反应)。
回答下列问题:
(1)A B C三种物质同属于氧化物,B是二氧化碳。若变化Ⅰ属于化合反应,变化Ⅱ的化学方程式为:______。
(2)A B C三种物质同属于单质,B是氢气写出变化Ⅱ的化学方程式:______,其基本反应类型属于______。
四、实验题
17.某化学小组对钢铁制品锈蚀的条件进行了探究,设计了如图所示的实验,据此回答下列有关问题。
(1)三天后,观察到序号为______的试管中的铁钉明显生锈,铁钉未生锈的是______。
(2)对照实验①和③,可知铁锈蚀的条件是什么______?
18.下图是实验室模拟炼铁的实验装置。请回答下列问题:
(1)写出一氧化碳还原氧化铁的化学反应方程式:_______
(2)写出上图实验中发生化学反应的实验现象:_______
五、计算题
19.小鸿设计如下实验,探究粗锌粒中锌的质量分数(粗锌所含的杂质不跟稀硫酸反应)。
计算:(写出计算过程)
(1)粗锌中锌的质量分数。(精确到0.1%)
(2)100g稀硫酸中硫酸的质量。
20.(1)2021河南春晚《唐宫夜宴》曾被刷上热搜,节目中展出的青铜器历史悠久,西汉时期就记载有“曾青(硫酸铜)得铁则化为铜”。请用化学方程式表示其原理。
(2)硅芯片是很多电子产品的核心。下面是某种制取硅反应的微观示意图,请计算反应前后乙与丁变化的质量比是多少?
21.锌与稀硫酸(H2SO4)反应生成氢气和硫酸锌。某实验小组将一定量的锌投入足量稀硫酸中,充分反应。产生氢气的质量与反应时间的关系如图所示:(反应方程式为:Zn+H2SO4=ZnSO4+H2↑)
(1)ZnSO4的相对分子质量为 ;
(2)反应生成的氢气的质量为 g;
(3)参加反应的锌的质量是多少?
22.请你仔细分析如图所示的实验过程和提供的数据,计算反应后所得溶液中溶质的质量分数是____?
试卷第1页,共3页
参考答案:
1.D
2.A
3.B
4.B
5.A
6.D
7.D
8.D
9.D
10.(1)吸附
(2)铝在空气中和氧气反应产生一层致密的氧化膜,阻止铝被腐蚀
(3)
11.(1)Zn+H2SO4= ZnSO4+H2↑
(2)黑色固体变为红色,W形管内壁有水珠生成
12. 不可再生 提供反应所需的热量 产生CO 将矿石中二氧化硅转化为炉渣 增大接触面积,加快反应速率,氧化铁反应更充分 3CO+ Fe2O3 2Fe + 3CO2 大 高
13. CaCO3 用作建筑材料、保护树木、配制农药波尔多液、改良酸性土壤等(任选一,合理均可) 置换 >
14. Cu Fe2O3+3CO2Fe+3CO2 CO2+Ca(OH)2═CaCO3↓+H2O 置换反应
15.(1)CaCO3
(2)或
16.(1)
(2)
置换反应
17. ③ ①② 要与水分接触
18.(1)
(2)玻璃管中红色粉末变黑色,石灰水变浑浊,末端导管有蓝色火焰
19.(1)解:设粗锌中锌的质量为x,100g稀硫酸中硫酸的质量为y
解得x=6.5g,y=9.8g
所以粗锌中锌的质量分数
答:粗锌中锌的质量分数为65%。
(2)答:100g稀硫酸中硫酸的质量为9.8g。
20.(1)
(2)2:73
21.(1)161
(2)0.4
(3)设参加反应的锌的质量为
答:参加反应的锌的质量是13g。
22.12.7%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列反应中,吸收热量的是
A.生石灰与水反应 B.硫燃烧
C.镁与稀盐酸反应 D.碳与二氧化碳反应
2.下列有关物质的性质与用途具有对应关系的是
A.铝导热性好,可用于制作炊具
B.氮气难溶于水,可用作保护气
C.一氧化碳有毒性,可用于炼铁
D.活性炭具有吸附性,可用作干燥剂
3.如图所示:将铁钉置于水中,则铁钉三个不同部位,最先生锈的是
A.a处 B.b处 C.c处 D.以上都有可能
4.化学就在我们身边,下列说法或做法中正确的是
A.用洗洁精清洗油污是因为洗洁精能溶解油污
B.用伍德合金做保险丝利用了它熔点低的物理性质
C.用活性炭净水是因为活性炭有吸附性,这属于它的化学性质
D.测定空气中氧气含量的实验中,未等装置冷却就读数会使测量结果偏大
5.化学知识常应用在生活中,下列做法正确的是
A.铁锅炖鱼后,应将铁锅洗净后擦干并放于干燥处
B.学校计算机房里放置了很多精密仪器建议配用干粉灭火器
C.发生一氧化碳中毒时,要立即送到医院救治
D.用炉具清洁剂清洗沾有油污的羊毛外套
6.现有一块合金,其质量为35g,使它与足量的稀硫酸完全反应后生成氢气2g,则此合金的组成可能为
A.和 B.和 C.和 D.和
7.下列图像与对应的叙述相符合的是
A.电解一定质量的水
B.高温煅烧一定质量的石灰石
C.氢气和氧气在密闭容器中燃烧
D.向等质量的铁和锌粉中分别逐滴加入相同的稀硫酸至过量
8.下列各组中,除去杂质所选用的试剂或方法正确的是
组别 物质 杂质(少量) 除杂试剂或操作方法
A CO CO2 通过灼热的氧化铜
B CuO C 隔绝空气加强热
C FeSO4 溶液 CuSO4 加入过量的锌粉,过滤
D 铜粉 镁粉 加入足量稀硫酸溶液,过滤、洗涤、烘干
A.A B.B C.C D.D
9.下列图象中正确的是
A. 甲:向相同质量的铁粉和锌粉中分别加入足量稀盐酸
B. 乙:向三份等质量、等浓度的稀盐酸中分别加入足量的镁、铝、铁
C. 丙:CH4气体的溶解度与温度、压强的关系
D. 丁:在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉
二、简答题
10.化学与生产生活密切相关。
(1)净水时加入活性炭除去颜色和利用了活性炭的___________性;
(2)日常生活中,铝制品耐腐蚀的原因是______________;
(3)《本草纲目拾遗》中说:“罐得火气合于肉,即牢不可脱肉上起红晕,罐中有气水出,风寒尽岀。”拔罐法通常利用燃烧酒精等物质排去罐内空气,酒精(C2H5OH)燃烧的化学反应方式______。
11.根据图示回答下列问题。
(1)写出A处发生反应的化学方程式______。
(2)B处氧化铜发生反应的现象是什么?
12.以煤为原料获得的化工产品有着广泛的用途。请回答下列问题:
(1)煤是______(填“可再生”或“不可再生”)的化石能源。
(2)煤加工得到的焦炭广泛应用于炼铁。如图是高炉炼铁的示意图,据图回答:
①焦炭在炼铁过程中的主要作用是_____、_____;原料中石灰石的作用是______。
②铁矿石(主要成分为Fe2O3)进入高炉前要粉碎成小颗粒,其原因是____。写出高炉内生成铁的化学方程式:_______。
③图中出铁口低于出渣口,说明生铁的密度比炉渣_______(填“大”或“小”)。
(3)生铁的含碳量比钢_______(填“高”或“低”)。
三、推断题
13.A~H内初中化学常见的物质。己知A属于盐,常用作建筑材料,E是红色固体,H的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全标出)。
(1)A的化学式为_____;
(2)F的一种用途是_____;
(3)写出反应②、④的化学方程式:反应②_____,反应④_____,其中反应④的基本反应类型_____是反应;
(4)比较D与G的活动性强弱关系为:D_____G(填“>”或“<”)。
14.A﹣J是初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去)。其中G是大理石的主要成分,A为红棕色化合物,I为红色单质,B、D为组成元素相同的气体。
请回答下列问题:
(1)I的化学式为_____。
(2)反应①的反应化学方程式为_____。
(3)反应②的反应化学方程式为_____。
(4)反应③的基本反应类型为_____。
15.已知A ~ H为初中化学常见的几种物质。其中A是一种难溶性的白色固体,B、C、D为氧化物,E、F、G、H为单质。各种物质间的反应和转化关系如图所示(“—”表示连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物己略去)。分析后回答:
(1)A的化学式_________;
(2)E → F反应的化学方程式__________。
16.物质间的转化关系图所示(注:图中各路线均为一步完成的化学反应)。
回答下列问题:
(1)A B C三种物质同属于氧化物,B是二氧化碳。若变化Ⅰ属于化合反应,变化Ⅱ的化学方程式为:______。
(2)A B C三种物质同属于单质,B是氢气写出变化Ⅱ的化学方程式:______,其基本反应类型属于______。
四、实验题
17.某化学小组对钢铁制品锈蚀的条件进行了探究,设计了如图所示的实验,据此回答下列有关问题。
(1)三天后,观察到序号为______的试管中的铁钉明显生锈,铁钉未生锈的是______。
(2)对照实验①和③,可知铁锈蚀的条件是什么______?
18.下图是实验室模拟炼铁的实验装置。请回答下列问题:
(1)写出一氧化碳还原氧化铁的化学反应方程式:_______
(2)写出上图实验中发生化学反应的实验现象:_______
五、计算题
19.小鸿设计如下实验,探究粗锌粒中锌的质量分数(粗锌所含的杂质不跟稀硫酸反应)。
计算:(写出计算过程)
(1)粗锌中锌的质量分数。(精确到0.1%)
(2)100g稀硫酸中硫酸的质量。
20.(1)2021河南春晚《唐宫夜宴》曾被刷上热搜,节目中展出的青铜器历史悠久,西汉时期就记载有“曾青(硫酸铜)得铁则化为铜”。请用化学方程式表示其原理。
(2)硅芯片是很多电子产品的核心。下面是某种制取硅反应的微观示意图,请计算反应前后乙与丁变化的质量比是多少?
21.锌与稀硫酸(H2SO4)反应生成氢气和硫酸锌。某实验小组将一定量的锌投入足量稀硫酸中,充分反应。产生氢气的质量与反应时间的关系如图所示:(反应方程式为:Zn+H2SO4=ZnSO4+H2↑)
(1)ZnSO4的相对分子质量为 ;
(2)反应生成的氢气的质量为 g;
(3)参加反应的锌的质量是多少?
22.请你仔细分析如图所示的实验过程和提供的数据,计算反应后所得溶液中溶质的质量分数是____?
试卷第1页,共3页
参考答案:
1.D
2.A
3.B
4.B
5.A
6.D
7.D
8.D
9.D
10.(1)吸附
(2)铝在空气中和氧气反应产生一层致密的氧化膜,阻止铝被腐蚀
(3)
11.(1)Zn+H2SO4= ZnSO4+H2↑
(2)黑色固体变为红色,W形管内壁有水珠生成
12. 不可再生 提供反应所需的热量 产生CO 将矿石中二氧化硅转化为炉渣 增大接触面积,加快反应速率,氧化铁反应更充分 3CO+ Fe2O3 2Fe + 3CO2 大 高
13. CaCO3 用作建筑材料、保护树木、配制农药波尔多液、改良酸性土壤等(任选一,合理均可) 置换 >
14. Cu Fe2O3+3CO2Fe+3CO2 CO2+Ca(OH)2═CaCO3↓+H2O 置换反应
15.(1)CaCO3
(2)或
16.(1)
(2)
置换反应
17. ③ ①② 要与水分接触
18.(1)
(2)玻璃管中红色粉末变黑色,石灰水变浑浊,末端导管有蓝色火焰
19.(1)解:设粗锌中锌的质量为x,100g稀硫酸中硫酸的质量为y
解得x=6.5g,y=9.8g
所以粗锌中锌的质量分数
答:粗锌中锌的质量分数为65%。
(2)答:100g稀硫酸中硫酸的质量为9.8g。
20.(1)
(2)2:73
21.(1)161
(2)0.4
(3)设参加反应的锌的质量为
答:参加反应的锌的质量是13g。
22.12.7%
答案第1页,共2页
答案第1页,共2页
