第九单元溶液测试题-2021-2022学九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 第九单元溶液测试题-2021-2022学九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 93.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-07 00:00:00 | ||
图片预览



文档简介
第九单元《溶液》测试题
一、单选题
1.下列有关水与溶液的说法错误的是
A.电解水实验说明水是由氢元素和氧元素组成的
B.农药、化肥不合理使用,会造成水体污染
C.饱和溶液就是不能再溶解任何物质的溶液
D.天然淡水生产自来水需要经过沉降、过滤、吸附、杀菌消毒等净化过程
2.下列方案不能达到实验目的的是
A.用燃着的木条鉴别O2和CO2 B.用点燃的方法除去CO2中的CO
C.用稀硫酸鉴别黄金和黄铜 D.用过滤的方法除去粗盐中的泥沙
3.a、b、c三种固体物质的溶解度曲线如图。下列说法正确的是
A.t3℃时三种饱和溶液降温到t1℃,a析出晶体最多
B.t2℃时,b的饱和溶液中溶质的质量分数为50%
C.t3℃时,等质量的三种物质配成饱和溶液,a溶液质量最大
D.t1℃时,质量不同的a、b、c饱和溶液升温到t3℃,b的质量分数最大
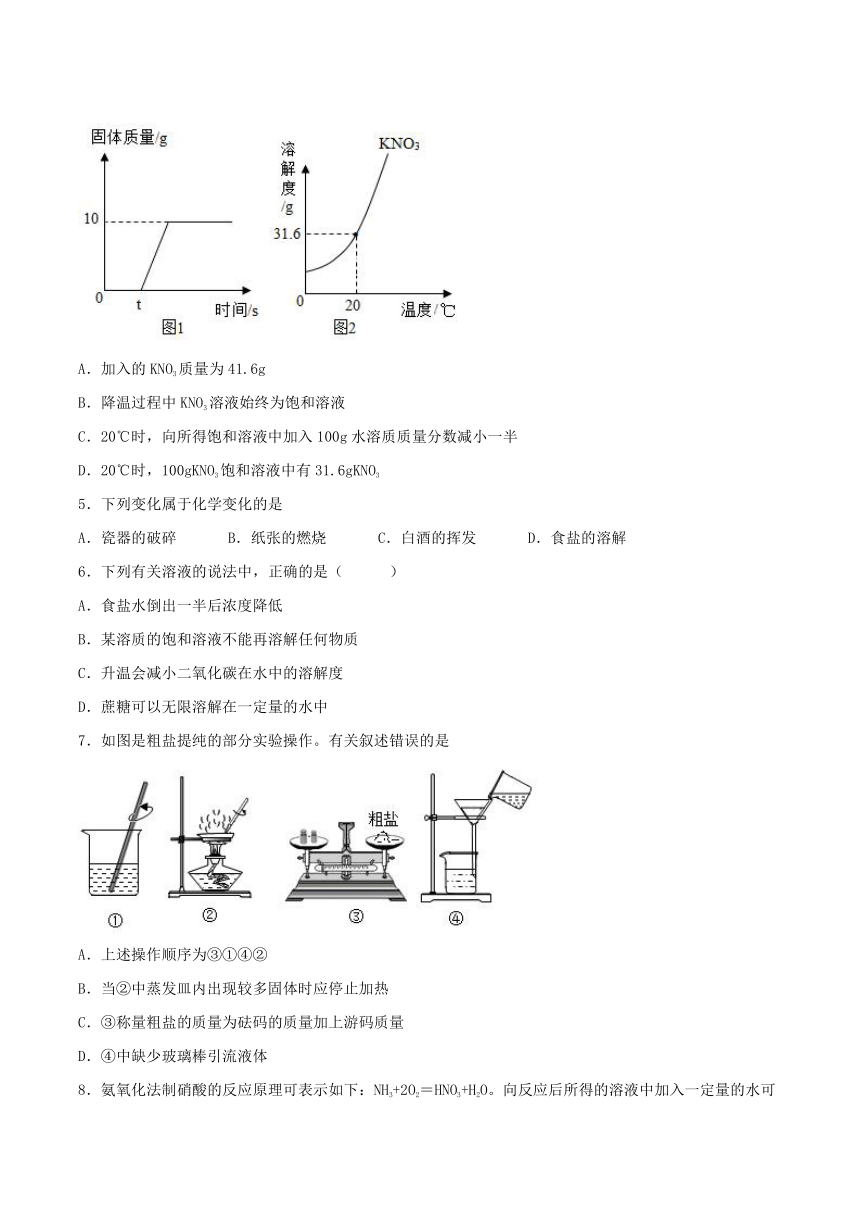
4.60℃时,向100g水中加入一定量KNO3固体形成溶液,再降温至20℃,析出固体质量的变化如图1所示,结合图2,下列说法正确的是
A.加入的KNO3质量为41.6g
B.降温过程中KNO3溶液始终为饱和溶液
C.20℃时,向所得饱和溶液中加入100g水溶质质量分数减小一半
D.20℃时,100gKNO3饱和溶液中有31.6gKNO3
5.下列变化属于化学变化的是
A.瓷器的破碎 B.纸张的燃烧 C.白酒的挥发 D.食盐的溶解
6.下列有关溶液的说法中,正确的是( )
A.食盐水倒出一半后浓度降低
B.某溶质的饱和溶液不能再溶解任何物质
C.升温会减小二氧化碳在水中的溶解度
D.蔗糖可以无限溶解在一定量的水中
7.如图是粗盐提纯的部分实验操作。有关叙述错误的是
A.上述操作顺序为③①④②
B.当②中蒸发皿内出现较多固体时应停止加热
C.③称量粗盐的质量为砝码的质量加上游码质量
D.④中缺少玻璃棒引流液体
8.氨氧化法制硝酸的反应原理可表示如下:NH3+2O2=HNO3+H2O。向反应后所得的溶液中加入一定量的水可制得溶质质量分数为60%的硝酸溶液,将反应后所得的溶液脱水可制得溶质质量分数为90%的硝酸溶液。现以17kg氨气为原料,反应后既不加水也不脱水,理论上可制得60%和90%的硝酸溶液的质量比为
A.5:8 B.8:11 C.11:25 D.11:16
9.厨房中蕴含着丰富的化学知识,下列说法错误的是
A.“高铁酱油”中的“铁”指的是铁元素
B.炒菜时油锅着火,可立即加入大量青菜灭火
C.燃气泄露时,应立即关闭阀门开窗通风
D.洗碗时加入洗涤剂,可以溶解餐具上的油污
10.下列物质的性质与用途对应关系正确的是
A.石墨质软,用作电池电极 B.氧气能支持燃烧,用作燃料
C.铜为紫红色固体,用于制作导线 D.洗洁精具有乳化作用,用于清洗油污
11.t℃时,M物质的溶解度为Sg,则bgM物质在t℃时,可配成的饱和溶液的质量是
A.b(100+S)/S g B.(100+S+b) g C.S(100+b)/b g D.100b/S g
二、简答题
12.根据所学知识请回答:
(1)人们用干冰制作口感类似汽水的“碳酸水果”,干冰与水果一起放置12小时候,水果变得冰凉,原因是______。
(2)饮用汽水时,将瓶盖打开,会有大量气泡冒出,该气体的成分是______,将该气体通入澄清石灰水中,观察到______,反应的化学方程式为______。
13.下图是硝酸钾和氯化钠的溶解度曲线图,其横坐标是温度(℃),请回答:
(1)从图中可以看出,当其中混有少量不与其反应的可溶性杂质时,____不适用冷却热饱和溶液的方法来提纯,原因是,由图中可以看出____,因此冷却热饱和溶液时,析出的固体不会太多。
(2)20℃时向100g水中加入25g硝酸钾,充分溶解后所得溶液为______溶液(填“饱和或“不饱和”):请计算此时溶液的溶质的质量分数为 ____
(3)将饱和的KNO3溶液倒入小试管中然后放入盛水的烧杯中,当向烧杯的水中加入某物质后试管中有晶体析出(如图)。加入的物质可能是下列中的____(填字母序号)。
A 氢氧化钠固体 B 生石灰固体 C 冰块 D 硝酸铵固体E.浓硫酸
对于“同温度下KNO3的饱和溶液都比NaCl饱和溶液的质量百分比浓度大”这一观点你同意吗?______理由是____
三、推断题
14.A、B、C、D和甲、乙均为初中化学中常见的物质,物质间存在着如图所示的相互转化关系(部分生成物未标出).请回答下列问题:
(1)若A为气体氧化物,与溶液甲和溶液乙反应均生成盐和水.则A的化学式为______;取溶液D少量于试管中,加入碳酸钠溶液,有白色沉淀生成,则溶液D中溶质为______(写化学式);③反应的化学方程式为______.
(2)若向一定质量的碳酸钠溶液中加入足量的氯化钙溶液,所得沉淀质量等于原碳酸钠溶液质量的,则原碳酸钠溶液中溶质的质量分数为______.
15.某兴趣小组的同学在实验室用含有少量CaCl2的NaCl固体配制一定质量分数的NaCl溶液。实验步骤如下图所示:
请回答下列问题:
(1)沉淀D的化学式为 _____
(2)加入“过量Na2CO3”所发生反应的化学方程式为 _____
(3)在“操作1”用的实验方法是 _____
(4)加入“适量HCl”的目的是 _____
(5)“操作2”的目的是测定溶液为中性,测定溶液pH的方法是 _____
(6)经测定“溶液C”的质量为50g,质量分数为6%的氯化钠溶液(密度为1.04g/cm3)。现要用该溶液配制50g质量分数为3%的氯化钠溶液,所需6%的氯化钠溶液和水的体积分别为 _____ ml和 _____ ml。(水密度为1.0g/cm3)。
四、实验题
16.实验室现要配制60g溶质质量分数为5%的氯化钠溶液,试完成下列填空。
【实验过程】
(1)计算:需要氯化钠的质量为3g,需要水的体积为______mL。
(2)称取氯化钠:在已调节平衡的天平两端的托盘上分别放上质量相等的纸片,移动游码至刻度如图______(选填“甲”或“乙”)所示。
(3)量取水:先向量筒内直接加水,当水接近刻度时改用______继续加水至所需刻度。
溶解:溶解时,用玻璃棒搅拌使氯化钠快速溶解。
(4)转移:将配得溶液移入______,贴上标签。
【实验反思】
(5)上述实验过程中会导致所配溶液的溶质质量分数偏小的是______。
A.将氯化钠粉末倒入烧杯时有少量洒出
B.用量筒量取水时俯视读数
C.配制溶液的烧杯事先用少量蒸馏水润洗
D.转移已配好的溶液时,有少量液体溅出
17.请根据图一、二、三、四中所示实验回答下列问题:
(1)若用图一装置来收集氧气,应从___________导管(填a、b)通入气体。
(2)图二电解水的实验中,___________管(填A、B)内所收集的气体是氢气;该实验中,常会在水中放少量硫酸或氢氧化钠,其目的是___________。
(3)在某温度下把相同质量的甲、乙两物质分别放入相同质量的水中,溶解情况如图三所示,请问:质量分数较大的是___________(甲或乙)的溶液。
(4)根据图四所示实验,滴管中的水挤入小试管后,请你推测U形管中___________端液面(填“a”或“b”)会下降。
五、计算题
18.溶液在人类的生产、生活和科学研究中具有广泛的应用。请完成下列配置溶液的问题:
(1)农业生产中通常用溶质质量分数为10%—20%的氯化钠溶液来选种。
①现要配制120kg溶质质量分数为20%的氯化钠溶液,需要取用固体氯化钠_____kg。
②用60kg溶质质量分数为20%的氯化钠溶液,可稀释成12%的氯化钠溶液______kg。
(2)制作“叶脉书签”需要配制100g12%的NaOH溶液(水的密度为1g/mL),需要称量NaOH固体______g,需要量取水____mL。
19.回答下列问题
(1)800kg质量分数为0.5%的过氧乙酸消毒液中,过氧乙酸的质量为_____kg。
(2)要配制800kg质量分数为0.5%的过氧乙酸消毒液,需质量分数为16%的过氧乙酸溶液的质量是多少?
20.某化学小组在实验里称取6克氯酸钾和2克二氧化锰混合加热来制取氧气,来做有关氧气性质的探究实验。实验完成后,称得试管内剩余固体质量为6.08克。试计算:
(1)根据质量守恒可得,生成氧气的质量为克。
(2)试管内剩余固体中氯酸钾的质量。
参考答案:
1.C 2.B 3.D 4.A 5.B 6.C 7.C 8.D 9.D 10.D 11.A
12.(1)干冰升华吸热
(2) CO2 澄清石灰水变浑浊
13. NaCl NaCl的溶解度受温度影响不大 不饱和 20% CD 不同意 在温度低于t℃时,KNO3的溶解度低于NaCl的溶解度,此时KNO3的饱和溶液的质量百分比浓度比NaCl饱和溶液的要小
14. CO2 NaOH、Ca(OH)2 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 53%
15. CaCO3 CaCl2+Na2CO3=CaCO3↓+2NaCl 过滤 反应掉过量的Na2CO3 用玻璃棒蘸取待测液,贴上干燥的pH试纸上,再与标准比色卡对比 24.0 25.0
16.(1)57
(2)甲
(3)胶头滴管
(4)细口瓶
(5)AC
17.(1)a
(2) A 增强水的导电性
(3)乙
(4)a
18.(1)24;100
(2)解:需要称量NaOH固体质量为100g×12%=12g;
需要量取水质量为100-12=88g,水的体积为88g÷1g/mL=88mL。
19.(1)4
(2)解:设需质量分数为16%的过氧乙酸溶液的质量是x,
根据溶液稀释前后溶质的质量不变,则,x=25kg。
答:需质量分数为16%的过氧乙酸溶液的质量是25kg。
20.(1)根据质量守恒定律可得,生成氧气的质量为6g+2g-6.08g=1.92g;
(2)设试管内剩余固体中氯酸钾的质量为x
x=1.1g
答:试管内剩余固体中氯酸钾的质量1.1g。
一、单选题
1.下列有关水与溶液的说法错误的是
A.电解水实验说明水是由氢元素和氧元素组成的
B.农药、化肥不合理使用,会造成水体污染
C.饱和溶液就是不能再溶解任何物质的溶液
D.天然淡水生产自来水需要经过沉降、过滤、吸附、杀菌消毒等净化过程
2.下列方案不能达到实验目的的是
A.用燃着的木条鉴别O2和CO2 B.用点燃的方法除去CO2中的CO
C.用稀硫酸鉴别黄金和黄铜 D.用过滤的方法除去粗盐中的泥沙
3.a、b、c三种固体物质的溶解度曲线如图。下列说法正确的是
A.t3℃时三种饱和溶液降温到t1℃,a析出晶体最多
B.t2℃时,b的饱和溶液中溶质的质量分数为50%
C.t3℃时,等质量的三种物质配成饱和溶液,a溶液质量最大
D.t1℃时,质量不同的a、b、c饱和溶液升温到t3℃,b的质量分数最大
4.60℃时,向100g水中加入一定量KNO3固体形成溶液,再降温至20℃,析出固体质量的变化如图1所示,结合图2,下列说法正确的是
A.加入的KNO3质量为41.6g
B.降温过程中KNO3溶液始终为饱和溶液
C.20℃时,向所得饱和溶液中加入100g水溶质质量分数减小一半
D.20℃时,100gKNO3饱和溶液中有31.6gKNO3
5.下列变化属于化学变化的是
A.瓷器的破碎 B.纸张的燃烧 C.白酒的挥发 D.食盐的溶解
6.下列有关溶液的说法中,正确的是( )
A.食盐水倒出一半后浓度降低
B.某溶质的饱和溶液不能再溶解任何物质
C.升温会减小二氧化碳在水中的溶解度
D.蔗糖可以无限溶解在一定量的水中
7.如图是粗盐提纯的部分实验操作。有关叙述错误的是
A.上述操作顺序为③①④②
B.当②中蒸发皿内出现较多固体时应停止加热
C.③称量粗盐的质量为砝码的质量加上游码质量
D.④中缺少玻璃棒引流液体
8.氨氧化法制硝酸的反应原理可表示如下:NH3+2O2=HNO3+H2O。向反应后所得的溶液中加入一定量的水可制得溶质质量分数为60%的硝酸溶液,将反应后所得的溶液脱水可制得溶质质量分数为90%的硝酸溶液。现以17kg氨气为原料,反应后既不加水也不脱水,理论上可制得60%和90%的硝酸溶液的质量比为
A.5:8 B.8:11 C.11:25 D.11:16
9.厨房中蕴含着丰富的化学知识,下列说法错误的是
A.“高铁酱油”中的“铁”指的是铁元素
B.炒菜时油锅着火,可立即加入大量青菜灭火
C.燃气泄露时,应立即关闭阀门开窗通风
D.洗碗时加入洗涤剂,可以溶解餐具上的油污
10.下列物质的性质与用途对应关系正确的是
A.石墨质软,用作电池电极 B.氧气能支持燃烧,用作燃料
C.铜为紫红色固体,用于制作导线 D.洗洁精具有乳化作用,用于清洗油污
11.t℃时,M物质的溶解度为Sg,则bgM物质在t℃时,可配成的饱和溶液的质量是
A.b(100+S)/S g B.(100+S+b) g C.S(100+b)/b g D.100b/S g
二、简答题
12.根据所学知识请回答:
(1)人们用干冰制作口感类似汽水的“碳酸水果”,干冰与水果一起放置12小时候,水果变得冰凉,原因是______。
(2)饮用汽水时,将瓶盖打开,会有大量气泡冒出,该气体的成分是______,将该气体通入澄清石灰水中,观察到______,反应的化学方程式为______。
13.下图是硝酸钾和氯化钠的溶解度曲线图,其横坐标是温度(℃),请回答:
(1)从图中可以看出,当其中混有少量不与其反应的可溶性杂质时,____不适用冷却热饱和溶液的方法来提纯,原因是,由图中可以看出____,因此冷却热饱和溶液时,析出的固体不会太多。
(2)20℃时向100g水中加入25g硝酸钾,充分溶解后所得溶液为______溶液(填“饱和或“不饱和”):请计算此时溶液的溶质的质量分数为 ____
(3)将饱和的KNO3溶液倒入小试管中然后放入盛水的烧杯中,当向烧杯的水中加入某物质后试管中有晶体析出(如图)。加入的物质可能是下列中的____(填字母序号)。
A 氢氧化钠固体 B 生石灰固体 C 冰块 D 硝酸铵固体E.浓硫酸
对于“同温度下KNO3的饱和溶液都比NaCl饱和溶液的质量百分比浓度大”这一观点你同意吗?______理由是____
三、推断题
14.A、B、C、D和甲、乙均为初中化学中常见的物质,物质间存在着如图所示的相互转化关系(部分生成物未标出).请回答下列问题:
(1)若A为气体氧化物,与溶液甲和溶液乙反应均生成盐和水.则A的化学式为______;取溶液D少量于试管中,加入碳酸钠溶液,有白色沉淀生成,则溶液D中溶质为______(写化学式);③反应的化学方程式为______.
(2)若向一定质量的碳酸钠溶液中加入足量的氯化钙溶液,所得沉淀质量等于原碳酸钠溶液质量的,则原碳酸钠溶液中溶质的质量分数为______.
15.某兴趣小组的同学在实验室用含有少量CaCl2的NaCl固体配制一定质量分数的NaCl溶液。实验步骤如下图所示:
请回答下列问题:
(1)沉淀D的化学式为 _____
(2)加入“过量Na2CO3”所发生反应的化学方程式为 _____
(3)在“操作1”用的实验方法是 _____
(4)加入“适量HCl”的目的是 _____
(5)“操作2”的目的是测定溶液为中性,测定溶液pH的方法是 _____
(6)经测定“溶液C”的质量为50g,质量分数为6%的氯化钠溶液(密度为1.04g/cm3)。现要用该溶液配制50g质量分数为3%的氯化钠溶液,所需6%的氯化钠溶液和水的体积分别为 _____ ml和 _____ ml。(水密度为1.0g/cm3)。
四、实验题
16.实验室现要配制60g溶质质量分数为5%的氯化钠溶液,试完成下列填空。
【实验过程】
(1)计算:需要氯化钠的质量为3g,需要水的体积为______mL。
(2)称取氯化钠:在已调节平衡的天平两端的托盘上分别放上质量相等的纸片,移动游码至刻度如图______(选填“甲”或“乙”)所示。
(3)量取水:先向量筒内直接加水,当水接近刻度时改用______继续加水至所需刻度。
溶解:溶解时,用玻璃棒搅拌使氯化钠快速溶解。
(4)转移:将配得溶液移入______,贴上标签。
【实验反思】
(5)上述实验过程中会导致所配溶液的溶质质量分数偏小的是______。
A.将氯化钠粉末倒入烧杯时有少量洒出
B.用量筒量取水时俯视读数
C.配制溶液的烧杯事先用少量蒸馏水润洗
D.转移已配好的溶液时,有少量液体溅出
17.请根据图一、二、三、四中所示实验回答下列问题:
(1)若用图一装置来收集氧气,应从___________导管(填a、b)通入气体。
(2)图二电解水的实验中,___________管(填A、B)内所收集的气体是氢气;该实验中,常会在水中放少量硫酸或氢氧化钠,其目的是___________。
(3)在某温度下把相同质量的甲、乙两物质分别放入相同质量的水中,溶解情况如图三所示,请问:质量分数较大的是___________(甲或乙)的溶液。
(4)根据图四所示实验,滴管中的水挤入小试管后,请你推测U形管中___________端液面(填“a”或“b”)会下降。
五、计算题
18.溶液在人类的生产、生活和科学研究中具有广泛的应用。请完成下列配置溶液的问题:
(1)农业生产中通常用溶质质量分数为10%—20%的氯化钠溶液来选种。
①现要配制120kg溶质质量分数为20%的氯化钠溶液,需要取用固体氯化钠_____kg。
②用60kg溶质质量分数为20%的氯化钠溶液,可稀释成12%的氯化钠溶液______kg。
(2)制作“叶脉书签”需要配制100g12%的NaOH溶液(水的密度为1g/mL),需要称量NaOH固体______g,需要量取水____mL。
19.回答下列问题
(1)800kg质量分数为0.5%的过氧乙酸消毒液中,过氧乙酸的质量为_____kg。
(2)要配制800kg质量分数为0.5%的过氧乙酸消毒液,需质量分数为16%的过氧乙酸溶液的质量是多少?
20.某化学小组在实验里称取6克氯酸钾和2克二氧化锰混合加热来制取氧气,来做有关氧气性质的探究实验。实验完成后,称得试管内剩余固体质量为6.08克。试计算:
(1)根据质量守恒可得,生成氧气的质量为克。
(2)试管内剩余固体中氯酸钾的质量。
参考答案:
1.C 2.B 3.D 4.A 5.B 6.C 7.C 8.D 9.D 10.D 11.A
12.(1)干冰升华吸热
(2) CO2 澄清石灰水变浑浊
13. NaCl NaCl的溶解度受温度影响不大 不饱和 20% CD 不同意 在温度低于t℃时,KNO3的溶解度低于NaCl的溶解度,此时KNO3的饱和溶液的质量百分比浓度比NaCl饱和溶液的要小
14. CO2 NaOH、Ca(OH)2 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 53%
15. CaCO3 CaCl2+Na2CO3=CaCO3↓+2NaCl 过滤 反应掉过量的Na2CO3 用玻璃棒蘸取待测液,贴上干燥的pH试纸上,再与标准比色卡对比 24.0 25.0
16.(1)57
(2)甲
(3)胶头滴管
(4)细口瓶
(5)AC
17.(1)a
(2) A 增强水的导电性
(3)乙
(4)a
18.(1)24;100
(2)解:需要称量NaOH固体质量为100g×12%=12g;
需要量取水质量为100-12=88g,水的体积为88g÷1g/mL=88mL。
19.(1)4
(2)解:设需质量分数为16%的过氧乙酸溶液的质量是x,
根据溶液稀释前后溶质的质量不变,则,x=25kg。
答:需质量分数为16%的过氧乙酸溶液的质量是25kg。
20.(1)根据质量守恒定律可得,生成氧气的质量为6g+2g-6.08g=1.92g;
(2)设试管内剩余固体中氯酸钾的质量为x
x=1.1g
答:试管内剩余固体中氯酸钾的质量1.1g。
同课章节目录
