河北省石家庄二高2021-2022学年高一下学期3月开学考试化学试题(Word版含答案)
文档属性
| 名称 | 河北省石家庄二高2021-2022学年高一下学期3月开学考试化学试题(Word版含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 274.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-09 21:56:04 | ||
图片预览


文档简介
石家庄二高2021-2022学年高一下学期3月开学考试
化 学
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教版必修第一册、必修第二册第五章。
5.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32
一、选择题:本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列生活中的常见物品或设施,其主要成分为硅单质的是
A.砖瓦 B.计算机芯片 C.门窗玻璃 D.石英钟
2.下列物质中,属于电解质的是
A.食盐固体 B.金属铜 C.液态HCl D.硫酸铜溶液
3.已知稀硝酸可以溶解金属铝,其反应为。下列表示该反应中相关微粒的化学用语错误的是
A.中子数为10的氧原子: B.的结构示意图:
C.和互为同位素 D.的电子式:H:O:H
4.化学在生产和日常生活中有着重要的应用,下表中用途与其性质或原理对应关系错误的是
选项 用途 性质或原理
A 葡萄酒中添加适量的起到保质作用 具有杀菌、抗氧化作用
B 胶体可用作自来水净水剂 胶体具有吸附性
C 在食品包装袋中放入装有硅胶、铁粉的透气小袋,可防止食物受潮、氧化变质 硅胶具有吸水性,铁粉具有氧化性
D 用小苏打治疗胃酸过多 可与胃液中的酸反应
5.下列物质中含有非极性共价键的是
A. B. C. D.
6.已知反应:,下列关于该反应的说法错误的是
A.氧化性:
B.当反应中有4.48L气体生成时,转移电子的物质的量为0.7mol
C.反应中被氧化的元素有Fe和Cr
D.产物可以用作油漆、涂料的红色颜料
7.下列指定反应的离子方程式正确的是
A.氯化铁溶液腐蚀铜箔:
B.向溶液中滴加稀氨水:
C.向溶液中通入过量:
D.向硫酸铝溶液中滴加少量氢氧化钠溶液:
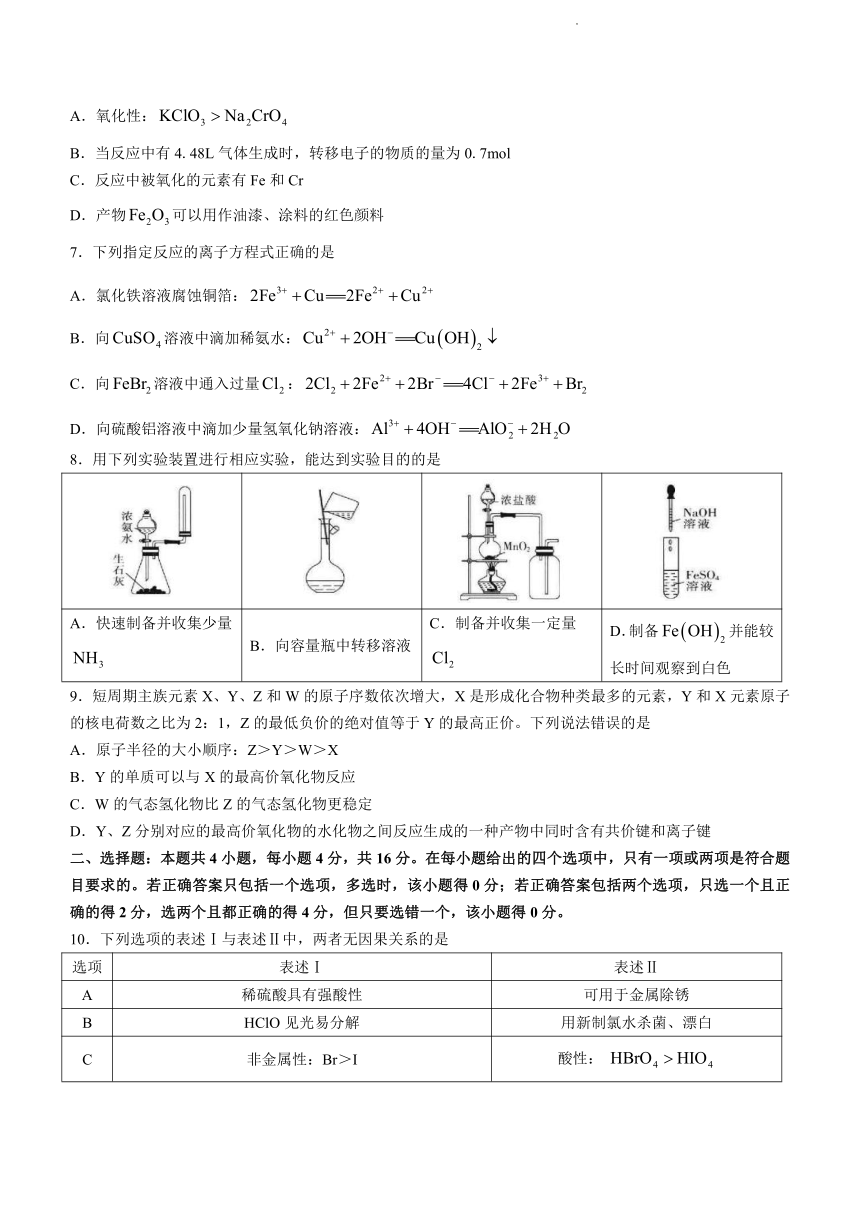
8.用下列实验装置进行相应实验,能达到实验目的的是
A.快速制备并收集少量 B.向容量瓶中转移溶液 C.制备并收集一定量 D.制备并能较长时间观察到白色
9.短周期主族元素X、Y、Z和W的原子序数依次增大,X是形成化合物种类最多的元素,Y和X元素原子的核电荷数之比为2:1,Z的最低负价的绝对值等于Y的最高正价。下列说法错误的是
A.原子半径的大小顺序:Z>Y>W>X
B.Y的单质可以与X的最高价氧化物反应
C.W的气态氢化物比Z的气态氢化物更稳定
D.Y、Z分别对应的最高价氧化物的水化物之间反应生成的一种产物中同时含有共价键和离子键
二、选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,只有一项或两项是符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
10.下列选项的表述Ⅰ与表述Ⅱ中,两者无因果关系的是
选项 表述Ⅰ 表述Ⅱ
A 稀硫酸具有强酸性 可用于金属除锈
B HClO见光易分解 用新制氯水杀菌、漂白
C 非金属性:Br>I 酸性:
D 与反应生成 用作防毒面具供氧剂
11.下列除杂试剂的选择及除杂操作均正确的是(括号内为杂质)
选项 物质 除杂试剂 除杂操作
A Al(Fe) NaOH溶液 加入过量NaOH溶液并过滤
B NO() 水、浓硫酸 将气体依次通过装有水和浓硫酸的洗气瓶
C 溶液() Zn 加入过量的锌粉,充分反应后过滤
D 固体(KCl固体) 蒸馏水 溶解、过滤、洗涤、干燥
12.用表示阿伏加德罗常数的值,下列叙述正确的是
A.18g水中所含有的电子数目为10
B.常温下,22.4L由与组成的混合气体所含分子数为
C.0.5的NaOH溶液中,含有0.5mol
D.1.42g溶于500mL水所得的溶液中,数目为0.02
13.下列有关化学键的说法中,正确的是
①非极性键只存在于双原子单质分子中
②活泼金属与非金属化合时,能形成离子键
③由非金属元素形成的化合物一定是共价化合物
④第ⅠA族和第ⅥA族原子化合时,一定生成离子键
⑤含有离子键的化合物一定是离子化合物
⑥离子化合物中可能同时含有离子键和共价键
A.①②⑤ B.①③④ C.②③⑥ D.②⑤⑥
三、非选择题:本题共4小题,共57分。
14.(15分)
认识氧化物的性质,能帮助我们更好地认识自然和保护环境。
(1)摩擦剂是牙膏的主体成分,是一种常见的摩擦剂。
①Si在元素周期表中的位置是 。
②根据用途推测在水中的溶解性: (填“易溶”或“难溶”)。
③比较酸性强弱: (填“>”或“<”)。
(2)和的任意排放均会污染环境。
①从物质分类角度看,属于酸性氧化物,能与NaOH溶液反应生成亚硫酸盐。写出与过量的NaOH溶液反应的离子方程式: 。
②从元素价态看,中S元素为+4价,既具有氧化性,又具有还原性。则反应中体现了的 (填“氧化性”或“还原性”)。
③是一种 色的有毒气体,易溶于水,与水反应有无色气体生成,写出与水反应的化学方程式: ,反应中每生成标准状况下的气体2.24L,则转移电子的物质的量为 mol。
15.(14分)
某研究性学习小组的甲,乙同学分别设计了以下实验来验证元素周期律。
(1)甲同学将NaOH溶液滴加在溶液中,可观察到的现象为 。由此得出碱性的强弱关系为 (用化学式表示)。
(2)乙同学设计了如图装置来验证元素非金属性的变化规律,根据要求完成下列各小题。
①实验装置:仪器A名称为 。
②实验步骤:连接仪器、 、加药品后,打开活塞,然后滴入试剂。
③已知常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品溶液、、浓盐酸、,请选择合适药品设计实验验证氯的非金属性大于硫的,装置C中所装药品为 ,装置C中发生反应的离子方程式为 。
④已知为难溶于水的白色胶状沉淀。若要证明非金属性:S>C>Si,则A中加 、B中加、C中加,能说明碳元素的非金属性比硅元素的非金属性强的实验现象是 。试管C中发生反应的离子方程式是 。
16.(14分)
在人类社会的发展进程中,金属起着重要的作用。请回答下列问题:
(1)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,错误的是 (填标号)。
A.青铜、不锈钢、硬铝都是合金 B.铜表面易形成致密的氧化膜
C.铜与反应可生成黑色的CuO D.是一种混合物,加热后变为白色固体
(2)生铁中含有一种铁碳化合物X()。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是 (填离子符号)。
(3)铁及其化合物在生产生活中具有广泛应用。一定条件下,铁及其化合物之间发生相互转化。可完全溶于水且与水反应生成两种碱,写出发生反应的离子方程式: 。
(4)某溶液中有、、等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是 (填离子符号)。
(5)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是 。
②加入稍过量溶液时,不仅有沉淀生成,还有无色无味的气体生成,请写出生成沉淀的离子方程式: 。
③在空气中加热反应生成时,氧化剂和还原剂的物质的量之比为 。
17.(14分)
A、B、C、D、E、F、G、H是八种原子序数依次增大的短周期主族元素。常温下,A、C、D、H的常见单质均为气体且仅有H的单质为有色气体。A和B的原子序数之和等于C,A.E同主族,D、G同主族,F的最外层电子数等于其电子层数。
请回答下列问题:
(1)F的原子结构示意图为 。
(2)化合物中所包含的化学键类型为 。
(3)写出E的单质与反应的化学方程式: 。
(4)用电子式表示化合物EH的形成过程: 。
(5)B、C、D三种元素形成的最简单氢化物的稳定性由强到弱的顺序是 (用化学式表示)。
(6)H的单质通入淀粉-KI溶液中,溶液变蓝,写出该反应的离子方程式: ,该实验说明H的非金属性强于碘,请从原子结构的角度解释其原因: 。
石家庄二高2021-2022学年高一下学期3月开学考试
化学参考答案
1.B 2.C 3.D 4.C 5.C 6.B 7.A 8.B 9.A 10.B 11.BD 12.AD
13.D
14.
(1)①第三周期第ⅣA族 ②难溶 ③>
(2)① ②还原性 ③红棕;;0.2
15.
(1)有白色沉淀生成;
(2)①分液漏斗 ②检查装置的气密性 ③溶液; ④稀硫酸;试管C中出现白色沉淀;(或,2分)
16.
(1)BD
(2)、、
(3)
(4)
(5)①漏斗、玻璃棒 ② ③1:4
17.
(1)
(2)离子键共价键(或离子键、非极性共价键,2分)
(3)
(4)
(5)
(6);Cl和I是同主族元素,最外层电子数均为7,电子层数I>Cl,原子半径I>Cl,原子得电子能力I<Cl,元素非金属性I<Cl
化 学
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教版必修第一册、必修第二册第五章。
5.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32
一、选择题:本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列生活中的常见物品或设施,其主要成分为硅单质的是
A.砖瓦 B.计算机芯片 C.门窗玻璃 D.石英钟
2.下列物质中,属于电解质的是
A.食盐固体 B.金属铜 C.液态HCl D.硫酸铜溶液
3.已知稀硝酸可以溶解金属铝,其反应为。下列表示该反应中相关微粒的化学用语错误的是
A.中子数为10的氧原子: B.的结构示意图:
C.和互为同位素 D.的电子式:H:O:H
4.化学在生产和日常生活中有着重要的应用,下表中用途与其性质或原理对应关系错误的是
选项 用途 性质或原理
A 葡萄酒中添加适量的起到保质作用 具有杀菌、抗氧化作用
B 胶体可用作自来水净水剂 胶体具有吸附性
C 在食品包装袋中放入装有硅胶、铁粉的透气小袋,可防止食物受潮、氧化变质 硅胶具有吸水性,铁粉具有氧化性
D 用小苏打治疗胃酸过多 可与胃液中的酸反应
5.下列物质中含有非极性共价键的是
A. B. C. D.
6.已知反应:,下列关于该反应的说法错误的是
A.氧化性:
B.当反应中有4.48L气体生成时,转移电子的物质的量为0.7mol
C.反应中被氧化的元素有Fe和Cr
D.产物可以用作油漆、涂料的红色颜料
7.下列指定反应的离子方程式正确的是
A.氯化铁溶液腐蚀铜箔:
B.向溶液中滴加稀氨水:
C.向溶液中通入过量:
D.向硫酸铝溶液中滴加少量氢氧化钠溶液:
8.用下列实验装置进行相应实验,能达到实验目的的是
A.快速制备并收集少量 B.向容量瓶中转移溶液 C.制备并收集一定量 D.制备并能较长时间观察到白色
9.短周期主族元素X、Y、Z和W的原子序数依次增大,X是形成化合物种类最多的元素,Y和X元素原子的核电荷数之比为2:1,Z的最低负价的绝对值等于Y的最高正价。下列说法错误的是
A.原子半径的大小顺序:Z>Y>W>X
B.Y的单质可以与X的最高价氧化物反应
C.W的气态氢化物比Z的气态氢化物更稳定
D.Y、Z分别对应的最高价氧化物的水化物之间反应生成的一种产物中同时含有共价键和离子键
二、选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,只有一项或两项是符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
10.下列选项的表述Ⅰ与表述Ⅱ中,两者无因果关系的是
选项 表述Ⅰ 表述Ⅱ
A 稀硫酸具有强酸性 可用于金属除锈
B HClO见光易分解 用新制氯水杀菌、漂白
C 非金属性:Br>I 酸性:
D 与反应生成 用作防毒面具供氧剂
11.下列除杂试剂的选择及除杂操作均正确的是(括号内为杂质)
选项 物质 除杂试剂 除杂操作
A Al(Fe) NaOH溶液 加入过量NaOH溶液并过滤
B NO() 水、浓硫酸 将气体依次通过装有水和浓硫酸的洗气瓶
C 溶液() Zn 加入过量的锌粉,充分反应后过滤
D 固体(KCl固体) 蒸馏水 溶解、过滤、洗涤、干燥
12.用表示阿伏加德罗常数的值,下列叙述正确的是
A.18g水中所含有的电子数目为10
B.常温下,22.4L由与组成的混合气体所含分子数为
C.0.5的NaOH溶液中,含有0.5mol
D.1.42g溶于500mL水所得的溶液中,数目为0.02
13.下列有关化学键的说法中,正确的是
①非极性键只存在于双原子单质分子中
②活泼金属与非金属化合时,能形成离子键
③由非金属元素形成的化合物一定是共价化合物
④第ⅠA族和第ⅥA族原子化合时,一定生成离子键
⑤含有离子键的化合物一定是离子化合物
⑥离子化合物中可能同时含有离子键和共价键
A.①②⑤ B.①③④ C.②③⑥ D.②⑤⑥
三、非选择题:本题共4小题,共57分。
14.(15分)
认识氧化物的性质,能帮助我们更好地认识自然和保护环境。
(1)摩擦剂是牙膏的主体成分,是一种常见的摩擦剂。
①Si在元素周期表中的位置是 。
②根据用途推测在水中的溶解性: (填“易溶”或“难溶”)。
③比较酸性强弱: (填“>”或“<”)。
(2)和的任意排放均会污染环境。
①从物质分类角度看,属于酸性氧化物,能与NaOH溶液反应生成亚硫酸盐。写出与过量的NaOH溶液反应的离子方程式: 。
②从元素价态看,中S元素为+4价,既具有氧化性,又具有还原性。则反应中体现了的 (填“氧化性”或“还原性”)。
③是一种 色的有毒气体,易溶于水,与水反应有无色气体生成,写出与水反应的化学方程式: ,反应中每生成标准状况下的气体2.24L,则转移电子的物质的量为 mol。
15.(14分)
某研究性学习小组的甲,乙同学分别设计了以下实验来验证元素周期律。
(1)甲同学将NaOH溶液滴加在溶液中,可观察到的现象为 。由此得出碱性的强弱关系为 (用化学式表示)。
(2)乙同学设计了如图装置来验证元素非金属性的变化规律,根据要求完成下列各小题。
①实验装置:仪器A名称为 。
②实验步骤:连接仪器、 、加药品后,打开活塞,然后滴入试剂。
③已知常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品溶液、、浓盐酸、,请选择合适药品设计实验验证氯的非金属性大于硫的,装置C中所装药品为 ,装置C中发生反应的离子方程式为 。
④已知为难溶于水的白色胶状沉淀。若要证明非金属性:S>C>Si,则A中加 、B中加、C中加,能说明碳元素的非金属性比硅元素的非金属性强的实验现象是 。试管C中发生反应的离子方程式是 。
16.(14分)
在人类社会的发展进程中,金属起着重要的作用。请回答下列问题:
(1)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,错误的是 (填标号)。
A.青铜、不锈钢、硬铝都是合金 B.铜表面易形成致密的氧化膜
C.铜与反应可生成黑色的CuO D.是一种混合物,加热后变为白色固体
(2)生铁中含有一种铁碳化合物X()。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是 (填离子符号)。
(3)铁及其化合物在生产生活中具有广泛应用。一定条件下,铁及其化合物之间发生相互转化。可完全溶于水且与水反应生成两种碱,写出发生反应的离子方程式: 。
(4)某溶液中有、、等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是 (填离子符号)。
(5)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是 。
②加入稍过量溶液时,不仅有沉淀生成,还有无色无味的气体生成,请写出生成沉淀的离子方程式: 。
③在空气中加热反应生成时,氧化剂和还原剂的物质的量之比为 。
17.(14分)
A、B、C、D、E、F、G、H是八种原子序数依次增大的短周期主族元素。常温下,A、C、D、H的常见单质均为气体且仅有H的单质为有色气体。A和B的原子序数之和等于C,A.E同主族,D、G同主族,F的最外层电子数等于其电子层数。
请回答下列问题:
(1)F的原子结构示意图为 。
(2)化合物中所包含的化学键类型为 。
(3)写出E的单质与反应的化学方程式: 。
(4)用电子式表示化合物EH的形成过程: 。
(5)B、C、D三种元素形成的最简单氢化物的稳定性由强到弱的顺序是 (用化学式表示)。
(6)H的单质通入淀粉-KI溶液中,溶液变蓝,写出该反应的离子方程式: ,该实验说明H的非金属性强于碘,请从原子结构的角度解释其原因: 。
石家庄二高2021-2022学年高一下学期3月开学考试
化学参考答案
1.B 2.C 3.D 4.C 5.C 6.B 7.A 8.B 9.A 10.B 11.BD 12.AD
13.D
14.
(1)①第三周期第ⅣA族 ②难溶 ③>
(2)① ②还原性 ③红棕;;0.2
15.
(1)有白色沉淀生成;
(2)①分液漏斗 ②检查装置的气密性 ③溶液; ④稀硫酸;试管C中出现白色沉淀;(或,2分)
16.
(1)BD
(2)、、
(3)
(4)
(5)①漏斗、玻璃棒 ② ③1:4
17.
(1)
(2)离子键共价键(或离子键、非极性共价键,2分)
(3)
(4)
(5)
(6);Cl和I是同主族元素,最外层电子数均为7,电子层数I>Cl,原子半径I>Cl,原子得电子能力I<Cl,元素非金属性I<Cl
同课章节目录
