化学人教版(2019)必修第二册 同步练习第五章第一节第二课时硫酸
文档属性
| 名称 | 化学人教版(2019)必修第二册 同步练习第五章第一节第二课时硫酸 |

|
|
| 格式 | docx | ||
| 文件大小 | 91.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-10 00:00:00 | ||
图片预览

文档简介
第一节 硫及其化合物
第二课时 硫酸
一、单选题
下列关于浓硫酸的性质叙述正确的是
A. 加热时与铜反应只体现酸性 B. 干燥氢气体现脱水性
C. 使白纸变黑体现吸水性 D. 加热时与碳反应体现强氧化性
下列有关说法不正确的是
A. 把浓硫酸沿着烧杯内壁加入水中配制稀硫酸
B. 少量金属钠保存在煤油中
C. 向紫色石蕊试液中不断滴入新制氯水,石蕊试液先变红后褪色
D. 溶液和胶体的本质区别是丁达尔效应
下列离子检验的方法正确的是
A. 向某溶液中加入少量硝酸银溶液,生成白色沉淀,说明原溶液中有
B. 向某溶液中加入少量氯化钡溶液,生成白色沉淀,说明原溶液中有
C. 向某溶液中加入少量氢氧化钙溶液,生成白色沉淀,说明原溶液中有
D. 向某溶液中加入足量盐酸,无现象,再加入少量溶液,产生白色沉淀,说明原溶液中有
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速度加大的是
A. 加热 B. 不用稀硫酸而用浓硫酸
C. 往溶液中加入少量固体 D. 不能铁片而用铁粉
下列反应中,浓硫酸既表现强氧化性,又表现酸性的是
固浓
浓
浓
浓
A. B. C. D.
鉴别稀硫酸和浓硫酸既简单又安全的方法是
A. 各取少量于试管中加入几片铜片
B. 用玻璃棒各蘸少许点在滤纸上
C. 各取少量于试管中滴加NaOH溶液
D. 各取少量于试管中滴加溶液
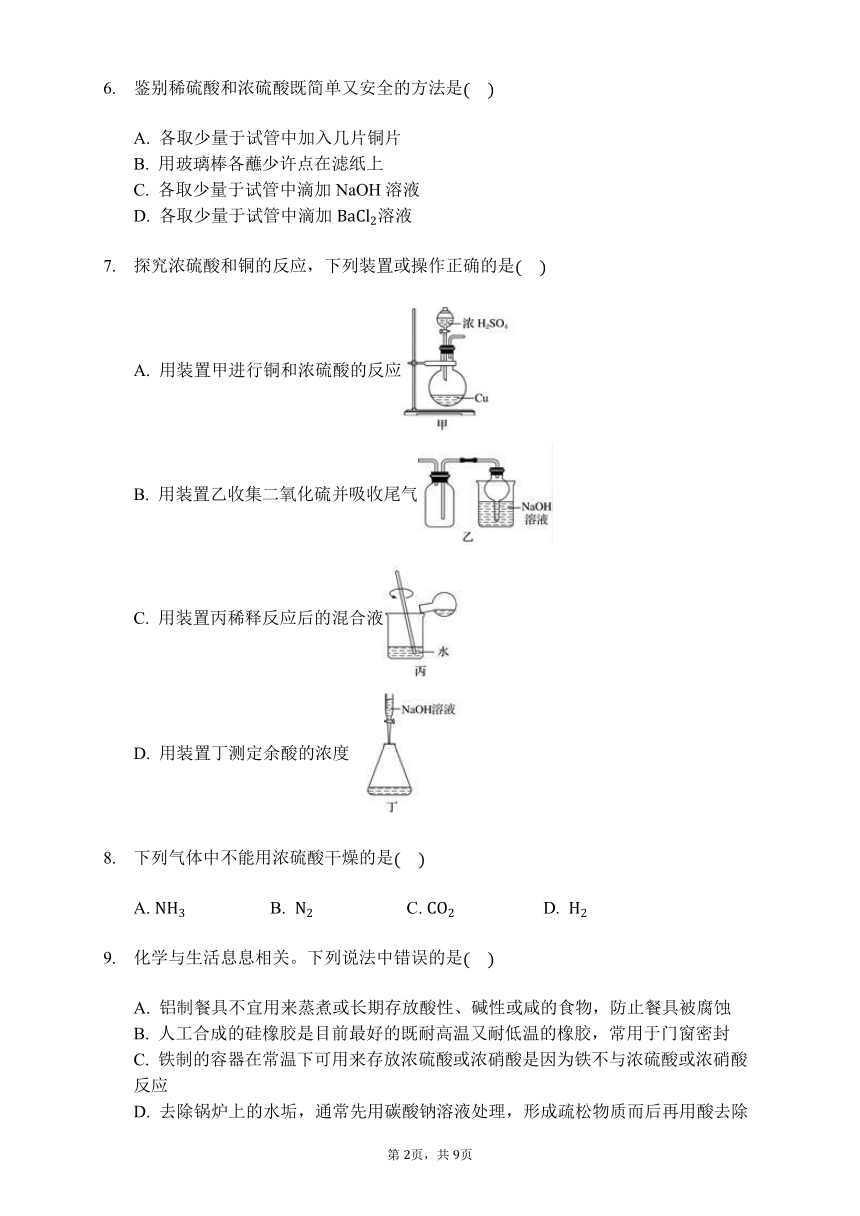
探究浓硫酸和铜的反应,下列装置或操作正确的是
A. 用装置甲进行铜和浓硫酸的反应
B. 用装置乙收集二氧化硫并吸收尾气
C. 用装置丙稀释反应后的混合液
D. 用装置丁测定余酸的浓度
下列气体中不能用浓硫酸干燥的是
A. B. C. D.
化学与生活息息相关。下列说法中错误的是
A. 铝制餐具不宜用来蒸煮或长期存放酸性、碱性或咸的食物,防止餐具被腐蚀
B. 人工合成的硅橡胶是目前最好的既耐高温又耐低温的橡胶,常用于门窗密封
C. 铁制的容器在常温下可用来存放浓硫酸或浓硝酸是因为铁不与浓硫酸或浓硝酸反应
D. 去除锅炉上的水垢,通常先用碳酸钠溶液处理,形成疏松物质而后再用酸去除
下列有关浓硫酸的说法正确的是
A. 浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体
B. 浓硫酸具有脱水性,因而能使蔗糖炭化
C. 浓硫酸在加热条件下能与单质碳反应,体现了浓硫酸的酸性和强氧化性
D. 因为浓硫酸在常温下不与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸
常温下,将液体Y一次性加入到充满的锥形瓶中装置气密性良好,若锥形瓶内气体的最大物质的量为amol,久置后气体的物质的量为bmol,则下列不满足的是
选项 X Y
A 过量c、Fe碎屑 稀盐酸
B 过量粉末 稀硫酸
C 过量Fe、Al碎屑 浓硫酸
D 过量Cu、CuO粉末 浓硝酸
A. A B. B C. C D. D
二、填空题
浓具有酸性;强氧化性;吸水性;脱水性等性质,根据题意填空填序号,可多选:
将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有 ;
浓与木炭共热生成二氧化碳、二氧化硫和水,该反应体现了浓的
把锌粒放入稀硫酸中时,有气体产生 ;
盛有浓硫酸的烧杯敞口放置一段时间后,质量增加 ;
浓硫酸和铜片加热反应,体现了浓硫酸的 。
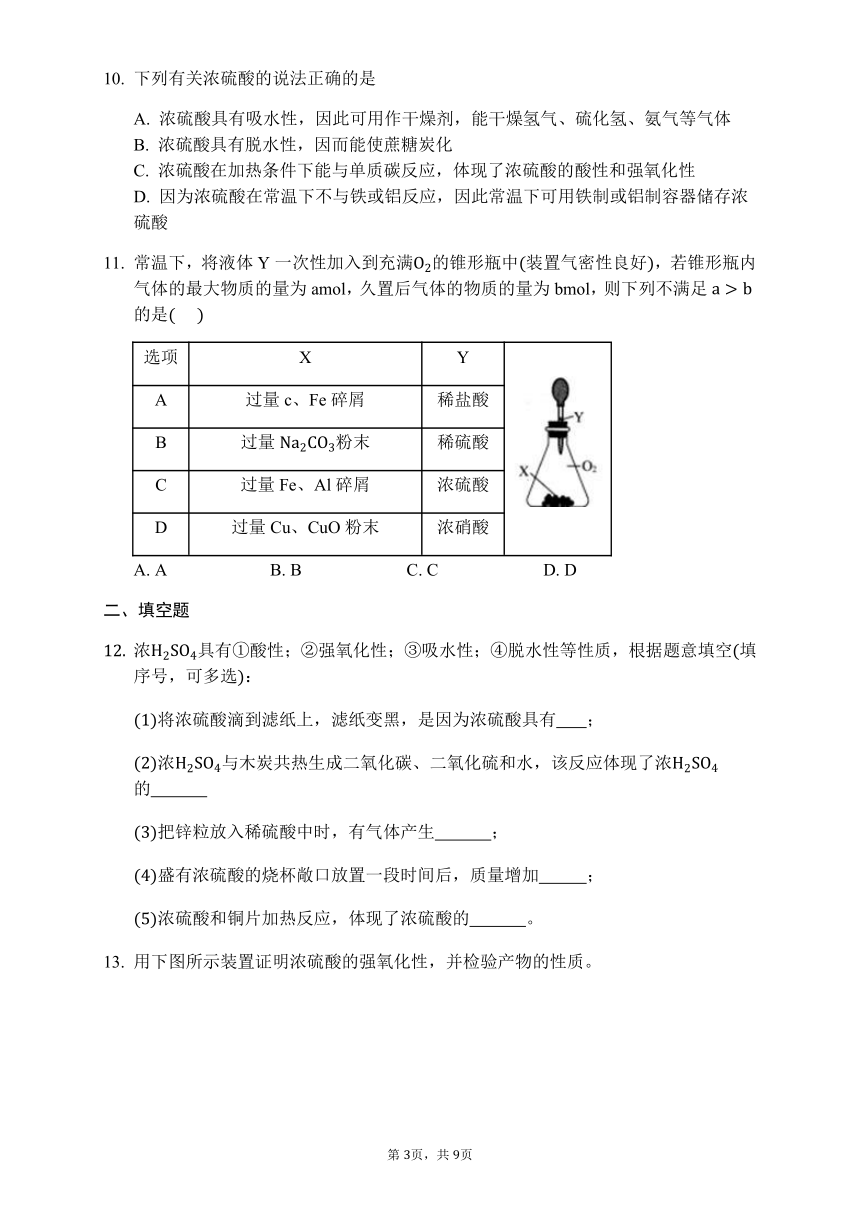
用下图所示装置证明浓硫酸的强氧化性,并检验产物的性质。
请回答下列问题:
写出装置中的化学方程式____________。
装置中的现象为____________________。
装置中的现象为_______ ,生成除水以外的物质名称为________。
装置中的现象为____ __,反应的化学方程式为_______。
装置中的现象为____________ 。
装置中NaOH溶液的作用是__________,反应的离子方程式为:_____________________________。
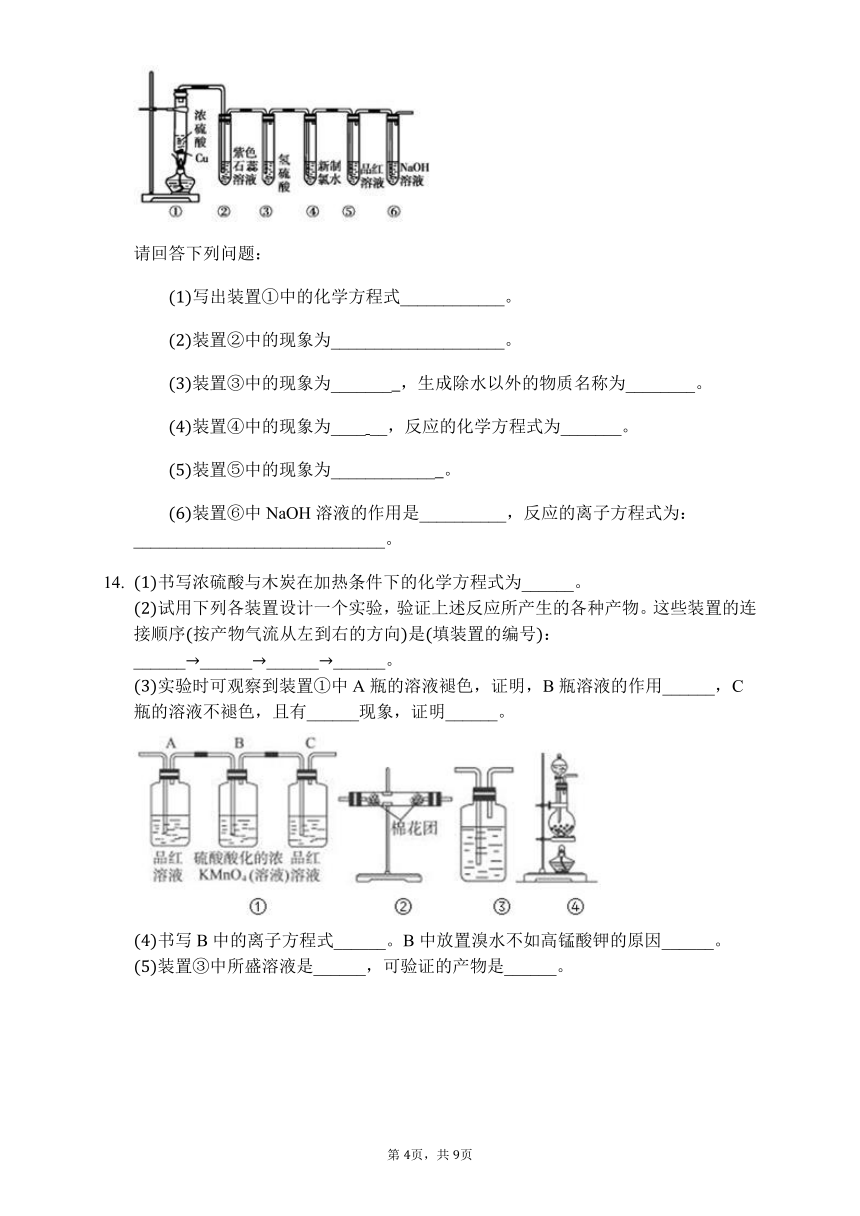
书写浓硫酸与木炭在加热条件下的化学方程式为______。
试用下列各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序按产物气流从左到右的方向是填装置的编号:________________________。
实验时可观察到装置中A瓶的溶液褪色,证明,B瓶溶液的作用______,C瓶的溶液不褪色,且有______现象,证明______。
书写B中的离子方程式______。B中放置溴水不如高锰酸钾的原因______。
装置中所盛溶液是______,可验证的产物是______。
答案
1.【答案】D
【解答】A.加热时浓硫酸与金属铜反应生成二氧化硫和硫酸铜,表现了氧化性和酸性,故A错误;
B.浓硫酸具有吸水性,可以干燥中性和酸性气体,干燥氢气体现吸水性,故B错误;
C.浓硫酸具有脱水性,能使有机物中的H、O元素以水的形式脱出,使白纸变黑表现的是浓硫酸的脱水性,故C错误;
D.浓硫酸与非金属单质反应只体现浓硫酸的强氧化性,故D正确。
故选:D。
2.【答案】D
【解答】A、浓硫酸稀释放热,且密度比水大,故配制稀硫酸时应将浓硫酸沿着烧杯内壁注入水中,故A正确;
B、金属钠能和氧气、水反应,故钠应该保存在煤油中,故B正确;
C、氯水有酸性和漂白性,故能使石蕊溶液先变红后褪色,故C正确;
D、分散系根据分散质粒子直径大小分为溶液、胶体和浊液,而不是根据丁达尔效应,故D错误。
故选:D。
3.【答案】D
【解答】A.向某溶液中加入少量硝酸银溶液,有白色沉淀生成,该白色沉淀可能是碳酸银,原溶液中可能含有碳酸根离子,不一定含有氯离子,故A错误;
B.向某溶液中加入氯化钡溶液,有白色沉淀生成,该白色沉淀可能为氯化银,原溶液中可能含有银离子,不一定含有硫酸根离子,故B错误;
C.向某溶液中加入少量氢氧化钙溶液,生成白色沉淀,该白色沉淀可能为亚硫酸钙,原溶液中可能存在亚硫酸根离子,不一定有碳酸根,故C错误;
D.向某溶液中加入足量的盐酸无明显现象,说明溶液中不存在银离子,然后再加入溶液,产生白色沉淀,该白色沉淀为硫酸钡,证明原溶液中存在硫酸根离子,故D正确.
故选D.
4.【答案】B
【解答】A.加热时,温度升高,反应速率加快,故A不选;
B.常温下铁与浓硫酸发生钝化,故B选;
C.加入少量固体,铁置换出铜构成原电池,反应速率加快,故C不选;
D.铁片改用铁粉,接触面积增大,反应速率加快,故D不选;
故选B。
5.【答案】B
【解答】固体浓,只表现为酸性,故错误;
和浓硫酸反应生成、和水,没有盐生成,只表现为氧化性,故错误;
浓 ,S元素的化合价降低,浓硫酸表现为氧化性,生成,又表现为酸性,故正确;
和浓反应生成、和水,S元素的化合价降低,浓硫酸表现为氧化性,生成,又表现为酸性,故正确;
故选B。
6.【答案】B
【解答】A.Cu与稀硫酸不反应,与浓硫酸反应需要加热,可鉴别,但需要加热且生成有毒气体,故A不选;
B.用玻璃棒各蘸少许点在滤纸上,变黑的为浓硫酸,可鉴别,既简单又安全,故B选;
C.二者均反应生成硫酸钠和水,现象相同,不能鉴别,故C不选;
D.各取少量于试管中滴加溶液,均生成硫酸钡沉淀,现象相同,不能鉴别,故D不选;
故选B.
7.【答案】C
【解答】A.铜与浓硫酸常温下不反应,此反应需要加热设备,图中无加热装置,故A错误;
B.二氧化硫的密度大于空气,适用与向上排空气法收集,即应长进短出,此图方向相反,故B错误;
C.反应后的混合液中可能还含有浓硫酸,而浓硫酸在稀释过程中会释放大量热量,故正确的操作是:将混合液沿着烧杯内壁慢慢注入水中,注入过程中不断的用玻璃棒搅拌以散发热量,故C正确;
D.氢氧化钠溶液显碱性,应盛放在碱式滴定管中,图中滴定管为酸式滴定管,故D错误。
故选C。
8.【答案】A
【解答】A、氨气能与浓硫酸反应,不可以用浓硫酸干燥,故A选;
B、氮气不与浓硫酸反应,可以用浓硫酸干燥,故B不选;
C、二氧化碳不与浓硫酸反应,可以用浓硫酸干燥,故C不选;
D、氢气不与浓硫酸反应,可以用浓硫酸干燥,故D不选;
故选:A。
9.【答案】C
【解答】A.铝及其氧化铝能与酸、碱发生化学反应,在电解质溶液中易发生电化学腐蚀;
B.硅橡胶具有空间网状结构,具有耐磨、耐高温、耐低温等性能,硅橡胶是目前最好的既耐高温又耐低温的橡胶;
C.常温下可用铁制容器运输浓硫酸和浓硝酸,利用铁在浓硫酸、浓硝酸中发生钝化现象,阻止反应进行;
D.先用碳酸钠溶液处理,使之转化为疏松、易溶于酸的碳酸钙,碳酸钙与盐酸反应,而硫酸钙不能。
本题考查了铝、硅橡胶、浓硝酸、浓硫酸性质分析应用,为高考高频点,注意反应条件分析,钝化现象的理解应用,掌握物质性质是解题关键,侧重考查学生的分析能力,题目难度不大。
10.【答案】B
A.浓硫酸具有吸水性,因此可用作干燥剂,但不能干燥还原性气体如:硫化氢、碱性气体如:氨气等气体,故A错误;
B.浓硫酸具有脱水性,因而能使蔗糖脱水炭化,故B正确;
C.浓硫酸在加热条件下能与单质碳反应,体现了浓硫酸的强氧化性,故C错误;
D.因为浓硫酸在常温下可使铁或铝钝化,因此常温下可用铁制或铝制容器储存浓硫酸,故D错误。
故选B。
11.【答案】C
【解答】A.铁与盐酸反应生成氢气,由于铁过量,则久置过程中铁发生吸氧腐蚀,则消耗氧气,故A错误;
B.碳酸钠和稀硫酸反应生成二氧化碳气体,由于碳酸钠过量,则久置过程中碳酸钠与二氧化碳反应生成碳酸氢钠,气体总物质的量减小,,故B错误;
C.Fe、Al与浓硫酸发生钝化,气体体积基本不变,,故C正确;
D.铜和浓硝酸反应生成二氧化氮气体,久置过程中二氧化氮与水反应生成NO,体积变小,,故D错误。
故选C。
12.【答案】;
;
;
;
。
【解答】浓硫酸滴到滤纸上,滤纸变黑,纸中H、O以水的形式脱出,体现浓硫酸具有脱水性;
故答案为:;
浓与木炭共热生成二氧化碳、二氧化硫和水,C元素的化合价升高,而S元素的化合价降低,体现浓硫酸具有强氧化性
故答案为:
把锌粒放入稀硫酸中时,有氢气产生,体现硫酸的酸性;
故答案为:;
盛有浓硫酸的烧杯敞口放置一段时间后,质量增加是因为吸收了空气中的水蒸气,体现浓硫酸的吸水性;
故答案为:;
浓与铜片共热生成、和,部分S元素的化合价降低,体现浓硫酸具有强氧化性,同时另一部分S元素未变价生成盐,体现酸性;
故答案为:。
13.【答案】浓;
溶液变成红色
产生淡黄色沉淀;硫;
溶液浅黄绿色褪去;;
溶液褪色;
吸收尾气,防止污染空气; 。
【解答】铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫气体和水,反应为浓,
故答案为:浓;
二氧化硫溶于水生成亚硫酸,亚硫酸为弱酸,所以二氧化硫溶液显示酸性,能够使紫色石蕊溶液变成红色,故答案为:溶液变成红色
装置中盛放硫化氢,硫化氢能够与二氧化硫发生氧化还原反应生成淡黄色的硫单质和水,
故答案为:产生淡黄色沉淀;硫;
氯气和二氧化硫反应生成盐酸和硫酸,氯气的颜色褪去,方程式为;
故答案为:溶液浅黄绿色褪去;;
二氧化硫具有漂白性,能够使有色物质褪色,所以装置中品红溶液褪色,故答案为:溶液褪色;
二氧化硫是一种有毒气体,多余的二氧化硫不能直接排放,避免污染空气;二氧化硫能够与氢氧化钠溶液反应:,可以用氢氧化钠溶液吸收多余的二氧化硫,
故答案为:吸收尾气,防止污染空气; 。
14.【答案】浓 将全部氧化吸收 气泡 产物中已被B瓶溶液全部吸收 溴易挥发、干扰二氧化碳的检验 澄清石灰水
【解答】浓硫酸与木炭在加热条件下的化学方程式为浓,
故答案为:浓;
二氧化碳、二氧化硫均在溶液中检验,且二者均使石灰水变浑浊,则先检验水,无水遇到水变蓝,后检验二氧化硫,除去二氧化硫后检验二氧化碳,由于产物气流通过时会带出水蒸气,所以必须设置在之前,则装置的顺序为,
故答案为:;;;;
装置中A瓶的溶液褪色,证明产物气流中有,B瓶溶液的作用为将全部氧化吸收,C瓶的溶液不褪色,且有气泡现象,证明产物中已被B瓶溶液全部吸收,
故答案为:产物气流中有;将全部氧化吸收;气泡;产物中已被B瓶溶液全部吸收;
中的离子方程式为,B中放置溴水不如高锰酸钾的原因为溴易挥发、干扰二氧化碳的检验,
故答案为:;溴易挥发、干扰二氧化碳的检验;
装置中所盛溶液是澄清石灰水,可验证的产物是,
故答案为:澄清石灰水;。
第2页,共2页
第1页,共1页
第二课时 硫酸
一、单选题
下列关于浓硫酸的性质叙述正确的是
A. 加热时与铜反应只体现酸性 B. 干燥氢气体现脱水性
C. 使白纸变黑体现吸水性 D. 加热时与碳反应体现强氧化性
下列有关说法不正确的是
A. 把浓硫酸沿着烧杯内壁加入水中配制稀硫酸
B. 少量金属钠保存在煤油中
C. 向紫色石蕊试液中不断滴入新制氯水,石蕊试液先变红后褪色
D. 溶液和胶体的本质区别是丁达尔效应
下列离子检验的方法正确的是
A. 向某溶液中加入少量硝酸银溶液,生成白色沉淀,说明原溶液中有
B. 向某溶液中加入少量氯化钡溶液,生成白色沉淀,说明原溶液中有
C. 向某溶液中加入少量氢氧化钙溶液,生成白色沉淀,说明原溶液中有
D. 向某溶液中加入足量盐酸,无现象,再加入少量溶液,产生白色沉淀,说明原溶液中有
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速度加大的是
A. 加热 B. 不用稀硫酸而用浓硫酸
C. 往溶液中加入少量固体 D. 不能铁片而用铁粉
下列反应中,浓硫酸既表现强氧化性,又表现酸性的是
固浓
浓
浓
浓
A. B. C. D.
鉴别稀硫酸和浓硫酸既简单又安全的方法是
A. 各取少量于试管中加入几片铜片
B. 用玻璃棒各蘸少许点在滤纸上
C. 各取少量于试管中滴加NaOH溶液
D. 各取少量于试管中滴加溶液
探究浓硫酸和铜的反应,下列装置或操作正确的是
A. 用装置甲进行铜和浓硫酸的反应
B. 用装置乙收集二氧化硫并吸收尾气
C. 用装置丙稀释反应后的混合液
D. 用装置丁测定余酸的浓度
下列气体中不能用浓硫酸干燥的是
A. B. C. D.
化学与生活息息相关。下列说法中错误的是
A. 铝制餐具不宜用来蒸煮或长期存放酸性、碱性或咸的食物,防止餐具被腐蚀
B. 人工合成的硅橡胶是目前最好的既耐高温又耐低温的橡胶,常用于门窗密封
C. 铁制的容器在常温下可用来存放浓硫酸或浓硝酸是因为铁不与浓硫酸或浓硝酸反应
D. 去除锅炉上的水垢,通常先用碳酸钠溶液处理,形成疏松物质而后再用酸去除
下列有关浓硫酸的说法正确的是
A. 浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体
B. 浓硫酸具有脱水性,因而能使蔗糖炭化
C. 浓硫酸在加热条件下能与单质碳反应,体现了浓硫酸的酸性和强氧化性
D. 因为浓硫酸在常温下不与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸
常温下,将液体Y一次性加入到充满的锥形瓶中装置气密性良好,若锥形瓶内气体的最大物质的量为amol,久置后气体的物质的量为bmol,则下列不满足的是
选项 X Y
A 过量c、Fe碎屑 稀盐酸
B 过量粉末 稀硫酸
C 过量Fe、Al碎屑 浓硫酸
D 过量Cu、CuO粉末 浓硝酸
A. A B. B C. C D. D
二、填空题
浓具有酸性;强氧化性;吸水性;脱水性等性质,根据题意填空填序号,可多选:
将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有 ;
浓与木炭共热生成二氧化碳、二氧化硫和水,该反应体现了浓的
把锌粒放入稀硫酸中时,有气体产生 ;
盛有浓硫酸的烧杯敞口放置一段时间后,质量增加 ;
浓硫酸和铜片加热反应,体现了浓硫酸的 。
用下图所示装置证明浓硫酸的强氧化性,并检验产物的性质。
请回答下列问题:
写出装置中的化学方程式____________。
装置中的现象为____________________。
装置中的现象为_______ ,生成除水以外的物质名称为________。
装置中的现象为____ __,反应的化学方程式为_______。
装置中的现象为____________ 。
装置中NaOH溶液的作用是__________,反应的离子方程式为:_____________________________。
书写浓硫酸与木炭在加热条件下的化学方程式为______。
试用下列各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序按产物气流从左到右的方向是填装置的编号:________________________。
实验时可观察到装置中A瓶的溶液褪色,证明,B瓶溶液的作用______,C瓶的溶液不褪色,且有______现象,证明______。
书写B中的离子方程式______。B中放置溴水不如高锰酸钾的原因______。
装置中所盛溶液是______,可验证的产物是______。
答案
1.【答案】D
【解答】A.加热时浓硫酸与金属铜反应生成二氧化硫和硫酸铜,表现了氧化性和酸性,故A错误;
B.浓硫酸具有吸水性,可以干燥中性和酸性气体,干燥氢气体现吸水性,故B错误;
C.浓硫酸具有脱水性,能使有机物中的H、O元素以水的形式脱出,使白纸变黑表现的是浓硫酸的脱水性,故C错误;
D.浓硫酸与非金属单质反应只体现浓硫酸的强氧化性,故D正确。
故选:D。
2.【答案】D
【解答】A、浓硫酸稀释放热,且密度比水大,故配制稀硫酸时应将浓硫酸沿着烧杯内壁注入水中,故A正确;
B、金属钠能和氧气、水反应,故钠应该保存在煤油中,故B正确;
C、氯水有酸性和漂白性,故能使石蕊溶液先变红后褪色,故C正确;
D、分散系根据分散质粒子直径大小分为溶液、胶体和浊液,而不是根据丁达尔效应,故D错误。
故选:D。
3.【答案】D
【解答】A.向某溶液中加入少量硝酸银溶液,有白色沉淀生成,该白色沉淀可能是碳酸银,原溶液中可能含有碳酸根离子,不一定含有氯离子,故A错误;
B.向某溶液中加入氯化钡溶液,有白色沉淀生成,该白色沉淀可能为氯化银,原溶液中可能含有银离子,不一定含有硫酸根离子,故B错误;
C.向某溶液中加入少量氢氧化钙溶液,生成白色沉淀,该白色沉淀可能为亚硫酸钙,原溶液中可能存在亚硫酸根离子,不一定有碳酸根,故C错误;
D.向某溶液中加入足量的盐酸无明显现象,说明溶液中不存在银离子,然后再加入溶液,产生白色沉淀,该白色沉淀为硫酸钡,证明原溶液中存在硫酸根离子,故D正确.
故选D.
4.【答案】B
【解答】A.加热时,温度升高,反应速率加快,故A不选;
B.常温下铁与浓硫酸发生钝化,故B选;
C.加入少量固体,铁置换出铜构成原电池,反应速率加快,故C不选;
D.铁片改用铁粉,接触面积增大,反应速率加快,故D不选;
故选B。
5.【答案】B
【解答】固体浓,只表现为酸性,故错误;
和浓硫酸反应生成、和水,没有盐生成,只表现为氧化性,故错误;
浓 ,S元素的化合价降低,浓硫酸表现为氧化性,生成,又表现为酸性,故正确;
和浓反应生成、和水,S元素的化合价降低,浓硫酸表现为氧化性,生成,又表现为酸性,故正确;
故选B。
6.【答案】B
【解答】A.Cu与稀硫酸不反应,与浓硫酸反应需要加热,可鉴别,但需要加热且生成有毒气体,故A不选;
B.用玻璃棒各蘸少许点在滤纸上,变黑的为浓硫酸,可鉴别,既简单又安全,故B选;
C.二者均反应生成硫酸钠和水,现象相同,不能鉴别,故C不选;
D.各取少量于试管中滴加溶液,均生成硫酸钡沉淀,现象相同,不能鉴别,故D不选;
故选B.
7.【答案】C
【解答】A.铜与浓硫酸常温下不反应,此反应需要加热设备,图中无加热装置,故A错误;
B.二氧化硫的密度大于空气,适用与向上排空气法收集,即应长进短出,此图方向相反,故B错误;
C.反应后的混合液中可能还含有浓硫酸,而浓硫酸在稀释过程中会释放大量热量,故正确的操作是:将混合液沿着烧杯内壁慢慢注入水中,注入过程中不断的用玻璃棒搅拌以散发热量,故C正确;
D.氢氧化钠溶液显碱性,应盛放在碱式滴定管中,图中滴定管为酸式滴定管,故D错误。
故选C。
8.【答案】A
【解答】A、氨气能与浓硫酸反应,不可以用浓硫酸干燥,故A选;
B、氮气不与浓硫酸反应,可以用浓硫酸干燥,故B不选;
C、二氧化碳不与浓硫酸反应,可以用浓硫酸干燥,故C不选;
D、氢气不与浓硫酸反应,可以用浓硫酸干燥,故D不选;
故选:A。
9.【答案】C
【解答】A.铝及其氧化铝能与酸、碱发生化学反应,在电解质溶液中易发生电化学腐蚀;
B.硅橡胶具有空间网状结构,具有耐磨、耐高温、耐低温等性能,硅橡胶是目前最好的既耐高温又耐低温的橡胶;
C.常温下可用铁制容器运输浓硫酸和浓硝酸,利用铁在浓硫酸、浓硝酸中发生钝化现象,阻止反应进行;
D.先用碳酸钠溶液处理,使之转化为疏松、易溶于酸的碳酸钙,碳酸钙与盐酸反应,而硫酸钙不能。
本题考查了铝、硅橡胶、浓硝酸、浓硫酸性质分析应用,为高考高频点,注意反应条件分析,钝化现象的理解应用,掌握物质性质是解题关键,侧重考查学生的分析能力,题目难度不大。
10.【答案】B
A.浓硫酸具有吸水性,因此可用作干燥剂,但不能干燥还原性气体如:硫化氢、碱性气体如:氨气等气体,故A错误;
B.浓硫酸具有脱水性,因而能使蔗糖脱水炭化,故B正确;
C.浓硫酸在加热条件下能与单质碳反应,体现了浓硫酸的强氧化性,故C错误;
D.因为浓硫酸在常温下可使铁或铝钝化,因此常温下可用铁制或铝制容器储存浓硫酸,故D错误。
故选B。
11.【答案】C
【解答】A.铁与盐酸反应生成氢气,由于铁过量,则久置过程中铁发生吸氧腐蚀,则消耗氧气,故A错误;
B.碳酸钠和稀硫酸反应生成二氧化碳气体,由于碳酸钠过量,则久置过程中碳酸钠与二氧化碳反应生成碳酸氢钠,气体总物质的量减小,,故B错误;
C.Fe、Al与浓硫酸发生钝化,气体体积基本不变,,故C正确;
D.铜和浓硝酸反应生成二氧化氮气体,久置过程中二氧化氮与水反应生成NO,体积变小,,故D错误。
故选C。
12.【答案】;
;
;
;
。
【解答】浓硫酸滴到滤纸上,滤纸变黑,纸中H、O以水的形式脱出,体现浓硫酸具有脱水性;
故答案为:;
浓与木炭共热生成二氧化碳、二氧化硫和水,C元素的化合价升高,而S元素的化合价降低,体现浓硫酸具有强氧化性
故答案为:
把锌粒放入稀硫酸中时,有氢气产生,体现硫酸的酸性;
故答案为:;
盛有浓硫酸的烧杯敞口放置一段时间后,质量增加是因为吸收了空气中的水蒸气,体现浓硫酸的吸水性;
故答案为:;
浓与铜片共热生成、和,部分S元素的化合价降低,体现浓硫酸具有强氧化性,同时另一部分S元素未变价生成盐,体现酸性;
故答案为:。
13.【答案】浓;
溶液变成红色
产生淡黄色沉淀;硫;
溶液浅黄绿色褪去;;
溶液褪色;
吸收尾气,防止污染空气; 。
【解答】铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫气体和水,反应为浓,
故答案为:浓;
二氧化硫溶于水生成亚硫酸,亚硫酸为弱酸,所以二氧化硫溶液显示酸性,能够使紫色石蕊溶液变成红色,故答案为:溶液变成红色
装置中盛放硫化氢,硫化氢能够与二氧化硫发生氧化还原反应生成淡黄色的硫单质和水,
故答案为:产生淡黄色沉淀;硫;
氯气和二氧化硫反应生成盐酸和硫酸,氯气的颜色褪去,方程式为;
故答案为:溶液浅黄绿色褪去;;
二氧化硫具有漂白性,能够使有色物质褪色,所以装置中品红溶液褪色,故答案为:溶液褪色;
二氧化硫是一种有毒气体,多余的二氧化硫不能直接排放,避免污染空气;二氧化硫能够与氢氧化钠溶液反应:,可以用氢氧化钠溶液吸收多余的二氧化硫,
故答案为:吸收尾气,防止污染空气; 。
14.【答案】浓 将全部氧化吸收 气泡 产物中已被B瓶溶液全部吸收 溴易挥发、干扰二氧化碳的检验 澄清石灰水
【解答】浓硫酸与木炭在加热条件下的化学方程式为浓,
故答案为:浓;
二氧化碳、二氧化硫均在溶液中检验,且二者均使石灰水变浑浊,则先检验水,无水遇到水变蓝,后检验二氧化硫,除去二氧化硫后检验二氧化碳,由于产物气流通过时会带出水蒸气,所以必须设置在之前,则装置的顺序为,
故答案为:;;;;
装置中A瓶的溶液褪色,证明产物气流中有,B瓶溶液的作用为将全部氧化吸收,C瓶的溶液不褪色,且有气泡现象,证明产物中已被B瓶溶液全部吸收,
故答案为:产物气流中有;将全部氧化吸收;气泡;产物中已被B瓶溶液全部吸收;
中的离子方程式为,B中放置溴水不如高锰酸钾的原因为溴易挥发、干扰二氧化碳的检验,
故答案为:;溴易挥发、干扰二氧化碳的检验;
装置中所盛溶液是澄清石灰水,可验证的产物是,
故答案为:澄清石灰水;。
第2页,共2页
第1页,共1页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
