第6章常用的金属和盐章末复习-2021-2022学年九年级化学沪教版(上海)下册(word版有答案)
文档属性
| 名称 | 第6章常用的金属和盐章末复习-2021-2022学年九年级化学沪教版(上海)下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 271.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-10 00:00:00 | ||
图片预览


文档简介
第6章《常用的金属和盐》章末复习
一、单选题
1.下列关于“合金”的叙述:①合金中至少含有两种金属;②合金中各元素以化合物的形式存在;③合金中一定含有金属;④合金一定是混合物;⑤合金具有金属特性。其中正确的是( )
A.①②④ B.①②③ C.③④ D.③④⑤
2.某新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属线,当玻璃被击碎时,与金属线相连的警报系统就会立刻报警。“防盗玻璃”能报警,这利用了金属的( )
A.可燃性 B.导电性 C.弹性 D.导热性
3.化肥碳酸铵、硫酸钾均为白色固体。分别取少量固体进行下列实验,不能将两者区别出来的是
A.与熟石灰粉末混合研磨 B.加入稀盐酸中
C.加入溶液中 D.加入溶液中
4.下列叙述、对应的化学方程式、所属基本反应类型都正确的是( )
A.木炭不充分燃烧产生有毒物质 2C+O22CO 化合反应
B.处理印染厂排放的碱性废水 H2SO4+2NaOH=Na2SO4+H2O 复分解反应
C.天然气做燃料 CH4+2O2CO2+2H2O 氧化反应
D.钟乳石形成过程中的一个反应 CaHCO3=CaCO3↓+H2O+CO2↑ 分解反应
5.下列对化肥的认识不正确的是
A.KNO3是一种复合肥 B.施用氮肥,能促进植物茎叶生长
C.铵态氮肥不能与碱性肥料混合使用 D.化肥能提高粮食产量,施用越多越好
6.下列各组转化中,一定条件下均能一步实现的组合是
A.①② B.①③ C.②③ D.①②③
7.“珍惜资源,保护环境”是每位公民应尽的义务,下列相关做法错误的是
A.我国稀土储量世界第一,可以任意开发利用
B.研发秸秆综合利用技术,避免因直接焚烧造成大气污染
C.利用二氧化碳捕捉技术,减少我国二氧化碳引起的“温室效应”
D.改造城市排水管网,实现雨水和生活用水的分流与处理
8.某博物馆藏有一柄古代铁剑,为防止其生锈,下列做法合理的是
A.定期用清水冲洗,除去灰尘 B.放于体验区,让观众触摸
C.用盐水除去铁剑上的锈斑 D.放在充满氮气的展览柜中
9.分别用以下三组物质比较锌和铜的金属活动性:①Zn、Cu、稀硫酸;②Zn、Cu、MgSO4溶液;③Zn、CuSO4溶液。仅用组内物质就能够直接达到目的是( )
A.仅有① B.②③ C.①③ D.①②③
二、简答题
10.结合金属的物理性质,试列举常见金属或金属用途:
(1)金属光泽:_______________________________
(2)导电性:_________________________________
(3)导热性:_________________________________
(4)延展性:_________________________________
11.在山西省人民医院消化科的宣传栏里,有这样一则宣传:
(1)观察图1,集体就餐时,为避免疾病传播应该注意的是______________(写一条)。
(2)胶囊中尿素的相对分子质量是______________。农业生产所使用的化肥中,尿素可用作______肥。
三、推断题
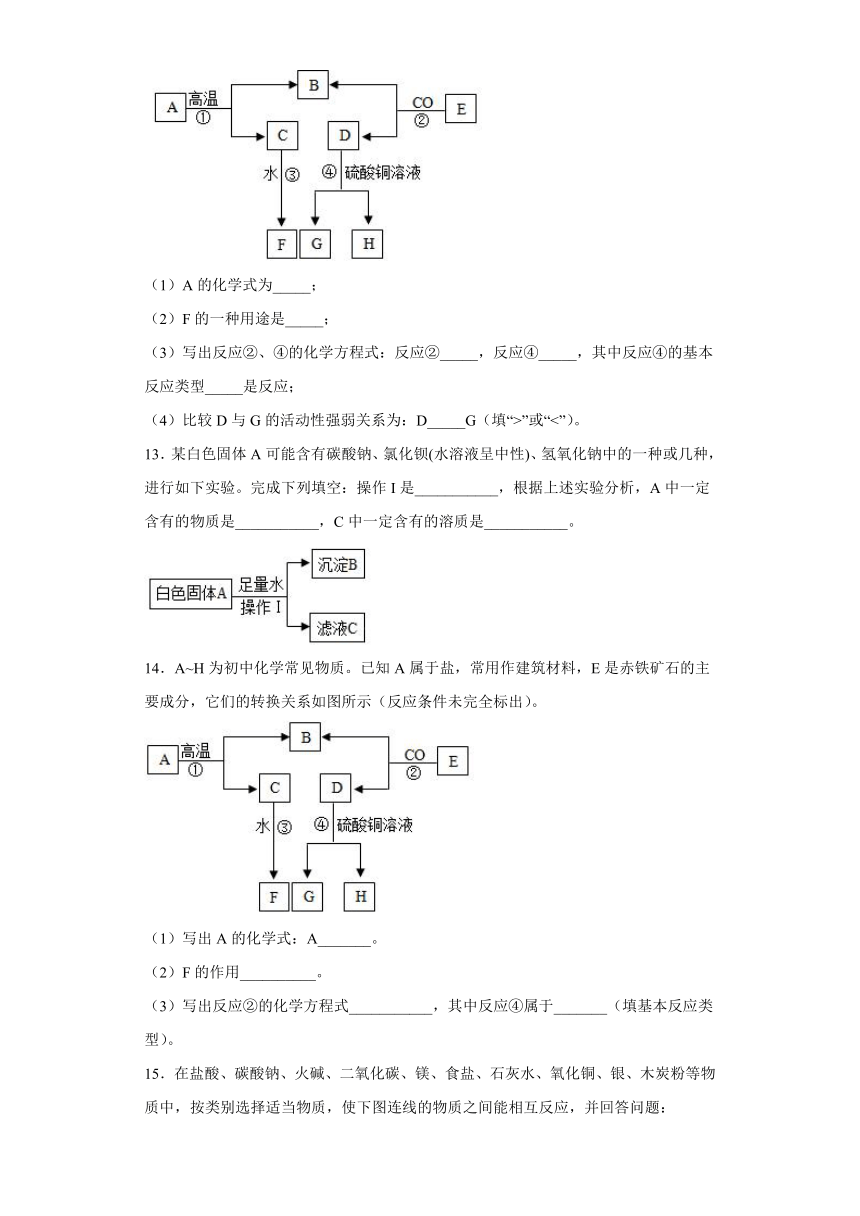
12.A~H内初中化学常见的物质。己知A属于盐,常用作建筑材料,E是红色固体,H的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全标出)。
(1)A的化学式为_____;
(2)F的一种用途是_____;
(3)写出反应②、④的化学方程式:反应②_____,反应④_____,其中反应④的基本反应类型_____是反应;
(4)比较D与G的活动性强弱关系为:D_____G(填“>”或“<”)。
13.某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性)、氢氧化钠中的一种或几种,进行如下实验。完成下列填空:操作I是___________,根据上述实验分析,A中一定含有的物质是___________,C中一定含有的溶质是___________。
14.A~H为初中化学常见物质。已知A属于盐,常用作建筑材料,E是赤铁矿石的主要成分,它们的转换关系如图所示(反应条件未完全标出)。
(1)写出A的化学式:A_______。
(2)F的作用__________。
(3)写出反应②的化学方程式___________,其中反应④属于_______(填基本反应类型)。
15.在盐酸、碳酸钠、火碱、二氧化碳、镁、食盐、石灰水、氧化铜、银、木炭粉等物质中,按类别选择适当物质,使下图连线的物质之间能相互反应,并回答问题:
(1)写出B的名称________.
(2)写出D的化学式________.
(3)写出E和F反应的化学方程式____________________________________________.
四、实验题
16.化学是以实验为基础的科学,根据以下实验探究回答下列问题。
(1)甲中同时向烧杯中加入等量品红,静置,发现整杯热水变红的时间比冷水短。请从微观角度分析,这是因为___________。
(2)根据乙中铜片上的不同现象可得出燃烧需要条件是___________。
(3)丙的目的是探究___________(填物质名称)对铁生锈有无影响。
(4)丁实验的现象是___________,可得到的结论是___________。
17.实验是学习化学的重要途径,下列是教材中的三个基本实验,请回答下列问题。
(1)实验A中标号①仪器的名称是____,利用该装置用高锰酸钾制取氧气,未能收集到两瓶氧气,可能的原因是____。
A 没有塞紧橡胶塞
B 试管口没有放棉花
C 收集时没有及时更换到第二瓶
D 加热前已将集气瓶灌满水倒立于水槽中
(2)实验B是通过证明生成物的___推断水的组成的。将燃着的木条靠近打开活塞后的两个玻璃管的尖嘴口,观察现象,得出关于水的组成的结论是_______。
(3)实验C中观察到的现象是__,反应的化学方程式为__。
五、计算题
18.尿素〔CO(NH2)2〕是化肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。
(1)尿素属于化肥中的______肥(填“氮”“钾”或“复合”)。
(2)CO(NH2)2中共含有______(写数字)种元素;
(3)CO(NH2)2的相对分子质量是______
(4)CO(NH2)2中C、H、N、O元素的质量比为______。
19.某碳酸钠样品中含少量氯化钠,化学兴趣小组的同学欲通过实验来测定样品中碳酸钠的质量分数。他们取6g该样品,配制成溶液,再向其中加入足量的氯化钙溶液(呈中性),测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示。请回答下列问题:
(1)该样品中碳酸钠的质量分数是多少?(写出计算步骤,计算结果精确到0.1%)
(2)如果反应开始前,向烧杯中滴加几滴无色酚酞试液,在整个测定过程中可观察到的现象是: 。
试卷第1页,共3页
参考答案:
1.D
2.B
3.C
4.A
5.D
6.C
7.A
8.D
9.C
10. 金银首饰 铝、铁制作导线 用铝合金、铁制造炊具 黄金拉制成金丝,铝能够做成很薄的铝箔
11. 用公筷(或分餐制) 62 氮
12. CaCO3 用作建筑材料、保护树木、配制农药波尔多液、改良酸性土壤等(任选一,合理均可) 置换 >
13. 过滤 碳酸钠、氯化钡 氯化钠
14. CaCO3 改良酸性土壤 置换反应
15. 盐酸 Ca(OH)2 C+CO22CO
16.(1)分子在不断的运动,且温度越高,分子运动速率越快
(2)温度达到可燃物的着火点
(3)蒸馏水##水
(4) 试管①中带火星木条不复燃,试管②中产生大量气泡,带火星的木条复燃。 二氧化锰能加快双氧水的分解
17. 试管 AC 元素组成(或元素种类) 水是由氢元素和氧元素组成的 铁钉表面覆盖一层红色固体,溶液由蓝色变为浅绿色
18.(1)尿素中含有氮元素,属于化肥中的氮肥。
(2)CO(NH2)2中共含有C、O、N、H,4种元素;
(3)CO(NH2)2的相对分子质量是12+16+(14+1×2)×2=60;
(4)CO(NH2)2中C、H、N、O元素的质量比为12:(1×4):(14×2):16=3:1:7:4。
19.(1)
解:根据图示,反应中生成的碳酸钙质量为5g。
设该纯碱样品中碳酸钠的质量为 x。
X=5.3g;
该纯碱样品中碳酸钠的质量分数为:;
答:纯碱样品中碳酸钠的质量分数为88.3%;
(2)溶液由红色变为无色,有白色沉淀生成
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列关于“合金”的叙述:①合金中至少含有两种金属;②合金中各元素以化合物的形式存在;③合金中一定含有金属;④合金一定是混合物;⑤合金具有金属特性。其中正确的是( )
A.①②④ B.①②③ C.③④ D.③④⑤
2.某新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属线,当玻璃被击碎时,与金属线相连的警报系统就会立刻报警。“防盗玻璃”能报警,这利用了金属的( )
A.可燃性 B.导电性 C.弹性 D.导热性
3.化肥碳酸铵、硫酸钾均为白色固体。分别取少量固体进行下列实验,不能将两者区别出来的是
A.与熟石灰粉末混合研磨 B.加入稀盐酸中
C.加入溶液中 D.加入溶液中
4.下列叙述、对应的化学方程式、所属基本反应类型都正确的是( )
A.木炭不充分燃烧产生有毒物质 2C+O22CO 化合反应
B.处理印染厂排放的碱性废水 H2SO4+2NaOH=Na2SO4+H2O 复分解反应
C.天然气做燃料 CH4+2O2CO2+2H2O 氧化反应
D.钟乳石形成过程中的一个反应 CaHCO3=CaCO3↓+H2O+CO2↑ 分解反应
5.下列对化肥的认识不正确的是
A.KNO3是一种复合肥 B.施用氮肥,能促进植物茎叶生长
C.铵态氮肥不能与碱性肥料混合使用 D.化肥能提高粮食产量,施用越多越好
6.下列各组转化中,一定条件下均能一步实现的组合是
A.①② B.①③ C.②③ D.①②③
7.“珍惜资源,保护环境”是每位公民应尽的义务,下列相关做法错误的是
A.我国稀土储量世界第一,可以任意开发利用
B.研发秸秆综合利用技术,避免因直接焚烧造成大气污染
C.利用二氧化碳捕捉技术,减少我国二氧化碳引起的“温室效应”
D.改造城市排水管网,实现雨水和生活用水的分流与处理
8.某博物馆藏有一柄古代铁剑,为防止其生锈,下列做法合理的是
A.定期用清水冲洗,除去灰尘 B.放于体验区,让观众触摸
C.用盐水除去铁剑上的锈斑 D.放在充满氮气的展览柜中
9.分别用以下三组物质比较锌和铜的金属活动性:①Zn、Cu、稀硫酸;②Zn、Cu、MgSO4溶液;③Zn、CuSO4溶液。仅用组内物质就能够直接达到目的是( )
A.仅有① B.②③ C.①③ D.①②③
二、简答题
10.结合金属的物理性质,试列举常见金属或金属用途:
(1)金属光泽:_______________________________
(2)导电性:_________________________________
(3)导热性:_________________________________
(4)延展性:_________________________________
11.在山西省人民医院消化科的宣传栏里,有这样一则宣传:
(1)观察图1,集体就餐时,为避免疾病传播应该注意的是______________(写一条)。
(2)胶囊中尿素的相对分子质量是______________。农业生产所使用的化肥中,尿素可用作______肥。
三、推断题
12.A~H内初中化学常见的物质。己知A属于盐,常用作建筑材料,E是红色固体,H的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全标出)。
(1)A的化学式为_____;
(2)F的一种用途是_____;
(3)写出反应②、④的化学方程式:反应②_____,反应④_____,其中反应④的基本反应类型_____是反应;
(4)比较D与G的活动性强弱关系为:D_____G(填“>”或“<”)。
13.某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性)、氢氧化钠中的一种或几种,进行如下实验。完成下列填空:操作I是___________,根据上述实验分析,A中一定含有的物质是___________,C中一定含有的溶质是___________。
14.A~H为初中化学常见物质。已知A属于盐,常用作建筑材料,E是赤铁矿石的主要成分,它们的转换关系如图所示(反应条件未完全标出)。
(1)写出A的化学式:A_______。
(2)F的作用__________。
(3)写出反应②的化学方程式___________,其中反应④属于_______(填基本反应类型)。
15.在盐酸、碳酸钠、火碱、二氧化碳、镁、食盐、石灰水、氧化铜、银、木炭粉等物质中,按类别选择适当物质,使下图连线的物质之间能相互反应,并回答问题:
(1)写出B的名称________.
(2)写出D的化学式________.
(3)写出E和F反应的化学方程式____________________________________________.
四、实验题
16.化学是以实验为基础的科学,根据以下实验探究回答下列问题。
(1)甲中同时向烧杯中加入等量品红,静置,发现整杯热水变红的时间比冷水短。请从微观角度分析,这是因为___________。
(2)根据乙中铜片上的不同现象可得出燃烧需要条件是___________。
(3)丙的目的是探究___________(填物质名称)对铁生锈有无影响。
(4)丁实验的现象是___________,可得到的结论是___________。
17.实验是学习化学的重要途径,下列是教材中的三个基本实验,请回答下列问题。
(1)实验A中标号①仪器的名称是____,利用该装置用高锰酸钾制取氧气,未能收集到两瓶氧气,可能的原因是____。
A 没有塞紧橡胶塞
B 试管口没有放棉花
C 收集时没有及时更换到第二瓶
D 加热前已将集气瓶灌满水倒立于水槽中
(2)实验B是通过证明生成物的___推断水的组成的。将燃着的木条靠近打开活塞后的两个玻璃管的尖嘴口,观察现象,得出关于水的组成的结论是_______。
(3)实验C中观察到的现象是__,反应的化学方程式为__。
五、计算题
18.尿素〔CO(NH2)2〕是化肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。
(1)尿素属于化肥中的______肥(填“氮”“钾”或“复合”)。
(2)CO(NH2)2中共含有______(写数字)种元素;
(3)CO(NH2)2的相对分子质量是______
(4)CO(NH2)2中C、H、N、O元素的质量比为______。
19.某碳酸钠样品中含少量氯化钠,化学兴趣小组的同学欲通过实验来测定样品中碳酸钠的质量分数。他们取6g该样品,配制成溶液,再向其中加入足量的氯化钙溶液(呈中性),测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示。请回答下列问题:
(1)该样品中碳酸钠的质量分数是多少?(写出计算步骤,计算结果精确到0.1%)
(2)如果反应开始前,向烧杯中滴加几滴无色酚酞试液,在整个测定过程中可观察到的现象是: 。
试卷第1页,共3页
参考答案:
1.D
2.B
3.C
4.A
5.D
6.C
7.A
8.D
9.C
10. 金银首饰 铝、铁制作导线 用铝合金、铁制造炊具 黄金拉制成金丝,铝能够做成很薄的铝箔
11. 用公筷(或分餐制) 62 氮
12. CaCO3 用作建筑材料、保护树木、配制农药波尔多液、改良酸性土壤等(任选一,合理均可) 置换 >
13. 过滤 碳酸钠、氯化钡 氯化钠
14. CaCO3 改良酸性土壤 置换反应
15. 盐酸 Ca(OH)2 C+CO22CO
16.(1)分子在不断的运动,且温度越高,分子运动速率越快
(2)温度达到可燃物的着火点
(3)蒸馏水##水
(4) 试管①中带火星木条不复燃,试管②中产生大量气泡,带火星的木条复燃。 二氧化锰能加快双氧水的分解
17. 试管 AC 元素组成(或元素种类) 水是由氢元素和氧元素组成的 铁钉表面覆盖一层红色固体,溶液由蓝色变为浅绿色
18.(1)尿素中含有氮元素,属于化肥中的氮肥。
(2)CO(NH2)2中共含有C、O、N、H,4种元素;
(3)CO(NH2)2的相对分子质量是12+16+(14+1×2)×2=60;
(4)CO(NH2)2中C、H、N、O元素的质量比为12:(1×4):(14×2):16=3:1:7:4。
19.(1)
解:根据图示,反应中生成的碳酸钙质量为5g。
设该纯碱样品中碳酸钠的质量为 x。
X=5.3g;
该纯碱样品中碳酸钠的质量分数为:;
答:纯碱样品中碳酸钠的质量分数为88.3%;
(2)溶液由红色变为无色,有白色沉淀生成
答案第1页,共2页
答案第1页,共2页
