第6章常用的金属和盐单元练习-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案)
文档属性
| 名称 | 第6章常用的金属和盐单元练习-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 156.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-10 00:00:00 | ||
图片预览




文档简介
第6章《常用的金属和盐》单元练习
一、单选题
1.下列关于“合金”的叙述:①合金中至少含有两种金属;②合金中各元素以化合物的形式存在;③合金中一定含有金属;④合金一定是混合物;⑤合金具有金属特性。其中正确的是( )
A.①②④ B.①②③ C.③④ D.③④⑤
2.下列有关金属的说法正确的是
A.所有金属都呈银白色 B.常温下所有的金属都是固体
C.合金的硬度一般比各成分金属小 D.铝制品耐腐蚀是因为表面生成致密氧化膜
3.下列反应属于复分解反应的是
A.CO2+ H2O=H2CO3 B.2HC1 +Ca(OH)2=CaCl2+ 2H2O
C.2KMnO4K2MnO4+MnO2+O2↑ D.2Na+2H2O=2NaOH + H2↑
4.某同学总结的Ca(OH)2的化学性质如图,下列说法错误的是
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
5.如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是
A.水、硝酸铵
B.水、烧碱
C.稀硫酸、铁粉
D.稀盐酸、小苏打
6.工业上利用赤铁矿石(主要成分是Fe2O3,还含少量SiO2等杂质)冶炼生铁的过程如图所示,下列说法不正确的是
A.CaSiO3中硅元素显+4价
B.高炉气体中SO2会形成酸雨,不能直接排放到空气中
C.原料中焦炭的作用之一是生成具有还原性的物质CO
D.高炉炼铁的原理是,该反应属于置换反应
7.科学家发现一种新金属。根据右表信息推测其用途错误的是
熔点 2500℃
密度 3g/cm3
强度 与钢相似
导电性 良好
导热性 良好
抗腐蚀性 优异
A.用于焊接金属 B.制造航天飞机
C.制外科手术刀 D.用于通讯设备
8.X、R表示两种金属,在溶液中发生反应:X+3RNO3=3R+X(NO3)3。下列说法不正确的是
A.该反应是置换反应
B.若X是Al,R是Ag,则反应后溶液质量减少
C.X可能是Fe,R可能是Cu
D.X的金属活动性比R强
9.为了验证镁、铜、银三种金属的活动性顺序,某同学设计了如下实验,只需进行其中三个就能达到实验目的,你认为不必进行的是
A.将镁片放入稀盐酸中
B.将铜片放入稀盐酸中
C.将镁片放入硝酸银溶液中
D.将铜片放入硝酸银溶液中
10.“庄稼一枝花,全靠肥当家”。下列关于农作物和化肥的说法正确的是( )
A.(NH4)2SO4属于复合肥料
B.农作物所必需的营养元素只有氮、磷和钾三种
C.磷肥能使作物根系发达,耐寒耐旱
D.铵态氮肥与熟石灰混合施用可以明显提高肥效
11.下列说法正确的是
A.向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐
B.把燃着的木条插入某瓶无色气体中,木条熄灭,证明瓶中的气体是二氧化碳
C.取少量溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,证明该溶液中一定有硫酸根离子
D.不用任何试剂就可以把KOH、HNO3、CuSO4、MgCl2四种溶液鉴别出来
二、简答题
12.微笑自行车、高铁、网购和扫码支付等方便我们的日常生活。
(1)微笑自行车的推行符合 ______ 环保理念。
(2)高铁车体外壳采用铝合金材料,是利用该合金的 ______ 性能。
(3)许多商品的二维码印在PVC不干胶贴纸上,PVC是一种塑料。下列图标中表示塑料回收标志的是 ______ (填字母)。
(4)芯片是智能手机的核心部件,单质硅是由石英固体(SiO2)与碳在高温条件下反应制得,同时生成一种可燃性气体,该反应的化学方程式为 ______ 。
13.早在17世纪,质量守恒定律发现之前,英国化学家波义耳曾经做过一个实验:在密闭的容器中燃烧金属时,得到了金属灰,然后打开容器盖,称量金属灰的质量,发现比原来金属质量增加了。
(1)试解释金属灰质量比原金属质量增加的原因_____________。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律_______________________。
三、推断题
14.A~H内初中化学常见的物质。己知A属于盐,常用作建筑材料,E是红色固体,H的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全标出)。
(1)A的化学式为_____;
(2)F的一种用途是_____;
(3)写出反应②、④的化学方程式:反应②_____,反应④_____,其中反应④的基本反应类型_____是反应;
(4)比较D与G的活动性强弱关系为:D_____G(填“>”或“<”)。
15.A、B、C、D、E是初中化学常见的五种物质,且都含有一种相同的元素,其中A是红棕色固体,D能供给呼吸,B、E组成元素相同,它们之间的关系如图所示。“”表示物质间可一步转化,“一”表示物质间能相互反应(部分反应物、生成物及反应条件略去)。分析辨识,回答问题。
(1)D的化学式为______。
(2)写出B的一种用途______。
(3)A与E反应的化学方程式为______。
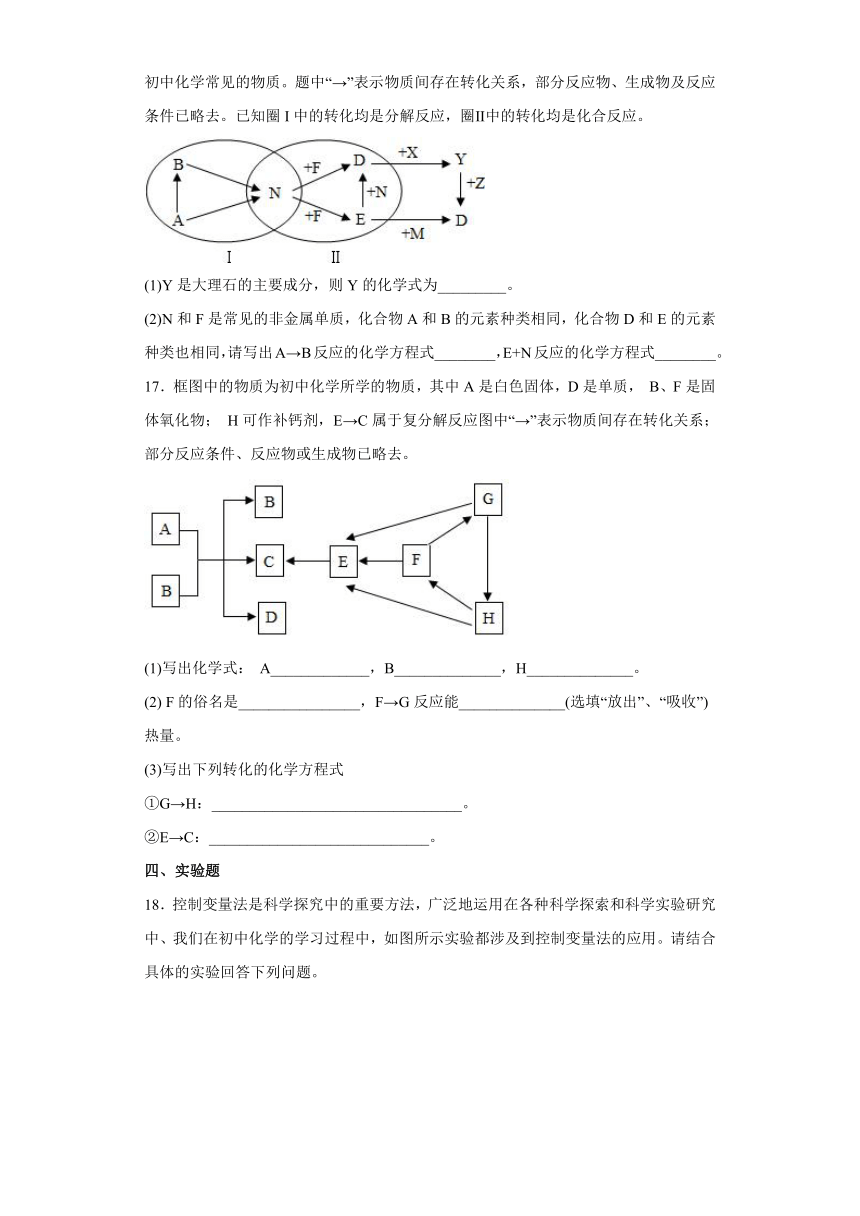
16.下列用字母表示的10种物质是由H、C、O、Ca、Cl、Fe中的几种元素组成它们是初中化学常见的物质。题中“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去。已知圈I中的转化均是分解反应,圈Ⅱ中的转化均是化合反应。
(1)Y是大理石的主要成分,则Y的化学式为_________。
(2)N和F是常见的非金属单质,化合物A和B的元素种类相同,化合物D和E的元素种类也相同,请写出A→B反应的化学方程式________,E+N反应的化学方程式________。
17.框图中的物质为初中化学所学的物质,其中A是白色固体,D是单质, B、F是固体氧化物; H可作补钙剂,E→C属于复分解反应图中“→”表示物质间存在转化关系;部分反应条件、反应物或生成物已略去。
(1)写出化学式: A_____________,B______________,H______________。
(2) F的俗名是________________,F→G反应能______________(选填“放出”、“吸收”)热量。
(3)写出下列转化的化学方程式
①G→H:_________________________________。
②E→C:_____________________________。
四、实验题
18.控制变量法是科学探究中的重要方法,广泛地运用在各种科学探索和科学实验研究中、我们在初中化学的学习过程中,如图所示实验都涉及到控制变量法的应用。请结合具体的实验回答下列问题。
(1)实验1是“探究铁的锈蚀条件”中的一组对比实验,根据①中铁钉生锈的现象,得出铁生锈的条件是______;其中试管②中的水需要事先煮沸,目的是______;
(2)实验2中向等量的井水和纯净水中分别滴入等量的X试剂,观察到井水中产生大量浮渣,则X试剂为______;
(3)实验3中紫色的干石蕊纸花喷水后放入二氧化碳中,观察到的现象是______。
19.利用下图所示装置进行实验。
(1)A中电子秤示数变化的原因是______。
(2)B中观察到的现象为______。
(3)C中反应的化学方程式为______。
(4)以上实验能验证质量守恒定律的是______(填序号)。
20.如图三个实验均可验证无现象的化学反应发生了。
【实验一】当观察到______现象时,证明化学反应发生,化学方程式是______。
【实验二】加入 X 可验证稀硫酸与NaOH 能发生反应,符合此条件的X 是______。
A.FeCl3 B. C.Na2CO3 D.
【实验三】用气压传感器测得曲线1 和2,要证明CO2 与NaOH 一定发生了反应,左瓶中应加入______;曲线 1 变化平缓的原因是______。
【反思】上述实验的设计思想是通过证明______,来判断化学反应的发生。
五、计算题
21.向一定量的稀硫酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如图所示。求:
(1)此过程中产生氢气的最大质量是 克。
(2)锌粉中锌的质量分数为多少。(请写出计算过程)
22.某工厂生产的NaCl产品中含有杂质MgCl2,化学兴趣小组取100g样品完全溶解于313.6g水中,向该溶液中分5次加入一定浓度的氢氧化钠溶液,每次30g,充分反应。测得实验数据如下表所示:
次数 第1次 第2次 第3次 第4次 第5次
加入氢氧化钠溶液的质量/g 30 30 30 30 30
累计生成沉淀的质量/g 2.9 5.8 8.7 11.6 11.6
(注:发生反应的化学方程式为 MgCl2+2NaOH = Mg(OH)2↓+2NaCl)
请完成下列各题:
(1)第___________次恰好完全反应。
(2)样品中MgCl2的质量是___________g。
(3)计算恰好完全反应时所得溶液的溶质质量分数(写出规范的计算过程)。
23.生铁和钢都是铁和碳的合金,生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%,化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取11.5g铁合金样品盛放到锥形瓶中,将100g稀盐酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
次数 加盐酸前 第1次 第2次 第3次 第4次 第5次
加入稀盐酸的质量(g) 0 20 20 20 20 20
锥形瓶内物质的总质量(g) 11.5 31.4 m 71.2 91.1 111.1
【查阅资料】碳不与稀盐酸反应。
请回答下列问题:
(1)根据质量守恒定律,该反应中生成气体的总质量为 。
(2)实验数据表中m的值为 。
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到0.1%)。
试卷第1页,共3页
参考答案:
1.D
2.D
3.B
4.A
5.A
6.D
7.A
8.C
9.C
10.C
11.D
12. 低碳或节能减排等 密度小或耐腐蚀或硬度大或熔点高等 A SiO2+2C2CO↑+Si
13. 金属燃烧是金属和氧气发生化合反应,生成金属氧化物。根据质量守恒定律可知,参加反应的金属与氧气的质量之和等于生成的金属氧化物的质量。生成的金属灰是金属氧化物,所以金属灰的质量比原来金属的质量增加了。 分别称量反应前后密闭容器的质量。
14. CaCO3 用作建筑材料、保护树木、配制农药波尔多液、改良酸性土壤等(任选一,合理均可) 置换 >
15. O2 灭火
16.(1)CaCO3
(2)
17. KClO3 MnO2 CaCO3 生石灰 放出
18.(1) 与氧气接触 除去水中溶有的少量的氧气
(2)肥皂水
(3)紫色石蕊纸花变红
19. 浓硫酸具有吸水性,会吸收空气中的水分 产生气泡,溶液由无色变为浅绿色 C
20. 溶液由红色变为无色 A 20mL水 CO2 在水中的溶解度较小且与水反应的量小 反应物已转化为其他物质
21.(1)0.8g;(2)80%
22.(1) 4 (2) 解:设生成氢氧化镁的质量为y
y=19g。
答:样品中MgCl2的质量是19g。
(3)解:设生成氯化钠的质量为x
得x = 23.4 g
恰好完全反应后所得溶液的溶质质量为:100g-19g+23.4g=104.4g
恰好完全反应后所得溶液的质量为:100g+313.6g+4×30g-11.6g=522g
恰好完全反应后所得溶液的溶质质量分数为:
答:恰好完全反应后所得溶液溶质质量分数为20%。
23.(1)0.4g;(2)51.3;(3)2.6%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列关于“合金”的叙述:①合金中至少含有两种金属;②合金中各元素以化合物的形式存在;③合金中一定含有金属;④合金一定是混合物;⑤合金具有金属特性。其中正确的是( )
A.①②④ B.①②③ C.③④ D.③④⑤
2.下列有关金属的说法正确的是
A.所有金属都呈银白色 B.常温下所有的金属都是固体
C.合金的硬度一般比各成分金属小 D.铝制品耐腐蚀是因为表面生成致密氧化膜
3.下列反应属于复分解反应的是
A.CO2+ H2O=H2CO3 B.2HC1 +Ca(OH)2=CaCl2+ 2H2O
C.2KMnO4K2MnO4+MnO2+O2↑ D.2Na+2H2O=2NaOH + H2↑
4.某同学总结的Ca(OH)2的化学性质如图,下列说法错误的是
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
5.如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是
A.水、硝酸铵
B.水、烧碱
C.稀硫酸、铁粉
D.稀盐酸、小苏打
6.工业上利用赤铁矿石(主要成分是Fe2O3,还含少量SiO2等杂质)冶炼生铁的过程如图所示,下列说法不正确的是
A.CaSiO3中硅元素显+4价
B.高炉气体中SO2会形成酸雨,不能直接排放到空气中
C.原料中焦炭的作用之一是生成具有还原性的物质CO
D.高炉炼铁的原理是,该反应属于置换反应
7.科学家发现一种新金属。根据右表信息推测其用途错误的是
熔点 2500℃
密度 3g/cm3
强度 与钢相似
导电性 良好
导热性 良好
抗腐蚀性 优异
A.用于焊接金属 B.制造航天飞机
C.制外科手术刀 D.用于通讯设备
8.X、R表示两种金属,在溶液中发生反应:X+3RNO3=3R+X(NO3)3。下列说法不正确的是
A.该反应是置换反应
B.若X是Al,R是Ag,则反应后溶液质量减少
C.X可能是Fe,R可能是Cu
D.X的金属活动性比R强
9.为了验证镁、铜、银三种金属的活动性顺序,某同学设计了如下实验,只需进行其中三个就能达到实验目的,你认为不必进行的是
A.将镁片放入稀盐酸中
B.将铜片放入稀盐酸中
C.将镁片放入硝酸银溶液中
D.将铜片放入硝酸银溶液中
10.“庄稼一枝花,全靠肥当家”。下列关于农作物和化肥的说法正确的是( )
A.(NH4)2SO4属于复合肥料
B.农作物所必需的营养元素只有氮、磷和钾三种
C.磷肥能使作物根系发达,耐寒耐旱
D.铵态氮肥与熟石灰混合施用可以明显提高肥效
11.下列说法正确的是
A.向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐
B.把燃着的木条插入某瓶无色气体中,木条熄灭,证明瓶中的气体是二氧化碳
C.取少量溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,证明该溶液中一定有硫酸根离子
D.不用任何试剂就可以把KOH、HNO3、CuSO4、MgCl2四种溶液鉴别出来
二、简答题
12.微笑自行车、高铁、网购和扫码支付等方便我们的日常生活。
(1)微笑自行车的推行符合 ______ 环保理念。
(2)高铁车体外壳采用铝合金材料,是利用该合金的 ______ 性能。
(3)许多商品的二维码印在PVC不干胶贴纸上,PVC是一种塑料。下列图标中表示塑料回收标志的是 ______ (填字母)。
(4)芯片是智能手机的核心部件,单质硅是由石英固体(SiO2)与碳在高温条件下反应制得,同时生成一种可燃性气体,该反应的化学方程式为 ______ 。
13.早在17世纪,质量守恒定律发现之前,英国化学家波义耳曾经做过一个实验:在密闭的容器中燃烧金属时,得到了金属灰,然后打开容器盖,称量金属灰的质量,发现比原来金属质量增加了。
(1)试解释金属灰质量比原金属质量增加的原因_____________。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律_______________________。
三、推断题
14.A~H内初中化学常见的物质。己知A属于盐,常用作建筑材料,E是红色固体,H的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全标出)。
(1)A的化学式为_____;
(2)F的一种用途是_____;
(3)写出反应②、④的化学方程式:反应②_____,反应④_____,其中反应④的基本反应类型_____是反应;
(4)比较D与G的活动性强弱关系为:D_____G(填“>”或“<”)。
15.A、B、C、D、E是初中化学常见的五种物质,且都含有一种相同的元素,其中A是红棕色固体,D能供给呼吸,B、E组成元素相同,它们之间的关系如图所示。“”表示物质间可一步转化,“一”表示物质间能相互反应(部分反应物、生成物及反应条件略去)。分析辨识,回答问题。
(1)D的化学式为______。
(2)写出B的一种用途______。
(3)A与E反应的化学方程式为______。
16.下列用字母表示的10种物质是由H、C、O、Ca、Cl、Fe中的几种元素组成它们是初中化学常见的物质。题中“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去。已知圈I中的转化均是分解反应,圈Ⅱ中的转化均是化合反应。
(1)Y是大理石的主要成分,则Y的化学式为_________。
(2)N和F是常见的非金属单质,化合物A和B的元素种类相同,化合物D和E的元素种类也相同,请写出A→B反应的化学方程式________,E+N反应的化学方程式________。
17.框图中的物质为初中化学所学的物质,其中A是白色固体,D是单质, B、F是固体氧化物; H可作补钙剂,E→C属于复分解反应图中“→”表示物质间存在转化关系;部分反应条件、反应物或生成物已略去。
(1)写出化学式: A_____________,B______________,H______________。
(2) F的俗名是________________,F→G反应能______________(选填“放出”、“吸收”)热量。
(3)写出下列转化的化学方程式
①G→H:_________________________________。
②E→C:_____________________________。
四、实验题
18.控制变量法是科学探究中的重要方法,广泛地运用在各种科学探索和科学实验研究中、我们在初中化学的学习过程中,如图所示实验都涉及到控制变量法的应用。请结合具体的实验回答下列问题。
(1)实验1是“探究铁的锈蚀条件”中的一组对比实验,根据①中铁钉生锈的现象,得出铁生锈的条件是______;其中试管②中的水需要事先煮沸,目的是______;
(2)实验2中向等量的井水和纯净水中分别滴入等量的X试剂,观察到井水中产生大量浮渣,则X试剂为______;
(3)实验3中紫色的干石蕊纸花喷水后放入二氧化碳中,观察到的现象是______。
19.利用下图所示装置进行实验。
(1)A中电子秤示数变化的原因是______。
(2)B中观察到的现象为______。
(3)C中反应的化学方程式为______。
(4)以上实验能验证质量守恒定律的是______(填序号)。
20.如图三个实验均可验证无现象的化学反应发生了。
【实验一】当观察到______现象时,证明化学反应发生,化学方程式是______。
【实验二】加入 X 可验证稀硫酸与NaOH 能发生反应,符合此条件的X 是______。
A.FeCl3 B. C.Na2CO3 D.
【实验三】用气压传感器测得曲线1 和2,要证明CO2 与NaOH 一定发生了反应,左瓶中应加入______;曲线 1 变化平缓的原因是______。
【反思】上述实验的设计思想是通过证明______,来判断化学反应的发生。
五、计算题
21.向一定量的稀硫酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如图所示。求:
(1)此过程中产生氢气的最大质量是 克。
(2)锌粉中锌的质量分数为多少。(请写出计算过程)
22.某工厂生产的NaCl产品中含有杂质MgCl2,化学兴趣小组取100g样品完全溶解于313.6g水中,向该溶液中分5次加入一定浓度的氢氧化钠溶液,每次30g,充分反应。测得实验数据如下表所示:
次数 第1次 第2次 第3次 第4次 第5次
加入氢氧化钠溶液的质量/g 30 30 30 30 30
累计生成沉淀的质量/g 2.9 5.8 8.7 11.6 11.6
(注:发生反应的化学方程式为 MgCl2+2NaOH = Mg(OH)2↓+2NaCl)
请完成下列各题:
(1)第___________次恰好完全反应。
(2)样品中MgCl2的质量是___________g。
(3)计算恰好完全反应时所得溶液的溶质质量分数(写出规范的计算过程)。
23.生铁和钢都是铁和碳的合金,生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%,化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取11.5g铁合金样品盛放到锥形瓶中,将100g稀盐酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
次数 加盐酸前 第1次 第2次 第3次 第4次 第5次
加入稀盐酸的质量(g) 0 20 20 20 20 20
锥形瓶内物质的总质量(g) 11.5 31.4 m 71.2 91.1 111.1
【查阅资料】碳不与稀盐酸反应。
请回答下列问题:
(1)根据质量守恒定律,该反应中生成气体的总质量为 。
(2)实验数据表中m的值为 。
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到0.1%)。
试卷第1页,共3页
参考答案:
1.D
2.D
3.B
4.A
5.A
6.D
7.A
8.C
9.C
10.C
11.D
12. 低碳或节能减排等 密度小或耐腐蚀或硬度大或熔点高等 A SiO2+2C2CO↑+Si
13. 金属燃烧是金属和氧气发生化合反应,生成金属氧化物。根据质量守恒定律可知,参加反应的金属与氧气的质量之和等于生成的金属氧化物的质量。生成的金属灰是金属氧化物,所以金属灰的质量比原来金属的质量增加了。 分别称量反应前后密闭容器的质量。
14. CaCO3 用作建筑材料、保护树木、配制农药波尔多液、改良酸性土壤等(任选一,合理均可) 置换 >
15. O2 灭火
16.(1)CaCO3
(2)
17. KClO3 MnO2 CaCO3 生石灰 放出
18.(1) 与氧气接触 除去水中溶有的少量的氧气
(2)肥皂水
(3)紫色石蕊纸花变红
19. 浓硫酸具有吸水性,会吸收空气中的水分 产生气泡,溶液由无色变为浅绿色 C
20. 溶液由红色变为无色 A 20mL水 CO2 在水中的溶解度较小且与水反应的量小 反应物已转化为其他物质
21.(1)0.8g;(2)80%
22.(1) 4 (2) 解:设生成氢氧化镁的质量为y
y=19g。
答:样品中MgCl2的质量是19g。
(3)解:设生成氯化钠的质量为x
得x = 23.4 g
恰好完全反应后所得溶液的溶质质量为:100g-19g+23.4g=104.4g
恰好完全反应后所得溶液的质量为:100g+313.6g+4×30g-11.6g=522g
恰好完全反应后所得溶液的溶质质量分数为:
答:恰好完全反应后所得溶液溶质质量分数为20%。
23.(1)0.4g;(2)51.3;(3)2.6%
答案第1页,共2页
答案第1页,共2页
