第6章常用的金属和盐测试题-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案)
文档属性
| 名称 | 第6章常用的金属和盐测试题-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 202.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-10 00:00:00 | ||
图片预览



文档简介
第6章《常用的金属和盐》测试题
一、单选题
1.农作物生长需要含较多氮、磷、钾元素的化肥,下列化肥属于含磷复合肥料的是
A.NH4NO3 B.Ca(H2PO4)2 C.(NH4)2HPO4 D.KNO3
2.金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是
A.熔点很高 B.有良好的导电性、导热性
C.银白色的固体 D.硬度很大
3.空气中含①N2 ②O2 ③稀有气体 ④水蒸气等成分,其中与钢铁生锈有关的是( )
A.①③ B.②④ C.③④ D.①④
4.2018年3月9日,特朗普正式签署关税令“对进口钢铁和铝分别征收25%的关税”,这一做法严重违反国际贸易规则,严重损害我国利益。下列选项中不属于合金的是
A.钢 B.金刚石 C.焊锡 D.黄铜
5.已知金属锰在金属活动性顺序中位于铝和锌之间.下列化学反应不能发生的是( )
A.Mn+2HCl=MnCl2+H2↑ B.Mg+MnSO4=MgSO4+Mn
C.Fe+MnSO4=FeSO4+Mn D.Mn+CuSO4=MnSO4+Cu
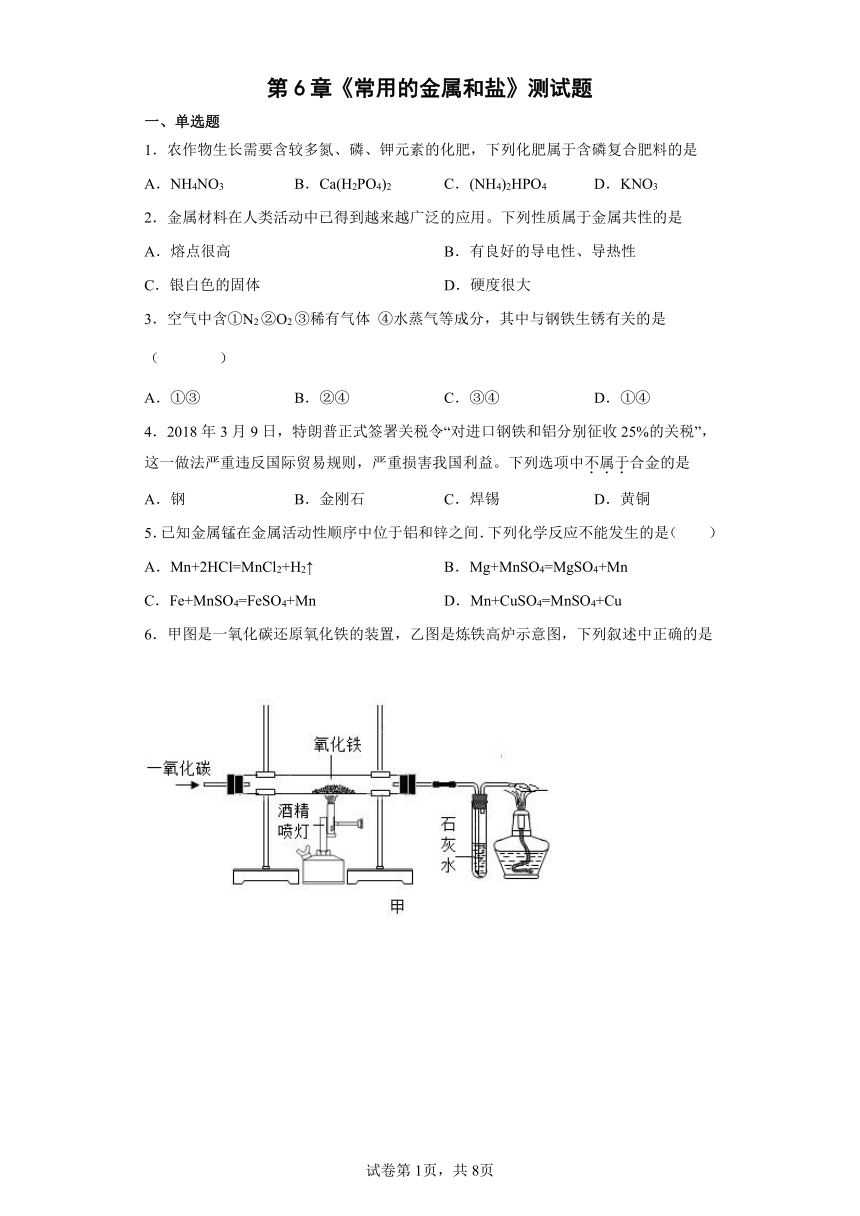
6.甲图是一氧化碳还原氧化铁的装置,乙图是炼铁高炉示意图,下列叙述中正确的是
A.甲图中实验开始时应先点燃加热氧化铁的酒精喷灯,再通CO
B.乙图炼铁中原料焦炭的作用只是提供热量
C.高炉炼制出的生铁是铁合金的一种,属于合成材料
D.一氧化碳还原氧化铁的反应中,一氧化碳是还原剂,一氧化碳发生了氧化反应
7.河道两旁有甲、乙两厂,它们排放的工业废水中共含有H+、Na+、Ba2+、Cl-、SO、CO六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,甲厂废水中的离子是( )
A.H+、Na+、Ba2+
B.H+、Ba2+、Cl-
C.Na+、SO、CO
D.H+、SO、CO
8.下列有关实验操作、现象、解释或结论都正确的一组是( )
选项 实验操作 现象 解释或结论
A 将水加入浓硫酸中配置成稀硫酸,将镁条置于其中 有气泡产生 Mg是活泼金属
B 验纯后,将纯净氢气直接在空气中点燃 产生淡蓝色火焰 氢气可以在空气中安静的燃烧
C 向一未知无色溶液中,加入适量的稀盐酸溶液 有无色气体产生 该无色未知溶液中一定有CO32﹣
D 将ag的铁钉投入到硫酸铜溶液中,反应一段时间后,取出、洗净、烘干、称量为bg 铁钉上覆盖一层红色的物质 金属活动顺序为:Fe>Cu,且析出铜的质量为(b﹣a)g
A.A B.B C.C D.D
9.向AgNO3和 Cu(NO3)2混合溶液中加入一定量的Zn、Fe和Cu的混合粉末,充分反应后过滤,洗涤,得到滤渣和滤液。下列说法正确的有( )
①滤渣中一定有Ag,滤液中可能有Fe(NO3)2、Cu(NO3)2、AgNO3
②当滤液为蓝色时,滤渣中一定有Cu、Ag,一定没有Zn、Fe
③向滤渣中加入盐酸,有气泡产生,则滤渣中一定有Fe、Cu、Ag,可能有Zn
④向滤液中加入KCl溶液,无明显现象,则滤液中一定有Zn(NO3)2,可能有Fe(NO3)2、Cu(NO3)2,滤渣中可能有Zn、Fe、Cu
A.1种 B.2种 C.3种 D.4种
10.线上学习,居家实验。小明用三枚洁净无锈的铁钉,设计如右图所示实验,探究铁生锈的条件。下列说法错误的是
A.乙试管中植物油的作用是隔绝空气
B.只有甲试管中的铁钉有明显锈迹
C.乙丙两支试管的实验现象说明铁生锈需要水
D.实验表明铁生锈是铁与空气和水共同作用的结果
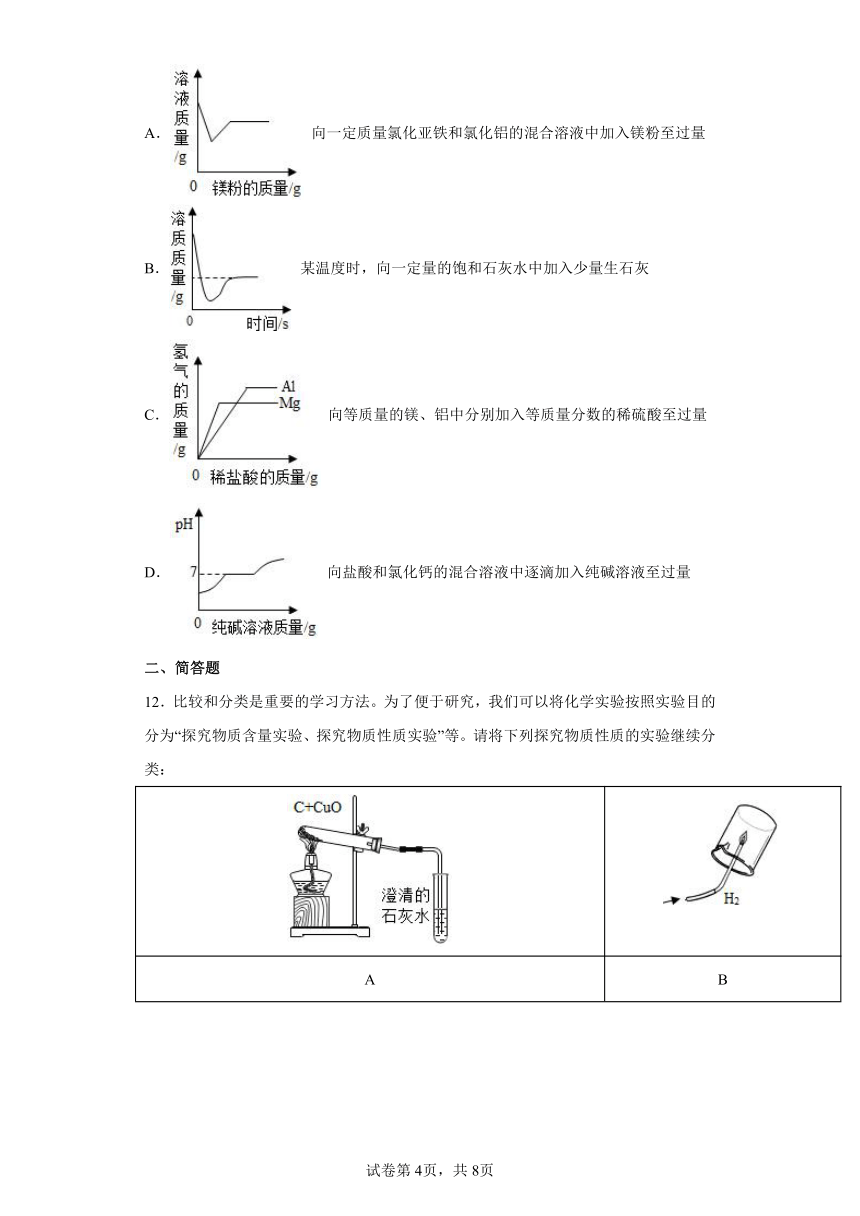
11.下列图像不能正确反映对应变化关系的是
A. 向一定质量氯化亚铁和氯化铝的混合溶液中加入镁粉至过量
B. 某温度时,向一定量的饱和石灰水中加入少量生石灰
C. 向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量
D. 向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
二、简答题
12.比较和分类是重要的学习方法。为了便于研究,我们可以将化学实验按照实验目的分为“探究物质含量实验、探究物质性质实验”等。请将下列探究物质性质的实验继续分类:
A B
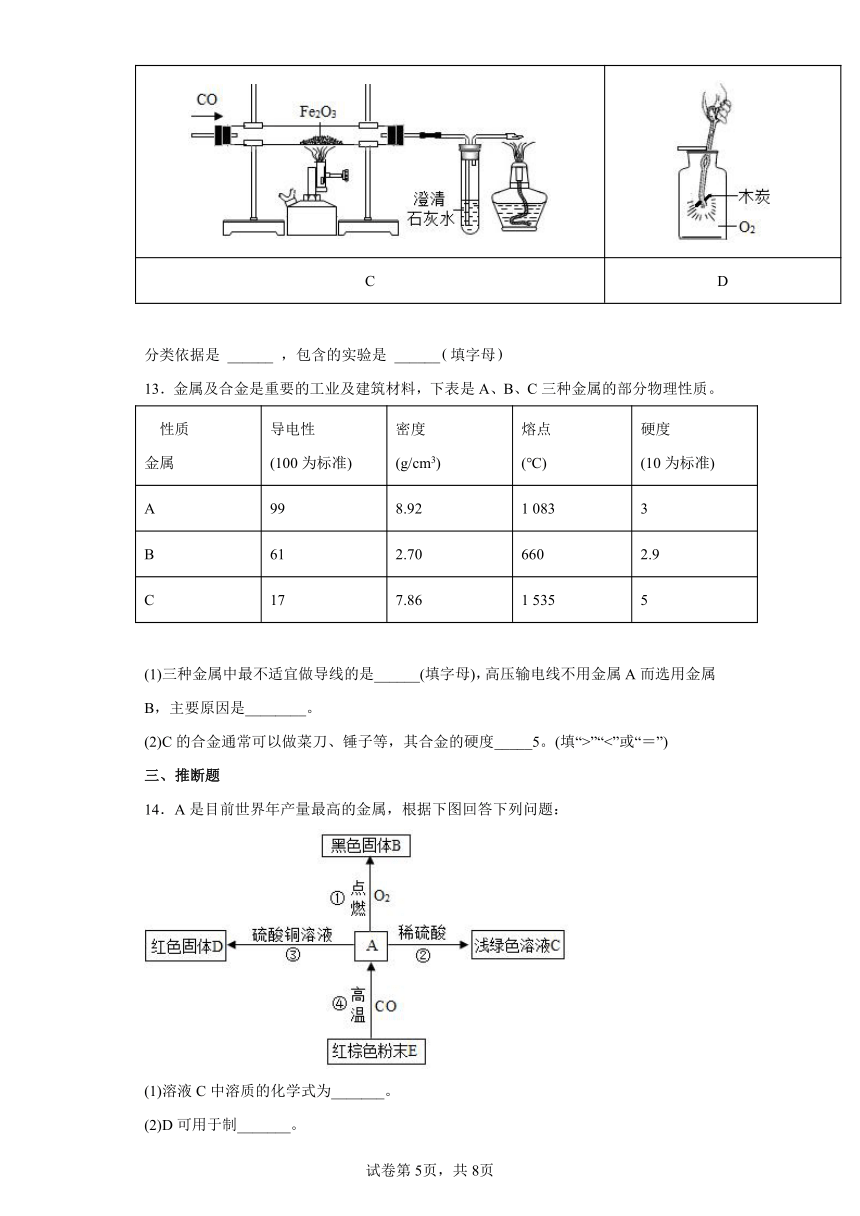
C D
分类依据是 ______ ,包含的实验是 ______填字母
13.金属及合金是重要的工业及建筑材料,下表是A、B、C三种金属的部分物理性质。
性质 金属 导电性 (100为标准) 密度 (g/cm3) 熔点 (℃) 硬度 (10为标准)
A 99 8.92 1 083 3
B 61 2.70 660 2.9
C 17 7.86 1 535 5
(1)三种金属中最不适宜做导线的是______(填字母),高压输电线不用金属A而选用金属B,主要原因是________。
(2)C的合金通常可以做菜刀、锤子等,其合金的硬度_____5。(填“>”“<”或“=”)
三、推断题
14.A是目前世界年产量最高的金属,根据下图回答下列问题:
(1)溶液C中溶质的化学式为_______。
(2)D可用于制_______。
(3)③的化学反应方程式为_______,此反应可证明铜的金属活动性比铁_______。
(4)④的化学反应方程式为_______。①的基本反应类型是_______。
15.A~J是初中化学常见的物质,其中B与D可配制波尔多液F是黑色氧化物、I是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为_______。
(2)G 的一种用途是_______。
(3)反应②的基本反应类型为_______。
(4)反应③的化学方程式为_______。
16.已知A B C D 甲为初中化学常见的物质,A在农业上用于改良酸性土壤,C用于生产玻璃,造纸纺织等工业,甲为参与大气循环的物质,它们之间的转化关系如图所示
(1)D的化学式为______。
(2)反应②的化学方程式为______。它属于______(填基本反应类型)
四、实验题
17.设计对比实验是化学研究常用的方法,如图是化学小组设计的铁钉锈蚀条件的探究实验。
(1)要达到实验目的还需补充什么实验______?
(2)写出用盐酸除铁锈(Fe2O3)的化学方程式______。
18.小杰设计了如下图所示装置(铁架台等固定装置略去)来验证石蜡中含碳、氢两种元素。装置A中可观察到_______________,证明石蜡中含有__________元素;装置B中可观察到__________,证明石蜡中含有______________元素。
19.无土栽培是利用营养液栽培作物的一种方法.
(1)下列化学肥料中属于复合肥的是 __________ (填序号).
①硝酸铵 ②磷酸二氢铵 ③硝酸钾 ④硫酸
(2)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量为 _________ g.
(3)现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验.
根据以上实验,请你进行有关推断.
①由实验1可确定原营养液中一定没有的物质是 _____________ ;
②根据实验1、实验2推测原营养液的组成可能有 ____________ 种情况;
③若测得原营养液中K+和Cl一的数目之比为1:1,则原营养液的组成中的溶质是 ____________ .
五、计算题
20.为测定某黄铜(铜锌合金)样品中铜的含量,某化学兴趣小组分三次进行实验,实验数据如下表,请计算。
所取药品 第一次 第二次 第三次
黄铜样品质量(g) 12 10 10
稀盐酸质量(g) 100 100 150
生成气体质量(g) 0.2 0.2 0.2
(1)第___________次实验中,药品成分恰好完全反应;
(2)所用稀盐酸中溶质的质量分数(写计算过程,精确到0.1%)
21.2019年12月我国第一艘国产航母“山东舰”投入使用,航母的许多元件使用了黄铜。为测定某黄铜(假设合金中仅含铜,锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得数据如下表所示:
实验序号 ① ② ③ ④
加入稀硫酸的质量(g) 20 20 20 20
烧杯中剩余物质的质量(g) 39.92 59.84 79.80 99.80
(1)第①次反应生成氢气的质量为_____g。
(2)实验序号为_____的实验,硫酸完全反应。
(3)计算稀硫酸中溶质的质量分数(写出计算过程)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.B
4.B
5.C
6.D
7.B
8.B
9.C
10.C
11.C
12. 都是探究物质的还原性实验(合理即可) AC(合理即可)
13. C 高压输电线一般需横截面较大的导线,且架设较高,故需导电性较好,密度较小的金属B而不用A >
14. FeSO4 作导线 弱 化合
15. Cu 清洁燃料,或冶炼金属 置换反应 Ca(OH)2+H2SO4=CaSO4+2H2O
16. NaOH 复分解反应
17. 补充铁钉在干燥空气中不(或“是否”)生锈的实验 Fe2O3 + 6HCl ===2 FeCl 3+ 3H2O
18. 白色固体变成蓝色 氢 澄清石灰水变浑浊 碳
19. ②③ 3 K2CO3 两 KCl、Ca(NO3)2
20.(1)二;
(2)解:设所用稀盐酸中溶质的质量分数为x
x=7.3%
答:所用稀盐酸中溶质的质量分数为7.3%。
21.(1)0.08
(2)①②
(3)解:设20g稀硫酸中溶质的质量分数为x
x=19.6%
答:稀硫酸中溶质的质量分数为19.6%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.农作物生长需要含较多氮、磷、钾元素的化肥,下列化肥属于含磷复合肥料的是
A.NH4NO3 B.Ca(H2PO4)2 C.(NH4)2HPO4 D.KNO3
2.金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是
A.熔点很高 B.有良好的导电性、导热性
C.银白色的固体 D.硬度很大
3.空气中含①N2 ②O2 ③稀有气体 ④水蒸气等成分,其中与钢铁生锈有关的是( )
A.①③ B.②④ C.③④ D.①④
4.2018年3月9日,特朗普正式签署关税令“对进口钢铁和铝分别征收25%的关税”,这一做法严重违反国际贸易规则,严重损害我国利益。下列选项中不属于合金的是
A.钢 B.金刚石 C.焊锡 D.黄铜
5.已知金属锰在金属活动性顺序中位于铝和锌之间.下列化学反应不能发生的是( )
A.Mn+2HCl=MnCl2+H2↑ B.Mg+MnSO4=MgSO4+Mn
C.Fe+MnSO4=FeSO4+Mn D.Mn+CuSO4=MnSO4+Cu
6.甲图是一氧化碳还原氧化铁的装置,乙图是炼铁高炉示意图,下列叙述中正确的是
A.甲图中实验开始时应先点燃加热氧化铁的酒精喷灯,再通CO
B.乙图炼铁中原料焦炭的作用只是提供热量
C.高炉炼制出的生铁是铁合金的一种,属于合成材料
D.一氧化碳还原氧化铁的反应中,一氧化碳是还原剂,一氧化碳发生了氧化反应
7.河道两旁有甲、乙两厂,它们排放的工业废水中共含有H+、Na+、Ba2+、Cl-、SO、CO六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,甲厂废水中的离子是( )
A.H+、Na+、Ba2+
B.H+、Ba2+、Cl-
C.Na+、SO、CO
D.H+、SO、CO
8.下列有关实验操作、现象、解释或结论都正确的一组是( )
选项 实验操作 现象 解释或结论
A 将水加入浓硫酸中配置成稀硫酸,将镁条置于其中 有气泡产生 Mg是活泼金属
B 验纯后,将纯净氢气直接在空气中点燃 产生淡蓝色火焰 氢气可以在空气中安静的燃烧
C 向一未知无色溶液中,加入适量的稀盐酸溶液 有无色气体产生 该无色未知溶液中一定有CO32﹣
D 将ag的铁钉投入到硫酸铜溶液中,反应一段时间后,取出、洗净、烘干、称量为bg 铁钉上覆盖一层红色的物质 金属活动顺序为:Fe>Cu,且析出铜的质量为(b﹣a)g
A.A B.B C.C D.D
9.向AgNO3和 Cu(NO3)2混合溶液中加入一定量的Zn、Fe和Cu的混合粉末,充分反应后过滤,洗涤,得到滤渣和滤液。下列说法正确的有( )
①滤渣中一定有Ag,滤液中可能有Fe(NO3)2、Cu(NO3)2、AgNO3
②当滤液为蓝色时,滤渣中一定有Cu、Ag,一定没有Zn、Fe
③向滤渣中加入盐酸,有气泡产生,则滤渣中一定有Fe、Cu、Ag,可能有Zn
④向滤液中加入KCl溶液,无明显现象,则滤液中一定有Zn(NO3)2,可能有Fe(NO3)2、Cu(NO3)2,滤渣中可能有Zn、Fe、Cu
A.1种 B.2种 C.3种 D.4种
10.线上学习,居家实验。小明用三枚洁净无锈的铁钉,设计如右图所示实验,探究铁生锈的条件。下列说法错误的是
A.乙试管中植物油的作用是隔绝空气
B.只有甲试管中的铁钉有明显锈迹
C.乙丙两支试管的实验现象说明铁生锈需要水
D.实验表明铁生锈是铁与空气和水共同作用的结果
11.下列图像不能正确反映对应变化关系的是
A. 向一定质量氯化亚铁和氯化铝的混合溶液中加入镁粉至过量
B. 某温度时,向一定量的饱和石灰水中加入少量生石灰
C. 向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量
D. 向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
二、简答题
12.比较和分类是重要的学习方法。为了便于研究,我们可以将化学实验按照实验目的分为“探究物质含量实验、探究物质性质实验”等。请将下列探究物质性质的实验继续分类:
A B
C D
分类依据是 ______ ,包含的实验是 ______填字母
13.金属及合金是重要的工业及建筑材料,下表是A、B、C三种金属的部分物理性质。
性质 金属 导电性 (100为标准) 密度 (g/cm3) 熔点 (℃) 硬度 (10为标准)
A 99 8.92 1 083 3
B 61 2.70 660 2.9
C 17 7.86 1 535 5
(1)三种金属中最不适宜做导线的是______(填字母),高压输电线不用金属A而选用金属B,主要原因是________。
(2)C的合金通常可以做菜刀、锤子等,其合金的硬度_____5。(填“>”“<”或“=”)
三、推断题
14.A是目前世界年产量最高的金属,根据下图回答下列问题:
(1)溶液C中溶质的化学式为_______。
(2)D可用于制_______。
(3)③的化学反应方程式为_______,此反应可证明铜的金属活动性比铁_______。
(4)④的化学反应方程式为_______。①的基本反应类型是_______。
15.A~J是初中化学常见的物质,其中B与D可配制波尔多液F是黑色氧化物、I是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为_______。
(2)G 的一种用途是_______。
(3)反应②的基本反应类型为_______。
(4)反应③的化学方程式为_______。
16.已知A B C D 甲为初中化学常见的物质,A在农业上用于改良酸性土壤,C用于生产玻璃,造纸纺织等工业,甲为参与大气循环的物质,它们之间的转化关系如图所示
(1)D的化学式为______。
(2)反应②的化学方程式为______。它属于______(填基本反应类型)
四、实验题
17.设计对比实验是化学研究常用的方法,如图是化学小组设计的铁钉锈蚀条件的探究实验。
(1)要达到实验目的还需补充什么实验______?
(2)写出用盐酸除铁锈(Fe2O3)的化学方程式______。
18.小杰设计了如下图所示装置(铁架台等固定装置略去)来验证石蜡中含碳、氢两种元素。装置A中可观察到_______________,证明石蜡中含有__________元素;装置B中可观察到__________,证明石蜡中含有______________元素。
19.无土栽培是利用营养液栽培作物的一种方法.
(1)下列化学肥料中属于复合肥的是 __________ (填序号).
①硝酸铵 ②磷酸二氢铵 ③硝酸钾 ④硫酸
(2)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量为 _________ g.
(3)现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验.
根据以上实验,请你进行有关推断.
①由实验1可确定原营养液中一定没有的物质是 _____________ ;
②根据实验1、实验2推测原营养液的组成可能有 ____________ 种情况;
③若测得原营养液中K+和Cl一的数目之比为1:1,则原营养液的组成中的溶质是 ____________ .
五、计算题
20.为测定某黄铜(铜锌合金)样品中铜的含量,某化学兴趣小组分三次进行实验,实验数据如下表,请计算。
所取药品 第一次 第二次 第三次
黄铜样品质量(g) 12 10 10
稀盐酸质量(g) 100 100 150
生成气体质量(g) 0.2 0.2 0.2
(1)第___________次实验中,药品成分恰好完全反应;
(2)所用稀盐酸中溶质的质量分数(写计算过程,精确到0.1%)
21.2019年12月我国第一艘国产航母“山东舰”投入使用,航母的许多元件使用了黄铜。为测定某黄铜(假设合金中仅含铜,锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得数据如下表所示:
实验序号 ① ② ③ ④
加入稀硫酸的质量(g) 20 20 20 20
烧杯中剩余物质的质量(g) 39.92 59.84 79.80 99.80
(1)第①次反应生成氢气的质量为_____g。
(2)实验序号为_____的实验,硫酸完全反应。
(3)计算稀硫酸中溶质的质量分数(写出计算过程)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.B
4.B
5.C
6.D
7.B
8.B
9.C
10.C
11.C
12. 都是探究物质的还原性实验(合理即可) AC(合理即可)
13. C 高压输电线一般需横截面较大的导线,且架设较高,故需导电性较好,密度较小的金属B而不用A >
14. FeSO4 作导线 弱 化合
15. Cu 清洁燃料,或冶炼金属 置换反应 Ca(OH)2+H2SO4=CaSO4+2H2O
16. NaOH 复分解反应
17. 补充铁钉在干燥空气中不(或“是否”)生锈的实验 Fe2O3 + 6HCl ===2 FeCl 3+ 3H2O
18. 白色固体变成蓝色 氢 澄清石灰水变浑浊 碳
19. ②③ 3 K2CO3 两 KCl、Ca(NO3)2
20.(1)二;
(2)解:设所用稀盐酸中溶质的质量分数为x
x=7.3%
答:所用稀盐酸中溶质的质量分数为7.3%。
21.(1)0.08
(2)①②
(3)解:设20g稀硫酸中溶质的质量分数为x
x=19.6%
答:稀硫酸中溶质的质量分数为19.6%。
答案第1页,共2页
答案第1页,共2页
