第6章常用的金属和盐单元练习-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案)
文档属性
| 名称 | 第6章常用的金属和盐单元练习-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 118.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-10 00:00:00 | ||
图片预览


文档简介
第6章《常用的金属和盐》单元练习
一、单选题
1.下列有关金属材料的说法中正确的是( )
A.地壳中含量最高的金属元素是铁
B.钢的性能优良,所以钢是纯净的铁
C.多数合金的抗腐蚀性能比组成它们的纯金属更好
D.银的导电性最好,大多数电线都是用银作材料
2.某农用物资店的货架上待售的化肥有(NH4)2SO4、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是
A.氮肥
B.磷肥
C.钾肥
D.复合肥料
3.下列四种化肥样品中,分别加入熟石灰混合,研磨后能闻到刺激性气味的是( )
A.尿素 B.磷矿粉 C.氯化铵 D.硝酸钾
4.下列化学方程式书写正确的是( )
A.2H2+O2=2H2O
B.2NaOH+H2SO4=Na2SO4+H2O
C.2Fe+6HCl=2FeCl3+3H2↑
D.2KMnO4K2MnO4+MnO2+O2↑
5.验证铝、铜、银的金属活动性强弱,小明设计了以下四组实验,下列说法不正确的是
A.通过①②实验,可以证明金属活动性Al>Cu
B.通过①②③实验,可以证明金属活动性Al>Cu>Ag
C.若要用实验④证明金属活动性Al>Cu,X可以为Al,Y为CuSO4溶液
D.若要用实验④证明金属活动性Cu>Ag,X可以为Cu,Y为AgNO3溶液
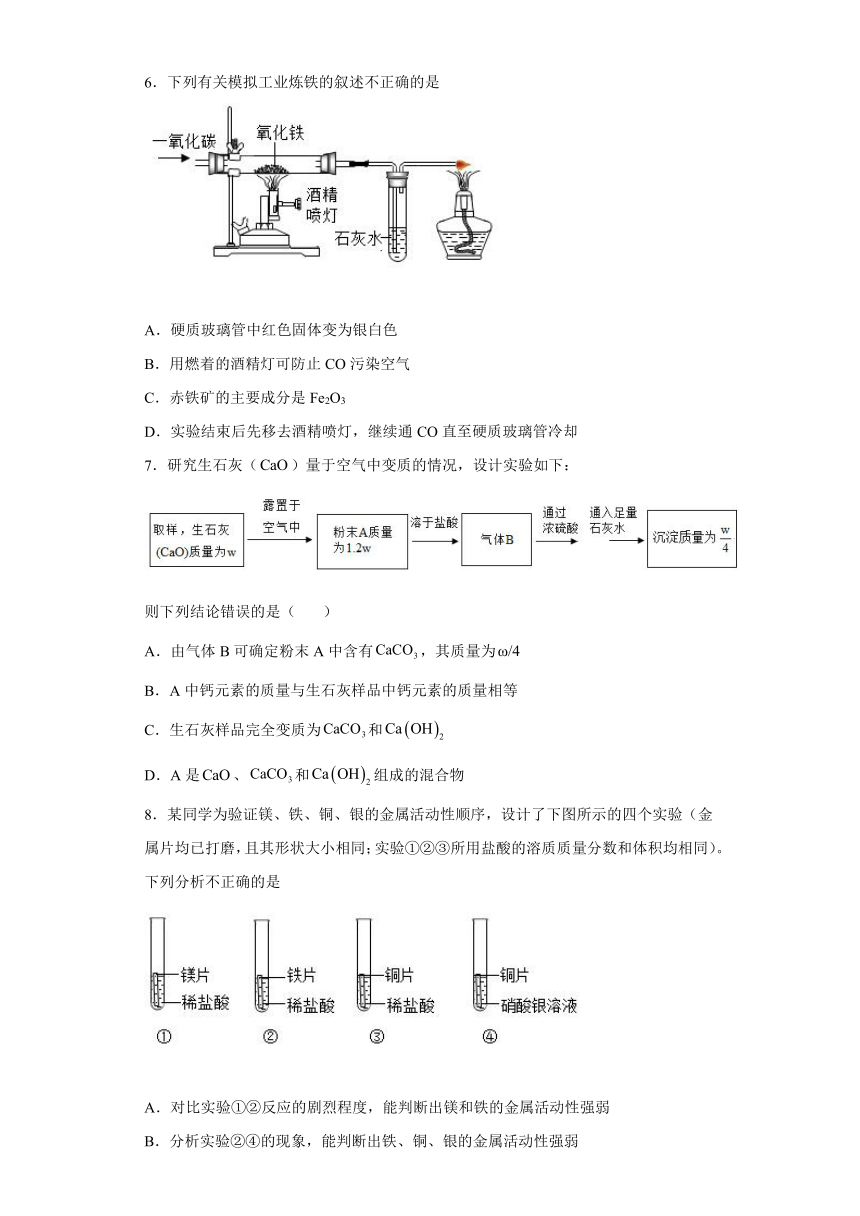
6.下列有关模拟工业炼铁的叙述不正确的是
A.硬质玻璃管中红色固体变为银白色
B.用燃着的酒精灯可防止CO污染空气
C.赤铁矿的主要成分是Fe2O3
D.实验结束后先移去酒精喷灯,继续通CO直至硬质玻璃管冷却
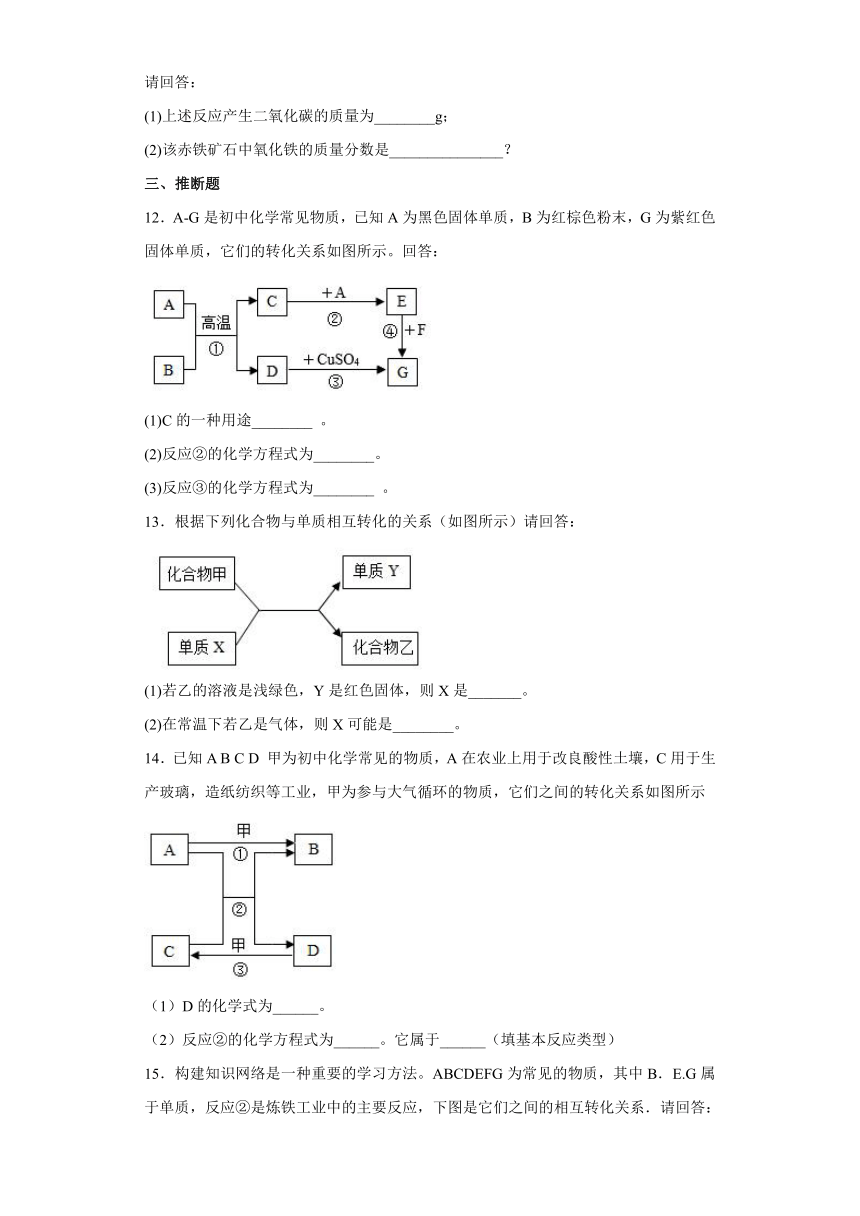
7.研究生石灰()量于空气中变质的情况,设计实验如下:
则下列结论错误的是( )
A.由气体B可确定粉末A中含有,其质量为
B.A中钙元素的质量与生石灰样品中钙元素的质量相等
C.生石灰样品完全变质为和
D.A是、和组成的混合物
8.某同学为验证镁、铁、铜、银的金属活动性顺序,设计了下图所示的四个实验(金属片均已打磨,且其形状大小相同;实验①②③所用盐酸的溶质质量分数和体积均相同)。下列分析不正确的是
A.对比实验①②反应的剧烈程度,能判断出镁和铁的金属活动性强弱
B.分析实验②④的现象,能判断出铁、铜、银的金属活动性强弱
C.分析实验④的现象,能判断出铜和银的金属活动性强弱
D.分析四个实验的现象,能判断出镁、铁、铜、银的金属活动性顺序
二、简答题
9.下列是初中化学常见仪器与实验。
(1)A图中仪器的名称是_______。
(2)取用块状大理石用到的是_______(填字母)图中仪器。
(3)D图为检验氧气是否收集满的操作,请将明显的错误加以改正_______。
(4)E图中能够说明Cu和Ag活动性顺序的现象是_______。
10.某同学用下图所示方法检验铵盐(所用硫酸铵、氢氧化钠、试纸均未失效)。一段时间后,发现试纸的颜色无明显变化。
(1)请分析没有观察到实验现象的可能原因(答两点)____________、_____________;
(2)硫酸铵属于化肥中的_______肥,该化肥不能与碱性物质混合使用的原因是___________。
11.为测定某赤铁矿石中氧化铁的质量分数,小雨同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,氢氧化钠溶液总质量与反应时间的变化关系如图。
请回答:
(1)上述反应产生二氧化碳的质量为________g;
(2)该赤铁矿石中氧化铁的质量分数是_______________?
三、推断题
12.A-G是初中化学常见物质,已知A为黑色固体单质,B为红棕色粉末,G为紫红色固体单质,它们的转化关系如图所示。回答:
(1)C的一种用途________ 。
(2)反应②的化学方程式为________。
(3)反应③的化学方程式为________ 。
13.根据下列化合物与单质相互转化的关系(如图所示)请回答:
(1)若乙的溶液是浅绿色,Y是红色固体,则X是_______。
(2)在常温下若乙是气体,则X可能是________。
14.已知A B C D 甲为初中化学常见的物质,A在农业上用于改良酸性土壤,C用于生产玻璃,造纸纺织等工业,甲为参与大气循环的物质,它们之间的转化关系如图所示
(1)D的化学式为______。
(2)反应②的化学方程式为______。它属于______(填基本反应类型)
15.构建知识网络是一种重要的学习方法。ABCDEFG为常见的物质,其中B.E.G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系.请回答:
(1)A物质的化学式 _____
(2)写出反应②的化学方程式 _____ ;固态C物质在实际生活中的一种用途是 _____
(3)写出反应③中生成红色固体的化学方程式 _____
(4)写出物质G和A在加热条件下反应的化学方程式 _____
四、实验题
16.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
17.为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。【提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性】。
(1)以上操作中所发生的复分解反应共有_______个。
(2)操作①、③、⑤用到同一种玻璃仪器,该仪器在操作⑤中的作用是什么______?
(3)请设计实验方案证明操作是③所得溶液中含有NaOH______。(写出实验步骤和现象)
18.小明同学为了研究影响铁生锈的因素,进行了如下实验:在A、B、C、D四只烧瓶中分别放入干燥的细铁丝,浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝(使细铁丝完全浸没在食盐水中)(四只烧瓶中细铁丝的质量均相同),然后装配成如图所示的四套装置,每隔0.5小时测量导管中水面上升的高度,结果如表所示:请回答:
烧瓶 时间(h) 0 0.5 1.0 1.5 2.0 2.5 3.0
A 干燥的细铁丝 0 0 0 0 0 0 0
B 浸过食盐水的细铁丝 0 0.4 1.2 3.4 5.6 7.6 9.8
C 浸过清水的细铁丝 0 0 0 0.3 0.8 2.0 3.5
D 完全浸没在食盐水中的细铁丝 0 0 0 0 0 0 0
(1)以上实验中,铁生锈速率最大的是___________瓶(填烧瓶号,下同)
(2)证明铁生锈需要水参与,应选择的烧瓶是___________。
(3)证明食盐能促进铁生锈,应选择的烧瓶是___________。
(4)为了防止钢铁生锈,人们常采用表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法,这些方法的共同原理是___________。
五、计算题
19.生铁是含碳量为2%~4.3%的铁合金,其特点为坚硬、耐磨、铸造性好。实验小组同学为测定某生铁样品(假设生铁样品中只含铁和碳)中的含碳量,设计并完成了如图所示实验。
请计算:
(1)产生氢气的质量为 g。
(2)该生铁样品中碳的质量分数为多少?(计算结果精确到0.1%)。
20.洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
第一次 第二次 第三次 第四次 第五次
加入Na2CO3溶液的质量/g 20.0 20.0 20.0 20.0 20.0
反应后溶液的总质量/g 118.9 137.8 M 175.6 195.6
请根据实验数据分析解答下列问题:
(1)表格中M的数值为 。
(2)恰好完全反应时消耗Na2CO3的质量是多少
(3)该洁厕灵中HC1的质量分数是多少?
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.D
5.B
6.A
7.C
8.B
9. 蒸发皿 C 应将带火星的木条放在集气瓶口 铜片的表面覆盖一层银白色物质,溶液颜色由无色变为蓝色
10. 没有加热 反应物浓度过低(或所用药品均为稀溶液等,其他合理答案均可) 氮 防止降低肥效(或反应放出氨气使化肥失效等,其他合理答案均可)
11. 6.6 80%
12.(1)灭火(不唯一)
(2)CO2+C2CO
(3)Fe+CuSO4=Cu+FeSO4
13.(1)Fe
(2)C
14. NaOH 复分解反应
15. CuO 3CO+Fe2O32Fe+3CO2 人工降雨 CuCl2+Fe=FeCl2+Cu CuO+H2Cu+H2O
16. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
17. 6 防止因局部温度过高,造成液滴飞溅 取操作③后溶液,加入过量的氯化钙溶液,静置,取上层清液,滴加酚酞试液溶液变红色,证明存在氢氧化钠
18.(1)B
(2)AC
(3)BC
(4)隔绝氧气和水
19.(1)0.4
(2)解:设该生铁样品中碳的质量分数为x
答:生铁样品中碳的质量分数为2.6%。
20.(1)156.7;(2)10.6g;(3)7.3%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列有关金属材料的说法中正确的是( )
A.地壳中含量最高的金属元素是铁
B.钢的性能优良,所以钢是纯净的铁
C.多数合金的抗腐蚀性能比组成它们的纯金属更好
D.银的导电性最好,大多数电线都是用银作材料
2.某农用物资店的货架上待售的化肥有(NH4)2SO4、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是
A.氮肥
B.磷肥
C.钾肥
D.复合肥料
3.下列四种化肥样品中,分别加入熟石灰混合,研磨后能闻到刺激性气味的是( )
A.尿素 B.磷矿粉 C.氯化铵 D.硝酸钾
4.下列化学方程式书写正确的是( )
A.2H2+O2=2H2O
B.2NaOH+H2SO4=Na2SO4+H2O
C.2Fe+6HCl=2FeCl3+3H2↑
D.2KMnO4K2MnO4+MnO2+O2↑
5.验证铝、铜、银的金属活动性强弱,小明设计了以下四组实验,下列说法不正确的是
A.通过①②实验,可以证明金属活动性Al>Cu
B.通过①②③实验,可以证明金属活动性Al>Cu>Ag
C.若要用实验④证明金属活动性Al>Cu,X可以为Al,Y为CuSO4溶液
D.若要用实验④证明金属活动性Cu>Ag,X可以为Cu,Y为AgNO3溶液
6.下列有关模拟工业炼铁的叙述不正确的是
A.硬质玻璃管中红色固体变为银白色
B.用燃着的酒精灯可防止CO污染空气
C.赤铁矿的主要成分是Fe2O3
D.实验结束后先移去酒精喷灯,继续通CO直至硬质玻璃管冷却
7.研究生石灰()量于空气中变质的情况,设计实验如下:
则下列结论错误的是( )
A.由气体B可确定粉末A中含有,其质量为
B.A中钙元素的质量与生石灰样品中钙元素的质量相等
C.生石灰样品完全变质为和
D.A是、和组成的混合物
8.某同学为验证镁、铁、铜、银的金属活动性顺序,设计了下图所示的四个实验(金属片均已打磨,且其形状大小相同;实验①②③所用盐酸的溶质质量分数和体积均相同)。下列分析不正确的是
A.对比实验①②反应的剧烈程度,能判断出镁和铁的金属活动性强弱
B.分析实验②④的现象,能判断出铁、铜、银的金属活动性强弱
C.分析实验④的现象,能判断出铜和银的金属活动性强弱
D.分析四个实验的现象,能判断出镁、铁、铜、银的金属活动性顺序
二、简答题
9.下列是初中化学常见仪器与实验。
(1)A图中仪器的名称是_______。
(2)取用块状大理石用到的是_______(填字母)图中仪器。
(3)D图为检验氧气是否收集满的操作,请将明显的错误加以改正_______。
(4)E图中能够说明Cu和Ag活动性顺序的现象是_______。
10.某同学用下图所示方法检验铵盐(所用硫酸铵、氢氧化钠、试纸均未失效)。一段时间后,发现试纸的颜色无明显变化。
(1)请分析没有观察到实验现象的可能原因(答两点)____________、_____________;
(2)硫酸铵属于化肥中的_______肥,该化肥不能与碱性物质混合使用的原因是___________。
11.为测定某赤铁矿石中氧化铁的质量分数,小雨同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,氢氧化钠溶液总质量与反应时间的变化关系如图。
请回答:
(1)上述反应产生二氧化碳的质量为________g;
(2)该赤铁矿石中氧化铁的质量分数是_______________?
三、推断题
12.A-G是初中化学常见物质,已知A为黑色固体单质,B为红棕色粉末,G为紫红色固体单质,它们的转化关系如图所示。回答:
(1)C的一种用途________ 。
(2)反应②的化学方程式为________。
(3)反应③的化学方程式为________ 。
13.根据下列化合物与单质相互转化的关系(如图所示)请回答:
(1)若乙的溶液是浅绿色,Y是红色固体,则X是_______。
(2)在常温下若乙是气体,则X可能是________。
14.已知A B C D 甲为初中化学常见的物质,A在农业上用于改良酸性土壤,C用于生产玻璃,造纸纺织等工业,甲为参与大气循环的物质,它们之间的转化关系如图所示
(1)D的化学式为______。
(2)反应②的化学方程式为______。它属于______(填基本反应类型)
15.构建知识网络是一种重要的学习方法。ABCDEFG为常见的物质,其中B.E.G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系.请回答:
(1)A物质的化学式 _____
(2)写出反应②的化学方程式 _____ ;固态C物质在实际生活中的一种用途是 _____
(3)写出反应③中生成红色固体的化学方程式 _____
(4)写出物质G和A在加热条件下反应的化学方程式 _____
四、实验题
16.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
17.为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。【提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性】。
(1)以上操作中所发生的复分解反应共有_______个。
(2)操作①、③、⑤用到同一种玻璃仪器,该仪器在操作⑤中的作用是什么______?
(3)请设计实验方案证明操作是③所得溶液中含有NaOH______。(写出实验步骤和现象)
18.小明同学为了研究影响铁生锈的因素,进行了如下实验:在A、B、C、D四只烧瓶中分别放入干燥的细铁丝,浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝(使细铁丝完全浸没在食盐水中)(四只烧瓶中细铁丝的质量均相同),然后装配成如图所示的四套装置,每隔0.5小时测量导管中水面上升的高度,结果如表所示:请回答:
烧瓶 时间(h) 0 0.5 1.0 1.5 2.0 2.5 3.0
A 干燥的细铁丝 0 0 0 0 0 0 0
B 浸过食盐水的细铁丝 0 0.4 1.2 3.4 5.6 7.6 9.8
C 浸过清水的细铁丝 0 0 0 0.3 0.8 2.0 3.5
D 完全浸没在食盐水中的细铁丝 0 0 0 0 0 0 0
(1)以上实验中,铁生锈速率最大的是___________瓶(填烧瓶号,下同)
(2)证明铁生锈需要水参与,应选择的烧瓶是___________。
(3)证明食盐能促进铁生锈,应选择的烧瓶是___________。
(4)为了防止钢铁生锈,人们常采用表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法,这些方法的共同原理是___________。
五、计算题
19.生铁是含碳量为2%~4.3%的铁合金,其特点为坚硬、耐磨、铸造性好。实验小组同学为测定某生铁样品(假设生铁样品中只含铁和碳)中的含碳量,设计并完成了如图所示实验。
请计算:
(1)产生氢气的质量为 g。
(2)该生铁样品中碳的质量分数为多少?(计算结果精确到0.1%)。
20.洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
第一次 第二次 第三次 第四次 第五次
加入Na2CO3溶液的质量/g 20.0 20.0 20.0 20.0 20.0
反应后溶液的总质量/g 118.9 137.8 M 175.6 195.6
请根据实验数据分析解答下列问题:
(1)表格中M的数值为 。
(2)恰好完全反应时消耗Na2CO3的质量是多少
(3)该洁厕灵中HC1的质量分数是多少?
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.D
5.B
6.A
7.C
8.B
9. 蒸发皿 C 应将带火星的木条放在集气瓶口 铜片的表面覆盖一层银白色物质,溶液颜色由无色变为蓝色
10. 没有加热 反应物浓度过低(或所用药品均为稀溶液等,其他合理答案均可) 氮 防止降低肥效(或反应放出氨气使化肥失效等,其他合理答案均可)
11. 6.6 80%
12.(1)灭火(不唯一)
(2)CO2+C2CO
(3)Fe+CuSO4=Cu+FeSO4
13.(1)Fe
(2)C
14. NaOH 复分解反应
15. CuO 3CO+Fe2O32Fe+3CO2 人工降雨 CuCl2+Fe=FeCl2+Cu CuO+H2Cu+H2O
16. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
17. 6 防止因局部温度过高,造成液滴飞溅 取操作③后溶液,加入过量的氯化钙溶液,静置,取上层清液,滴加酚酞试液溶液变红色,证明存在氢氧化钠
18.(1)B
(2)AC
(3)BC
(4)隔绝氧气和水
19.(1)0.4
(2)解:设该生铁样品中碳的质量分数为x
答:生铁样品中碳的质量分数为2.6%。
20.(1)156.7;(2)10.6g;(3)7.3%
答案第1页,共2页
答案第1页,共2页
