第6章常用的金属和盐综合练习-2021-2022学年九年级化学沪教版(上海)第二学期(word版 含答案)
文档属性
| 名称 | 第6章常用的金属和盐综合练习-2021-2022学年九年级化学沪教版(上海)第二学期(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 110.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-10 00:00:00 | ||
图片预览


文档简介
第6章常用的金属和盐综合练习2021-2022学年九年级化学沪教版(上海)
一、单选题
1.食品安全问题日益引起人们的重视,下列做法会损害人体健康的是 ( )
A.用小苏打烘焙糕点 B.加工火腿肠时放入过量亚硝酸钠防腐
C.用干冰冷藏食物 D.在酱油中加入铁强化剂补充铁元素
2.下列有关碳及碳的化合物的说法正确的是
A.金刚石、石墨和C60的化学性质相似,物理性质有很大差异,是因为它们由不同的原子构成
B.煤炉上放一盆水就能防止一氧化碳中毒
C.碳酸钙在医疗上可用作补钙剂
D.空气中二氧化碳含量过高可形成酸雨
3.下列说法正确的是
A.化学变化都遵循质量守恒定律,所以质量不发生改变的变化一定是化学变化
B.铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀
C.相同的木炭在氧气中燃烧比在空气中剧烈,说明反应的剧烈程度与反应物浓度有关
D.化学变化伴随有能量变化,所以有能量变化的一定是化学变化
4.“一带一路”赋予古丝绸之路崭新的时代内涵。古代染坊常用下列物质中的一种盐来处理丝绸,这种盐是
A.熟石灰 B.碳酸钾 C.乙醇 D.烧碱
5.下列防锈措施合理的是
A.经常用水冲洗自行车链条 B.在铁制暖气片上刷“银粉”
C.用“钢丝球”打磨铝锅表面 D.用过的菜刀及时用盐水清洗
6.有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,甲、丙表面出现红色物质,乙没有明显现象;再将大小相同的甲、丙分别放到相同的盐酸中,甲、丙均产生气泡,但甲产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是
A.甲>丙>乙 B.丙>乙>甲 C.甲>乙>丙 D.丙>甲>乙
7.草木灰是一种农家肥,其主要成分是K2CO3,它属于( )
A.钾肥 B.磷肥 C.氮肥 D.复合肥
8.有甲、乙、丙、丁四种金属,只有丙在自然界能以单质形态存在。含甲化合物的水溶液不能用乙制的容器盛放。将甲和丁分别放入硝酸铜溶液中,在甲表面有铜析出,而丁没有变化。这四种金属活动性顺序由弱到强的是
A.丙<丁<甲<乙 B.乙<甲<丁<丙 C.丁<甲<乙<丙 D.丙< 乙<甲<丁
9.化肥碳酸铵、硫酸钾均为白色固体。分别取少量固体进行下列实验,不能将两者区别出来的是
A.与熟石灰粉末混合研磨 B.加入稀盐酸中
C.加入溶液中 D.加入溶液中
10.下图所示反应,有关说法的错误的是
A.铝丝需要砂纸打磨
B.溶液由蓝色变为无色
C.金属活动性强弱:Al>Cu
D.反应的化学方程式为:Al+CuSO4=Cu+AlSO4
二、简答题
11.生活处处是化学。请回答:
(1)下列水的净化方法中净化程度最高的是________(填字母序号)。
A静置沉淀 B吸附沉淀 C蒸馏 D过滤
(2)制衣行业大量使用合成纤维,可用______方法区别合成纤维和羊毛制品。
(3)过度使用化肥也会造成水污染,但为了提高农作物产量又必须合理使用化肥。某稻田禾苗出现泛黄现象,此时应及时追施________(填“氮肥”或“钾肥”)。
(4)燃气公司给用户输送燃气,在初次使用之前需要通入氮气,通入氮气的目的是什么?______________。关闭燃气开关灭火,运用的原理是______
(5)植树造林提高绿化面积可降低_____ (填“温室效应”或“白色污染”)。
12.现有相同质量且相同形状的锌和铁两种金属,分别加入足量的溶质质量分数相同的稀硫酸中,产生氢气的质量与反应时间的关系如图所示。
(1)图中M代表___________(填“铁”或“锌”)。
(2)请写出锌和铁两种金属中与稀硫酸反应速率较快的化学方程式:___________。
13.用珍珠(主要成分CaCO3)加工成的“珍珠粉”是一种名贵中药材、保健品,可近年来市场上出现了一些假冒的“珍珠粉”,仅用肉眼观察难辨真假.为了向消费者提供鉴别方法,需找出真假“珍珠粉”理化性质上的差异,工商局提供了真、假“珍珠粉”样品,请你展开探究:(主要写出猜想、方案,不需要说出方案实施的具体结果)
猜想一:_____.
方案一:_____.
猜想二:_____.
方案二:_____.
猜想三:_____.
方案三:_____.
三、推断题
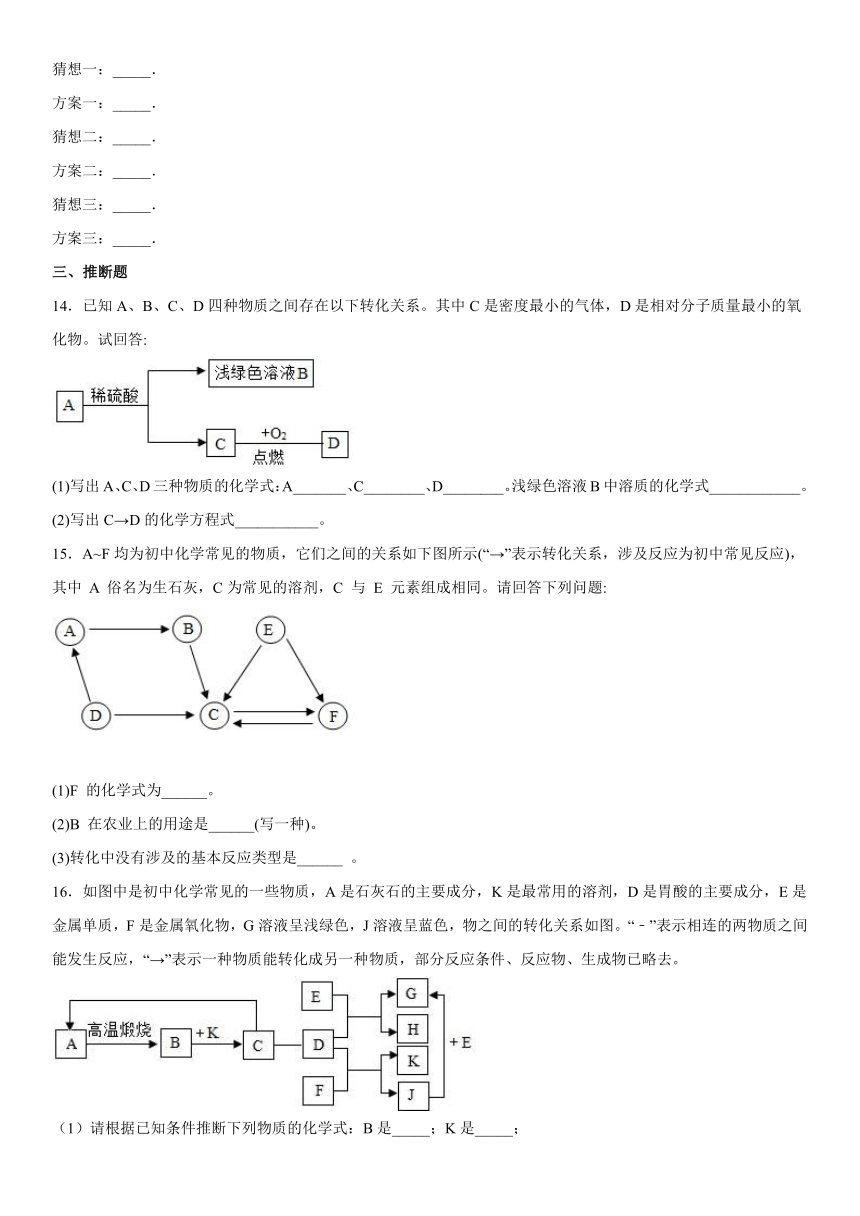
14.已知A、B、C、D四种物质之间存在以下转化关系。其中C是密度最小的气体,D是相对分子质量最小的氧化物。试回答:
(1)写出A、C、D三种物质的化学式:A_______、C________、D________。浅绿色溶液B中溶质的化学式____________。
(2)写出C→D的化学方程式___________。
15.A~F均为初中化学常见的物质,它们之间的关系如下图所示(“→”表示转化关系,涉及反应为初中常见反应),其中 A 俗名为生石灰,C为常见的溶剂,C 与 E 元素组成相同。请回答下列问题:
(1)F 的化学式为______。
(2)B 在农业上的用途是______(写一种)。
(3)转化中没有涉及的基本反应类型是______ 。
16.如图中是初中化学常见的一些物质,A是石灰石的主要成分,K是最常用的溶剂,D是胃酸的主要成分,E是金属单质,F是金属氧化物,G溶液呈浅绿色,J溶液呈蓝色,物之间的转化关系如图。“﹣”表示相连的两物质之间能发生反应,“→”表示一种物质能转化成另一种物质,部分反应条件、反应物、生成物已略去。
(1)请根据已知条件推断下列物质的化学式:B是_____;K是_____;
(2)请写出下列反应的化学方程式:
C→A:_____;
D+E→G+H:_____;
J+E→G:_____。
17.A、B、C、D、E、F是初中化学内容所涉及到的物质,其中A、B是氧化物,在一定条件下,它们的转化关系如图所示:
根据上图推断:
(1)C的化学式为 ___ 。
(2)D物质在氧气中燃烧,也能生成B,则B的化学式为 ___ 。
(3)写出D与稀硫酸反应的化学方程式 ___ 。
四、实验题
18.根据如图所示的实验探究过程,回答下列问题。
(1)图中操作①②的名称_____;
(2)固体甲的成分是_____;
(3)液体A中含有的成分除水外,还含有_____;
(4)下列有关说法中,正确的是_____;
A 无色气体是氢气
B 向固体乙中加人稀硫酸一定不会产生气泡
C 液体A的质量比原混合溶液的质量小
D 液体A和液体B均可除去铁粉中的锌粉
19.盛放氢氧化钠溶液的试剂瓶口和橡皮塞上出现了白色粉末。甲同学和乙同学对这种白色粉末的成分进行了如下猜想和验证。
(a)可能是氢氧化钠 (b)可能是碳酸钠 (c)可能是氢氧化钠与碳酸钠的混合物
(1)甲同学向所取少量粉末中滴加一种溶液后,排除了(a)的可能性。请你推测他所加的试剂和观察到的现象。_______________
(2)为了进一步探究白色粉末的成分,请你帮助乙同学设计一种方案进行鉴定,确定其成分,并写出简要的实验步骤、现象和结论。__________________
五、计算题
20.家庭厨房就是一个化学小世界,“柴米油盐”中包含着许多化学知识。食醋、食盐和纯碱都是日常生活中常用的物质。食醋中通常含有3%~5%的乙酸,乙酸俗称醋酸(化学式为CH3COOH),是一种无色液体。食盐和纯碱都是白色固体。
(1)醋酸和纯碱中属于无机物的是________(写化学式)。
(2)醋酸中,C、O两元素的质量之比为________(填最简整数比)。
21.长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。某研究性学习小组为测定水垢中碳酸钙的质量分数,将100.0g稀盐酸加人到10.0g水垢中。恰好完全反应后,容器内剩余物质的质量为106.7g。请回答:
(1)生成CO2气体的质量为________g。
(2)求测得水垢中碳酸钙的质量分数。
22.某钢铁厂用含Fe2O380%的赤铁矿石炼铁。
(1)计算Fe2O3中铁元素和氧元素的质量比______(填最简整数比)。
(2)该钢铁厂购买含Fe2O380%的赤铁矿石1000t,理论上可炼铁多少吨?
23.侯德榜成功研制了“侯氏制碱法”,打破了西方发达国家对我国制碱技术的封锁,为世界制碱工业做出了杰出贡献。某工厂为了测定用“侯氏制碱法”制得的纯碱样品中纯碱的质量分数,工厂技术员完成了图所示的测定工作(不考虑其它因素对测定结果的影响),请根据图中数据计算:样品中纯碱的质量分数。(计算结果精确到0.1%)
试卷第1页,共3页
参考答案:
1.B
2.C
3.C
4.B
5.B
6.A
7.A
8.A
9.C
10.D
11. C 燃烧闻气味 氮肥 赶走里面的空气,防止点燃时发生爆炸 清除可燃物 温室效应
12. 铁 Zn+H2SO4=ZnSO4+H2↑
13. 真假“珍珠粉”灼烧后可能有不同现象 取样,在酒精灯火焰上灼烧片刻,观察颜色、状态变化 真、假“珍珠粉”的溶解性可能不同 取样,分别将它们的放入足量的水中,分辨溶解性有无差异 真、假“珍珠粉”的是否与盐酸反应冒气泡 取样,分别将它们的放入装有盐酸的试管中,观察气泡有无差异
14.(1) Fe H2 H2O FeSO4
(2)
15. O2; 改良酸性土壤 置换反应
16. CaO H2O Ca(OH)2+ CO2== CaCO3↓+H2O 2HCl+ Fe== FeCl2+H2↑ CuCl2+ Fe== FeCl2+Cu
17.
18. 过滤 Fe和Ag Zn(NO3)2 Fe(NO3)2 ACD
19. 氯化钙溶液;产生白色沉淀 实验步骤:取少量溶液于试管中,加入足量氯化钙溶液,静置,滴加酚酞试液;实验现象:产生白色沉淀,溶液变红色;实验结论:溶液中含有碳酸钠和氢氧化钠。
20.(1)Na2CO3;(2)3:4
21.(1)3.3;
(2)解:设水垢中碳酸钙的质量分数为x
x=75%。
答:水垢中碳酸钙的质量分数为75%。
22.(1)7:3
(2)解:反应前后元素种类质量不变;故理论上可炼铁质量为:
1000t×80%=560t
答:理论上可炼铁质量为560t。
23.解:由质量守恒定律可得,反应产生的二氧化碳的质量=378.5g-376.3g=2.2g
设样品中纯碱的质量为x,
样品中纯碱的质量分数=
答:样品中纯碱的质量分数为96.4%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.食品安全问题日益引起人们的重视,下列做法会损害人体健康的是 ( )
A.用小苏打烘焙糕点 B.加工火腿肠时放入过量亚硝酸钠防腐
C.用干冰冷藏食物 D.在酱油中加入铁强化剂补充铁元素
2.下列有关碳及碳的化合物的说法正确的是
A.金刚石、石墨和C60的化学性质相似,物理性质有很大差异,是因为它们由不同的原子构成
B.煤炉上放一盆水就能防止一氧化碳中毒
C.碳酸钙在医疗上可用作补钙剂
D.空气中二氧化碳含量过高可形成酸雨
3.下列说法正确的是
A.化学变化都遵循质量守恒定律,所以质量不发生改变的变化一定是化学变化
B.铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀
C.相同的木炭在氧气中燃烧比在空气中剧烈,说明反应的剧烈程度与反应物浓度有关
D.化学变化伴随有能量变化,所以有能量变化的一定是化学变化
4.“一带一路”赋予古丝绸之路崭新的时代内涵。古代染坊常用下列物质中的一种盐来处理丝绸,这种盐是
A.熟石灰 B.碳酸钾 C.乙醇 D.烧碱
5.下列防锈措施合理的是
A.经常用水冲洗自行车链条 B.在铁制暖气片上刷“银粉”
C.用“钢丝球”打磨铝锅表面 D.用过的菜刀及时用盐水清洗
6.有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,甲、丙表面出现红色物质,乙没有明显现象;再将大小相同的甲、丙分别放到相同的盐酸中,甲、丙均产生气泡,但甲产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是
A.甲>丙>乙 B.丙>乙>甲 C.甲>乙>丙 D.丙>甲>乙
7.草木灰是一种农家肥,其主要成分是K2CO3,它属于( )
A.钾肥 B.磷肥 C.氮肥 D.复合肥
8.有甲、乙、丙、丁四种金属,只有丙在自然界能以单质形态存在。含甲化合物的水溶液不能用乙制的容器盛放。将甲和丁分别放入硝酸铜溶液中,在甲表面有铜析出,而丁没有变化。这四种金属活动性顺序由弱到强的是
A.丙<丁<甲<乙 B.乙<甲<丁<丙 C.丁<甲<乙<丙 D.丙< 乙<甲<丁
9.化肥碳酸铵、硫酸钾均为白色固体。分别取少量固体进行下列实验,不能将两者区别出来的是
A.与熟石灰粉末混合研磨 B.加入稀盐酸中
C.加入溶液中 D.加入溶液中
10.下图所示反应,有关说法的错误的是
A.铝丝需要砂纸打磨
B.溶液由蓝色变为无色
C.金属活动性强弱:Al>Cu
D.反应的化学方程式为:Al+CuSO4=Cu+AlSO4
二、简答题
11.生活处处是化学。请回答:
(1)下列水的净化方法中净化程度最高的是________(填字母序号)。
A静置沉淀 B吸附沉淀 C蒸馏 D过滤
(2)制衣行业大量使用合成纤维,可用______方法区别合成纤维和羊毛制品。
(3)过度使用化肥也会造成水污染,但为了提高农作物产量又必须合理使用化肥。某稻田禾苗出现泛黄现象,此时应及时追施________(填“氮肥”或“钾肥”)。
(4)燃气公司给用户输送燃气,在初次使用之前需要通入氮气,通入氮气的目的是什么?______________。关闭燃气开关灭火,运用的原理是______
(5)植树造林提高绿化面积可降低_____ (填“温室效应”或“白色污染”)。
12.现有相同质量且相同形状的锌和铁两种金属,分别加入足量的溶质质量分数相同的稀硫酸中,产生氢气的质量与反应时间的关系如图所示。
(1)图中M代表___________(填“铁”或“锌”)。
(2)请写出锌和铁两种金属中与稀硫酸反应速率较快的化学方程式:___________。
13.用珍珠(主要成分CaCO3)加工成的“珍珠粉”是一种名贵中药材、保健品,可近年来市场上出现了一些假冒的“珍珠粉”,仅用肉眼观察难辨真假.为了向消费者提供鉴别方法,需找出真假“珍珠粉”理化性质上的差异,工商局提供了真、假“珍珠粉”样品,请你展开探究:(主要写出猜想、方案,不需要说出方案实施的具体结果)
猜想一:_____.
方案一:_____.
猜想二:_____.
方案二:_____.
猜想三:_____.
方案三:_____.
三、推断题
14.已知A、B、C、D四种物质之间存在以下转化关系。其中C是密度最小的气体,D是相对分子质量最小的氧化物。试回答:
(1)写出A、C、D三种物质的化学式:A_______、C________、D________。浅绿色溶液B中溶质的化学式____________。
(2)写出C→D的化学方程式___________。
15.A~F均为初中化学常见的物质,它们之间的关系如下图所示(“→”表示转化关系,涉及反应为初中常见反应),其中 A 俗名为生石灰,C为常见的溶剂,C 与 E 元素组成相同。请回答下列问题:
(1)F 的化学式为______。
(2)B 在农业上的用途是______(写一种)。
(3)转化中没有涉及的基本反应类型是______ 。
16.如图中是初中化学常见的一些物质,A是石灰石的主要成分,K是最常用的溶剂,D是胃酸的主要成分,E是金属单质,F是金属氧化物,G溶液呈浅绿色,J溶液呈蓝色,物之间的转化关系如图。“﹣”表示相连的两物质之间能发生反应,“→”表示一种物质能转化成另一种物质,部分反应条件、反应物、生成物已略去。
(1)请根据已知条件推断下列物质的化学式:B是_____;K是_____;
(2)请写出下列反应的化学方程式:
C→A:_____;
D+E→G+H:_____;
J+E→G:_____。
17.A、B、C、D、E、F是初中化学内容所涉及到的物质,其中A、B是氧化物,在一定条件下,它们的转化关系如图所示:
根据上图推断:
(1)C的化学式为 ___ 。
(2)D物质在氧气中燃烧,也能生成B,则B的化学式为 ___ 。
(3)写出D与稀硫酸反应的化学方程式 ___ 。
四、实验题
18.根据如图所示的实验探究过程,回答下列问题。
(1)图中操作①②的名称_____;
(2)固体甲的成分是_____;
(3)液体A中含有的成分除水外,还含有_____;
(4)下列有关说法中,正确的是_____;
A 无色气体是氢气
B 向固体乙中加人稀硫酸一定不会产生气泡
C 液体A的质量比原混合溶液的质量小
D 液体A和液体B均可除去铁粉中的锌粉
19.盛放氢氧化钠溶液的试剂瓶口和橡皮塞上出现了白色粉末。甲同学和乙同学对这种白色粉末的成分进行了如下猜想和验证。
(a)可能是氢氧化钠 (b)可能是碳酸钠 (c)可能是氢氧化钠与碳酸钠的混合物
(1)甲同学向所取少量粉末中滴加一种溶液后,排除了(a)的可能性。请你推测他所加的试剂和观察到的现象。_______________
(2)为了进一步探究白色粉末的成分,请你帮助乙同学设计一种方案进行鉴定,确定其成分,并写出简要的实验步骤、现象和结论。__________________
五、计算题
20.家庭厨房就是一个化学小世界,“柴米油盐”中包含着许多化学知识。食醋、食盐和纯碱都是日常生活中常用的物质。食醋中通常含有3%~5%的乙酸,乙酸俗称醋酸(化学式为CH3COOH),是一种无色液体。食盐和纯碱都是白色固体。
(1)醋酸和纯碱中属于无机物的是________(写化学式)。
(2)醋酸中,C、O两元素的质量之比为________(填最简整数比)。
21.长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。某研究性学习小组为测定水垢中碳酸钙的质量分数,将100.0g稀盐酸加人到10.0g水垢中。恰好完全反应后,容器内剩余物质的质量为106.7g。请回答:
(1)生成CO2气体的质量为________g。
(2)求测得水垢中碳酸钙的质量分数。
22.某钢铁厂用含Fe2O380%的赤铁矿石炼铁。
(1)计算Fe2O3中铁元素和氧元素的质量比______(填最简整数比)。
(2)该钢铁厂购买含Fe2O380%的赤铁矿石1000t,理论上可炼铁多少吨?
23.侯德榜成功研制了“侯氏制碱法”,打破了西方发达国家对我国制碱技术的封锁,为世界制碱工业做出了杰出贡献。某工厂为了测定用“侯氏制碱法”制得的纯碱样品中纯碱的质量分数,工厂技术员完成了图所示的测定工作(不考虑其它因素对测定结果的影响),请根据图中数据计算:样品中纯碱的质量分数。(计算结果精确到0.1%)
试卷第1页,共3页
参考答案:
1.B
2.C
3.C
4.B
5.B
6.A
7.A
8.A
9.C
10.D
11. C 燃烧闻气味 氮肥 赶走里面的空气,防止点燃时发生爆炸 清除可燃物 温室效应
12. 铁 Zn+H2SO4=ZnSO4+H2↑
13. 真假“珍珠粉”灼烧后可能有不同现象 取样,在酒精灯火焰上灼烧片刻,观察颜色、状态变化 真、假“珍珠粉”的溶解性可能不同 取样,分别将它们的放入足量的水中,分辨溶解性有无差异 真、假“珍珠粉”的是否与盐酸反应冒气泡 取样,分别将它们的放入装有盐酸的试管中,观察气泡有无差异
14.(1) Fe H2 H2O FeSO4
(2)
15. O2; 改良酸性土壤 置换反应
16. CaO H2O Ca(OH)2+ CO2== CaCO3↓+H2O 2HCl+ Fe== FeCl2+H2↑ CuCl2+ Fe== FeCl2+Cu
17.
18. 过滤 Fe和Ag Zn(NO3)2 Fe(NO3)2 ACD
19. 氯化钙溶液;产生白色沉淀 实验步骤:取少量溶液于试管中,加入足量氯化钙溶液,静置,滴加酚酞试液;实验现象:产生白色沉淀,溶液变红色;实验结论:溶液中含有碳酸钠和氢氧化钠。
20.(1)Na2CO3;(2)3:4
21.(1)3.3;
(2)解:设水垢中碳酸钙的质量分数为x
x=75%。
答:水垢中碳酸钙的质量分数为75%。
22.(1)7:3
(2)解:反应前后元素种类质量不变;故理论上可炼铁质量为:
1000t×80%=560t
答:理论上可炼铁质量为560t。
23.解:由质量守恒定律可得,反应产生的二氧化碳的质量=378.5g-376.3g=2.2g
设样品中纯碱的质量为x,
样品中纯碱的质量分数=
答:样品中纯碱的质量分数为96.4%。
答案第1页,共2页
答案第1页,共2页
