【人教版】化学九年级全一册 8.2.2 金属的活动性顺序及应用 习题课件
文档属性
| 名称 | 【人教版】化学九年级全一册 8.2.2 金属的活动性顺序及应用 习题课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 311.0KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-11 00:00:00 | ||
图片预览







文档简介
(共26张PPT)
课题2 金属的化学性质
第2课时 金属的活动性顺序及应用
第八单元 金属与金属材料
目录
学习目标
课堂导学
例题导学
课堂检测
化学用语天天练
写出下列反应的化学方程式:
铝与氧气反应________________________________
铁与盐酸反应________________________________
4Al + 3O2 ==== 2Al2O3
Fe + 2HCl==== FeCl2 + H2↑
课程标准:1. 能用金属活动性顺序对有关置换反应进行判断;2. 能用金属活动性顺序解释日常生活中的一些化学现象;3. 掌握金属活动性顺序表。
核心考点:金属活动性顺序的应用。
学习目标
课堂导学
金属与其他金属化合物溶液的反应
【温故知新】已知铁钉放在硫酸铜溶液中,观察到的现象是:铁钉表面覆盖一层 色固体,溶液颜色由 色变成 色。反应的化学方程式为 。
红
蓝
浅绿
Fe + CuSO4 ==== FeSO4 + Cu
【课堂活动】完成课本P11的探究实验,并填写下表。
实 验 现 象
铝丝浸入硫酸铜溶液中 铝丝表面有 色的物质产生,溶液由 色变成 色
实 验 反应的化学方程式
铝丝浸入硫酸铜溶液中
紫红
蓝
无
2Al + 3CuSO4 ==== Al2 (SO4) 3 + 3Cu
实 验 现 象
铜丝浸入硝酸银溶液中 铜丝表面有 色的物质产生,溶液由 色变成 色
实 验 反应的化学方程式
铜丝浸入硝酸银溶液中
白
无
蓝
Cu + 2AgNO3 ====Cu(NO3) 2 + 2Ag
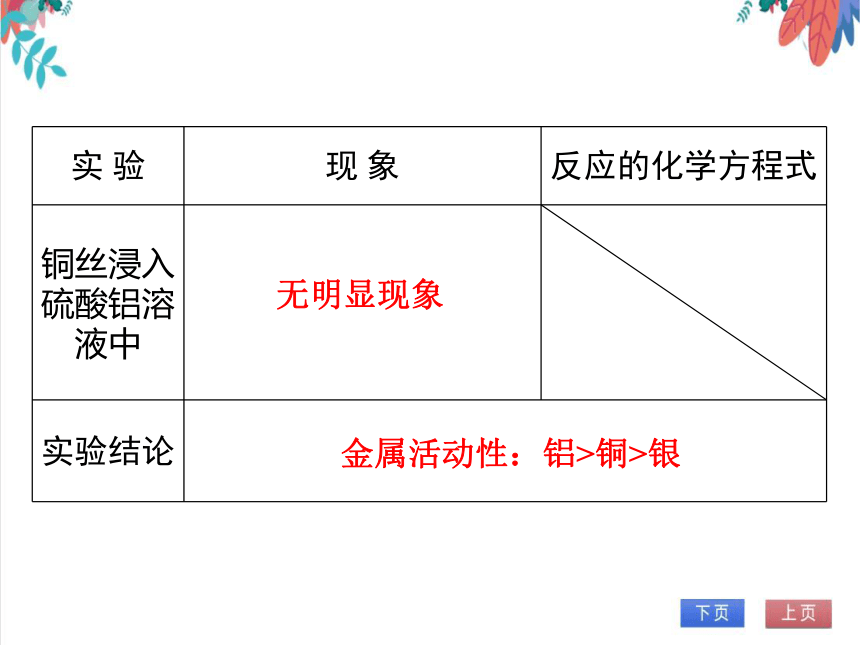
实 验 现 象 反应的化学方程式
铜丝浸入硫酸铝溶液中
实验结论 无明显现象
金属活动性:铝>铜>银
【规律总结】根据金属与其他金属化合物的溶液能否发生置换反应,可以判断两种金属的活动性强弱。
【注意】①铝丝在反应前表面要先打磨,目的是除去金属表面的氧化膜。②铁与其他金属的化合物溶液反应后,生成的铁的化合物中铁元素的化合价为+2价。
金属活动性顺序及其应用
【自主学习】阅读课本P12,了解金属的活动性顺序。
1. 常见金属在溶液中的活动性顺序
金属活动性由强逐渐减弱
( )( )( )( )( )( )( ) Sn Pb (H) ( ) Hg ( ) Pt Au
K
Ca
Na
Mg
Al
Zn
Fe
Cu
Ag
2. 金属活动性顺序在工农业生产和科学研究中的重要应用
(1)在金属活动性顺序里,金属的位置越靠前,它的活动性就 。
(2)在金属活动性顺序里,位于氢前面的金属 (填“能”或“不能”)置换出盐酸、稀硫酸中的 。
越强
能
氢
(3)在金属活动性顺序里,位于前面的金属 (填“能”或“不能”)把位于后面的金属从它们化合物的溶液里置换出来。
【注意】①金属与盐溶液的反应,盐必须能溶于水,不溶性的盐与金属不反应。②不能用活泼的金属K、Ca、Na与盐溶液反应,与酸反应时,先发生的是与酸的反应,后发生的是与水的反应。③金属与酸反应,所用的酸是盐酸、稀硫酸,不能选择浓硫酸和硝酸。
能
3. 金属活动性顺序的应用
(1)判断金属活动性强弱。
(2)判断金属与酸或其他金属化合物溶液能否发生反应。
(3)关于“三种金属活动性顺序”探究试剂的选择。
(“两金夹一液”“两液夹一金”,采用“取中”原则)
例题导学
【例1】 (2020·永州)将用砂纸打磨后的铁丝插入CuSO4溶液中,一段时间后,下列叙述正确的是( )
A. 溶液的质量增加
B. 溶液由蓝色变成无色
C. 溶液中产生大量气泡
D. 溶液中铁丝表面有红色物质生成
金属与其他金属化合物溶液的反应
D
【点拨】掌握金属的化学性质是正确解答本题的关键,要注意生成的是,溶液质量减少;溶液颜色由蓝色变成浅绿色。
【变式1】下列金属不能与CuSO4溶液反应的是( )
A. Ag B. Mg
C. Zn D. Al
A
【例2】(2020·鄂州)现有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿在Y的表面有银析出,而Z没变化,则X、Y、Z的金属活动性顺序为( )
A. X>Y>Z B. Z>Y>X
C. X>Z>Y D. Y>Z>X
金属活动性顺序及其应用
A
【点拨】在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键。
【变式2】(2020·金昌)某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中能达到目的的是( )
A. 将Fe丝、Cu丝分别放入AgNO3溶液中
B. 将Fe丝、Ag丝分别放入CuSO4溶液中
C. 将Fe丝、Cu丝、Ag丝分别放入稀盐酸中
D. 将Fe丝分别放入CuSO4溶液、AgNO3溶液中
B
课堂检测
1. 《天工开物》是世界上第一部关于农业和手工业生产的综合性著作,里面详细记述了金、锌、铜、铁等金属的开采和冶炼方法。上述金属中金属活动性最强的是( )
A. 金 B. 锌
C. 铜 D. 铁
B
2. 按图进行实验,下列分析或结论正确的是( )
A. 图1反应的化学方程式为 Al + CuSO4===AlSO4 + Cu
B. 图2实验的现象是:铜丝表面出现银白色的金属银
C. 由图1、图2实验可知,金属的活动性顺序为
Al>Cu>Ag
D. 由图1、图2实验无法判断Al、Cu、Ag的金属活动性
强弱
C
3. 有甲、乙、丙、丁四种金属,只有丙在自然界能以单质形态存在。含甲化合物的水溶液不能用乙制的容器盛放。将甲和丁分别放入硝酸铜溶液中,在甲表面有铜析出,而丁没有变化。这四种金属活动性顺序由强到弱的是( )
A. 乙>甲>丁>丙 B. 甲>乙>丁>丙
C. 丙>乙>甲>丁 D. 丁>甲>乙>丙
A
4. (2020·郴州)为了验证镁、铜、银三种金属的活动性顺序,某同学设计了如下实验,只需进行其中三个就能达到实验目的,你认为不必进行的是( )
A. 将镁片放入稀盐酸中
B. 将铜片放入稀盐酸中
C. 将镁片放入硝酸银溶液中
D. 将铜片放入硝酸银溶液中
C
5. (教材母题:九下人教版)写出下列变化的化学方程式,并注明反应类型(CO与Fe3O4 的反应除外)。
C+O2 ===== CO2;化合反应
CO2 +C===== 2CO;化合反应
3Fe+2O2 ===== Fe3O4;化合反应
Fe + CuSO4 === FeSO4 + Cu(合理即可);置换反应
Fe + 2HCl=== FeCl2 + H2↑(合理即可);置换反应
点 燃
高 温
点 燃
谢谢!
课题2 金属的化学性质
第2课时 金属的活动性顺序及应用
第八单元 金属与金属材料
目录
学习目标
课堂导学
例题导学
课堂检测
化学用语天天练
写出下列反应的化学方程式:
铝与氧气反应________________________________
铁与盐酸反应________________________________
4Al + 3O2 ==== 2Al2O3
Fe + 2HCl==== FeCl2 + H2↑
课程标准:1. 能用金属活动性顺序对有关置换反应进行判断;2. 能用金属活动性顺序解释日常生活中的一些化学现象;3. 掌握金属活动性顺序表。
核心考点:金属活动性顺序的应用。
学习目标
课堂导学
金属与其他金属化合物溶液的反应
【温故知新】已知铁钉放在硫酸铜溶液中,观察到的现象是:铁钉表面覆盖一层 色固体,溶液颜色由 色变成 色。反应的化学方程式为 。
红
蓝
浅绿
Fe + CuSO4 ==== FeSO4 + Cu
【课堂活动】完成课本P11的探究实验,并填写下表。
实 验 现 象
铝丝浸入硫酸铜溶液中 铝丝表面有 色的物质产生,溶液由 色变成 色
实 验 反应的化学方程式
铝丝浸入硫酸铜溶液中
紫红
蓝
无
2Al + 3CuSO4 ==== Al2 (SO4) 3 + 3Cu
实 验 现 象
铜丝浸入硝酸银溶液中 铜丝表面有 色的物质产生,溶液由 色变成 色
实 验 反应的化学方程式
铜丝浸入硝酸银溶液中
白
无
蓝
Cu + 2AgNO3 ====Cu(NO3) 2 + 2Ag
实 验 现 象 反应的化学方程式
铜丝浸入硫酸铝溶液中
实验结论 无明显现象
金属活动性:铝>铜>银
【规律总结】根据金属与其他金属化合物的溶液能否发生置换反应,可以判断两种金属的活动性强弱。
【注意】①铝丝在反应前表面要先打磨,目的是除去金属表面的氧化膜。②铁与其他金属的化合物溶液反应后,生成的铁的化合物中铁元素的化合价为+2价。
金属活动性顺序及其应用
【自主学习】阅读课本P12,了解金属的活动性顺序。
1. 常见金属在溶液中的活动性顺序
金属活动性由强逐渐减弱
( )( )( )( )( )( )( ) Sn Pb (H) ( ) Hg ( ) Pt Au
K
Ca
Na
Mg
Al
Zn
Fe
Cu
Ag
2. 金属活动性顺序在工农业生产和科学研究中的重要应用
(1)在金属活动性顺序里,金属的位置越靠前,它的活动性就 。
(2)在金属活动性顺序里,位于氢前面的金属 (填“能”或“不能”)置换出盐酸、稀硫酸中的 。
越强
能
氢
(3)在金属活动性顺序里,位于前面的金属 (填“能”或“不能”)把位于后面的金属从它们化合物的溶液里置换出来。
【注意】①金属与盐溶液的反应,盐必须能溶于水,不溶性的盐与金属不反应。②不能用活泼的金属K、Ca、Na与盐溶液反应,与酸反应时,先发生的是与酸的反应,后发生的是与水的反应。③金属与酸反应,所用的酸是盐酸、稀硫酸,不能选择浓硫酸和硝酸。
能
3. 金属活动性顺序的应用
(1)判断金属活动性强弱。
(2)判断金属与酸或其他金属化合物溶液能否发生反应。
(3)关于“三种金属活动性顺序”探究试剂的选择。
(“两金夹一液”“两液夹一金”,采用“取中”原则)
例题导学
【例1】 (2020·永州)将用砂纸打磨后的铁丝插入CuSO4溶液中,一段时间后,下列叙述正确的是( )
A. 溶液的质量增加
B. 溶液由蓝色变成无色
C. 溶液中产生大量气泡
D. 溶液中铁丝表面有红色物质生成
金属与其他金属化合物溶液的反应
D
【点拨】掌握金属的化学性质是正确解答本题的关键,要注意生成的是,溶液质量减少;溶液颜色由蓝色变成浅绿色。
【变式1】下列金属不能与CuSO4溶液反应的是( )
A. Ag B. Mg
C. Zn D. Al
A
【例2】(2020·鄂州)现有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿在Y的表面有银析出,而Z没变化,则X、Y、Z的金属活动性顺序为( )
A. X>Y>Z B. Z>Y>X
C. X>Z>Y D. Y>Z>X
金属活动性顺序及其应用
A
【点拨】在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键。
【变式2】(2020·金昌)某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中能达到目的的是( )
A. 将Fe丝、Cu丝分别放入AgNO3溶液中
B. 将Fe丝、Ag丝分别放入CuSO4溶液中
C. 将Fe丝、Cu丝、Ag丝分别放入稀盐酸中
D. 将Fe丝分别放入CuSO4溶液、AgNO3溶液中
B
课堂检测
1. 《天工开物》是世界上第一部关于农业和手工业生产的综合性著作,里面详细记述了金、锌、铜、铁等金属的开采和冶炼方法。上述金属中金属活动性最强的是( )
A. 金 B. 锌
C. 铜 D. 铁
B
2. 按图进行实验,下列分析或结论正确的是( )
A. 图1反应的化学方程式为 Al + CuSO4===AlSO4 + Cu
B. 图2实验的现象是:铜丝表面出现银白色的金属银
C. 由图1、图2实验可知,金属的活动性顺序为
Al>Cu>Ag
D. 由图1、图2实验无法判断Al、Cu、Ag的金属活动性
强弱
C
3. 有甲、乙、丙、丁四种金属,只有丙在自然界能以单质形态存在。含甲化合物的水溶液不能用乙制的容器盛放。将甲和丁分别放入硝酸铜溶液中,在甲表面有铜析出,而丁没有变化。这四种金属活动性顺序由强到弱的是( )
A. 乙>甲>丁>丙 B. 甲>乙>丁>丙
C. 丙>乙>甲>丁 D. 丁>甲>乙>丙
A
4. (2020·郴州)为了验证镁、铜、银三种金属的活动性顺序,某同学设计了如下实验,只需进行其中三个就能达到实验目的,你认为不必进行的是( )
A. 将镁片放入稀盐酸中
B. 将铜片放入稀盐酸中
C. 将镁片放入硝酸银溶液中
D. 将铜片放入硝酸银溶液中
C
5. (教材母题:九下人教版)写出下列变化的化学方程式,并注明反应类型(CO与Fe3O4 的反应除外)。
C+O2 ===== CO2;化合反应
CO2 +C===== 2CO;化合反应
3Fe+2O2 ===== Fe3O4;化合反应
Fe + CuSO4 === FeSO4 + Cu(合理即可);置换反应
Fe + 2HCl=== FeCl2 + H2↑(合理即可);置换反应
点 燃
高 温
点 燃
谢谢!
同课章节目录
