【人教版】化学九年级全一册 9.2.1 饱和溶液与不饱和溶液 习题课件
文档属性
| 名称 | 【人教版】化学九年级全一册 9.2.1 饱和溶液与不饱和溶液 习题课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 275.8KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-11 00:00:00 | ||
图片预览






文档简介
(共28张PPT)
课题2 溶 解 度
第1课时 饱和溶液与不饱和溶液
第九单元 溶 液
目录
学习目标
课堂导学
例题导学
课堂检测
化学用语天天练
请写出下列反应的化学方程式:
生石灰与水反应________________________________
镁与稀盐酸反应________________________________
铁和稀硫酸反应________________________________
铜和硝酸银溶液反应____________________________
CaO+H2O === Ca(OH)2
Mg+2HCl === MgCl2+H2↑
Fe+H2SO4 === FeSO4+H2↑
Cu+2AgNO3 === 2Ag+Cu(NO3)2
课程标准:1. 理解饱和溶液的概念;2. 掌握饱和溶液与不饱和溶液的转化方法;3. 了解结晶的方法。
核心考点:饱和溶液与不饱和溶液的转化方法;结晶的方法。
学习目标
课堂导学
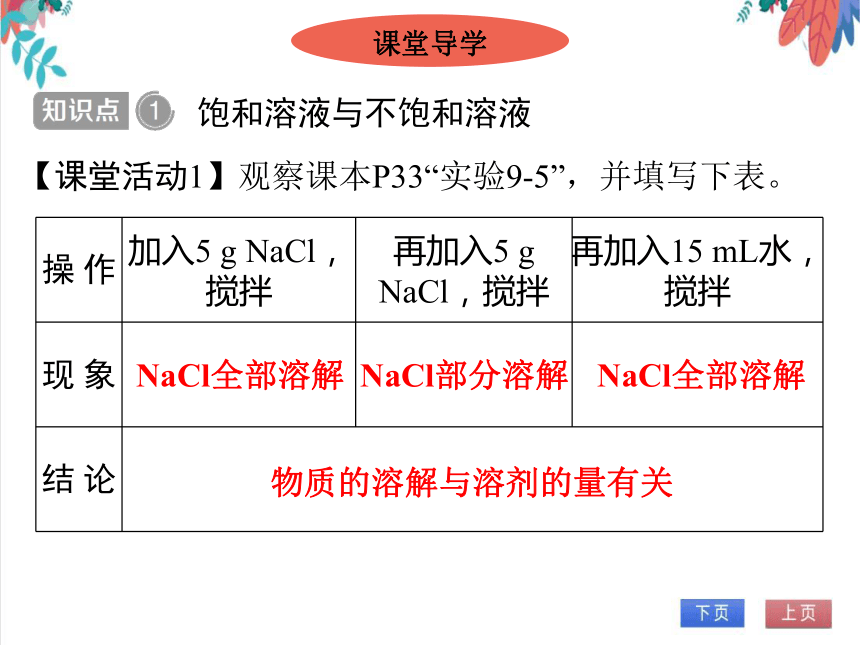
【课堂活动1】观察课本P33“实验9-5”,并填写下表。
饱和溶液与不饱和溶液
操 作 加入5 g NaCl,搅拌 再加入5 g NaCl,搅拌 再加入15 mL水,搅拌
现 象
结 论 NaCl全部溶解
NaCl部分溶解
NaCl全部溶解
物质的溶解与溶剂的量有关
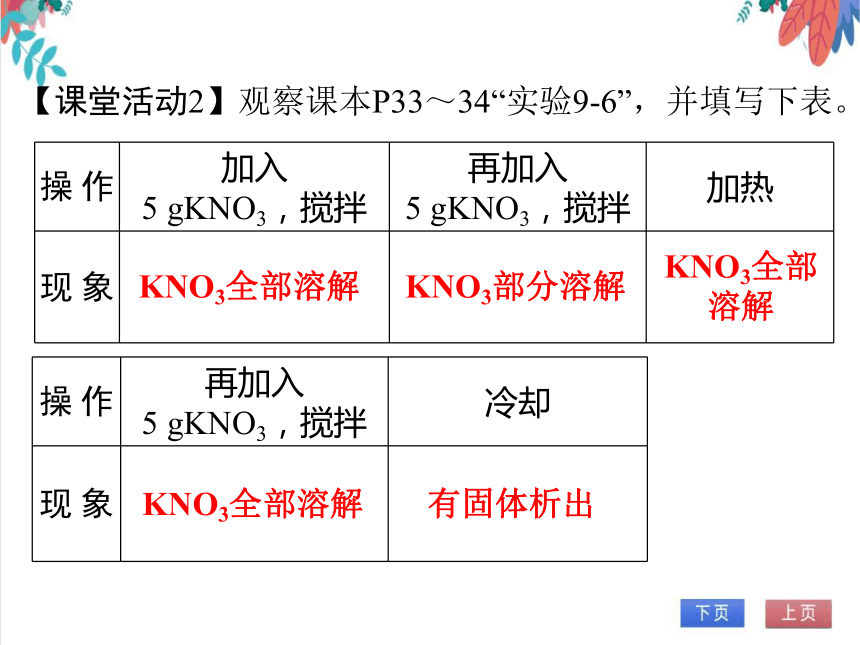
【课堂活动2】观察课本P33~34“实验9-6”,并填写下表。
操 作 加入 5 gKNO3,搅拌 再加入 5 gKNO3,搅拌 加热
现 象
操 作 再加入 5 gKNO3,搅拌 冷却
现 象
KNO3全部溶解
KNO3部分溶解
KNO3全部溶解
KNO3全部溶解
有固体析出
结 论
【小结归纳】
1. 在一定 下,向一定量 里加入某种溶质,当溶质 时,所得到的溶液叫做这种溶质的饱和溶液;当溶质 时,所得到的溶液叫做这种溶质的不饱和溶液。
不同温度下,物质的溶解能力不同
温度
溶剂
不能继续溶解
还能继续溶解
【注意】只有指明“在一定量溶剂里、在一定温度下”,溶液的“饱和”和“不饱和”才有确定的意义。2. 一定温度下,某溶质的饱和溶液 (填“能”或“不能”,下同)继续溶解该溶质,但 溶解其他溶质。
3. 判断某溶液是否饱和的方法:保持温度不变,向溶液中加入少量该溶质,若 ,则溶液为饱和溶液。
不能
能
溶质不再溶解
【自主学习】结合“实验9-5、实验9-6”的现象和结论,填写下列空格。
1. 饱和溶液与不饱和溶液的相互转化(一般情况下)
饱和溶液与不饱和溶液的相互转化
【注意】对极少数溶解度随温度升高而减小的物质[如Ca(OH)2],上述过程中温度的改变相反。
增加溶质、蒸发溶剂或降低温度
增加溶剂或升高温度
2. 浓溶液、稀溶液与饱和溶液、不饱和溶液的关系
(1)溶液的饱和、不饱和与溶液的浓和稀没有必然的关系。
(2)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液, 稀溶液不一定是不饱和溶液。
(3)在相同温度下同种溶剂、同种溶质的饱和溶液要比其不饱和溶液的浓度大。
结 晶
【自主学习】阅读课本P34~35,了解海水晒盐及结晶的方法。
1. 概念:热的溶液冷却后,不饱和溶液变成了饱和溶液,温度继续降低,已溶解在溶液中的溶质会从溶液中以 的形式析出,这一过程叫作结晶。(析出晶体后的溶液仍然是饱和溶液)
晶体
2. 结晶的方法
(1) :适用于溶解度随温度的降低而减小且溶解度受温度变化影响较大的固体物质。如从KNO3饱和溶液中得到KNO3晶体,就可以用冷却热饱和溶液法。
(2) :一般适用于溶解度受温度变化影响不大的固体物质。如从氯化钠溶液中得到氯化钠晶体,就可以用蒸发溶剂的方法。
冷却热饱和溶液
蒸发溶剂
3. 结晶的应用——海水晒盐
(1)原理:利用风吹和日晒使水分蒸发,食盐从溶液中结晶析出。
(2)主要过程如下:海水→贮水池→蒸发池→结晶池→粗盐→氯化钠。
例题导学
【例1】如图是小博进行的物质分离的相关实验。他将热的硫酸铜溶液(如图甲),静置一段时间后,变成如图乙。下列说法正确的是( )
A. 甲一定是不饱和溶液
B. 甲一定是饱和溶液
C. 乙一定是不饱和溶液
D. 乙一定是饱和溶液
饱和溶液与不饱和溶液
D
【点拨】理解饱和溶液是指在一定温度下、一定量的溶剂里,不能再继续溶解这种溶质的溶液是解题的关键。
【变式1】下列能证明硝酸钾溶液在50 ℃时已达到饱和状态的实验是( )
A. 取少量该溶液,升温后硝酸钾晶体析出
B. 取少量该溶液,降温到10 ℃时,有硝酸钾晶体析出
C. 在条件不改变的情况下,该溶液始终是稳定的
D. 温度不变时,向该溶液中加入少量硝酸钾晶体,晶体不再溶解
D
【例2】 现有一接近饱和的溶液,下列方法中一定能使之成为饱和溶液的是( )
①蒸发溶剂 ②增加溶质 ③降低温度 ④加热升温
A. ①② B. ②③
C. ①②③ D. ①②④
饱和溶液与不饱和溶液的相互转化
A
【点拨】增加溶质、蒸发溶剂都可以把不饱和溶液变成饱和溶液,但改变温度使不饱和溶液变成饱和溶液时要具体分析溶解度与温度的关系。
【变式2】下列叙述正确的是( )
A. 加溶剂可以使饱和溶液变成不饱和溶液
B. 某物质的饱和溶液就是不能再溶解该物质的溶液
C. 饱和溶液比不饱和溶液含溶质更多
D. 一种物质的饱和溶液中,不能再溶解其他溶质
A
【例3】 要想从食盐溶液中得到食盐晶体,宜采取的方法是( )
A. 蒸发溶剂的方法 B. 冷却热饱和溶液的方法
C. 倒掉部分溶液的方法 D. 升高温度的方法
结 晶
A
【点拨】了解结晶的原理与方法(降温结晶、蒸发结晶)并能灵活运用是正确解答本题的关键。
【变式3】(教材母题:九下人教版)如图是利用海水提取粗盐的过程:
(1)图中①是 池(填“蒸发”或“冷却”)。
蒸发
(2)根据海水晒盐的原理,下列说法中正确的是 (填字母)。
A. 海水进入贮水池,海水的成分基本不变
B. 在①中,海水中氯化钠的质量逐渐增加
C. 在①中,海水中水的质量逐渐减少
D. 析出晶体后的母液是氯化钠的不饱和溶液
AC
课堂检测
1. 将接近饱和的石灰水变成饱和溶液,不可行的方法是( )
A. 加入CaO B. 加入Ca(OH)2
C. 升高温度 D. 加入CaCO3
D
2. 降低温度使氯化钠饱和溶液析出晶体前后,不改变的是( )
A. 溶解度 B. 溶剂质量
C. 溶液质量 D. 溶质质量
B
3. 下列关于溶液的说法正确的是( )
A. 改变条件,能够使饱和溶液与不饱和溶液相互转化
B. 稀溶液一定是不饱和溶液
C. 降温一定可以使不饱和溶液变成饱和溶液
D. 饱和溶液的浓度一定比不饱和溶液的浓度大
A
4. 下列有关海水晒盐的说法,错误的是( )
A. 海水成为食盐的饱和溶液后才能析出晶体
B. 盐场必须建在阳光充足、雨量少的地区
C. 结晶池中析出盐后的母液没有用途,为防止污染须排入大海
D. 盐场得到的粗盐是混合物
C
5. 在一个温度不变的密闭容器内,放入一杯饱和的硫酸铜溶液,用细线吊住一块有缺口的硫酸铜晶体浸在溶液中(如图)。过几天后观察到:晶体上的缺口_____ (填“有”或“没有”)了;晶体的质量 (填“减小”“增大”或“没变”);此时的硫酸铜溶液是 (填“饱和”或“不饱和”溶液)。
没有
没变
饱和
谢谢!
课题2 溶 解 度
第1课时 饱和溶液与不饱和溶液
第九单元 溶 液
目录
学习目标
课堂导学
例题导学
课堂检测
化学用语天天练
请写出下列反应的化学方程式:
生石灰与水反应________________________________
镁与稀盐酸反应________________________________
铁和稀硫酸反应________________________________
铜和硝酸银溶液反应____________________________
CaO+H2O === Ca(OH)2
Mg+2HCl === MgCl2+H2↑
Fe+H2SO4 === FeSO4+H2↑
Cu+2AgNO3 === 2Ag+Cu(NO3)2
课程标准:1. 理解饱和溶液的概念;2. 掌握饱和溶液与不饱和溶液的转化方法;3. 了解结晶的方法。
核心考点:饱和溶液与不饱和溶液的转化方法;结晶的方法。
学习目标
课堂导学
【课堂活动1】观察课本P33“实验9-5”,并填写下表。
饱和溶液与不饱和溶液
操 作 加入5 g NaCl,搅拌 再加入5 g NaCl,搅拌 再加入15 mL水,搅拌
现 象
结 论 NaCl全部溶解
NaCl部分溶解
NaCl全部溶解
物质的溶解与溶剂的量有关
【课堂活动2】观察课本P33~34“实验9-6”,并填写下表。
操 作 加入 5 gKNO3,搅拌 再加入 5 gKNO3,搅拌 加热
现 象
操 作 再加入 5 gKNO3,搅拌 冷却
现 象
KNO3全部溶解
KNO3部分溶解
KNO3全部溶解
KNO3全部溶解
有固体析出
结 论
【小结归纳】
1. 在一定 下,向一定量 里加入某种溶质,当溶质 时,所得到的溶液叫做这种溶质的饱和溶液;当溶质 时,所得到的溶液叫做这种溶质的不饱和溶液。
不同温度下,物质的溶解能力不同
温度
溶剂
不能继续溶解
还能继续溶解
【注意】只有指明“在一定量溶剂里、在一定温度下”,溶液的“饱和”和“不饱和”才有确定的意义。2. 一定温度下,某溶质的饱和溶液 (填“能”或“不能”,下同)继续溶解该溶质,但 溶解其他溶质。
3. 判断某溶液是否饱和的方法:保持温度不变,向溶液中加入少量该溶质,若 ,则溶液为饱和溶液。
不能
能
溶质不再溶解
【自主学习】结合“实验9-5、实验9-6”的现象和结论,填写下列空格。
1. 饱和溶液与不饱和溶液的相互转化(一般情况下)
饱和溶液与不饱和溶液的相互转化
【注意】对极少数溶解度随温度升高而减小的物质[如Ca(OH)2],上述过程中温度的改变相反。
增加溶质、蒸发溶剂或降低温度
增加溶剂或升高温度
2. 浓溶液、稀溶液与饱和溶液、不饱和溶液的关系
(1)溶液的饱和、不饱和与溶液的浓和稀没有必然的关系。
(2)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液, 稀溶液不一定是不饱和溶液。
(3)在相同温度下同种溶剂、同种溶质的饱和溶液要比其不饱和溶液的浓度大。
结 晶
【自主学习】阅读课本P34~35,了解海水晒盐及结晶的方法。
1. 概念:热的溶液冷却后,不饱和溶液变成了饱和溶液,温度继续降低,已溶解在溶液中的溶质会从溶液中以 的形式析出,这一过程叫作结晶。(析出晶体后的溶液仍然是饱和溶液)
晶体
2. 结晶的方法
(1) :适用于溶解度随温度的降低而减小且溶解度受温度变化影响较大的固体物质。如从KNO3饱和溶液中得到KNO3晶体,就可以用冷却热饱和溶液法。
(2) :一般适用于溶解度受温度变化影响不大的固体物质。如从氯化钠溶液中得到氯化钠晶体,就可以用蒸发溶剂的方法。
冷却热饱和溶液
蒸发溶剂
3. 结晶的应用——海水晒盐
(1)原理:利用风吹和日晒使水分蒸发,食盐从溶液中结晶析出。
(2)主要过程如下:海水→贮水池→蒸发池→结晶池→粗盐→氯化钠。
例题导学
【例1】如图是小博进行的物质分离的相关实验。他将热的硫酸铜溶液(如图甲),静置一段时间后,变成如图乙。下列说法正确的是( )
A. 甲一定是不饱和溶液
B. 甲一定是饱和溶液
C. 乙一定是不饱和溶液
D. 乙一定是饱和溶液
饱和溶液与不饱和溶液
D
【点拨】理解饱和溶液是指在一定温度下、一定量的溶剂里,不能再继续溶解这种溶质的溶液是解题的关键。
【变式1】下列能证明硝酸钾溶液在50 ℃时已达到饱和状态的实验是( )
A. 取少量该溶液,升温后硝酸钾晶体析出
B. 取少量该溶液,降温到10 ℃时,有硝酸钾晶体析出
C. 在条件不改变的情况下,该溶液始终是稳定的
D. 温度不变时,向该溶液中加入少量硝酸钾晶体,晶体不再溶解
D
【例2】 现有一接近饱和的溶液,下列方法中一定能使之成为饱和溶液的是( )
①蒸发溶剂 ②增加溶质 ③降低温度 ④加热升温
A. ①② B. ②③
C. ①②③ D. ①②④
饱和溶液与不饱和溶液的相互转化
A
【点拨】增加溶质、蒸发溶剂都可以把不饱和溶液变成饱和溶液,但改变温度使不饱和溶液变成饱和溶液时要具体分析溶解度与温度的关系。
【变式2】下列叙述正确的是( )
A. 加溶剂可以使饱和溶液变成不饱和溶液
B. 某物质的饱和溶液就是不能再溶解该物质的溶液
C. 饱和溶液比不饱和溶液含溶质更多
D. 一种物质的饱和溶液中,不能再溶解其他溶质
A
【例3】 要想从食盐溶液中得到食盐晶体,宜采取的方法是( )
A. 蒸发溶剂的方法 B. 冷却热饱和溶液的方法
C. 倒掉部分溶液的方法 D. 升高温度的方法
结 晶
A
【点拨】了解结晶的原理与方法(降温结晶、蒸发结晶)并能灵活运用是正确解答本题的关键。
【变式3】(教材母题:九下人教版)如图是利用海水提取粗盐的过程:
(1)图中①是 池(填“蒸发”或“冷却”)。
蒸发
(2)根据海水晒盐的原理,下列说法中正确的是 (填字母)。
A. 海水进入贮水池,海水的成分基本不变
B. 在①中,海水中氯化钠的质量逐渐增加
C. 在①中,海水中水的质量逐渐减少
D. 析出晶体后的母液是氯化钠的不饱和溶液
AC
课堂检测
1. 将接近饱和的石灰水变成饱和溶液,不可行的方法是( )
A. 加入CaO B. 加入Ca(OH)2
C. 升高温度 D. 加入CaCO3
D
2. 降低温度使氯化钠饱和溶液析出晶体前后,不改变的是( )
A. 溶解度 B. 溶剂质量
C. 溶液质量 D. 溶质质量
B
3. 下列关于溶液的说法正确的是( )
A. 改变条件,能够使饱和溶液与不饱和溶液相互转化
B. 稀溶液一定是不饱和溶液
C. 降温一定可以使不饱和溶液变成饱和溶液
D. 饱和溶液的浓度一定比不饱和溶液的浓度大
A
4. 下列有关海水晒盐的说法,错误的是( )
A. 海水成为食盐的饱和溶液后才能析出晶体
B. 盐场必须建在阳光充足、雨量少的地区
C. 结晶池中析出盐后的母液没有用途,为防止污染须排入大海
D. 盐场得到的粗盐是混合物
C
5. 在一个温度不变的密闭容器内,放入一杯饱和的硫酸铜溶液,用细线吊住一块有缺口的硫酸铜晶体浸在溶液中(如图)。过几天后观察到:晶体上的缺口_____ (填“有”或“没有”)了;晶体的质量 (填“减小”“增大”或“没变”);此时的硫酸铜溶液是 (填“饱和”或“不饱和”溶液)。
没有
没变
饱和
谢谢!
同课章节目录
